Газета «Новости медицины и фармации» 4(309) 2010
Вернуться к номеру
Лучевая диагностика при бесплодии
О бесплодии принято говорить, если беременность не наступает в течение 1 года половой жизни без контрацепции [11]. От бесплодия страдает примерно 10 % женщин репродуктивного возраста [11]. Хотя патологические изменения матки служат причиной бесплодия только в 10 % случаев, ее визуализация необходима не только для установления более специфичного диагноза, но также для выбора тактики лечения [10, 19]. Выявление анатомических аномалий позволяет спрогнозировать возможные осложнения беременности, включая ее спонтанное прерывание, задержку развития плода, преждевременные роды, патологическое предлежание плода и задержку оплодотворенной яйцеклетки в маточной трубе.
Метод медицинской визуализации, используемый для исследования причин женского бесплодия, должен быть неинвазивным, недорогим и характеризоваться высокой диагностической точностью. В настоящее время в исследовании пациенток с бесплодием используются гистеросальпингография, УЗИ и МРТ.
Методы лучевой диагностики
Гистеросальпингография
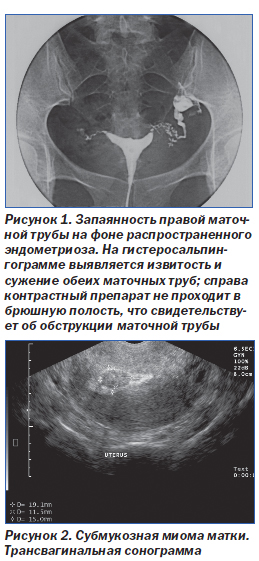
Гистеросальпингография представляет собой рентгеноскопическое исследование, при котором в полость матки и маточные трубы вводится рентгеноконтрастный препарат. Сегодня данная методика в основном применяется для оценки проходимости фаллопиевых труб, однако за счет визуализации внутренних контуров матки с ее помощью можно косвенно оценить состояние матки (рис. 1).
 Выполнение гистеросальпингографии не показано, если существует вероятность развития маточной беременности. Чтобы избежать воздействия излучения на раннем этапе беременности, используется правило «10 дней», согласно которому исследование не должно проводиться позже, чем через 10–12 дней от начала последней менструации. У пациенток с 28-дневным циклом (обычно менструация начинается через 14 дней после овуляции) этот период можно увеличить до 13–15 дней. При нерегулярном цикле или отсутствии менструации до исследования рекомендуется провести тест на беременность.
Выполнение гистеросальпингографии не показано, если существует вероятность развития маточной беременности. Чтобы избежать воздействия излучения на раннем этапе беременности, используется правило «10 дней», согласно которому исследование не должно проводиться позже, чем через 10–12 дней от начала последней менструации. У пациенток с 28-дневным циклом (обычно менструация начинается через 14 дней после овуляции) этот период можно увеличить до 13–15 дней. При нерегулярном цикле или отсутствии менструации до исследования рекомендуется провести тест на беременность.
Методика исследования
Исследование пациентки проводится в положении лежа на спине с согнутыми и разведенными коленями. Для фиксации ног используются специальные упоры. Для удобства визуализации шейки, особенно у женщин субтильной комплекции, таз пациентки приподнимается. После ведения гинекологических зеркал шейку матки и влагалище тщательно обрабатывают антисептическим раствором, например бетадином, затем устанавливается канюля для гистеросальпингографии. Существует несколько вариантов канюль, которые можно использовать [27]. После контроля расположения канюли зеркала можно удалить, их присутствие доставляет дискомфорт пациентке и ухудшает качество изображения. Под контролем флюороскопии в канюлю медленно (примерно 5–10 мл в минуту) вводится контрастный препарат комнатной температуры, после чего выполняются рентгенограммы. Введение препарата прекращается при появлении следов контраста в полости таза, попадании его в венозное русло либо при жалобах пациентки на чувство распирания, что характерно для непроходимости маточных труб.
Побочные эффекты и осложнения
При гистеросальпингографии пациентки могут испытывать дискомфорт и даже умеренные болевые ощущения [27]. Как правило, данное исследование не требует анестезии, но перед его началом целесообразно принять нестероидный противовоспалительный препарат (например, ибупрофен). После манипуляции могут появляться кровянистые влагалищные выделения, сильные кровотечения, требующие проведения кюретажа, развиваются редко, как правило, на фоне патологических изменений матки, например при полипах эндометрия. Также при исследовании могут развиваться сосудисто-вегетативные реакции и гипервентиляция, однако при адекватном настрое пациентки и опыте диагноста их, как правило, удается избежать.
При травматизации маточных труб во время гистеросальпингографии могут развиться серьезные инфекционные осложнения. В частной практике данное исследование осложняется инфекцией малого таза примерно в 1,4 % случаев, преимущественно у пациенток с расширенными маточными трубами [25]. В связи с этим при расширении маточных труб, в особенности если в них выявляется свободная жидкость, после исследования пациентке следует ввести профилактическую дозу антибиотика (например, 200 мг доксициклина per os) и назначить 5-дневный курс антибактериальной терапии.
Введение контрастного препарата может осложниться аллергической реакцией или идиосинкразией, однако такие осложнения наблюдаются достаточно редко и статистика их распространенности не исследована.
Воздействия рентгеновского излучения можно избежать при выполнении УЗ-гистеросальпингографии, а это имеет большое значение, так как обследуемые — это в основном женщины репродуктивного возраста. Случаи воздействия рентгеновского излучения на ранних стадиях беременности наблюдаются крайне редко, так как исследование выполняется в фолликулярную фазу цикла. Однако следует помнить, что выполнение гистеросальпингографии в ранний период беременности губительно для плода [16]. Лучевая нагрузка на яичники при исследовании минимальна, особенно при использовании современного флюороскопического оборудования и выполнении ограниченного числа рентгенограмм, необходимого для установления диагноза.
Анатомия и физиология маточных труб
Маточные трубы соединяют брюшинную полость с экстраперитонеальным пространством. В их функции входит транспорт спермы от маточного конца трубы по направлению к ампуле, продвижение яйцеклетки от яичникового конца трубы в ее ампулу, а также транспорт эмбриона из ампулы трубы в полость матки для последующей имплантации. В норме длина маточной трубы составляет от 7 до 16 см, в среднем 12 см. В ней выделяют 4 части: 1) интрамуральная или интерстициальная часть длиной от 1–2 см, которая проходит в толще стенки дна матки; 2) перешеек длиной 2–3 см; 3) ампула длиной 5–8 см; 4) воронка, которая представляет собой дистальную часть трубы характерной формы и заканчивается отверстием, обрамленным фимбриями. О проходимости трубы свидетельствует выход контрастного препарата в полость таза к яичнику или петлям кишки, что регистрируется на рентгенограммах или при УЗИ.
Диагностика патологических изменений
Узловой сальпингит
При узловом сальпингите в области перешейка маточной трубы формируются дивертикулы. Установить данные изменения при УЗИ достаточно сложно. Это заболевание было описано более 100 лет назад как неравномерная доброкачественная пролиферация эпителия с его инвагинацией в мышечный слой стенки с развитием реактивной гипертрофии миоцитов и иногда воспалительной реакции. В ряде случаев узловой сальпингит перешейка маточной трубы сочетается с воспалением соседних структур таза; остается неясным, является ли внутритазовый воспалительный процесс причиной сальпингита или это врожденное заболевание и перифокальное воспаление является вторичным.
Обструкция труб может произойти в любом сегменте. При УЗИ можно пропустить обструкцию в средней части перешейка трубы, так как здесь она имеет наименьший диаметр и не сопровождается дилатацией проксимально расположенного сегмента.
Полипы
Полипы визуализируются как небольшие дефекты наполнения с ровными гладкими контурами, они могут быть как одиночными, так и множественными и не изменяют конфигурацию и размеры полости матки.
Миомы
Миомы матки чаще являются одиночными, имеют более крупные размеры и дольчатую структуру, частично выходят на внутренний контур матки, деформируя ее полость.
Синехии
Синехии представляют собой фиброзные спайки, формирующиеся после осложненной беременности, воспалительных изменений, кюретажа и операций на матке. В основном синехии имеют линейный ход и неправильные контуры, распространяясь от одной стенки матки к другой, поэтому контраст обтекает их только в одной плоскости. В связи с этим выявить спайки в полости матки легче, чем вышеописанные объемные образования, которые обтекаются контрастным препаратом сразу в двух плоскостях. Синехии могут приводить к отсутствию контрастирования всей полости матки или ее части, что можно ошибочно принять за аномалию развития.
Синдром Ашермана
Сочетание бесплодия, гипо- или аменореи после перенесения кюретажа объединяют в синдром Ашермана. Он диагностируется у 68 % женщин с бесплодием, перенесших 2 и более эпизодов кюретажа [7]. Патогенез данного синдрома включает формирование синехий после травматизации эндометрия в процессе кюретажа полости матки после родов или после аборта. Реже данный синдром развивается в исходе эндометрита [19]. Предполагается, что синехии и рубцовые изменения в полости матки нарушают нормальный транспорт спермы и препятствуют имплантации эмбриона, вызывая бесплодие.
Противопоказания и недостатки метода
Противопоказанием к проведению гистеросальпингографии является активное влагалищное кровотечение, так как при этом есть риск ретроградного заброса тромбов в брюшинную полость. При активном воспалительном процессе данное исследование также следует отложить. Гистеросальпингография противопоказана в течение 6 недель после беременности, операции на матке или маточных трубах, а также после кюретажа матки, так как наличие дефектов эндометрия способствует попаданию контраста в венозное русло. К основным ограничениям метода относятся возможность визуализации только полых отделов матки и маточных труб и невозможность оценить наружные контуры матки. Кроме того, следует помнить, что гистеросальпингография предполагает воздействие ионизирующего излучения на организм, что имеет значение при обследовании молодых женщин.
Ультразвуковое исследование
Благодаря высокой диагностической точности, минимальному дискомфорту для пациентки, низкой стоимости и широкой доступности УЗИ широко используется для исследования матки. С появлением трансвагинального УЗИ, цветного допплеровского сканирования и УЗ-гистерографии оно стало еще более чувствительным методом диагностики изменений эндометрия и миометрия.
Оценить проходимость и морфологию фаллопиевых труб позволяет УЗ-сальпингография (синоним: соносальпингография), при которой для изучения проходимости труб используется физиологический раствор и/или контрастный препарат.
УЗИ следует проводить в секреторную фазу менструального цикла, когда эндометрий имеет максимальную толщину, что удобно для исследования его эхо-структуры [22]. Однако для изучения аномалий развития стадия менструального цикла не имеет особого значения. Соносальпингография выполняется в ту же стадию цикла, что и традиционная гистеросальпингография.
Методика исследования
Необходимо получать изображения не только в классических для малого таза сагиттальной и аксиальной плоскостях, но и в плоскости, направленной вдоль длинной оси матки, что позволяет лучше оценить ее наружный контур. УЗИ через переднюю брюшную стенку лучше выполнять с использованием датчика с частотой от 2 до 6 МГц. Для трансвагинального исследования применяются датчики с частотой от 5 до 8 МГц. Преимуществом трансвагинального УЗИ является более высокое разрешение, которого удается достичь за счет уменьшения поля обзора.
Соносальпингография представляет собой разновидность трансвагинального УЗИ с введением в полость матки и просвет труб физиологического раствора или контрастного препарата. При этом оценивается состояние поверхности эндометрия и удается выявить синехии и объемные образования, например полипы и субмукозные миомы. Осторожное надавливание на датчик во время исследования позволяет диагносту дополнительно оценить подвижности матки, маточных труб и яичников.
Сначала для определения проходимости фаллопиевых труб можно использовать физиологический раствор. Если после этого сохраняются сомнения в их проходимости, следует использовать контрастный препарат. Во время введения препарата рекомендуется применять баллонный катетер, предотвращающий вытекание жидкости из полости матки. Перед введением контрастного препарата из полости матки необходимо удалять физиологический раствор.
Ряд исследователей считают, что использование цветного допплеровского сканирования вместе с введением физиологического раствора позволяет лучше оценить проходимость труб [18, 24]. Использовать эту технологию можно и при исследовании с контрастом.
Контрастные препараты, содержащие микропузырьки, позволяют получить позитивное контрастирование и задокументировать проходимость труб, а также выход контраста в брюшинную полость. Безопасность таких препаратов была доказана во многих исследованиях, однако из-за высокой стоимости их целесообразно применять по определенной группе показаний.
Появление болей при введении контрастного препарата может являться признаком непроходимости труб за счет компрессии извне или внутренней обструкции. Спазм трубы может вызывать транзиторное отсутствие контрастирования ее проксимальной части.
УЗ-анатомия и диагностика патологических изменений
В норме при введении физиологического раствора или контрастного препарата просвет трубы имеет вид тонкой неровной полоски.
При гидросальпинксе маточная труба приобретает вид веретеновидной или кистозной структуры. При этом контрастный препарат может растворяться в скопившейся в трубе жидкости, в образовавшейся взвеси могут появляться пузырьки воздуха, что затрудняет интерпретацию.
Диагностическая точность УЗИ, по данным литературы, составляет 90–92 % [22, 24]. Соносальпингография с введением физиологического раствора позволяет более четко оценить поверхность эндометрия и полость матки. Трехмерное УЗИ с получением поверхностных и прозрачных реконструкций матки имеет преимущество перед стандартным двухмерным исследованием. В руках опытного диагноста чувствительность метода достигает 93 %, а специфичность — 100 % [18].
Недостатки метода, побочные эффекты и осложнения
Соногистеросальпингография имеет те же ограничения, что и трансвагинальное УЗИ в целом, позволяя дополнительно оценить лишь проходимость маточных труб и полости матки [24].
Основным недостатком метода является его высокая операторозависимость. Кроме того, при УЗИ существует ряд факторов, которые могут помешать выполнению полноценного исследования, в их числе избыточная масса тела и наличие крупных миом матки (рис. 2, 3).
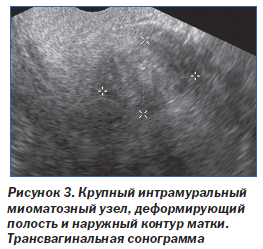 Побочные эффекты и осложнения соносальпингографии в основном те же, что и при традиционной гистеросальпингографии.
Побочные эффекты и осложнения соносальпингографии в основном те же, что и при традиционной гистеросальпингографии.
Магнитно-резонансная томография
Как известно, к причинам женского бесплодия относятся расстройства овуляции (например, при аденомах гипофиза или синдроме поликистоза яичников), заболевания фаллопиевых труб (гидросальпинкс, воспалительные изменения), аномалии мюллеровых протоков и доброкачественные заболевания матки (аденомиоз, миомы), а также эндометриоз.
МРТ позволяет оценить структуру и функцию матки и яичников, визуализировать аденомы гипофиза, дифференцировать пороки развития мюллеровых протоков и установить диагноз аденомиоза без выполнения инвазивных манипуляций. Помимо прочего, данный метод позволяет спрогнозировать результаты лечения аденомиоза, миом матки и эндометриоза, а также выбрать оптимальный метод и тактику лечения.
С помощью МРТ удается в нескольких плоскостях оценить наружную и внутреннюю структуру матки, однако оценить проходимость маточных труб и выявить небольшие перитубулярные спайки при этом не представляется возможным. Благодаря высочайшей тканевой контрастности МР-изображений данный метод позволяет установить диагноз при большинстве гинекологических заболеваний.
Зачастую методом выбора в лечении причин бесплодия является лапароскопия, точная диагностика в предоперационном периоде имеет особенно большое значение в планировании соответствующего вмешательства.
Методика исследования
Для исследования оптимально использовать поверхностную катушку для тела. Протокол исследования для установления причин бесплодия включает быстрые спин-эхо последовательности с получением изображений в аксиальной, сагиттальной и коронарной, а также в дополнительных косых плоскостях, которые позволяют визуализировать матку в истинной аксиальной и коронарной плоскости.
Для исключения сопутствующих аномалий развития почек следует дополнительно получить изображение с большим полем обзора. Дополнительно рекомендуется выполнение Т1-ВИ таза в аксиальной плоскости. Для дифференциальной диагностики сложных образований яичников, в частности с целью исключения злокачественного характера процесса, может понадобиться введение гадолинийсодержащего контрастного препарата.
Некоторые авторы рекомендуют перед исследованием внутривенно или внутримышечно вводить ингибитор перистальтики (1 единицу глюкагона или 20 мг бромида бутилскополамина).
К недостаткам МРТ относится высокая стоимость исследования, ограниченная доступность оборудования, а также более длительное время исследования, чем при УЗИ. В связи с этим данный метод используется для дополнительного исследования в случаях, когда результаты УЗИ малоинформативны [15, 24].
Нормальная МРТ-анатомия в репродуктивном возрасте
Оптимально оценить зональную анатомию матки можно на Т2-ВИ. Эндометрий дает МР-сигнал высокой интенсивности; переходная зона, соответствующая внутреннему слою миометрия, выглядит как граничащий с эндометрием гипоинтенсивный слой. Наружные отделы миометрия характеризуются гипоизоинтенсивным
МР-сигналом, но по сравнению с поперечнополосатыми мышцами выглядят более яркими. Толщина эндометрия и переходной зоны варьирует в зависимости от фазы менструального цикла и достигает максимума в позднюю секреторную фазу (рис. 4).
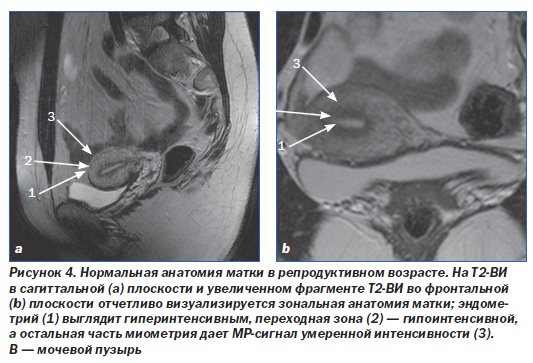
В репродуктивном возрасте тело матки преобладает над шейкой, в среднем тело матки составляет 6–8 см в длину и 5–6 см в ширину и высоту [13].
В шейке матки на Т2-ВИ также удается дифференцировать отдельные слои стенки. Центральная зона дает гиперинтенсивный МР-сигнал и соответствует слизистой оболочке и слизи, расположенной в цервикальном канале; средняя гипоинтенсивная зона соответствует фиброзной строме, а наружная — миометрию, она характеризуется МР-сигналом средней интенсивности. Стенка влагалища на Т2-ВИ дает гипоинтенсивный МР-сигнал. В репродуктивном возрасте на Т2-ВИ в структуре яичников можно четко дифференцировать гипоинтенсивную строму и гиперинтенсивные фолликулы.
В норме маточные трубы на МР-изображениях не визуализируются, ввиду небольшого диаметра и извитого хода.
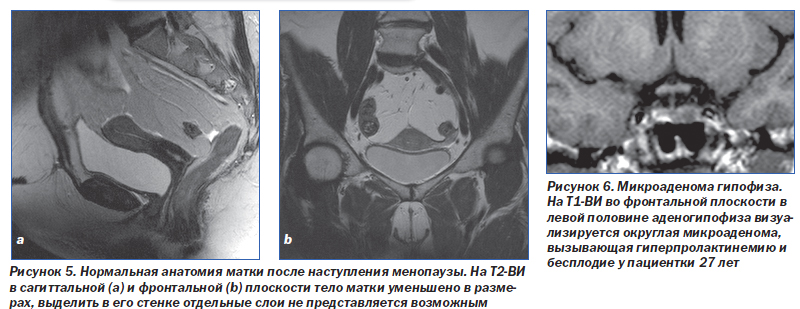
Нормальная МРТ-анатомия после наступления менопаузы
После наступления менопаузы тело матки уменьшается в размерах и по длине становится сопоставимо с шейкой. Зональная анатомия матки перестает дифференцироваться, за исключением случаев получения заместительной гормональной терапии (рис. 5). Хотя шейка матки не подвергается значительной атрофии, наружный слой ее миометрия в постменопаузе обычно утрачивает четкость. Яичники больше не содержат фолликулы и потому редко визуализируются при МРТ.
Если в репродуктивном возрасте матка уменьшена в размерах и утрачивает дифференцировку зональной анатомии, как после наступления менопаузы, необходимо исключать заболевания, сопровождающиеся недостаточной секрецией гормонов [14].
Лучевая диагностика патологических изменений
Овуляторная дисфункция
Нарушения овуляции являются причиной женского бесплодия примерно в 30–40 % случаев [11]. Для оценки функции яичников проводятся измерения базальной температуры тела, биопсия эндометрия, определение сывороточной концентрации прогестерона, исследование эндокринных желез и мониторинг цикла фолликулов с помощью УЗИ. Роль МРТ при этом ограничивается исключением аденомы гипофиза [14].
Аденома гипофиза
Наиболее часто из гормонально активных аденом гипофиза встречается пролактинома. Пик заболеваемости приходится на возраст 20–30 лет. Гиперпролактинемия может проявляться бесплодием, вызывать снижение секреции гонадотропина, вторичную аменорею и галакторею. Перед началом обследования по поводу бесплодия следует исключить гиперпролактинемию, индуцированную приемом лекарственных препаратов. Известно, что секрецию пролактина могут усиливать антидепрессанты, циметидин, антагонисты допамина, резерпин, сульпирид, верапамил, метилдопа и эстрогенные препараты.
При исключении гиперпролактинемии как побочного эффекта лекарственного препарата методом выбора для дальнейшего исследования является МРТ, которая позволяет диагностировать микроаденомы гипофиза (диаметром ≤ 1см). В большинстве случаев на Т1-ВИ микроаденомы выглядят гипоинтенсивными на фоне ткани гипофиза (рис. 6). Косвенными признаками микроаденом являются конвексное выпячивание верхнего контура железы и девиация ее ножки. Наиболее точным методом диагностики микроаденом является динамическое контрастирование, позволяющее максимально дифференцировать опухоль на фоне нормальной паренхимы железы. При исследовании с динамическим контрастированием нормальная паренхима гипофиза и его ножка быстро и интенсивно накапливают контрастный препарат на ранней фазе контрастирования, тогда как микроаденомы демонстрируют слабое отсроченное контрастное усиление [21].
Макроаденомы гипофиза (более 1 см) занимают турецкое седло и, оказывая давление на перекрест зрительных нервов, могут проявляться нарушениями зрения. Опухоли таких размеров склонны распространяться в кавернозный синус и вызывать эрозии дна турецкого седла. Границы опухоли оптимально оценивать на ранних постконтрастных МР-изображениях.
Синдром поликистоза яичников
Диагноз синдрома поликистоза яичников основывается на изменении гормонального статуса и лабораторных данных. У пациенток с данным синдромом изменяется соотношение концентраций лютеинизирующего и фолликулостимулирующего гормонов. Клиническая картина складывается из гирсутизма, отсутствия овуляции и бесплодия. Макроскопически такие яичники содержат множество мелких фолликулярных кист, окруженных утолщенной лютеинизирующей оболочкой.

Мониторинг роста фолликулов обычно осуществляется с помощью УЗИ (рис. 7), преимущество МРТ в этом аспекте не доказано. На Т2-ВИ при синдроме поликистоза вокруг гипоинтенсивной центральной стромы яичников определяются множественные гиперинтенсивные кисты небольших размеров [17]. Однако данные МРТ при этом неспецифичны и могут служить лишь подтверждением диагноза. Множественные мелкие гиперинтенсивные кисты по периферии яичника также выявляются при ановуляции, медицинской стимуляции овуляции и агенезии влагалища [17].
Патология маточных труб
На долю патологических изменений маточных труб приходится примерно 30–40 % женского бесплодия [11]. Данная группа изменений объединяет повреждение, обструкцию фаллопиевых труб и перитубальные спайки.
Основным методом исследования проходимости маточных труб остается гистеросальпингография, для оценки состояния перитубальных тканей преимущество отдается лапароскопии. МРТ позволяет неинвазивно диагностировать расширение труб и перитубальные изменения. Расширенные маточные трубы на МР-изображениях имеют вид кистозных структур, заполненных жидкостью и имеющих вытянутую, С- или S-образную форму [13, 16]. Тонкие продольно ориентированные складки по нижнему краю трубы представляют собой не полностью расправленные складки слизистой или подслизистой оболочки [23]. Одной из основных причин изменений труб и перитубальных тканей является воспаление органов малого таза. В большинстве случаев диагноз основывается на данных клиники и трансвагинального УЗИ. МРТ имеет дополнительное значение в исследовании воспалительных изменений структур малого таза, а также позволяет выявлять тубоовариальные абсцессы, расширение маточных труб со скоплением в них жидкости и наличие свободной жидкости в полости таза [31].

Причиной перитубальных спаек может стать эндометриоз, наиболее чувствительным методом диагностики которого является МРТ. Расширение маточных труб с наличием в них гиперинтенсивной на Т1-ВИ жидкости (гематосальпинкс) может быть одним из проявлений наружного генитального эндометриоза (рис. 8) [23].
Из книги «Лучевая диагностика в гинекологии: Руководство для врачей» /
Под ред. Г.Е. Труфанова, В.О. Панова. — СПб.: ЭЛБИ-СПб, 2008