Газета «Новости медицины и фармации» Антимикробная и противовирусная терапия (310) 2010 (тематический номер)
Вернуться к номеру
Стартовая антибактериальная терапия при внегоспитальной пневмонии (разбор клинических случаев)
Авторы: Л.В. Юдина, Киевская медицинская академия последипломного образования им. П.Л. Шупика
Версия для печати
Вопрос об антибактериальной терапии инфекций нижних дыхательных путей неоднократно обсуждался на страницах печати, однако по-прежнему выбор стартовой эмпирической терапии при лечении больных внегоспитальной пневмонией (ВП) вызывает затруднения. Позволю себе на клинических примерах обосновать выбор антибактериального (АБ) препарата для амбулаторных больных ВП.
Клиническая ситуация 1
Больная Б., 65 лет, обратилась с ВП верхней доли правого легкого, по поводу которой она лечилась амбулаторно без эффекта (сохранялся кашель и субфебрилитет). Принимала ципрофлоксацин 5 дней, а затем азитромицин в течение 3 дней. При рентгенологическом исследовании выявлена ВП верхней доли правого легкого (рис. 1).
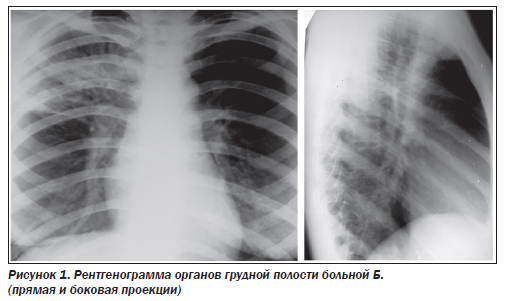
Для обсуждения правильности выбора АБ-препарата следует вспомнить, что основными возбудителями при ВП являются S.pneumoniaе, H.influenzae, Staphylococcus aureus, Legionella spp., Mycoplasma pneumoniae, Chlamydophila pneumonia грамотрицательные энтеробактерии и вирусы.
Для стартовой терапии пациентке был выбран ципрофлоксацин. Микробиологическими особенностями фторхинолонов (ФХ) II поколения является то, что к ним чувствительны грамотрицательные палочки семейства Enterobacteriaceae, P.aeruginosa и некоторые внутриклеточные микроорганизмы (Legionella spp.), однако к препаратам этой группы малочувствительны большинство стрептококков (в том числе пневмококк), энтерококк, хламидии, микоплазмы, что может привести к неудачам при лечении ВП. Отсутствие эффекта от назначенного препарата могло навести на мысль о пневмококковой этиологии заболевания. С этой точки зрения назначенный пациентке азитромицин мог бы сыграть свою положительную роль. Макролиды активны в отношении типичных и атипичных возбудителей инфекций дыхательных путей, однако растет число S.pneumoniae, устойчивых к макролидам. Кроме того, слабым звеном этих препаратов является их низкая активность в отношении H.influenzae. Ввиду отсутствия эффекта от применения азитромицина можно предположить, что этиологическую роль при ВП у данной пациентки сыграл пенициллинорезистентный пневмококк. При выборе антибиотика для лечения внебольничной пневмонии (на догоспитальном этапе и в стационаре) необходимо учитывать следующие критерии:
 Этим критериям соответствуют такие группы препаратов, как защищенные аминопенициллины, современные макролиды, респираторные фторхинолоны и цефалоспорины II–III поколения, которые и являются приоритетными в лечении больных ВП.
Этим критериям соответствуют такие группы препаратов, как защищенные аминопенициллины, современные макролиды, респираторные фторхинолоны и цефалоспорины II–III поколения, которые и являются приоритетными в лечении больных ВП.
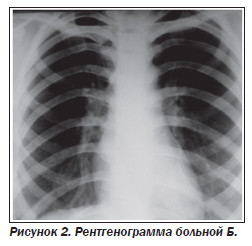
Учитывая то, что больная уже принимала азитромицин, что абсолютно приемлемо для стартовой терапии на амбулаторном этапе, ей были рекомендованы следующие лекарственные препараты: амоксициллин/клавуланат (Аугментин™) в таблетках по 875/125 мг дважды в день на протяжении 7 дней, амброксол внутрь, фенспирид по схеме. Через две недели было проведено конт-рольное рентгенологическое исследование: инфильтрация легочной ткани практически рассосалась (рис. 2). Это подтверждает правильность подбора АБ-препарата.
Клиническая ситуация 2
Больная К., 18 лет, заболела остро с повышения температуры тела до 39 °С, кашля с трудноотделяемой мокротой, одышки. Общий анализ крови: гем. — 124 г/л, эр. — 3,8 х 1012/л, лейк. — 10,8 х 109/л, п/я — 1 %, с/я — 30 %, эоз. — 4 %, лимф. — 53 %, мон. — 8 %, СОЭ — 35 мм/ч. До поступления в стационар больная самостоятельно лечилась аспирином, ко-тримоксазолом и домашними средствами. Участковый врач назначил цефазолин на 10 дней. Состояние улучшилось незначительно. При рентгенологическом исследовании выявлена инфильтрация нижней доли правого легкого (рис. 3). У больной диагностирована внегоспитальная пневмония нижней доли правого легкого.
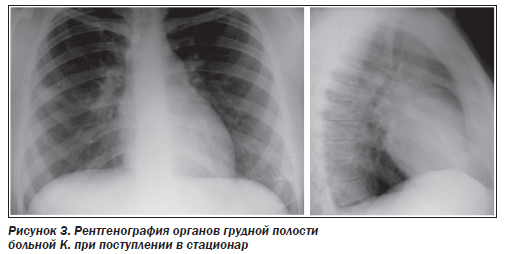
Дома лечение своего заболевания пациентка самостоятельно начала с бисептола. Согласно некоторым статистическим исследованиям, ко-тримоксазол — это наиболее частое противомикробное средство в домашних аптечках. Если принять во внимание, что основная патология, по поводу которой пациенты сами начинают принимать антибиотики в амбулаторных условиях, — инфекции дыхательных путей, то подобная популярность препарата внушает страх. К ко-тримоксазолу существует значительная резистентность пневмококков и гемофильной палочки по всему земному шару. К бисептолу устойчивы более 50 % пневмококков. Совершенно очевидно, что для эмпирического лечения болезней дыхательных путей антимикробный препарат с подобным уровнем резистентности использоваться не может [2]. Неизвестно ни одной бактерии, за исключением редких микробов вроде Burkholderia cepacia, Stenotrophomonas maltophilia или пневмоцист, которые обладали бы минимально приемлемой чувствительностью, хотя бы на уровне 70 % штаммов, к ко-тримоксазолу. Поэтому, если больной внегоспитальной пневмонией принимал ко-тримоксазол, можно вообще не обращать на это внимание и считать, что пациент ничем из антибиотиков не лечился. По данным М.Б. Богданова и соавт. [3], при ВП после лечения ко-тримоксазолом, гентамицином и ципрофлоксацином ведущим возбудителем как был, так и оставался пневмококк. Кроме того, при использовании этого препарата часто наблюдаются кожно-аллергические реакции (вплоть до синдрома Стивенса — Джонсона и Лайелла) [1, 4].
Таким образом, отсутствие эффекта от бисептола у пациентки К. закономерно. Надо заметить, однако, что врач не отменил бисептол, а добавил цефазолин внутримышечно на 10 дней. Цефазолин относится к цефалоспоринам (ЦФ) первой генерации. Микробиологические показания к применению этих препаратов ограничены стрептококками и оксациллин-чувствительными стафилококками. Цефазолин не обладает реальной активностью против H.influenzae и атипичных возбудителей, разрушается β-лактамазами, поэтому выбор стартовой терапии нельзя назвать рациональным. Как известно, заметного улучшения после приема цефазолина пациентка не отмечала. Можно предположить, что после не-эффективной терапии ЦФ I поколения инфекция может продолжаться из-за оксациллин-устойчивых стафилококков, энтерококков и грамотрицательных бактерий, что, очевидно, и произошло в данном случае с нашей пациенткой.
Хотелось бы обратить внимание также на длительность приема цефазолина. Известно, что эффективность препарата оценивается через 48–72 часа. При отсутствии эффекта антибиотик следует заменить другим. Пациентка, к сожалению, продолжала прием цефазолина в течение 10 дней, что было неоправданным. Применение неэффективного препарата имеет немало негативных последствий. В первую очередь при этом затягивается назначение другого, более адекватного антибиотика, что ведет к прогрессированию воспаления (особенно важно при тяжелых пневмониях, у больных с сопутствующей патологией) и развитию осложнений, а также удлиняет сроки лечения. Кроме того, повышается риск возникновения побочных (токсических) эффектов препаратов, а также развития и усиления антибиотикорезистентности. Продолжение лечения, несмотря на неэффективность проводимой терапии, подрывает доверие больного и его родственников к лечащему врачу. Очевидна и неэкономичность такой ошибочной тактики антибактериальной терапии (напрасный расход неэффективного антибиотика, дополнительные затраты на лечение нежелательных явлений и др.).
Какой же препарат назначить пациентке К.? Ответ на этот вопрос можно найти в национальном согласительном документе, которым является Наказ № 128 від 19.03.2007 р. «Про затвердження клінічних протоколів надання медичної допомоги за спеціальністю «пульмонологія». В приказе говорится, что при эмпирической антибактериальной терапии ВП у больных с нетяжелым течением болезни при госпитализации в стационар (III группа) рекомендуется назначить следующие АБ-препараты:
— амоксициллин/клавулановую кислоту (Аугментин™) или ампициллин/сульбактам + макролид;
— цефалоспорин II–III поколения (цефуроксим, цефотаксим, цефтриаксон) + макролид;
— в случае неэффективности препарата через 48 часов необходимо заменить его фторхинолоном III–IV поколения (монотерапия) или карбапенемами.
Что предпочесть: защищенные аминопенициллины или цефалоспорины? Выбор остается за лечащим врачом, но, к сожалению, широкое использование ЦС III поколения (часто без достаточных показаний) является основной причиной увеличения количества β-лактамаз расширенного спектра. Ввиду этого ЦС III поколения больше не должны быть «рабочими лошадками» в госпитальных учреждениях. Доказано, что уменьшение использования ЦС III поколения приводит к существенному уменьшению β-лактамазопродуцирующих штаммов микроорганизмов [5].
Пациентке в стационаре была предложена следующая терапия: амоксициллин/клавуланат (Аугментин™) 1000/200 мг в/в через 8 часов три дня, затем Аугментин™ таблетки по 875/125 мг два раза в день на протяжении 7 дней. Одновременно кларитромицин 500 мг по 1 таблетке в день 7 дней и амброксол 2,0 мл в/в 10 дней.
Амоксициллин/клавулановая кислота (Аугментин™) является препаратом выбора при лечении больных ВП как на амбулаторном этапе, так и в стационаре. Результаты рандомизированных клинических исследований свидетельствуют о том, что комбинация амоксициллина/клавулановой кислоты эффективна примерно у 90 % пациентов с пневмококковой пневмонией, в том числе вызванной пенициллино- и цефалоспоринорезистентными штаммами микроорганизмов [6]. Аугментин™ отвечает основным требованиям, предъявляемым к антибиотикам для лечения ВП:
Амоксициллин/клавулановая кислота (Аугментин™) не только оказывает прямое бактерицидное действие на широкий спектр грамположительных, грамотрицательных, аэробных и анаэробных микроорганизмов, включая устойчивые штаммы, но и обладает постантибиотическим эффектом. Эффект потенцирования активности полиморфноядерных лейкоцитов и фагоцитоза выражен у амоксициллина/клавулановой кислоты достоверно сильнее, чем у амоксициллина. Оказалось, что клавулановая кислота потенцирует действие аминопенициллинов против грамотрицательной флоры; обладает собственной бактерицидной активностью против анаэробов; оказывает пост-β-лактамазоингибирующее действие (против H.influenzae и K.pneumoniae) в интервалах между приемами и существенно продлевает постантибиотическое действие амоксициллина [7–9].
Составные части препарата Аугментин™ (амоксициллин и клавулановая кислота) быстро проникают в мокроту и накапливаются в слизистой оболочке бронхов. Содержание обоих веществ значительно превышает дозы, необходимые для подавления роста большинства патогенных микроорганизмов, вызывающих инфекции дыхательных путей, включая продуцирующие β-лактамазу штаммы H.influenzae и M.сatarrhalis. По результатам Alexander Project, чувст-вительность St.pneumoniae, H.influenzae, M.catarrhalis сохраняется на высоком уровне — от 95,5 до 100 %. Резистентность основных возбудителей ВП к амоксициллину/клавулановой кислоте развивается медленнее, чем к макролидам, цефалоспоринам, фторхинолонам, и сохраняется на низком уровне, несмотря на 25-летний опыт применения. Кроме того, амоксициллин/клавуланат не уступает по уровню чувствительности и резистентности респираторным ФХ и цефалоспоринам III поколения. Именно поэтому амоксициллин/клавуланат рекомендован в качестве препарата первого выбора для лечения внебольничных инфекций дыхательных путей и на сегодняшний день остается основным средством борьбы с этими инфекциями наряду с современными макролидами и респираторными фторхинолонами.
Терапия, назначенная больной К., оказалась эффективной: состояние пациентки восстановилось, данные лабораторных исследований нормализовались. При рентгенологическом исследовании органов грудной полости инфильтрация легочной ткани рассосалась (рис. 4).
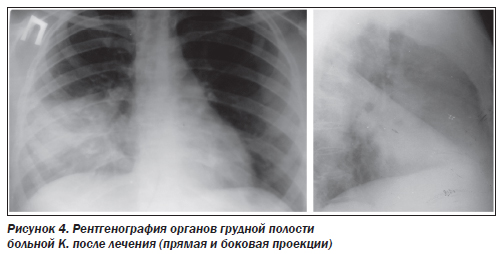
Таким образом, лечение больных ВП должно проводиться строго по протоколу. Препаратами первой линии являются защищенные аминопенициллины в сочетании с макролидами или без них. Препаратами второго ряда являются респираторные фторхинолоны. Использование в своей практике протоколов лечения инфекций дыхательных путей позволит избежать ошибок при назначении эмпирической терапии и сократить сроки выздоровления пациентов.
Печатается при поддержке компании ГлаксоСмитКляйн.
AGMT/10/UA/01.03.2010/3230
1. Страчунский Л.С., Кречикова О.И., Решедько Г.К. и др. Чувствительность к антибиотикам пневмококков, выделенных у здоровых детей из организованных коллективов // Клиническая микробиология и антимикробная химиотерапия. — 1999. — № 1. — 31-40.
2. Богданов М.Б., Черненькая Т.В. Алгоритмы и организация антибиотикотерапии. — М., 2004. — 219 с.
3. Богданов М.Б., Черненькая Т.В. Влияние антибиотического анамнеза на этиологию внебольничных пневмоний // Клиническая фармакология и терапия. — 1999. — 8 (5). — 20-22.
4. Страчунский Л.С., Козлов С.Н. Современная антимикробная химио-терапия. Руководство для врачей. — М.: Борес, 2002. — 432 с.
5. Страчунский Л.С. Бета-лактамазы расширенного спектра — быстро растущая и плохо осознаваемая угроза // Клиническая микробиология и антимикробная химиотерапия. — 2005. — Т. 7, № 1. — С. 92-96.
6. Roson B., Carratala J., Juban F. et al. Usefulness of betalactam therapy for community-acquired pneumonia in the era of drug-resistant Streptococcus pneumoniae: a randomized study of amoxicillin — clavulanate and ceftriaxone // Microb. Drug Resist. — 2001. — 7. — 85-96.
7. Geiss H.K. et al. Comparative activity of 3 betalactamase-inhibitors in combination with ampicillin and piperacillin against gram-negative bacteria // Clin. Microb. Infect. — 2000. — 6 (Suppl. 1). — 78.
8. Aguilar L. et al. // J. Antimicrob. Chemother. — 1999. — 44 (Suppl. A). — 70.
9. Murbach V. et al. Evidence for a true post-β-lactamase-inhibitor effect of clavulanic acid against Klebsiella pneumoniae and Haemophilus influenzae // Clin. Microbiol. Infect. — 2001. — 7. — 661-665.
10. Дворецкий Л.И. Ведение пожилого больного ХОБЛ. — М.: Литтерра, 2005. — 216 с.
11. Дворецкий Л.И. Антибактериальная терапия обострений хронического бронхита // Врач. — 2007 Май. — 19-21.
