Журнал «Здоровье ребенка» 2 (23) 2010
Вернуться к номеру
Итоги и перспективы изучения физиологических, патогенетических и фармакологических эффектов мелатонина
Авторы: Каладзе Н.Н., Соболева Е.М., Скоромная Н.Н., Крымский государственный медицинский университет им. С.И. Георгиевского, г. Симферополь
Рубрики: Педиатрия/Неонатология
Версия для печати
В последнее время уделялось большое внимание изучению мелатонина, гормона шишковидной железы, в связи с его участием во многих физиологических процессах. В этом обзоре рассматриваются и обсуждаются основные данные о роли мелатонина в физиологических и патологических процессах, а также возможность его терапевтического применения.
Из истории открытия и изучения мелатонина
История изучения мелатонина насчитывает более 50 лет, но интерес к нему не уменьшается, а возрастает в связи с тем, что с каждым годом появляются все новые данные о многогранности его влияния на человеческий организм. Получены убедительные данные о том, что мелатонин участвует практически во всех процессах жизнедеятельности, контролирует многие функции организма: сон, деятельность сердечно-сосудистой, эндокринной и иммунной систем. За рубежом организован и работает «Мелатониновый клуб», в США регулярно выходит Journal of Pineal Research , издаются Advances in Pineal Research , European Pineal Society News .
Мелатонин — одно из древнейших биохимических веществ, регулирующее биоритмы живых организмов. Он присутствует уже у одноклеточных организмов и растений. В организме позвоночных животных главный источник мелатонина — эпифиз, или шишковидная (пинеальная) железа.
Считают, что шишковидная железа была известна еще за 2000 лет до н.э. в Древней Индии. Древнеиндийские философы и врачи считали ее органом ясновидения и размышлений о перевоплощении души. В Древней Греции эпифизу отводили роль клапана, регулирующего опять-таки количество души и участвующего в контроле за психическим равновесием.
Эпифиз впервые описал александрийский врач Герофил за 300 лет до н.э., а свое название он получил от великого врача Древнего Рима Клавдия Галена (II век н.э.), которому форма железы напомнила сосновую шишку (пинию). Позднее другой выдающийся врач и анатом эпохи Возрождения Андреас Везалий представил первое топографически точное описание расположения эпифиза в человеческом мозге, локализовав его между буграми четверохолмия. В 1632 г . Рене Декартом был написан классический «Трактат о человеке». Декарт описал эпифиз как непарный орган с очень важными задачами. По его мнению, железа обеспечивала синтез информации от обеих половин тела через парные органы чувств (глаза, уши, ноздри), где она сливалась воедино. Декарт рассматривал эпифиз в качестве особого клапанного механизма, который регулирует движение животных «духов» из одного желудочка мозга в другой, определяя таким образом «количество души». Тем самым повторялось стремление древних локализовать душу не где-нибудь, а именно в эпифизе. Кроме того, Декарт связывал с нарушениями эпифизарной деятельности происхождение психических болезней, а также связывал функции эпифиза со зрением, что весьма интересно в свете современных знаний. На протяжении XVIII–XIX вв. эпифиз рассматривали лишь как рудиментарный придаток мозга. Только в самом конце XIX в. немецкий педиатр О. Хюбнер описал мальчика, отличавшегося преждевременным половым созреванием, у которого при посмертном вскрытии обнаружили опухоль эпифиза. Как теперь очевидно, она препятствовала выработке мелатонина. В истории эндокринологии эпифиз является первым органом, описанным и изученным как эндокринная железа.
В начале XX в. невролог О. Марбург предположил, что эпифиз — верхний придаток мозга-выделяет какое-то вещество, угнетающее функции гипоталамуса и, как следствие, развитие репродуктивной системы. Примерно тогда же установили, что эпифиз содержит субстанцию, вызывающую депигментацию (побледнение) кожи головастиков. Через 40 лет этот факт сыграл решающую роль в открытии мелатонина.
Мелатонин был открыт американским дерматологом Аароном Лернером более полувека назад. Сама история его открытия была довольно драматична. Лернер, ученый из Йельского университета, занимавшийся изучением природы витилиго, задался целью выявить факторы (химические субстанции), отвечающие за формирование пигментации кожи и разрушение пигментов. Ему принадлежит честь открытия меланоцитостимулирующего гормона. В ходе литературного поиска Лернер обнаружил статью, датированную 1917 годом, в которой сообщалось о том, что измельченные эпифизы коров, помещенные в банку с головастиками, в течение 30 минут вызывают обесцвечивание их кожи, которая просто становилась прозрачной, и можно было наблюдать за работой сердца и кишечника. Других публикаций на эту тему с тех пор не было.
В 1953 году Лернеру удалось выделить из бычьих эпифизов экстракт, осветляющий кожу лягушки. С этого времени вся работа была направлена на поиски ключевого компонента. Неутомимым исследователем и его коллегами была проделана поистине титаническая работа: они переработали 250 тысяч эпифизов, однако выделенной активной субстанции было катастрофически мало. Лернер понимал, что имеет дело со сверхактивным гормоном, ведь его способность обесцвечивать кожу превышала таковую способность адреналина в тысячи раз! Тем не менее было принято решение закрыть затянувшийся эксперимент. Однако за 4 недели, отведенные на завершение работ, все же удалось идентифицировать структуру основного действующего вещества. Им оказался N-ацетил-5-метокситриптамин, которому первооткрыватель дал более романтичное название «мелатонин» (от гр. melas — черный и tosos — труд). Свое открытие Лернер представил на суд общественности в одностраничной статье, опубликованной в 1958 году в Journal of American Chemical.
Биосинтез мелатонина
Одна из причин того, что о мелатонине очень долго практически ничего не было известно, состоит в том, что уровень биохимических исследований просто не позволял обнаруживать такое небольшое содержание вещества в кровотоке. Только в середине 70-х годов XX в. с развитием техники радиоиммунологического анализа появилась возможность обнаружения мелатонина в крови.
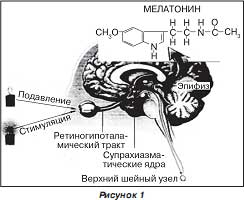
Мелатонин является основным гормоном, продуцируемым пинеалоцитами в эпифизе, расположенном в центре мозга, позади третьего желудочка.
Эта эндокринная железа состоит из клеток двух видов: пинеалоцитов (которые доминируют и продуцируют индоламины, главным образом мелатонин, и пептиды, такие как аргининвазотоцин) и нейроглиальных клеток. В эпифизе информация от нейронов, модифицированная условиями освещения, превращается в химические сигналы. Получая информацию о состоянии внешнего фотопериодизма, эпифиз трансформирует ее в эндокринный ответ, вырабатывая мелатонин.
У человека световой цикл воспринимается сетчаткой глаза. Затем нервный сигнал по ретиногипоталамическому тракту поступает в супрахиазматические ядра гипоталамуса, а далее в верхний шейный ганглий [29].Из верхнего шейного ганглия информация об освещенности поступает в эпифиз: она опосредуется норадреналином, который выделяется нервными окончаниями непосредственно в паренхиму (пинеалоциты) эпифиза, что в конечном итоге приводит к запуску синтеза мелатонина [13]. По своей химической структуре он является биогенным амином, относящимся к классу индолов. Начальным звеном является аминокислота триптофан. Затем происходят следующие превращения: 5-гидрокситриптофан ® 5-гидрокситриптамин (серотонин) ® N-ацетилсеротонин ® мелатонин (при участии ферментов N-ацетилтрансферазы и гидроксииндол-О-метилтрансферазы).
Биосинтез, секреция и деградация мелатонина
Основные этапы биосинтеза мелатонина и временная динамика его образования сегодня хорошо изучены. Эпифизом продуцируется около 80 % циркулирующего в крови мелатонина, который не накапливается в эпифизе, а сразу путем пассивной диффузии поступает из пинеалоцитов в кровоток. Его источником служит триптофан, который поступает в пинеалоциты из сосудистого русла и через 5-окситриптофан превращается в серотонин. Лимитирующим фактором в синтезе гормона служит активность фермента арилалкиламин-N-ацетилтрансферазы (NАТ), контролирующего образование предшественника — N-ацетилсеротонина, в дальнейшем при участии гидроксииндол-О-метилтрансферазы, превращающегося непосредственно в мелатонин.
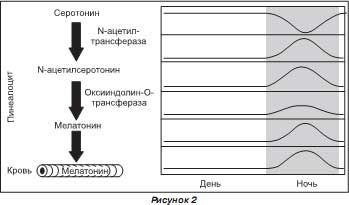
Принципиально важным является факт циркадианной (околосуточной) периодичности выработки в пинеалоцитах биологически активных соединений. Синтез мелатонина эффективно происходит только с наступлением темноты и снижается в светлую фазу суток. Достаточно короткого светового импульса силой 0,1–1 lux, чтобы подавить этот процесс. Дневной ритм продукции мелатонина зависит от активности NАТ в сетчатке, которая, в свою очередь, зависит от ионов кальция, дофамина и гамма-аминомасляной кислоты. Сетчатка является независимым и важным местом продукции мелатонина, по содержанию которого она стоит на втором месте после эпифиза. По-видимому, сетчатка играет определенную роль в поддержании уровня плазменного мелатонина в случае ослабления эпифизарной активности. Важно отметить, что в организме присутствует и экстрапинеальный мелатонин, т.е. синтезируемый вне эпифиза. После получения специфических антител к индолалкиламинам оказалось возможным найти экстрапинеальные источники синтеза мелатонина. Ими оказались энтерохромаффинные клетки желудочно-кишечного тракта (ЕС-клетки), основные клетки-депо серотонина (содержат до 95 % всего эндогенного серотонина) — предшественника мелатонина. Количество этих клеток в желудочно-кишечном тракте значительно больше, чем пинеалоцитов. Честь открытия этого явления принадлежит российским ученым Н.Т. Райхлину и И.М. Кветному.В 1974 году ими было установлено, что способностью синтезировать мелатонин обладают клетки червеобразного отростка кишечника — аппендикса. Далее выяснилось, что мелатонин синтезируется не только в них. Синтез этого гормона выявлен и в большом количестве нейроэндокринных клеток воздухоносных путей, легких, под печеночной капсулой, в корковом слое почек и вдоль границы между корковым и мозговым слоем надпочечников, в параганглиях, желчном пузыре, яичниках, эндометрии, предстательной железе, плаценте и внутреннем ухе. В последние годы обнаружили синтез мелатонина и в неэндокринных клетках: в тимусе, поджелудочной железе, мозжечке, сетчатке глаза, в клетках крови — тучных клетках, лимфоцитах, естественных киллерах, тромбоцитах, эозинофильных лейкоцитах, а также в некоторых эндотелиальных клетках. Биологическое действие экстрапинеального мелатонина реализуется непосредственно там, где он синтезируется. Вопрос о том, является ли этот путь синтеза гормона фотонезависимым, до сих пор окончательно не решен.
Функционально все клетки, продуцирующие мелатонин, относятся к так называемой диффузной нейроэндокринной системе, универсальной системе адаптации и поддержания гомеостаза организма. Выдвигается также предположение, что экстрапинеальный мелатонин может играть ключевую роль в качестве паракринной сигнальной молекулы взаимодействия клеток и локальной координации клеточных функций, однако полностью роль его до сих пор не ясна и исследования в этом направлении идут очень интенсивно.
Транспортной формой для мелатонина является сывороточный альбумин. Высокая плотность связывающих мелатонин участков была выявлена на молекуле гемоглобина, что может свидетельствовать о роли гемоглобина как переносчика мелатонина в кровотоке до органов-мишеней [37]. Высокая липофильность данного гормона обеспечивает его быстрое проникновение через мембраны клеток в другие биологические среды. После освобождения из связанного с альбумином состояния мелатонин взаимодействует со специфическими мембранными и ядерными рецепторами. Мелатонин имеет короткий период полураспада (около 30 минут) и быстро устраняется из кровотока. Он поступает в печень, где гидроксилируется и конъюгируется с серной (на 70–80 %) или глюкуроновой (5 %) кислотой и в виде сульфатов и глюкуронидов экскретируется с мочой. Основной метаболит мелатонина в моче — 6-гидроксимелатонин-сульфат, по концентрации которого можно судить о продукции мелатонина эпифизом [39].
Механизм действия мелатонина на клеточном уровне
Взаимодействие мелатонина с клетками происходит двумя путями.
Он опосредует свои эффекты в результате воздействия на собственные рецепторы, расположенные как на мембране клеток, так и на ядре. В последние годы были идентифицированы рецепторы к мелатонину у многих видов позвоночных, включая человека.
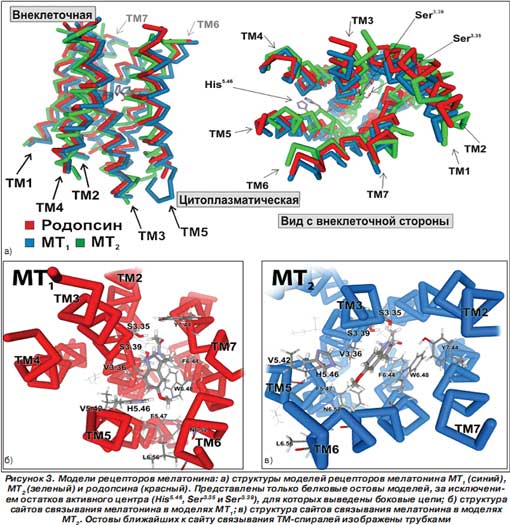
Группа мембранных рецепторов мелатонина, сопряженных с G-белками, включает в себя следующие подтипы — MT 1 , MT 2 , которые принадлежат к четко определенным фармакологическим и кинетическим группам: MT 1 (высокоаффинный наномолекулярный сайт) и MT 2 (низкоаффинный наномолекулярный сайт) [34, 35]. Кроме того, ранее были выделены также рецепторы MT 3 , но позже было установлено, что на самом деле они являются ферментом хинонредуктаза-2.
Учеными лаборатории терапевтической химии университета г. Лилль (Франция) совместно с российскими коллегами были созданы структуры моделей рецепторов MT 1 и MT 2 с наложенной структурой шаблона — зрительного родопсина, а также структуры сайтов связывания в комплексе с молекулой мелатонина.
Они обладают высоким сродством к своему лиганду и обнаружены в супрахиазматическом ядре, гипоталамусе, гиппокампе, коре больших полушарий и мозжечке [51]. Взаимодействие мелатонина с данным типом рецепторов приводит к активации различных сигнальных систем клетки и синтезу вторичных посредников — цАМФ, изменению концентрации ионов кальция. Связываясь с цитозольным кальмодулином, гормон может непосредственно влиять на кальциевые сигналы путем взаимодействия с ферментами, такими как аденилатциклаза и фосфодиэстераза, а также со структурными белками [52].
Ядерные рецепторы к мелатонину обнаружены в различных ядрах гипоталамуса, сетчатке глаза и других тканях. Они относятся к новому подклассу семейства так называемых орфановых ядерных ретиноидных рецепторов ROR/RZR [27]. Данное семейство включает продукты экспрессии генов альфа-ROR, бета-ROR и гамма-ROR. Члены подсемейства связываются с ДНК в форме мономеров и «узнают» гормоночувствительные элементы (RORE). Результатом такого взаимодействия является изменение уровня экспрессии генов специфических факторов транскрипции и эффекторных белков, что является общим для липофильных гормонов. Важно отметить, что ядерные рецепторы обнаружены в трех органах млекопитающих, определяющих суточные ритмы организма: в супрахиазматическом ядре, сетчатке глаза и эпифизе.
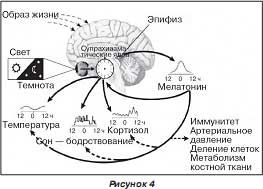
Авторадиография и радиоиммунный анализ показали присутствие мелатониновых рецепторов в разных структурах мозга человека, кишечнике [42], яичниках [62] и кровеносных сосудах [34]. Рецепторы в супрахиазматических ядрах гипоталамуса, очевидно, регулируют циркадианный ритм. Рецепторы, которые находятся в эпителиальных тканях (например, в эндотелии артерий), регулируют кардиоваскулярную функцию [34]. Известно, что мелатонин оказывает релаксирующее влияние на гладкую мускулатуру сосудов, улучшая тем самым микроциркуляцию.
Таким образом, биологическое действие мелатонина как гормона реализуется благодаря наличию специфических рецепторов различной локализации и различных систем передачи сигнала в живой клетке.
Биологические ритмы секреции
Ритм продукции мелатонина эпифизом носит циркадианный характер.
В аспекте циркадианного ритма организма данный гормон поддерживает цикл «сон — бодрствование» (сам по себе он обладает снотворным действием), суточные изменения локомоторной активности и температуры тела.
Повышение концентрации мелатонина в крови с наступлением темноты снижает у человека температуру тела, уменьшает эмоциональную напряженность, индуцирует сон, а также незначительно угнетает функцию половых желез, что выражается в задержке пролиферации опухолевых клеток молочной и предстательной желез. Мелатонин участвует в гормональном обеспечении околосуточного и сезонного периодизма поведенческой активности.
Синтез и выделение мелатонина стимулируются темнотой и ингибируются светом [4]. В течение светового периода фоторецепторные клетки сетчатки глаза гиперполяризованы, нервный сигнал не поступает в супрахиазматические ядра, и это тормозит выделение адреналина [29]. В это время система «ретиногипоталамус — эпифиз» находится в покое, секретируется мало мелатонина. С наступлением темноты гиперполяризация фоторецепторов исчезает, нервный сигнал освобождает норадреналин, активируя, таким образом, систему «ретиногипоталамус — эпифиз»; количество a 1- и b 1-адренорецепторов в эпифизе увеличивается. Растет активность ферментов, которые регулируют синтез мелатонина, инициируя его выделение. У диурнальных (дневных) животных (в том числе у человека) секреция мелатонина эпифизом совпадает с привычными часами сна. Концентрация его в крови нарастает с наступлением темноты и достигает своего максимума за 1–2 ч до пробуждения. В это время сон человека наиболее глубокий, а температура тела достигает своего минимума.
Кроме суточного существует и сезонный ритм мелатонина. Поздней осенью и зимой в связи с уменьшением освещенности уровень гормона в организме повышается. Весной и летом, наоборот, концентрация мелатонина в организме снижается [48]. Однако при этом сохраняется суточная ритмика образования мелатонина. Эти изменения обусловлены флуктуацией ферментативной активности ключевых ферментов синтеза мелатонина — N-ацетилтрансферазы и гидроксииндол-О-метилтрансферазы, что превращает эпифиз в своеобразные биологические часы, имеющие прямое отношение к регуляции циркадных и циркадианных ритмов в организме. Концентрация мелатонина в плазме существенно изменяется в зависимости от возраста. Циркадианный ритм синтеза мелатонина появляется сразу после рождения плода и у доношенных младенцев устанавливается к 9–12 нед. жизни, на 2–3 нед. позже — у недоношенных детей.
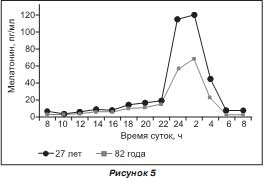
Наиболее высокая пиковая ночная концентрация мелатонина (около 325 пг/мл или 1400 пмоль/л) наблюдается в возрасте 1–3 лет, после чего она постепенно снижается [45]. У молодых людей среднее количество мелатонина днем и пик в середине ночи составляет 10 и 60 пг/мл (40 и 260 пмоль/л) соответственно. Максимальная продукция данного гормона приходится на возраст от 10 до 40 лет. После этого происходит снижение продукции мелатонина, уменьшается амплитуда суточного ритма его секреции эпифизом.
Показано, что мелатониновый паттерн у каждого человека на удивление стабилен от ночи к ночи, в то время как паттерны разных людей одного пола и возраста в деталях настолько различны, что есть основание говорить об индивидуальном паттерне, характеризующем данную личность.
Ранее считалось, что снижение содержания мелатонина при старении вызвано кальцификацией эпифиза. Однако исследования с использованием электронной микроскопии показали развитие в эпифизе при старении морфофункциональных изменений, свидетельствующих о снижении его активности [38] вследствие уменьшения адренергической иннервации и количества b 1-адренергических рецепторов на поверхности пинеалоцитов [41].
Сегодня ученые могут сказать, что изменения в образовании мелатонина в течение жизни не являются простым совпадением со стадиями развития организма. Они органически связаны с ними и оказывают непосредственное влияние на физиологические процессы. К сожалению, информация о всех важнейших открытиях фрагментарно публикуется лишь в некоторых научных журналах.
Основные физиологические функции мелатонина
В последние годы получены новые данные о механизмах, обеспечивающих комплексное взаимодействие нервной, иммунной и эндокринной систем. Предполагается, что интегратором этого взаимодействия является эпифиз, а его основной гормон — мелатонин участвует в регуляции деятельности центральной и вегетативной нервной систем, эндокринных органов и иммунной системы.
Проведенные исследования показали, что мелатонин обладает чрезвычайно широким спектром физиологических функций [3]. Основными физиологическими функциями мелатонина являются:
— биоритмологическая функция;
— терморегуляция и индукция сна;
— антиоксидантный эффект;
— иммуномодулирующее действие;
— антистрессорное действие;
— регуляция полового развития.
Биоритмологическая функция
Способность организма адекватно реагировать на различные стимулы путем перестройки биоритмов обеспечивает стабильность и здоровье человеческого организма. Поэтому способность мелатонина осуществлять коррекцию эндогенных ритмов относительно экзогенных ритмов окружающей среды является наиболее важной физиологической функцией этого гормона [54]. Эпифиз выступает в качестве своеобразных биологических часов. Биоритмологическая функция обеспечивается непосредственным воздействием мелатонина и модулирующим влиянием на секрецию других гормонов и биологически активных веществ, концентрация которых изменяется в зависимости от времени суток. Мелатонин опосредует по существу все наиболее важные функции эпифиза, связанные с контролем деятельности периферических эндокринных желез и центральной нервной системы. В норме функциональная активность эпифиза находится в противофазе с деятельностью гипофиза. Так, если гипофиз за счет тропных гормонов активирует эндокринную функцию, то шишковидное тело, наоборот, ее тормозит. Такое чередование деятельности этих двух нейроэндокринных образований мозга обеспечивает циркадианное ритмичное функционирование не только желез внутренней секреции, но и организма в целом [17]. Существуют отдельные наблюдения, касающиеся взаимодействия эпифиза и гипоталамо-гипофизарно-надпочечниковой оси. Показано, что гиперсекреция кортизола и сниженная реакция его при подавлении дексаметазоном сочетается со сниженной секрецией мелатонина. Непосредственно воздействуя на клетки и модулируя секрецию других гормонов и биологически активных веществ, концентрация которых изменяется в зависимости от времени суток, мелатонин выполняет биоритмологическую функцию. Показано, что мелатонин ингибирует выброс адренокортикотропного гормона, уменьшая таким образом концентрацию кортизола [15, 33], снижает продукцию норадреналина [32]. Ингибирование мелатонином тиреоидной паренхимы наблюдается на всех этапах ее функциональной активности. В сезонных перестройках организма основополагающую роль играют связанные с фотопериодизмом изменения продукции мелатонина [54].
Терморегуляция и индукция сна
Мелатонин играет основную роль в регуляции циркадианных ритмов и сна [29]. Он поддерживает цикл «сон — бодрствование», суточные изменения локомоторной активности и температуры тела. Так, показано, что циркадианные ритмы температуры у человека [32] характеризуются максимальными показателями днем и минимальными ночью и ассоциированы с особенностями биоэлектрической активности мозга. Повышение секреции мелатонина в темное время суток обусловливает более 40 % амплитуды суточного ритма температуры тела. В связи с этим предложен косвенный метод оценки выработки мелатонина по измерению суточной динамики температуры тела: размах суточной температуры менее 0,5 °С может свидетельствовать о снижении продукции мелатонина.
Мелатонин называют гормоном ночи, так как пик его синтеза приходится на темное время суток [3]. У человека циркадианный ритм секреции мелатонина эпифизом тесно синхронизирован с типичными часами сна. Мелатонин может модифицировать уровень моноаминовых нейротрансмиттеров в мозге, инициируя каскад реакций, которые при достижении кульминации активируют механизмы сна [13]. Функциональная активность шишковидного тела, как правило, увеличивается с нарастанием темноты и достигает максимума к полуночи (пик продукции мелатонина в молодом возрасте отмечается между 2 и 3 часами ночи). К утру функциональная активность этого органа резко падает, достигая минимума к полудню [1].
Антиоксидантный эффект
Механизм антиоксидантного действия мелатонина связан прежде всего с его способностью связывать образующиеся при перикисном окислении липидов наиболее токсичные гидроксильные радикалы, а также пероксинитрит, оксид азота, синглетный кислород и пероксильный радикал [55]. Являясь активным донором электронов и эффективным перехватчиком активных форм кислорода, особенно гидроксильного радикала ОН, он также уничтожает радикал оксида азота (NО). Наряду с прямым антиоксидантным эффектом гормон действует как вторичный антиоксидант. Он стимулирует активность глутатион-пероксидазы, которая переводит перекись водорода в воду, активизирует супероксиддисмутазу, глюкозо-6-фосфатдегидрогеназу, а также угнетает активность прооксидантного фермента NO-синтазы. Кроме этого, гормон обладает способностью непосредственно связывать ионы металлов с переменной валентностью (Fe 2+ , Cu 2+ , Mn 2+ ) которые проявляют в организме прооксидантное действие. Антиоксидантные эффекты мелатонина не связаны с его воздействием на рецепторы клеточных мембран, а обусловлены проникновением гормона в клетки и его взаимодействием практически со всеми субклеточными структурами, включая ядро. Поэтому мелатонин может воздействовать на свободнорадикальные процессы в любой клетке человеческого организма, а не только в клетках, которые имеют рецепторы к мелатонину. Антиоксидантный эффект мелатонина обеспечивает защиту ДНК, липидов и белков от свободнорадикального повреждения [56]. Таким образом, мелатонин может быть главной молекулой в системе защиты организма от окислительного стресса благодаря нейтрализации перекиси водорода и уничтожению гидроксильных радикалов.
Иммуномодулирующее действие
Мелатонин принимает участие в регуляции функции иммунной системы. Иммунологи обнаружили, что увеличение активности Т- и В-иммунных клеток в течение суток происходит параллельно с возрастанием концентрации мелатонина. Было выяснено, что мелатонин участвует в регуляции функции тимуса и щитовидной железы, повышает активность Т-клеток и фагоцитов. Об этом свидетельствует присутствие рецепторов к мелатонину на иммунокомпетентных клетках вилочковой железы и селезенки, периферических иммунокомпетентных клетках (лимфоциты, нейтрофилы), активирующий эффект мелатонина в отношении выработки этими клетками цитокинов [44]. В отношении иммунной функции установлено, что у взрослых и старых мышей под действием пептидного препарата эпифиза стимулируется Т- и В-клеточный иммунитет, в сыворотке растут титр тимического сывороточного фактора, титр тимозиновых компонентов, а также колониестимулирующая активность спленоцитов у пинеалэктомированных крыс.
Одной из причин ухудшения функционирования иммунной системы считается ослабление деятельности тимуса. Экзогенное введение мелатонина восстанавливает массу тимуса, улучшает активность клеток, что усиливает дифференцировку Т-лимфоцитов и восстанавливает чувствительность кожи к аллергенам, что может означать восстановление памяти Т-клеток (увеличивается способность к идентификации антигенов). Но функцией иммунной системы является не только непосредственная защита организма от вирусов и бактерий. Не менее важна ее способность отличить «свои» клетки от «чужих». Нарушение такой способности приводит к аутоиммунным заболеваниям.
Иммуномодулирующая активность гормона наиболее полно продемонстрирована в работах I. Maestroni [50] и P. Lissoni [46]. Данный гормон стимулирует иммунный ответ как по В-, так и по Т-системе, но это зависит от исходного состояния иммунокомпетентных органов. Между количеством лимфоцитов и уровнем мелатонина определяется обратная взаимосвязь, то есть прослеживается определенная адаптивная направленность в воздействии мелатонина на иммунитет [16]. Путем увеличения продукции цитокинов, которые вырабатываются Т-хелперами, мелатонин усиливает иммунный ответ. В эксперименте in vitro с помощью анти-ИЛ-4-моноклональных антител показана нейтрализация колониестимулирующей активности и вызванной мелатонином защиты гемопоэза. Показано снижение уровня ИЛ-6 в лимфоцитах-хелперах Т 1 , которые определяют клеточный ответ. Мелатонин повышает уровень ИЛ-2 и g -интерферона в лимфоцитах-хелперах Т 1 , [36] и ИЛ-4 в лимфоцитах-хелперах Т 2 [49, 53], а у моноцитов катализирует выделение интерлейкина-1 (ИЛ-1) и фактора некроза опухоли альфа (ФНО- a ). Только в одной работе продемонстрировано снижение под влиянием гормона природной киллерной активности лимфоцитов [43].
Допускается его действие через секрецию лимфокинов, опиоидов или же через другие эндокринные изменения, в частности возможно прямое действие мелатонина на лимфоидную ткань [17]. В пользу тесной взаимосвязи мелатонина и иммунной системы говорит факт стимуляции g -интерфероном продукции мелатонина эпифизом, свидетельствующий о существовании регуляции секреции мелатонина со стороны иммунной системы [61]. В исследовании Н.А. Деденкова, Н.Т. Райхлена и соавт. была показана возможность синтеза пептидных гормонов и биогенных аминов, таких как серотонин, мелатонин и b -эндорфин в гранулах естественных киллеров, что может быть связано с механизмами цитотоксического действия данных клеток [5].
Еще одним свидетельством взаимосвязи иммунной системы и мелатонина в организме человека являются циркадианные изменения количества нейтрофилов, Т- и В-лимфоцитов в кровотоке с максимумом в темное время суток. Таким образом, мелатонин принимает участие в регуляции как клеточного, так и гуморального звена иммунитета.
Антистрессорный эффект
Мелатонин играет существенную роль в нормализации послестрессового состояния организма, которая обусловлена его влиянием на нейромедиаторные системы, воздействием на синхронизацию циркадианной ритмики. Воздействуя одновременно на нейроэндокринную и иммунную системы, мелатонин оптимизирует гомеостаз и осуществляет защиту от стресса [50].
В механизме противострессорной активности мелатонина существенную роль играет уменьшение активности тонуса симпатической нервной системы и активности гипофизарно-надпочечниковой системы, снижение уровня кортикостероидов, влияющих на кардиоваскулярную систему. В процессе реализации стресса на иммунологические реакции участвуют опиоидные пептиды, которые модулируют иммунологические функции, влияя на активность Т-клеток — натуральных киллеров, и макрофагов. Наибольшей активностью и продолжительностью действия отличается b -эндорфин, который является не только трансмиттером, но и гормоном. На основании экспериментальных исследований установлена важнейшая роль b -эндорфина в развитии стресс-синдрома, что проявляется увеличением концентрации данного пептида в крови при различных видах стресса. Наряду со снижением уровня кортизола мелатонин стимулирует выделение эндорфинов [59].
Новая страница в изучении развития нейроэндокринных и биохимических механизмов (в эксперименте на животных с синдромом перинатального стресса) открыта исследованиями С.С. Ткачук и отражена в докторской диссертации «Нейроэндокринные и биохимические механизмы нарушений стресс-реализующей и стресс-лимитирующей систем мозга крыс с синдромом перинатального стресса». При использовании доз мелатонина, близких к физиологическим, в условиях эмоционального стресса отмечали четкое стимулирующее влияние гормона на уровень пролактина в плазме крови, что дало возможность считать этот механизм одним из коррелятов участия мелатонина в стресс-реакции. У животных, подвергшихся стрессу пренатально, мелатонин не влиял на стресс-индуцированный уровень суммарных глюкокортикоидов и пролактина, что свидетельствует об утрате способности мелатонина моделировать активированные стрессом эндокринные механизмы. Высказано предположение о возможных нарушениях функции эпифиза или же десенситизации мелатониновых рецепторов гипоталамуса и гипофиза с потерей антистрессового влияния [24].
Регуляция полового развития
Существует достаточно доказательств влияния эпифиза на половое развитие и репродукцию. Он проявляет четко выраженное антигонадотропное действие [29, 13].
Снижение содержания мелатонина в крови стимулирует выделение гипофизом половых гормонов — лютеинезирующего и фолликулостимулирующего (пролактина и окситоцина). Начало полового созревания у людей связано с уменьшением секреции мелатонина. Снижение уровня мелатонина ускоряет половое созревание. У подростков с более высоким содержанием мелатонина в крови чаще наблюдается задержка полового развития. В работе Е.И. Плеховой и соавт. изложены результаты исследования уровня мелатонина у здоровых мальчиков-подростков в процессе полового созревания. Были сформированы 4 группы (количество человек в каждой группе от 6 до 10), в которые вошли пациенты различных возрастных периодов: 10–12 лет, 13, 14 и 15 лет, а также группа здоровых мужчин 32–35 лет. Представленные в работе данные свидетельствуют о достоверно более низких значениях эпифизарного гормона у мальчиков, находящихся на ранних этапах полового развития. В процессе полового созревания на фоне общего увеличения уровня мелатонина в моче происходит уменьшение его экскреции в ночное время. Данные наблюдения позволяют предположить, что отсутствие выраженного подъема мелатонина в ночное время в период полового созревания создает условия для формирования принципиально иных взаимоотношений эпифиза и гипоталамо-гипофизарно-гонадного комплекса, сопровождающихся усилением гормонопродуцирующей активности гонад [19]. Однако у девочек такие изменения отмечены не были [22]. Кривая ночного содержания мелатонина в сыворотке крови в разные периоды жизни людей имеет обратный вид по отношению к кривой гонадотропина — лютеинизирующего гормона. Утренние концентрации мелатонина с возрастом не изменяются и являются низкими во всех возрастных группах.
Патогенетическое значение мелатонина
Нарушение ритма и количественной продукции мелатонина является пусковым моментом, приводящим на начальных этапах к возникновению десинхроноза, за которым следует органическая патология. Любые изменения продукции мелатонина, выходящие за рамки нормальных физиологических колебаний, ведут к рассогласованию как собственно биологических ритмов организма между собой (внутренний десинхроноз), так и ритмов организма с ритмами окружающей среды (внешний десинхроноз) [57]. С биоритмологических позиций сезонные обострения хронических болезней внутренних органов представляют собой клиническую реализацию дезадаптации организма в условиях, требующих повышенной активности адаптивной системы организма при изменении условий окружающей среды [15]. Следовательно, даже сам факт нарушения ритма продукции мелатонина может стать причиной различных заболеваний.
Показана роль эпифиза в развитии депрессии [60]. Выявлены нарушение циркадианных ритмов мелатонина при нарушениях сна, снижение содержания мелатонина в крови и отсутствие суточного ритма его секреции при псориазе, при гипертонической болезни [21]. Отмечена патогенетическая роль мелатонина при рассеянном склерозе (РС). Первые проявления заболевания часто приходятся на период окончания полового созревания, сопровождающийся критическим снижением секреции мелатонина, нарушением его нейроиммуномодулирующего действия. «Мелатониновая» гипотеза может объяснять эпидемиологический феномен РС: низкую его частоту в «черных» африканской и американской популяциях [58].
Установлено, что раннее половое созревание или его задержка могут быть ассоциированы с измененным плазменным уровнем мелатонина. В большинстве случаев функциональная гипоталамическая аменорея связана с гиперпродукцией мелатонина, поэтому в лечении данной патологии эффективно назначение антагониста мелатонина — налтрексона. Установлено повышение продукции мелатонина на ранних стадиях колоректального рака [11].
Отдельными авторами установлено, что нарушения синтеза мелатонина или обратного захвата серотонина могут быть ответственными за возникновение ведущих клинических и внеорганных проявлений функциональных заболеваний желудочно-кишечного тракта (ФЗ ЖКТ) [1, 12, 25].
Более того, в ряде исследований показано, что лечение препаратами мелатонина уменьшает выраженность абдоминальной боли функционального генеза и способствует купированию симптомов ФЗ ЖКТ [14, 18]. Внимание ученых привлекли возможные цитокинопосредованные механизмы развития синдрома раздраженного кишечника (СРК), так как именно медиаторы межклеточного взаимодействия осуществляют связь между иммунной и серотонин-мелатониновой системами [10]. В исследованиях отдельных авторов у больных СРК, преимущественно с постинфекционной формой заболевания, выявлена увеличенная продукция провоспалительных цитокинов (ФНО- a , ИЛ-1, ИЛ-6), а при исследовании биоптатов слизистой оболочки толстой кишки у таких пациентов обнаружена их повышенная продукция. Установлено снижение секреции отдельных антивоспалительных цитокинов (ИЛ-10, ИЛ-12) у больных СРК по сравнению со здоровыми лицами [47].
В исследовании С.В. Коляденко, М.А. Станиславчук установлено, что у больных с фибромиалгией в плазме крови уровень мелатонина значительно снижается в 4.00, тогда как в 8.00 отмечали только тенденцию к снижению мелатонина. У больных с фибромиалгией зарегистрировано повышение на 10 % содержания в крови провоспалительного цитокина ИЛ-8 и снижение на 8 % противовоспалительного цитокина ИЛ-10, при этом коэффициент ИЛ-8/ИЛ-10 повышается на 21 %. Установлено, что низкий уровень мелатонина в ночное время ассоциируется с такими клиническими проявлениями фибромиалгии, как нарушения сна, а уровень ИЛ-8 имеет значительную положительную корреляционную связь с выраженностью болевого синдрома.
Широкий спектр биологической активности мелатонина не ограничивается изолированным влиянием на нервную и эндокринную системы, воздействие его носит интегративный и иммуномодулирующий характер.
С точки зрения хронобиологии бронхиальная астма (БА) — это синдром обратимой бронхиальной обструкции, возникающей у большинства больных в ночные и утренние часы, что является отражением суточных ритмов с ночным максимумом (концентрация мелатонина и гистамина в сыворотке, чувствительность бронхов к гистамину и ацетилхолину, повышение тонуса парасимпатической нервной системы) или минимумом (концентрация кортизола и катехоламинов в сыворотке крови, температура тела, показатели вентиляции легких). При астме, обструктивных процессах в легких отмечаются значительные смещения ритмов изменения легочных показателей, что может быть связано с нарушением обмена мелатонина. Е.В. Евсюковой, изучавшей у 17 взрослых пациентов с БА и у 6 здоровых людей влияние мелатонина на функции тромбоцитов, было обнаружено, что мелатонин непосредственно воздействует на функциональную активность тромбоцитов как у здоровых людей, так и у больных бронхиальной астмой, включая реакции агрегации, синтез метаболитов арахидоновой кислоты и транспорт серотонина. Тромбоциты играют существенную роль в патогенезе аллергических реакций и заболеваний, в частности БА. Наряду с тучными клетками, базофилами и эозинофилами они входят в систему «быстрого реагирования», осуществляющую местную регуляцию проходимости бронхов и гемодинамики легких. В эксперименте показано, что мелатонин вызывает бронхоконстрикторный эффект, а также вазодилатацию легочных артерий и вен. Возможно, подобная ситуация имеет место у больных БА в связи с высоким содержанием мелатонина не только ночью, но и днем [6].
В нашем исследовании, включавшем 119 детей, страдающих БА (различной степени тяжести, как в периоде обострения, так и ремиссии), были получены результаты, свидетельствующие о нарушении количественной продукции и циркадианного ритма секреции мелатонина. У данной категории пациентов была обнаружена инверсия суточного ритма мелатонина (с высокими дневными и низкими ночными значениями уровня данного гормона). Выявлена обратная зависимость между дневным уровнем мелатонина и степенью тяжести заболевания (от дневной (r = –0,547, р < 0,05) и ночной концентрации мелатонина (r = –0,705, р < 0,001)). Показано антистрессорное модулирующее действие мелатонина, направленное на ограничение активности гипофизарно-надпочечниковой оси (за счет изменения дневного содержания данного гормона) и активности симпатического отдела ВНС, а также возможность его участия в иммунорегуляции.
При обострении БА изменения гормонального статуса (повышение содержания АКТГ и дневного уровня мелатонина) отражались на состоянии гуморального звена иммунитета (увеличение IgЕ и снижение IgА), а в фазе ремиссии снижение активности парасимпатического отдела ВНС и низкий дневной уровень мелатонина были сопряжены с уменьшением относительного количества СД8, ИРИ и уровня IgЕ (что подтверждает участие эпифиза, ЦНС, ВНС и гормонального статуса в формировании иммунных нарушений при БА) [8, 9, 23].
Фармакологические эффекты мелатонина
Наиболее изучен снотворный эффект мелатонина, который принципиально отличается от механизма действия традиционных снотворных препаратов. Он вызывает сон, воздействуя на терморегуляторные процессы [30]. Уменьшая температуру тела, он увеличивает потребность в сне и снижает мотивацию к бодрствованию. Наиболее выраженный снотворный эффект отмечается у тех больных, у которых бессонница обусловлена недостаточным снижением температуры тела вследствие пониженного уровня мелатонина в плазме [63]. Его преимуществом является то, что он восстанавливает и сохраняет естественную структуру сна.
Мелатонин может использоваться для коррекции биологических ритмов, когда циклическая смена света и темноты ускоряется или замедляется и циркадианная система организма медленно адаптируется к новому положению фаз. В процессе адаптации эндогенные ритмы не совпадают по фазе с внешней средой и друг с другом. Возникающий десинхроноз нарушает функциональное состояние организма и может способствовать формированию патологических состояний и заболеваний. Мелатонин способствует перестройке биологических ритмов организма в соответствии с новым режимом дня [40].
Хотя влияние мелатонина на иммунную систему еще до конца не изучено, однако уже сегодня иммунологи предполагают, что его можно использовать для ускорения заживления ран, для поддержания сопротивляемости организма простудным и инфекционным заболеваниям. Возможно, в недалеком будущем страдающие онкологическими заболеваниями получат надежду облегчить свое состояние и смягчить негативные последствия курса химиотерапии и облучения, поддержать свой иммунный статус.
Предпосылками использования мелатонина в онкологии явились экспериментальные исследования, которые продемонстрировали способность этого гормона в физиологических дозах тормозить рост некоторых линий опухолевых клеток [28]. Данный эффект обусловлен онкостатическим и иммуномодулирующим действием. Установлено, что введение низкой дозы ИЛ-2 и мелатонина [26], потенцирующего положительный эффект и нейтрализующего негативное влияние ИЛ-2, является второй линией лечения метастатических колоректальных карцином. Показана эффективность нейроиммунотерапии в виде 2 циклов мелатонина и ИЛ-2 в качестве первой линии терапии у больных с метастатическим раком легкого [47]. Мелатонин оказывает влияние на количество и активность рецепторов к эстрогенам и таким образом может останавливать рост клеток рака молочной железы [28].
Помимо онкологических заболеваний еще одним из перспективных внедрений мелатонина в практику являются заболевания сердечно-сосудистой системы. В последние годы эти болезни значительно «помолодели». Какова бы ни была причина их развития (неправильное питание, образ жизни и т.д.), мелатонин можно использовать для предупреждения заболеваний сердечно-сосудистой системы, а может быть, и при их лечении. В эксперименте мелатонин препятствовал повышению уровня холестерина и образованию атеросклеротических бляшек на внутренней стенке артерий. Мелатонин уменьшал уровень общего холестерина и концентрацию в крови атерогенных липопротеинов низкой плотности [56]. Регулярный прием мелатонина способствует снижению артериального давления у больных артериальной гипертензией [7].
В Институте ревматологии РАМН (г. Москва) проведено 3-недельное рандомизированное исследование влияния мелатонина в дозе 3 мг/сут (на ночь) у больных ревматоидным артритом (РА), имевших нарушения сна. Было выявлено достоверное снижение частоты таких симптомов инсомии, как чувство неудовлетворенности ночным сном, сохранение усталости после сна и неприятных ощущений во время сна. Общий результат лечения мелатонином оценен пациентом и врачом как улучшение или значительное улучшение в 47,4–63, 2 % случаев. На фоне лечения мелатонином отмечено также достоверное снижение длительности утренней скованности, числа припухших и болезненных суставов, интенсивности боли. Показано влияние мелатонина на эндокринный статус больных РА: снижение уровня кортизола в сыворотке крови и достоверное повышение уровня 6-СОМТ в моче [20].
В нашем исследовании у детей, страдающих бронхиальной астмой, было показано положительное влияние метода биорезонансной вибростимуляции на нормализацию циркадианного ритма секреции и суточную продукцию мелатонина [23].
Таким образом, результаты экспериментальных и клинических исследований свидетельствуют о том, что мелатонин является адаптационным гормоном, который участвует в координации и синхронизации нейроиммунофизиологических процессов. Действие мелатонина проявляется в обеспечении нормальной биоэлектрической активности мозга, циркадианных ритмов, в регуляции активности гипоталамо-гипофизарной области и иммунной системы и антистрессорной защите организма. Нарушение продукции и рецепции мелатонина может быть одним из звеньев патогенеза большого круга заболеваний, сопровождающихся нейроиммунологическими нарушениями.
Данные литературы свидетельствуют, что мелатонин может использоваться в различных областях профилактической и клинической медицины. Однако при его назначении необходимо учитывать эндогенные ритмы функционального состояния эпифиза.
Список литературы находится в редакции
