Введение
По статистическим данным, госпитальные инфекции возникают у 2–30 % госпитализированных больных [9]. Среди госпитальных инфекций на первом месте находится хирургическая раневая инфекция, составляющая от 3 до 15 %. Это значительно увеличивает сроки и стоимость лечения, а также выступает основной причиной отсроченной послеоперационной летальности [8]. Поэтому необходимость антибактериальной профилактики является общепризнанным фактом [1–3, 5, 8]. При этом активно обсуждается вопрос о построении рациональных профилактических схем. Несмотря на большое количество публикаций о том, что золотым стандартом антибиотикопрофилактики являются цефалоспорины ІІ поколения [1–3, 5, 6, 8, 10], некоторые авторы продолжают рекомендовать схемы с использованием цефалоспоринов ІІІ поколения с продолжительностью их введения в режимах антибиотикотерапии в течение 5–7 дней [4]. К сожалению, цефалоспорины ІІІ поколения до последнего времени широко использовались с профилактической целью и в нашей клинике.
Подсчитано, что расходы на антибиотикотерапию составляют до 50–60 % всех расходов на лечение. Вместе с тем следствием неадекватной антибиотикопрофилактики / терапии являются развитие устойчивости к антибиотикам возбудителей внутрибольничных инфекций и необоснованное, но значительное удорожание лечения [5].
Поэтому ключевыми в выборе препарата для антибиотикопрофилактики являются:
1. Свойства антибактериального препарата, который должен отвечать следующим критериям [8]:
— иметь период полувыведения, достаточный для поддержания в тканях и крови бактерицидной концентрации активного вещества на протяжении всей операции;
— быть эффективным по отношению к вероятным доминирующим возбудителям раневой инфекции (не всем!);
— не влиять на фармакокинетику анестезиологических препаратов;
— не ускорять развитие резистентных патогенов;
— хорошо проникать в ткани в зоне оперативного вмешательства;
— иметь минимальное токсическое и аллергическое побочное действие;
— хорошо переноситься пациентом;
— существенно не влиять на нормальную микрофлору человека.
2. Оптимальное соотношение его эффективности и стоимости [5, 8, 10].
Исходя из этого, целью нашего исследования было определение схемы антибиотикопрофилактики при условно-чистых ургентных операциях на органах брюшной полости, оптимальной с позиции сравнительной клинической эффективности и соотношения эффективность / стоимость.
Материалы и методы
В 2006 году в ОИТ № 2 Клинического объединения скорой медицинской помощи г. днепропетровска было пролечено 1330 послеоперационных больных с острой хирургической и гинекологической патологией.
В исследуемую группу вошли 242 больных с острой хирургической патологией. В зависимости от степени контаминации ран по классификации Американской ассоциации хирургов [6, 8] их можно было отнести к группе условно-чистых операций: лапаротомные и лапароскопические холецистэктомии; ущемленные грыжи, без вскрытия просвета кишечника; аппендэктомии по поводу катаральных и флегмонозных форм (без дренирования брюшной полости).
Возраст больных колебался от 24 до 69 лет, большинство (59 %) составляли мужчины.
Из исследования было исключено 15 больных. Критериями исключения служили интраоперационное выявление гнойно-воспалительных очагов, серьезное инфицирование раны в ходе операции, наличие холедохолитиаза и/или холангита при операциях на желчных путях, значительное расширение объема и травматичности операции, диагностика внебольничной пневмонии в послеоперационном периоде, но до 48 часов пребывания в стационаре.
В зависимости от схемы проводимой антибиотикопрофилактики все больные были разделены на 3 группы.
Первая группа (100 человек) получала цефуроксим по схеме 1,5 г во время вводного наркоза с последующим двукратным введением по 0,75 г с интервалом в 8 часов. Методом случайного выбора первая группа была разделена на две равноценные подгруппы:
— 1-а подгруппа получала цефуроксим в виде оригинального препарата — 50 человек (лапароскопические холецистэктомии — 23, лапаротомные холецистэктомии — 8, грыжесечения — 10, аппендэктомии — 9);
— 1-б подгруппа получала цефуроксим в виде отечественного препарата Кимацеф (Артериум) — 50 человек (лапароскопические холецистэктомии — 26, лапаротомные холецистэктомии — 5, грыжесечения — 7, аппендэктомии — 12).
Вторая группа (97 человек) была создана при ретроспективном анализе историй болезни. Здесь антибиотикопрофилактика проводилась рутинным применением цефалоспоринов III поколения — цефтриаксона или цефотаксима, с последующим их бессистемным назначением в течение 2–5 суток послеоперационного периода (лапароскопические холецистэктомии — 18, лапаротомные холецистэктомии — 26, грыжесечения — 16, аппендэктомии — 37).
В третью группу вошло 30 больных, также отобранных ретроспективно. Им по различным причинам не был введен антибиотик до начала операции. В послеоперационном периоде, находясь в профильных отделениях, они в течение 2–3 дней получали либо цефтриаксон, либо фторхинолоны + метронидазол. Сюда вошло 9 больных с лапаротомными холецистэктомиями, 5 — с грыжесечениями и 16 — с аппендэктомиями.
Бактериологический контроль в исследуемой условно-чистой группе начинался в операционной, где изучались содержимое удаленного желчного пузыря, червеобразного отростка, грыжевого мешка, выпот в брюшной полости. Исследование повторялось через 24, 48, 72 часа.
В послеоперационном периоде учитывались все бактериологические и клинические проявления гнойно-септических осложнений: колонизация возбудителями и контаминация раны, нагноение раны, абсцессы, перитонит, внутрибольничные пневмонии, цистит, острый пиелонефрит и др. Наличие синдрома системного воспалительного ответа (ССВО) без клинических признаков нагноения ран, но потребовавшего перехода к антибиотикотерапии, тоже расценивалось как отрицательный результат антибиотикопрофилактики.
Результаты и их обсуждение
Проявления гнойно-септических осложнений были выявлены нами всего у 17 больных, что составило 7,48 %. Умерших в исследуемой группе не было.
Наибольшее число осложнений — 13,3 % (4 больных) — зафиксировано в третьей группе, в которой по различным причинам антибиотикопрофилактика не проводилась. У всех четырех больных в послеоперационном периоде развилась пневмония, у двух из них — в сочетании с нагноением раны. Начатое через несколько часов после операции введение антибиотиков не предотвратило развития гнойно-септических осложнений. По данным В.Ф. Саенко (2004), к концу операции в 80–90 % случаев раны уже обсеменены различной микрофлорой, чаще всего стафилококками [5]. Поэтому проведение антибиотикопрофилактики у больных с условно-чистой ургентной хирургической патологией должно быть обязательным.
Во второй группе, в которой для профилактики использовался цефтриаксон, полученные результаты существенно не отличались. Гнойные осложнения выявлены у 11 больных, что составило 11,3 %. У троих имелись признаки воспаления раны, у четверых признаки ССВО сохранялись до 5–6-х суток, что потребовало перехода на полноценную антибиотикотерапию. У троих больных развилась внутрибольничная пневмония, у одного — явления цистита.
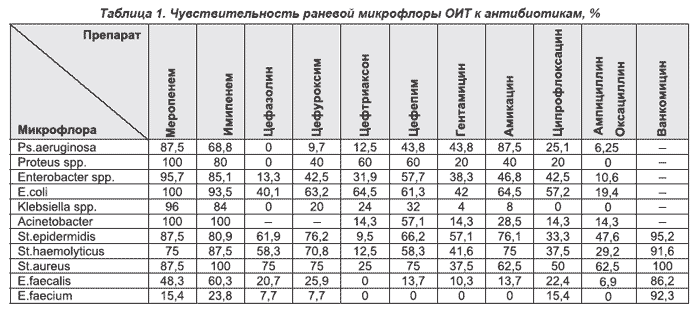
Отсутствие достоверных различий в клинических результатах между второй и третьей группами наглядно подтверждает неадекватность антибиотикопрофилактики, проводимой цефалоспоринами ІІІ поколения. На наш взгляд, это вызвано необоснованно широким использованием в последние годы цефалоспоринов III поколения, особенно цефтриаксона, что привело к образованию устойчивых штаммов и к потере чувствительности у многих микробов [7]. В нашем исследовании (табл. 1) чувствительными к цефтриаксону оказались только 31,9 % Enterobacter spp., 9,5 % Staphylococcus epidermidis, 12,5 % Staphylococcus haemolyticus. В семействе Enterococcus чувствительность к цефтриаксону отсутствовала полностью. Исходя из этого становится очевидным, что антибиотики, длительно применяемые в конкретном стационаре как лечебные препараты, должны быть исключены из схем профилактики.
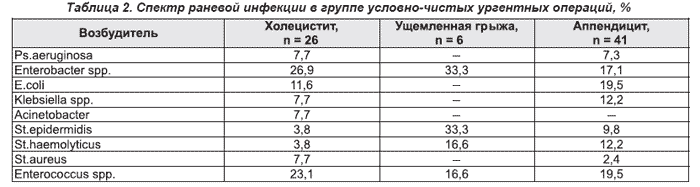
Проведенное ретроспективно бактериологическое исследование, к сожалению, не позволило охватить всех исследуемых больных из-за нерегулярности посевов в профильных отделениях. предполагаемый спектр возбудителей раневой инфекции при условно-чистых операциях приведен в табл. 2, составленной на основе обнаруженных положительных результатов посевов в 2006 году.
Наименьшая частота гнойно-септических осложнений — 2 больных (2 %) — выявлена в группе, получавшей в качестве антибиотикопрофилактики цефуроксим. При этом в подгруппах с использованием оригинального препарата и Кимацефа (Артериум) по одному больному имели бактериальную контаминацию раны с умеренным воспалением, что потребовало перехода на антибиотикотерапию.
Бактериологическое исследование в этой группе начиналось в операционной, где было получено 32 положительных результата. То есть 32 % условно-чистых ран уже исходно были инфицированы. Это еще раз подтверждает тезис об обязательном проведении антибиотикопрофилактики [5].
Из возбудителей чаще всего высевались: Enterobacter spp. — 37 %, St.haemolyticus — 25 %, Enterococcus spp. — 18 %, St.epidermidis — 12,5 %, E.сoli — 6,3 %.
уже через 24 часа после профилактического суточного введения цефуроксима колонизация возбудителями была определена только у 20 % больных: 9 — в 1-а и 11 — в 1-б подгруппах. Через 48 часов единичный рост зафиксирован только у 5 % больных. К 72-му часу колонизация возбудителем с умеренными клиническими проявлениями воспаления сохранялась только у 2 больных (по одному в каждой подгруппе). В посевах из раны в одном случае зафиксирован умеренный рост Enterococcus faecalis, в другом — St.haemolyticus. После 7-дневной антибиотикотерапии больные поправились и были выписаны на 11–14-е сутки.
Таким образом, наибольшую клиническую эффективность в нашем исследовании продемонстрировала профилактическая схема с использованием цефуроксима. Его применение позволило снизить с 13,3 до 2 % количество гнойно-септических осложнений у больных с условно-чистыми оперативными вмешательствами. При этом каких-либо различий в клинической и бактериологической эффективности между оригинальным препаратом и Кимацефом (Артериум) нами зафиксировано не было. Исходя из значительно меньшей стоимости последнего и одинаковой клинической эффективности, можно рекомендовать более широкое применение именно отечественного препарата Кимацеф, имеющего лучшие позиции в соотношении эффективность / стоимость. Использование цефалоспоринов ІІІ поколения в режиме 3–5?суточного введения не имеет ни клинического, ни экономического обоснования, поскольку не предотвращает развитие большого количества осложнений (11,3 %) и необоснованно увеличивает затраты на лечение.
Выводы
1. Антибиотикопрофилактика в ургентной абдоминальной хирургии является обязательной.
2. Наибольшую клиническую эффективность имеют схемы, в которых в качестве профилактического средства используется цефуроксим.
3. Антибиотики, длительно применяемые в данном стационаре в качестве лечебных препаратов, должны быть исключены из схем антибиотикопрофилактики.
4. Отечественный препарат Кимацеф (Артериум) имеет схожую с оригинальным препаратом клиническую эффективность и может быть рекомендован к более широкому применению с позиции эффективность / стоимость.
Список литературы
1. Гостищев В.К. Антибактериальная профилактика инфекционных осложнений в хирургии. Методические рекомендации. — М., 1997. — 10 с.
2. Грубник В.В. Эффективность профилактической антибиотикотерапии при хирургических вмешательствах на печени, желчном пузыре и желчных протоках // Лiки України. — 2003. — № 6. — С. 31-32.
3. Костюченко Л.А. Эмпирическая антимикробная химиопрофилактика и химиотерапия инфекции у хирургического больного // Анестезиология и реаниматология. — 1999. — № 2. — С. 45-48.
4. Принципы построения тактики антибактериальной терапии, профилактики и лечения септических состояний в раннем послеоперационном периоде. Методические рекомендации / Лозоришинец В.В., Лоскутов О.А., Крикунов А.А. и др. — К., 2005. — 28 с.
5. Саенко В.Ф., Мазур А.П., Горшевникова Э.В. и др. Руководство по антибиотикотерапии. — К.: Четверта хвиля, 2004. — 48 с.
6. Усенко Л.В., Клигуненко Е.Н. Профилактика и лечение инфекционных осложнений в практике врача-анестезиолога и хирурга. Методические рекомендации. — Днепропетровск, 2004. — 40 с.
7. Современные подходы к назначению антибактериальных препаратов в медицине критических состояний / Черний В.И., Колесников А.М., Кузнецова И.В. и др. — К.: Четверта хвиля, 2004. — 55 с.
8. Инфекционный контроль в хирургии / Шалимов А.А., Грубник В.В., Ткаченко А.И. и др. — К., 2001. — 182 с.
9. Яковлев В.П., Яковлев С.В. Рациональная антимикробная фармакотерапия — М.: Литера, 2003. — 667 с.
10. Lippert H., Gastinger J. Antimicrobial prophylaxis in laparoscopic and conventional cholecystectomy. Conclusions of a large prospective multicenter quality assurance study in Germany // Chemotherapy. — 1998. — vol. 44, № 5. — P. 355-363.


