Журнал «Боль. Суставы. Позвоночник» 3 (03) 2011
Вернуться к номеру
Эффективность препарата Терафлекс Адванс в лечении больных с остеоартрозом коленных суставов
Авторы: Поворознюк В.В., Григорьева Н.В., Орлик Т.В., Дзерович Н.И., Дубецкая Г.С., Атоян М.Л., Гриценко Г.Н., Колпакова Е.Ф., Копылова Н.В., Кривошеин В.М., Кундыч О.Н., Маркова Е.Я., Мархева И.Р., Мягкая Л.Д., Нам Л.В., Николаева Л.И., Норинская Н.П., Олексюк-Нехамес А.Г., Павлюк В.М., Стефюк О.З., Ференц А.П., Ференц И.В., Черненко В.А., Юнусова С.В., Международный остеоартрологический центр, Украинский научно-медицинский центр проблем остеопороза, г. Киев
Рубрики: Семейная медицина/Терапия, Ревматология, Травматология и ортопедия, Неврология
Версия для печати
Остеоартроз (ОА) — хроническое прогрессирующее дегенеративное заболевание суставов, характеризующееся деградацией суставного хряща с последующими изменениями в субхондральной кости и развитием краевых остеофитов, приводящее к потере хряща и сопутствующему поражению других компонентов сустава (синовиальная оболочка, связки). Остеоартроз — наиболее распространенная форма суставной патологии. В западных странах рентгенологические признаки ОА встречаются у большинства лиц старше 65 лет и приблизительно у 80 % людей старше 75 лет. Около 11 % лиц старше 60 лет имеют симптоматический (с клиническими проявлениями) ОА коленных суставов. Среди жителей США старше 30 лет симптоматический ОА коленных суставов встречается приблизительно у 6 %, а симптоматический ОА тазобедренного сустава — примерно у 3 % населения. В связи с высокой распространенностью и частой нетрудоспособностью, сопровождающими заболевание при локализации в коленном и тазобедренном суставах, ОА является частой причиной проблем, связанных с ходьбой и подъемом по лестнице. Хотя развитие ОА и не влияет на жизненный прогноз, заболевание является одной из основных причин преждевременной потери трудоспособности и инвалидности, а также хронического болевого синдрома, значительно снижающего качество жизни лиц пожилого и старческого возраста. В связи с существенным постарением населения и увеличением частоты заболевания в популяции вопросы его профилактики и лечения приобретают особую актуальность.
Согласно современной классификации препаратов, используемых в лечении остеоартроза, их подразделяют на две группы: симптоматические средства быстрого действия (нестероидные противовоспалительные препараты (НПВП), ацетаминофен, опиоидные анальгетики, кортикостероиды и др.), оказывающие влияние на клинические симптомы заболевания (боль, воспаление и др.), и модифицирующие средства замедленного действия (глюкозамин, диацереин, хондроитин, гиалуроновая кислота, неомыляемые соединения авокадо и сои), эффект которых проявляется более медленно по сравнению с симптоматическими средствами и длится после окончания их применения. В настоящее время проведено много исследований по изучению эффективности глюкозамина и хондроитина в лечении остеоартроза коленных и тазобедренных суставов. Результаты исследований были обобщены в обзорах и метаанализах [Leeb B.F. et al., 2000; McAlindon T.E. et al., 2000; Richi F. еt al., 2003; Towheed T.E. et al., 2005].
Пациенты и врачи продолжают часто задавать вопрос: что является более эффективным в лечении остеоартроза — глюкозамин, хондроитин или их комбинация? Ответ был получен после завершения первого этапа мультицентрового двойного слепого плацебо- и целекоксиб-контролируемого исследования (Glucosamine/chondroitin Arthritis Intervention Trial — GAIT), которое продемонстрировало, что только глюкозамина гидрохлорид в комбинации с хондроитина сульфатом является эффективным средством в лечении болевого синдрома в коленных суставах от умеренного до выраженного.
Однако глюкозамин и хондроитин не обладают прямым анальгезирующим эффектом. В экспериментальных исследованиях оценивалось антиноцицептивное синергическое и аддитивное взаимодействие комбинации глюкозамина сульфата и нестероидных противовоспалительных средств (ибупрофен, кетопрофен, диклофенак, индометацин, напроксен, пироксикам, аспирин, ацетаминофен). Результаты исследования показали, что комбинация глюкозамина сульфата и ибупрофена обладает синергическим антиноцицептивным взаимодействием (синергизм зависит от пропорционального соотношения данных препаратов), способствует снижению выраженности болевого синдрома при значительной меньшей дозе НПВП [Tallarida R.J. et al., 2003], что уменьшает риск побочных эффектов, частота которых существенно увеличивается у лиц старших возрастных групп.
Препаратом, при применении которого наблюдается сочетание противовоспалительного и обезболивающего действия со стойким модифицирующим эффектом, является Терафлекс Адванс производства компании «Байер», в состав которого входит 250 мг глюкозамина сульфата, 200 мг хондроитина сульфата и 100 мг ибупрофена.
Под руководством профессора В.В. Поворознюка в Украине проведено мультицентровое исследование по изучению эффективности препарата Терафлекс Адванс (11 центров: Днепропетровск, Дрогобыч, Запорожье, Киев, Кривой Рог, Львов, Николаев, Одесса, Тернополь, Харьков, Чернигов).
Цель исследования: изучение эффективности, переносимости и безопасности препарата Терафлекс Адванс в лечении пациентов с остеоартрозом коленных суставов.
Объект и методы исследования
Обследовано 238 больных из различных регионов Украины в возрасте 37–79 лет (средний возраст 54,1 ± ± 1,6 года, рост 164,1 ± 1,6 см, масса тела 64,1 ± 1,6 кг, индекс массы тела 34,1 ± 7,0; 80 % женщин, 20 % мужчин). В исследование включали пациентов с остеоартрозом коленных суставов II–III ст. по Kellgren — Lawrence и выраженным ирритативно-болевым синдромом. Все пациенты предъявляли жалобы на боли в коленных суставах (на момент включения в исследование уровень боли составлял 40 мм и более по визуально-аналоговой шкале (ВАШ) боли) и ограничение повседневной активности. Препарат принимали по две капсулы три раза в день в течение 20 дней, последующие 30 дней составили период наблюдения.
Пациентам проводили полное клиническое обследование (общий анализ крови с лейкоцитарной формулой, анализ биохимических показателей крови, рентгенографию коленных суставов). Оценку болевого синдрома при каждом визите к врачу проводили по Мак-Гилловскому опроснику боли, рассчитывая индекс дескрипторов, то есть количество выбранных слов-определений, и индекс рангов — сумму баллов, присвоенных каждому из выбранных дескрипторов. Выраженность болевого синдрома при каждом визите к врачу определяли с помощью четырехкомпонентной визуально-аналоговой шкалы, включающей четыре 10-балльные подшкалы: уровень боли на момент опроса (ВАШ-1), средний (типичный) уровень боли (ВАШ-2), минимальный (ВАШ-3) и максимальный (ВАШ-4) уровни боли. Результат определяли как сумму баллов по каждой из подшкал. Кроме того, оценку эффективности лечения проводили с использованием шкалы WOMAC (Western Ontario and McMaster University osteoarthritis index), которая включает три подшкалы: болевую (вопросы 1–5), шкалу утренней скованности (6, 7) и повседневной активности (8–24), и альгофункционального индекса Лекена. Оценку состояния больного проводили пациент и врач с использованием 5-балльной шкалы Ликерта (1 — очень плохое, 2 — плохое, 3 — удовлетворительное, 4 — хорошее, 5 — очень хорошее).
Качество жизни пациентов оценивали по шкале EuroQol-5D. Все опросники заполнялись самостоятельно пациентами под контролем врача. Повторное обследование проводили через 10, 20, 30, 40 и 50 дней. Статистический анализ полученных результатов проводили с помощью пакета программ Statistica 6.0, используя однофакторный дисперсионный анализ ANOVA, t-тест Стьюдента для связанных выборок с определением показателя достоверности (р). Различия показателей считали достоверными при р < 0,05. Результаты представлены в виде M ± SD.
Результаты исследования и их обсуждение
По результатам проведенного исследования нами установлено достоверное снижение показателя суммы дескрипторов боли у пациентов, принимавших Терафлекс Адванс, уже через 10 дней лечения (динамика показателя составила: –0,61 ± 3,43 балла; t = = 2,15, Р = 0,03); данная динамика поддерживалась и через 20 (–1,04 ± 3,35 балла; t = 3,67, Р = 0,0003), 30 (–1,61 ± 3,61 балла; t = 4,82, Р = 0,000004), 40 (–1,73 ± ± 3,73 балла; t = 5,01, Р = 0,000002) и 50 дней наблюдения (–2,89 ± 4,11 балла; t = 8,11, Р = 0,000000001). Подобная динамика отмечена и для показателей суммы рангов (соответственно через 10 (–3,65 ± ± 8,17 балла; t = 5,38, Р = 0,0000003) и 20 дней лечения (–5,11 ± 8,73 балла; t = 6,96, Р = 0,0000000001) и через 30 (–6,28 ± 9,77 балла; t = 6,96, Р = 0,0000000002), 40 (–5,96 ± 9,47 балла; t = 6,80, Р = 0,0000000005) и 50 дней наблюдения (–8,22 ± 10,00 балла; t = 9,48, Р = 0,00000000001). Сравнивая результаты показателей суммы дескрипторов и рангов у пациентов после окончания курса лечения (20-й день) и в течение последующего периода наблюдения, стоит отметить, что динамика показателей на 30-й и 40-й день исследования по сравнению с 20-м днем была недостоверной и только на 50-й день наблюдения вышеуказанные показатели были достоверно ниже по сравнению с таковыми в конце лечения (динамика показателей составила соответственно для суммы дескрипторов: –0,85 ± 2,84 балла; t = 3,22, Р = 0,002; для суммы рангов: –1,96 ± ± 7,18 балла; t = 2,92, Р = 0,004). Также нами отмечена достоверная положительная динамика показателя индекса боли через 10 (–1,02 ± 1,49 балла; t = 8,26, Р = 0,00000000001), 20 дней лечения (–1,55 ± 1,51 балла; t = 12,18, Р = 0,00000000003) и на 30-й (–1,81 ± ± 1,43 балла; t = 13,69, Р = 0,00000000001), 40-й (–1,94 ± ± 1,81 балла; t = 11,59, Р = 0,00000000002) и 50-й день наблюдения (–2,61 ± 1,96 балла; t = 15,37, Р = = 0,00000000001).
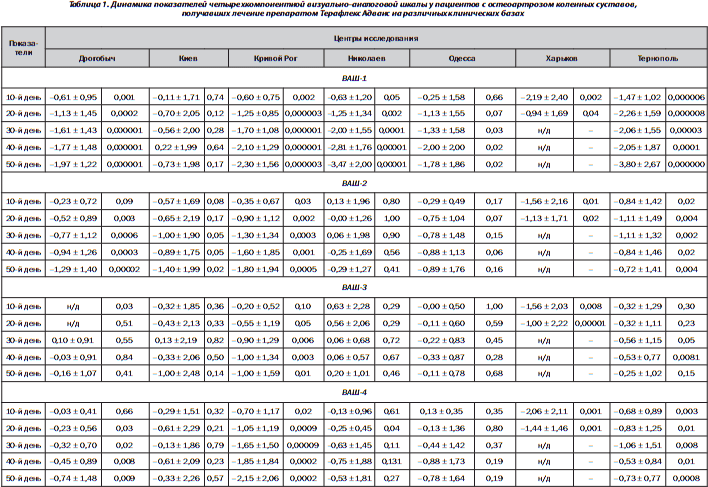
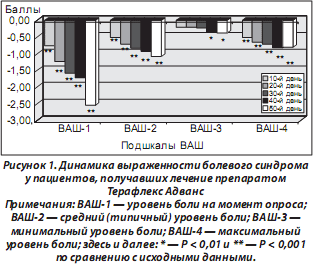
Подобная динамика снижения выраженности болевого синдрома наблюдалась и при его оценке с помощью визуально-аналоговых шкал. Так, уже через 10 дней лечения отмечено достоверное снижение показателей среднего и максимального уровня боли, а также уровня боли на момент опроса (рис. 1). Снижение показателя минимального уровня боли было менее выраженным на фоне проводимого лечения и достигало достоверных значений на 40-й день исследования. Результаты исследования показателей четырехсоставной анкеты ВАШ в зависимости от центра исследования представлены в табл. 1.
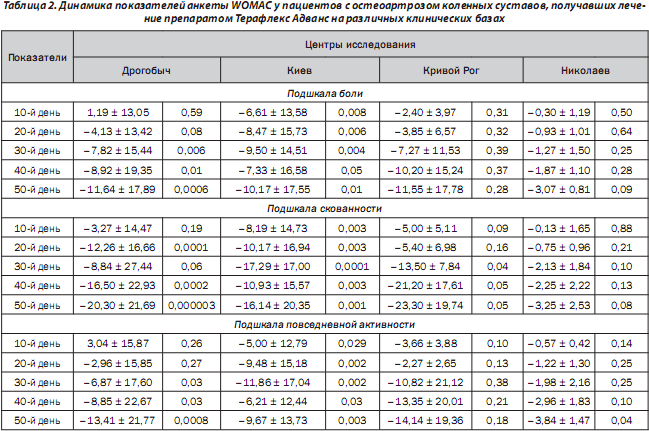
По результатам данного исследования нами установлено достоверное снижение суммарного показателя анкеты WOMAC у пациентов, принимавших Терафлекс Адванс, только через 20 дней лечения (динамика показателя через 10 дней составила: –1,55 ± ± 11,95 см; t = 1,08, Р = 0,28, через 20 дней: –5,89 ± ± 12,82 см; t = 3,84, Р = 0,0003). Несмотря на завершение курса лечения на 20-й день исследования, положительная динамика индекса WOMAC отмечалась и на 30, 40 и 50-й день наблюдения (динамика показателей составила соответственно на 30-й день: –8,81 ± 15,41 см; t = 4,78, Р = 0,00001; 40-й день: –8,37 ± 17,89 см; t = 3,80, Р = 0,0003; и 50-й день исследования: –11,79 ± 17,56 см; t = 5,46, Р = 0,000001). Сравнивая результаты показателей анкеты WOMAC у пациентов после окончания курса лечения (20-й день) и в течение последующего периода наблюдения, стоит отметить дальнейшее снижение показателей. Их динамика была достоверной на 30, 40, и 50-й дни исследования, вышеуказанные показатели были достоверно ниже по сравнению с таковыми в конце лечения (динамика показателей составила соответственно на 30-й день: –2,92 ± 8,72 см; t = 2,80, Р = = 0,007; 40-й день: –2,79 ± 12,63 см; t = 1,79, Р = 0,05; и 50-й день исследования: –6,37 ± 12,80 см; t = 4,04, Р = 0,0001).
Анализируя данные отдельных подшкал анкеты WOMAC у пациентов, принимавших Терафлекс Адванс, мы установили, что наибольшая положительная динамика показателей отмечена при оценке по шкале скованности (на 10-й день лечения), тогда как показатели снижения выраженности болевого синдрома и улучшения повседневной активности достигали достоверных различий только к окончанию курса лечения (20-й день). Показатели всех отдельно анализируемых подшкал на 30, 40 и 50-й день исследования были достоверно ниже по сравнению с исходными данными (рис. 2). Подобная динамика показателей анкеты WOMAC наблюдалась в различных центрах исследования (табл. 2).
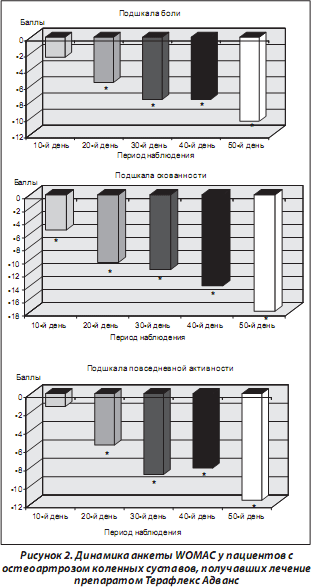
Анализ данных анкеты Ликерта также выявил до- стоверное улучшение состояния больных уже через 10 дней лечения (динамика показателя во всей группе составила –0,76 ± 2,24 балла, t = 3,91; Р = = 0,0001), которое поддерживалось к завершению курса лечения (на 20-й день динамика показателя –0,92 ± ± 2,08 балла, t = 5,01; Р = 0,000002). После завершения лечения отмечалось дальнейшее снижение показателя шкалы Ликерта на 30-й (–0,61 ± 1,41 балла, t = 4,47; Р = = 0,00002), 40-й (–0,79 ± 1,52 балла, t = 5,30; Р = = 0,000001) и 50-й день наблюдения (–0,82 ± 1,77 балла, t = 4,70; Р = 0,000008). Проводя сравнение данного показателя у пациентов с гонартрозом, получающих Терафлекс Адванс, после окончания курса лечения (20-й день) и в течение последующего периода наблюдения, стоит отметить дальнейшее уменьшение показателей. Их динамика была достоверной на 30 и 40 и 50-й день наблюдения, вышеуказанные показатели были достоверно ниже по сравнению с таковыми в конце лечения (их динамика составила соответственно на 30-й день: –0,17 ± 0,89 балла, t = 1,97, P = 0,05; 40-й день: –0,26 ± 0,92 балла, t = 2,86; Р = 0,01; и 50-й день исследования: –0,31 ± 1,48 балла, t = 2,13; Р = 0,04).
Достоверное уменьшение выраженности болевого синдрома у пациентов, принимавших Терафлекс Адванс, сопровождалось достоверным уменьшением индекса Лекена уже на 10-й день лечения. Достоверная динамика показателя наблюдалась к 20-му дню терапии и в течение всего периода наблюдения (рис. 3А). Сравнивая индекс Лекена у пациентов с гонартрозом, получающих Терафлекс Адванс, после окончания курса лечения (20-й день) и в течение последующего периода наблюдения, необходимо отметить дальнейшее уменьшение показателей. Вышеуказанные показатели были достоверно ниже по сравнению с таковыми в конце лечения (их динамика составила соответственно на 30-й день: –0,61 ± 2,73 балла, t = 2,12; Р = 0,04; 40-й день: –0,77 ± 2,93 балла, t = 2,48; Р = 0,02; и 50-й день исследования: –1,14 ± 3,48 балла, t = 3,02; Р = 0,003).
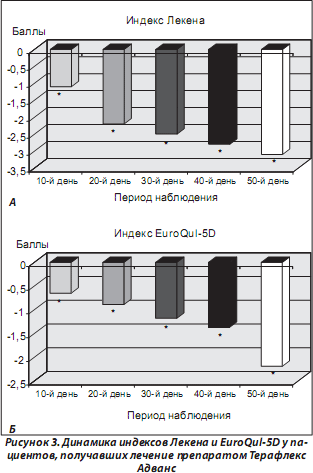
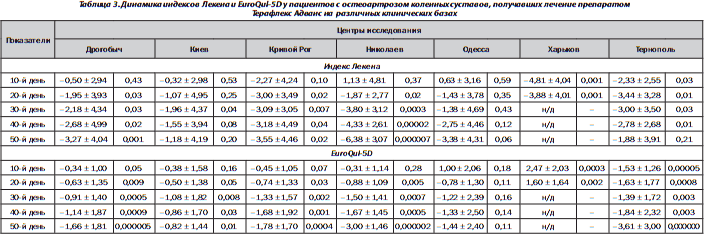
Достоверное уменьшение выраженности болевого синдрома в коленных суставах, утренней скованности, а также улучшение функциональной активности у пациентов, принимавших Терафлекс Адванс, сопровождалось достоверным улучшением качества жизни по данным анкеты EuroQul-5D уже на 10-й день лечения, которое было еще более выраженным к концу терапии и всего периода наблюдения (рис. 3Б). Сравнивая результаты данного показателя у пациентов с гонартрозом, получающих Терафлекс Адванс, после окончания курса лечения (20-й день) и в течение последующего периода наблюдения, стоит отметить дальнейшее снижение показателей. Их динамика была достоверной на 30, 40 и 50-й день наблюдения, вышеуказанные показатели были достоверно ниже по сравнению с таковыми в конце лечения (их динамика составила соответственно на 30-й день: –0,37 ± 1,15 балла, t = 3,59; Р = 0,0005; 40-й день: –0,53 ± 1,36 балла, t = 4,23; Р = = 0,00005; и 50-й день исследования: –0,86 ± 1,53 балла, t = 6,12; Р = 0,0000001). Результаты исследования показателей анкеты Лекена и EuroQul-5D на различных клинических базах представлены в табл. 3.
Исследователями различных клинических баз не было отмечено побочных эффектов при применении препарата Терафлекс Адванс в период лечения и наблюдения.
Выводы
— Препарат Терафлекс Адванс способствует быстрому снижению выраженности болевого синдрома и улучшению повседневной активности у больных, страдающих остеоартрозом коленных суставов. Положительный эффект сохраняется в течение 30 дней после завершения приема препарата.
— У пациентов, получающих Терафлекс Адванс, не выявлено побочных эффектов при приеме препарата, отмечено достоверное улучшение качества жизни как после периода лечения, так и на протяжении периода наблюдения.
1. Зупанець І.А., Шебеко С.К. Фармакологічне дослідження анальгетичної активності препаратів терафлекс і терафлекс адванс // Здоров’я України. — 2008. — № 21/1. — С. 70-71.
2. Поворознюк В.В., Дзерович Н.И. Эффективность препарата Терафлекс адванс в лечении болевого синдрома при остеоартрозе коленных суставов // Здоров’я України. — 2007. — № 21/1. — С.74-75.
3. Leeb B.F., Schweitzer H., Montag K., Smolen J.S. A meta-analysis of chondroitin sulfate in the treatment of osteoarthritis // J. Rheumatol. — 2000. — 27. — P. 205-211.
4. McAlindon T.E., LaValley M.P., Gulin J.P., Felson D.T. Glucosamine and chondroitin for treatment of osteoarthritis: a systematic quality assessment and meta-analysis // JAMA. — 2000. — 283. — P. 1469-1475.
5. Richy F., Bruyere O., Ethgen O. Structural and symptomatic efficacy of glucosamine and chondroitin in knee osteoarthritis: a comprehensive meta-analysis // Arch. Intern. Med. — 2003. — 163. — P. 1514-1522.
6. Tallarida R.J., Cowan A., Raffa R.B. Antinociceptive synergy, additivity, and subadditivity with combinations of oral glucosamine plus nonopioid analgesics in mice // Journal of Pharmacology аnd Experimental Therapeutics. — 2003. — P. 699-704.
7. Towheed T.E., Maxwell L., Anastassiades T.P. Glucosamine therapy for treating osteoarthritis // Cochrane Database Syst Rev. — 2005. — CD002946-CD002946.