Журнал «Боль. Суставы. Позвоночник» 3 (03) 2011
Вернуться к номеру
Можливості ультразвукового дослідження в ранній діагностиці патології опорно-рухового апарату
Авторы: Коваленко В.М., Борткевич О.П., Рекалов Д.Г., Шманько О.В., Лічман О.М., Національний науковий центр «Інститут кардіології ім. академіка М.Д. Стражеска» НАМН України, Поворознюк В.В., Дзерович Н.І., Григор’єва Н.В., ДУ «Інститут геронтології НАМН України», м. Київ
Рубрики: Семейная медицина/Терапия, Ревматология, Травматология и ортопедия, Неврология
Версия для печати
 На сьогодні ультразвукове дослідження (УЗД) є провідним інструментальним методом ранньої діагностики патології опорно-рухового апарату (ОРА), у тому числі при ревматичних хворобах, а також моніторингу стану компонентів ОРА конкретних хворих під впливом лікування [Коваленко В.М., Шуба Н.М., 2008; Рекалов Д.Г., Борткевич О.П., 2011; Шманько О.В., 2011; Alassaarela E. et al., 1998; Backhaus M. et al., 2001; Manger B., Kalden J.R., 1995; Manger B., Backhaus M., 1997; Grassi W., Cervini C., 1998; Gibbon W.W., Wakefield R.J., 1999]. Удосконалення технічних можливостей УЗД опорно-рухового апарату, зокрема розробка високочастотних датчиків, зробило УЗД основним методом оцінки патології м’яких тканин (у тому числі основних компонентів суглобів — хряща, синовіальної оболонки (СО), поверхневих кісткових структур; періартикулярних м’яких тканин — зв’язково-сухожильного апарату, шкіри та підшкірно-жирової клітковини (ПЖК), що має велике значення при проведенні диференціальної діагностики новоутворень у вказаних структурах), виявлення рідини та характеристики її властивостей, що визначає тактику локальної, у тому числі внутрішньосуглобової, терапії. Основними недоліками УЗД є неможливість візуалізації структури кісткової тканини, а також «оператор-залежність» процедури, що цілком залежить від кваліфікації лікаря-функціоналіста, який проводить УЗД. На жаль, недостатнім є застосування УЗД у діагностиці ревматичних хвороб суглобів, у першу чергу ревматоїдного артриту (РА) та спондилоартропатій (СпА). УЗД не приділяється достатньої уваги з боку спеціалістів-ревматологів, що обумовлене недостатньою обізнаністю фахівців даного профілю з методом УЗД опорно-рухового апарату, а також самою методикою проведення відповідного дослідження.
На сьогодні ультразвукове дослідження (УЗД) є провідним інструментальним методом ранньої діагностики патології опорно-рухового апарату (ОРА), у тому числі при ревматичних хворобах, а також моніторингу стану компонентів ОРА конкретних хворих під впливом лікування [Коваленко В.М., Шуба Н.М., 2008; Рекалов Д.Г., Борткевич О.П., 2011; Шманько О.В., 2011; Alassaarela E. et al., 1998; Backhaus M. et al., 2001; Manger B., Kalden J.R., 1995; Manger B., Backhaus M., 1997; Grassi W., Cervini C., 1998; Gibbon W.W., Wakefield R.J., 1999]. Удосконалення технічних можливостей УЗД опорно-рухового апарату, зокрема розробка високочастотних датчиків, зробило УЗД основним методом оцінки патології м’яких тканин (у тому числі основних компонентів суглобів — хряща, синовіальної оболонки (СО), поверхневих кісткових структур; періартикулярних м’яких тканин — зв’язково-сухожильного апарату, шкіри та підшкірно-жирової клітковини (ПЖК), що має велике значення при проведенні диференціальної діагностики новоутворень у вказаних структурах), виявлення рідини та характеристики її властивостей, що визначає тактику локальної, у тому числі внутрішньосуглобової, терапії. Основними недоліками УЗД є неможливість візуалізації структури кісткової тканини, а також «оператор-залежність» процедури, що цілком залежить від кваліфікації лікаря-функціоналіста, який проводить УЗД. На жаль, недостатнім є застосування УЗД у діагностиці ревматичних хвороб суглобів, у першу чергу ревматоїдного артриту (РА) та спондилоартропатій (СпА). УЗД не приділяється достатньої уваги з боку спеціалістів-ревматологів, що обумовлене недостатньою обізнаністю фахівців даного профілю з методом УЗД опорно-рухового апарату, а також самою методикою проведення відповідного дослідження.
Звичайно, структура кісткової тканини є недоступною для даної методики, але остання дозволяє детально дослідити кісткову поверхню, зокрема періостальну реакцію, а також зміни в режимі енергетичного допплерівського дослідження та ін. [Grassi W. еt al., 1993, 1999; Backhaus M. еt al., 1999].
Неінвазивність (на відміну від артроскопії), доступність, простота дослідження, економічність (порівняно з комп’ютерною томографією (КТ) і магнітно-резонансною томографією (МРТ)) забезпечили методу УЗД опорно-рухового апарату пріоритет серед інших інструментальних методів дослідження суглобів і м’яких тканин.
Техніка виконання УЗД щодо виявлення патологічних змін ОРА є особливо важливою й вимагає від лікаря, який виконує дослідження, детального знання можливостей сучасних діагностичних ультразвукових апаратів (УЗ-апаратів), а також ультразвукової анатомії досліджуваної ділянки та найбільш типових проявів патологічних змін.
УЗД опорно-рухового апарату повинне виконуватися за допомогою високочастотного лінійного датчика, що працює в діапазоні 7–20 Мгц. Зазвичай для отримання зображення достатньо навіть поверхневих структур діапазону до 12,5 МГц. Застосування датчика з меншою робочою частотою (3,5–5 Мгц) обмежується тільки дослі-дженням тазостегнового суглоба й суглобів у дуже повних пацієнтів. Важливо також вибрати правильні програми дослідження для різних суглобів. Багато УЗ-приладів уже сьогодні оснащені набором стандартних програм для дослідження різних відділів ОРА. Сучасні УЗ-апарати мають також велику кількість додаткових режимів сканування, що дозволяє значно розширювати діагностичні можливості звичайного сірошкального сканування, такі як режим нативної або тканинної гармоніки, режим панорамного сканування й режим тривимірної реконструкції. Так, сканування в режимі нативної гармоніки дозволяє одержати більш контрастне, ніж при звичайному сіро- шкальному скануванні, зображення ніжних гіпоехогенних структур, що відбивають зони розривів зв’язкового апарату або меніска. Режим панорамного сканування дозволяє отримати розширене зображення відразу декількох структур, наприклад, тих, що утворюють суглоб, і відобразити їх просторове розташування. Тривимірна реконструкція не тільки забезпечує отримання волюметричної інформації, але й надає можливість одержувати багатоплощинні зрізи досліджуваних структур (у тому числі фронтальні). Принципово новим є застосування високочастотних УЗ-датчиків, що забезпечують можливість візуалізації різних за ехогенністю та глибиною залягання структур. В останніх використається вузький УЗ-промінь, який працює у високочастотному діапазоні, що сприяє значному підвищенню латеральної роздільної здатності в зоні УЗ-фокусу. Можливості УЗД також істотно розширилися у зв’язку із впровадженням у практику нових УЗ-технологій, заснованих на ефекті Допплера. Нові методики УЗ-ангіографії дозволяють візуалізувати патологічний кровотік у зоні запальних змін органів і тканин (наприклад, при синовіті).
Артефакти при проведенні ультразвукового дослідження
Усі артефакти, що виникають при проведенні ультразвукового дослідження опорно-рухового апарату, розділяють умовно на стандартні, які виникають при всіх УЗ-дослідженнях, і специфічні, характерні для УЗ-досліджень ОРА.
Артефакти, що виникають за рахунок рефракції УЗ-променя. По краях округлих структур на межі двох різних акустичних середовищ може виникати дистальна тінь. У нормі цей ефект можна спостерігати при поперечному скануванні ахіллового сухожилля. Внутрішньом’язові перегородки також можуть давати тінь позаду себе. За рідинними структурами виникає ефект посилення ультразвукового сигналу. Тому структури, що розташовуються за утримуючими рідину об’єктами, можуть виглядати більш ехогенними, ніж у нормі. Наприклад, наявність невеликого випоту в синовіальній оболонці сухожилля підвищує його ехогенність.
Реверберація. Цей ефект може виникати позаду високовідбивних об’єктів (кістка, діафрагма тощо), призводячи до появи дзеркальних або фантомних зображень. При дослідженні ОРА такий ефект можна спостерігати за малогомілковою кісткою. Металеві та скляні об’єкти викликають ефект реверберації, що отримав назву «хвіст комети». Як правило, при дослідженні ОРА вони можуть зустрічатися після металевих протезів або металевих (скляних) сторонніх тіл.
Рефракція. Виникає на межі відбивних середовищ із різним звукопроведенням (наприклад, жирова тканина та м’язи) в результаті переломлення УЗ-променя, що при-водить до дислокації зображуваних структур. Зменшенню рефракції сприяє утримання датчика перпендикулярно до досліджуваних структур.
Анізотропія — специфічний для УЗД ОРА артефакт, що виникає при УЗ-скануванні лінійним датчиком сухожиль, коли скануючий УЗ-промінь не падає на них строго перпендикулярно. На тій ділянці сухожилля, де немає точного перпендикулярного відбиття УЗ-променя, будуть з’являтися зони зниженої ехогенності, що можуть симулювати наявність патологічних змін. М’язи, зв’язки та нерви також мають слабкий ефект анізотропії. Зниження ехогенності сухожилля призводить до погіршення якості візуалізації його фібрилярної структури. Проте в ряді випадків, коли необхідно візуалізувати сухожилля на тлі ехогенної клітковини, змінюючи кут сканування, тоді сухожилля буде виглядати контрастним (гіпоехогенним) на тлі ехогенної жирової клітковини.
Хід волокон сухожиль у місці прикріплення не завжди перпендикулярний УЗ-променю, тому ця зона видається гіпоехогенною (ефект анізотропії).
Досвід застосування ультразвукового дослідження при патології опорно-рухового апарату
На базі Національного наукового центру «Інститут кардіології ім. М.Д. Стражеска» АМН України проводиться УЗД ОРА на апаратах Kontron Medikal SAS, серії Sigma 5000 (Франція) датчиком 5–12 МГц та Medison Sonoace X8 (Корея) датчиком 5–12 МГц згідно з сучасними рекомендаціями [Backhaus M. et al., 2001; EULAR, Working Party on Imaging in Rheumatology, 2005].
УЗД опорно-рухового апарату виконується з використанням лінійних датчиків із робочою частотою 7,5 МГц і більше у разі дослідження найбільш поверхнево розта-шованих структур, із застосуванням конвексних датчиків із меншою робочою частотою — 3,5–5 МГц при дослідженні кульшового суглоба або інших великих суглобів у дуже повних пацієнтів [Михайлов Е.Е. и соавт., 1999].
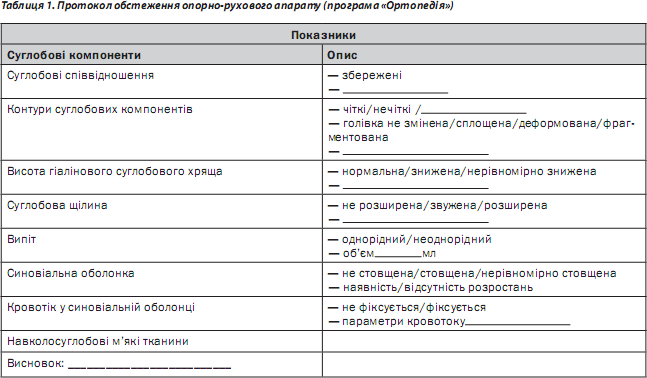
Згідно з методикою оцінюють кісткові суглобові поверхні (зміни поверхні субхондральної кістки — наявність кіст, ерозій, інших дефектів), синовіальні щілини, СО, навколосуглобові м’які тканини, наявність випоту, кровотоку в СО, зміни зв’язкового апарату тощо. Загальний протокол УЗ-обстеження хворого на ревматичні захворювання суглобів (РЗС), розроблений авторами, наведено в табл. 1.
Для оцінки вираженості синовіту та кровотоку в СО використовується допплерівське дослідження в кольо- ровому й енергетичному режимах. Поперечні сканування розділялися нами на три рівні сегменти — радіальний, медіальний і ульнарний — для зручності оцінки пануса і васкуляризації. Оцінка проводилася за методикою, запропонованою M. Hau et al. (1999), що включає трибальну шкалу (0 — відсутність візуалізації пануса і/або кольорових сигналів на отриманому зображенні в аналізованій ділянці; 1 — незначна візуалізація пануса і/або одиничні кольорові сигнали; 2 — помірна візуалізація пануса або помірна кількість кольорових сигналів; 3 — максимальна візуалізація пануса і/або висока щільність кольорових сигналів, які зливаються на отриманому зображенні) і розрахунок судинного індексу (vessel index), що дорівнює сумі усіх кольорових сигналів, зафіксованих в аналізованій ділянці на поздовжніх і поперечних скануваннях, поділеній на число обстежених суглобів у кожній дослідженій підгрупі хворих.
Дані ультразвукового дослідження опорно-рухового апарату в нормі
УЗ-зображення суглобового хряща (СХ), м’яких періартикулярних тканин, у тому числі зв’язок, сухожиль та м’язових структур, за умови дотримання правил УЗД щодо окремих анатомічних утворень є чіткими та інформативно порівнянними з анатомічними структурами.
Необхідно порівнювати УЗ-зображення ураженої ділянки з контралатеральною стороною!
Структури опорно-рухового апарату за даними ультразвукового дослідження в нормі
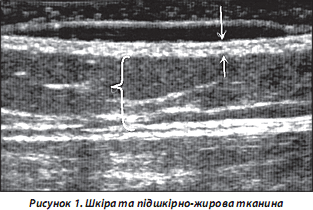
1. Шкіра та підшкірна жирова клітковина. Найкраще візуалізується при скануванні високочастотними датчиками (від 12,5 МГц) у вигляді гіперехогенної відносно гомогенної ділянки з різною товщиною, що залежить від локалізації ділянки, яка сканується, віку та статі хворих. Зазначимо, що в чоловіків товщина шкіри більша, ніж у жінок. Шари шкіри (епідерміс та дерма) практично не диференціюються при проведенні УЗД (рис. 1).
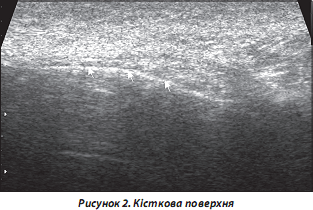
2. Кісткові структури. УЗД дозволяє отримати тільки зображення поверхні кістки у вигляді гіперехогенної лінії. Поздовжнє та поперечне сканування слід проводити перпендикулярно кістковій поверхні. При РЗС можлива візуалізація ураженого періосту у вигляді нечіткої гіперехогенної смуги (артрити, у тому числі РА, СпА, псевдоерозивний варіант ОА тощо) (рис. 2).
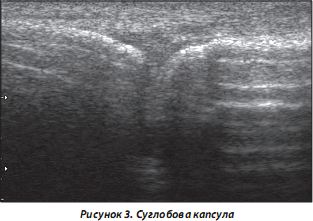
3. Суглобова капсула. У нормі виглядає як контрастна непотовщена гіперехогенна лінія (рис. 3). У більшості випадків при РЗС змінюються УЗ-характеристики (збільшується товщина, з’являються ознаки розволокніння, ча-сткових та суцільних надривів/розривів, витікання синовіальної рідини (СР) (наприклад, при кісті Бейкера).
4. Синовіальна оболонка. У нормі не візуалізується. Набуває характерної ехоструктури при запальних процесах (РА, СпА, остеоатроз (ОА) з вираженим запальним компонентом тощо) (рис. 4).
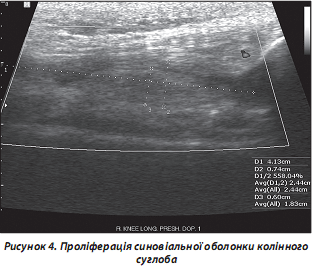
5. Гіаліновий суглобовий хрящ. Гіпо-/анехогенна структура, розташована на суглобовій поверхні кісток (рис. 5). У нормі ехогенність збільшується з віком, при розвитку ОА, хондрокальцинозу.
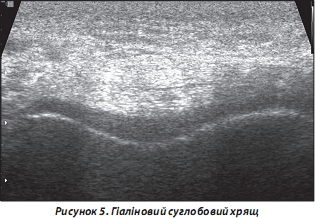
6. Суглобовий хрящ (СХ) (типовий приклад — структури менісків колінного суглоба). У нормі виглядає гіперехогенним унаслідок великої кількості різноспрямованих колагенових волокон (рис. 6).

7. Сухожилля при проведенні УЗД добре візуалізуються як при поздовжніх, так і поперечних скануваннях, у вигляді лінійно розташованих фібрилярних гіпер-/гіпоехогенних структур із досить чіткими контурами та візуалізацією волокнистої структури (рис. 7).
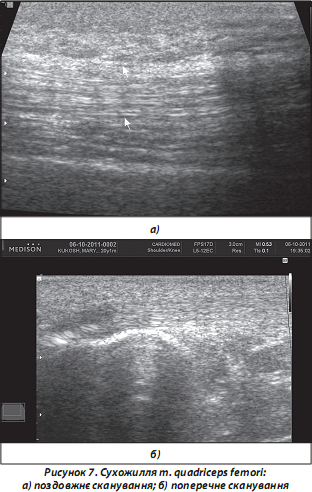
Деякі сухожилля (m. biceps brachii, m. quadriceps femori тощо) оточені гіпоехогенною зоною хало [Зубарев А.В., 2002], що відображає наявність СО, яка містить невелику кількість рідини навіть у нормі.
Інші сухожилля (наприклад, ахіллове), не мають СО, оточені сполучною тканиною (СТ), що формує навколосухожильний простір; у місці прикріплення завжди формують сухожильні сумки (бурси).
8. Зв’язки за ехоструктурою подібні до сухожиль. При УЗД виглядають, як:
а) гіперехогенні фібрилярні структури (власна зв’язка надколінка, lig. collater. med. тощо) (рис. 8а);
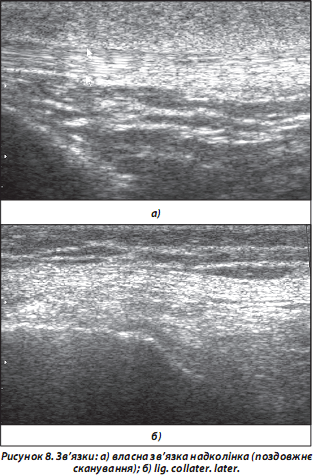
б) змішані фібрилярні структури (lig. collater. lat. тощо) — за рахунок контралатерально спрямованих волокон (рис. 8б);
в) гіпоехогенні структури (ligg. cruciata ant. et post., інші фрагменти внутрішньосуглобових структур) — за рахунок неперпендикулярного розташування ходу УЗ-променя.
9. М’язові структури — гіпоехогенні порівняно з підшкірно-жировою клітковиною, сухожиллями. Проведення функціональних проб зі скороченням м’язів призводить до зміни ходу м’язових волокон та незначного зниження ехогенності досліджуваного м’яза (рис. 9):
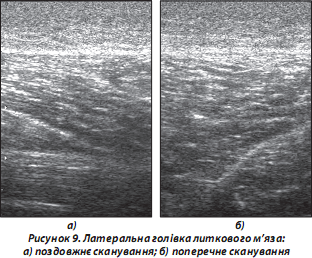
а) поздовжнє сканування: відносно гомогенні гіпоехогенні пучки, окреслені паралельними гіперехогенними утвореннями (сполучнотканинні прошарки — фасції тощо) у вигляді «пера», що поступово переходять у сухожильну частину досліджуваного м’яза [Зубарев А.В., 2002];
б) поперечне сканування: гіпоехогенна дрібно крапчаста структура з гіперехогенними (фіброзними) прошарками та переходом у сухожильну тканину.
Дані УЗД опорно-рухового апарату при патології
1. Патологія м’язів:
а) перерозтягнення (пошкоджується менше ніж 5 % поперечного перетину м’яза. Дані УЗД: мікророзриви у вигляді множинних кістозних ділянок, що при поздовжньому скануванні мають витягнуту структуру;
б) частковий розрив (УЗД-ознака — гіпоехогенна гематома в зоні пошкодженої ділянки м’язової тканини зі зникненням типового волокнистого малюнка в зоні роз-риву). У пізній стадії розриву за скороченням м’яза можна провести диференціальну діагностику: ушкоджений м’яз/ехогенна гематома різного генезу;
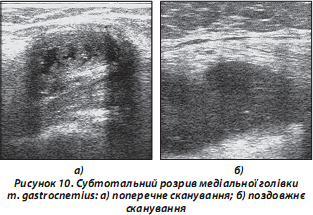
в) повний розрив (УЗД-ознака — гематома в місці м’язово-сухожильного переходу). М’яз при поперечному УЗ-скануванні «відірваний» від місця прикріплення (рис. 10). Давність гематоми визначається за такими ознаками: реєстрація перифокального кровотоку за даними допплерівського УЗД, а також наявність гіперехогенних включень (нитки фібрину) свідчить про підгострий/хронічний процес;
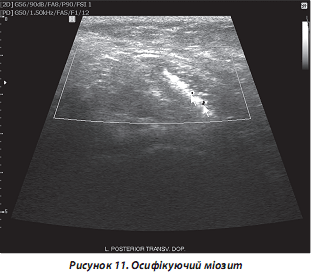
г) осифікуючий міозит локалізується найбільш часто в ліктьовій, тазостегновій, сідничній ділянках. За генезом у 60–75 % випадків він є посттравматичним, постінфарктним, ідіопатич- ним, нейрогенним. УЗД-ознаки — гіперехогенні структури в проекції м’язів, що скануються, з акустичною тінню (рис. 11).
2. Патологія зв’язок та сухожиль:
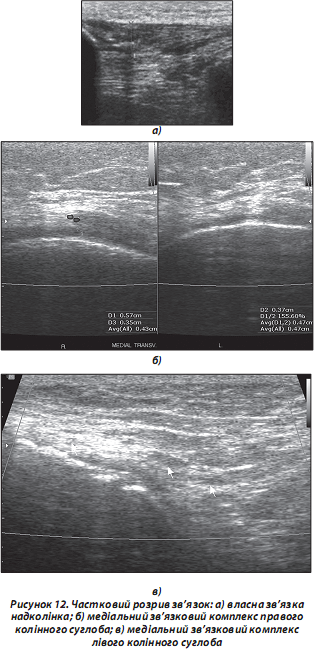
а) частковий чи повний розрив сухожилля — найчастіше виникає в місці прикріплення сухожилля до кістки чи м’яза (УЗД-ознака сухожиль з СО — часткове порушення фібрилярної структури сухожилля з формуванням анехогенного дефекту у вигляді синовіального випоту навколо ураженого сухожилля; УЗД-ознака сухожиль без СО — локальне потовщення сухожилля з порушенням контурів та фібрилярної структури останнього в місці дефекту; анехогенною ділянкою навколо ураженої зони за рахунок накопичення рідини в місці розриву). Розірвані кінці сухожиль, що не мають СО, скорочені, з повним порушенням їх фібрилярної структури, заповненням дефекту анехогенною рідиною (кров, жирова тканина чи СР) (рис. 12);
б) гострий тендиніт:
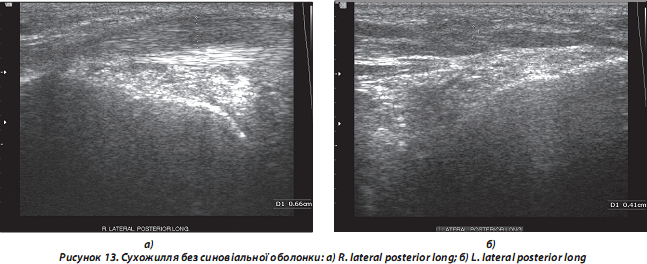
— сухожилля без СО: потовщені, ехогенність останніх знижена локально/дифузно. Ехоструктура неоднорідна, з наявністю дрібних гіпоехогенних ділянок, що нагадують мікророзриви, значним посиленням кровотоку за ходом сухожильних волокон при поздовжньому скануванні (рис. 13);
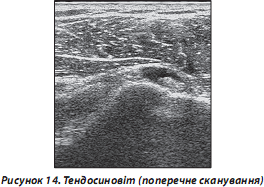
— сухожилля з СО: потовщені, їх ехоструктура, як правило, не змінена, в більшості випадків спостерігаються явища тендосиновіту (наявність анехогенної ділянки, обмеженої контуром СО, — рідини, що свідчить про запальний процес vaginae tendinum) (рис. 14);
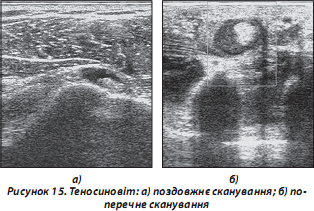
в) хронічний тендиніт: частіше спостерігається в сухожиллях надколінка, ротаторної манжети, ахілловому сухожиллі (рис. 15):
— сухожилля без СО: потовщені, ехоструктура неоднорідна, іноді наявні гіперехогенні включення — ділянки фіброзу чи кальцифікатів уздовж сухожильних волокон;
— сухожилля з СО: потовщені, можливі зміни ехоструктури (частіше — зниження ехогенності), часто — помірні явища теносиновіту з накопиченням незначної кількості рідини;
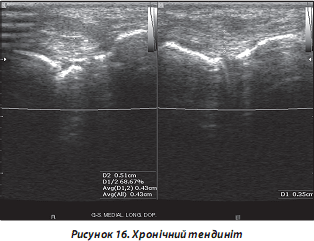
— кальцифікуючий тендиніт: виникає частіше в сухожиллях верхньої кінцівки на фоні системних захворювань сполучної тканини та метаболічних розладів (наприклад, подагра та метаболічні артропатії). При УЗД виявляються гіперехогенні включення (найчастіше — мінімальні (крапчасті), іноді — більші) в сухожиллях; останні часто потовщені (рис. 16);
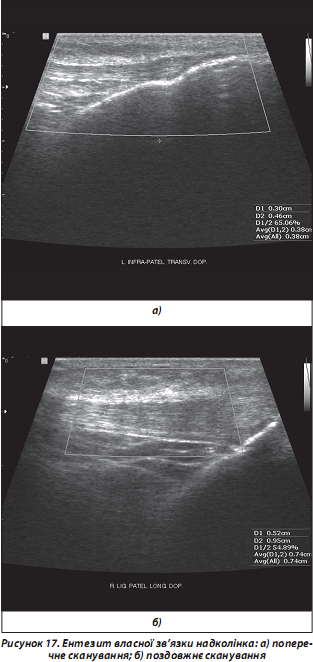
г) ентезити та ентезопатії. Досвід ревматологів-клініцистів свідчить, що упродовж тривалого часу ентезити (запалення ентезів — місць прикріплення до кістки зв’язок, сухожиль, апоневрозів, суглобових капсул) можуть бути єдиними клінічними ознаками РЗ у дебюті їх розвитку, а також передують розвитку синовітів суглобів нижніх кінцівок у хворих на РА та АС (рис. 17) [Коваленко В.Н., Борткевич О.П., 2004; Рекалов Д.Г., Борткевич О.П., 2011; McGonagle D. et al., 1998].
Таким чином, УЗД є набагато інформативнішим методом ранньої діагностики захворювань опорно-рухового апарату порівняно зі стандартним рентгенологічним до-слідженням.
3. Патологія суглобових сумок (бурсити):
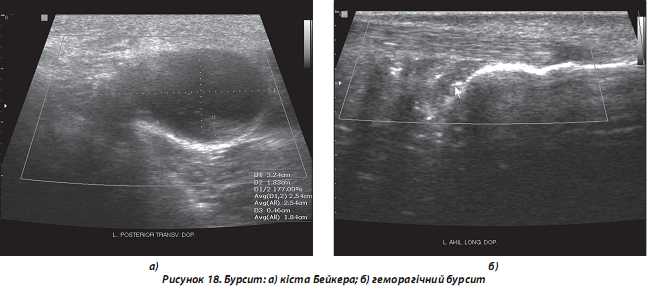
а) гострий та хронічний бурсит: частіше спостерігаються у верхньому та задньому заворотах колінного суглоба, міжфасціальних просторах гомілки (особливо при розриві кісти Бейкера) (рис. 18а), субакроміально-субдельтоподібній, ліктьовій, позап’ятковій сумках; рідше спостерігаються інші локалізації бурситів. УЗ-ознаки — збільшення розмірів сумки, анехогенна зона в проекції ураженої сумки (наявність вільної рідини), обмежена гіперехогенною оболонкою (стінка сумки);
б) геморагічний бурсит: виникає внаслідок прямої/непрямої травми даної ділянки, розриву прилеглого сухожилля/сухожиль, перелому кісток, патології згортання крові тощо. УЗ-ознаки: розміри суглобової сумки більші, ніж при звичайному гострому бурситі, стадійність змін ехоструктури вільної рідини в порожнині сумки швидка (див. нижче диференційні ознаки гострого та хронічного бурситу) (рис. 18б).
Диференційними УЗ-ознаками гострого та хронічного бурситу є:
1. Товщина стінки сумки (при гострому бурситі стінки тонкі, при хронічному — товсті, досить часто з нерівними контурами).
2. Особливості ехоструктури рідини в порожнині сумки (при гострому бурситі — гомогенна анехогенна, при хронічному часто негомогенна, з наявністю ехопозитивних включень різного розміру та ехощільності), рухомих при проведенні функціональних проб.
3. Наявність васкуляризації при допплерівському дослідженні (при гострому бурситі найчастіше кровотік у стінці сумки відсутній, при хронічному спостерігається часто).
4. Патологія підшкірно-жирової клітковини:
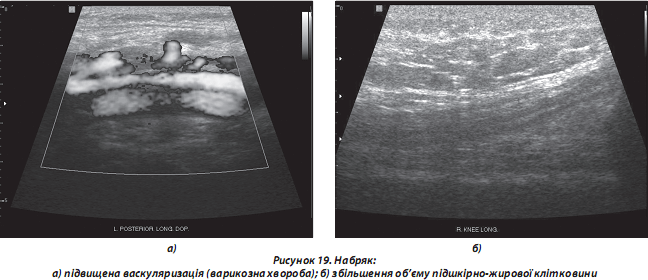
а) набряк спостерігається при запальному процесі (артрити, періартрит тощо), хронічній серцевій та венозній недостатності, лімфедемі, целюліті тощо). При УЗ-дослідженні визначають збільшення об’єму ПЖК, зміни ехогенності (найчастіше суттєва гіпоехогенність сполучнотканинних фіброзних перегородок на фоні відносно гіперехогенних прошарків жирової тканини) (рис. 19);
б) локальні патологічні утворення при ревматичних захворюваннях (зокрема, ревматоїдні вузлики при РА, вузлуваті утворення, переважно в м’яких тканинах гомілки, при вузлуватій еритемі, депозити при подагрі та метаболічних артропатіях), сторонні тіла тощо.
5. Патологія суглобів:
а) випіт у порожнину суглоба (рис. 20);
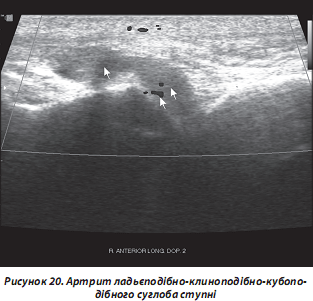
б) гіпертрофія синовіальної оболонки (рис. 21);
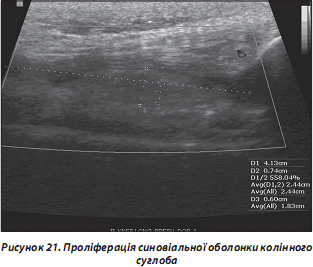
в) кровотік у синовіальній оболонці (рис. 22);
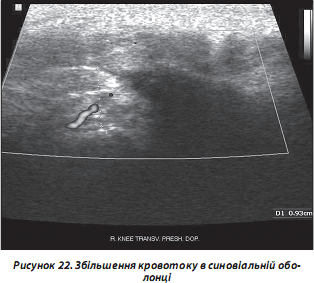
г) зміни кортикального шару кісткових суглобових поверхонь (ерозивні, дегенеративні, зокрема остеофітоз; пухлинні ураження; патологія періосту, у тому числі при остеомієліті; переломи/тріщини тощо) (рис. 23);
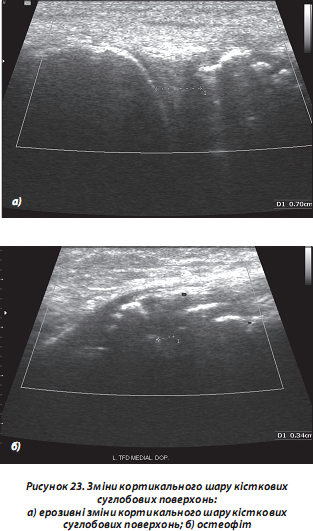
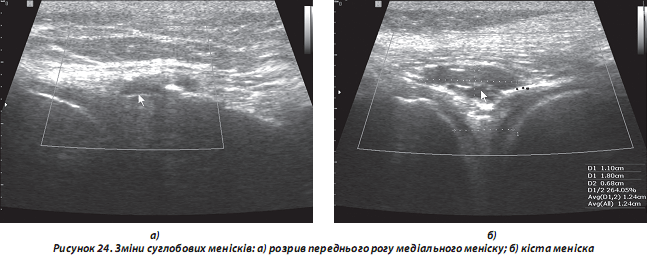
д) зміни суглобового хряща, менісків (зокрема, часткові та повні розриви), судин та інших м’якотканинних структур (рис. 24);
У наступній статті цього розділу серії будуть наведені принципи та методики дослідження окремих суглобів з наголосом на функціональні проби, що дозволяють проводити диференційну діагностику окремих ревматологічних нозологічних форм, зокрема, РА, ОА та інших хвороб кістково-м’язової системи та системних захворювань сполучної тканини.
1. Аллан П.Л. Клінічна допплерівська ультрасонографія: Пер. з англ. — Львів: Медицина світу, 2001. — 293 с.
2. Рекалов Д.Г., Борткевич О.П. Ранні інструментальні маркери ревматоїдного артриту як предиктори прогресування хвороби // Укр. мед. часопис. — 2011. — 4(84), VII–VIII. — С. 104-107.
3. Коваленко В.М., Шуба Н.М. та ін. Ультразвукове дослідження опор- но-рухового апарата: Метод. рекомендації. — К., 2008. — 40 с.
4. Шманько О.В. Предиктори розвитку ревматоїдного артриту у хворих із недиференційованим суглобовим синдромом // Ліки України. — 2003. — 1(5). — С. 61-64.
5. Борткевич О.П. Прогресування локальних змін кісткової тканини суглобів у хворих на ранній ревматоїдний артрит і прогнозування його перебігу // Укр. ревматол. журнал. — 2003. — 3(13). — С. 62-68.
6. Борткевич О.П., Терзов К.А. Оценка поражения суставов кистей у больных ранним ревматоидным артритом // Укр. ревматол. журнал. — 2005. — 2(20). — С. 45-48.
7. Ивашкин В.Т., Султанов В.К. Болезни суставов. Пропедевтика, дифференциальный диагноз, лечение. — М.: Литерра, 2005. — 544 с.
8. Коваленко В.Н., Борткевич О.П. Значение клинических и инструментальных методов в диагностике энтезитов у больных анкилозирующим спондилоартритом // Укр. ревматол. жур- нал. — 2004. — 1(15). — С. 45-48.
9. Коваленко В.М., Шуба Н.М. Номенклатура, класифікація, критерії діагностики та програми лікування ревматичних хвороб. — К.: Зовнішторгвидав України, 2004. — 156 с.
10. Коваленко В.Н., Борткевич О.П. Остеоартроз: Практическое руко- водство. — К.: Морион, 2005. — 2-е изд., перераб. и доп. — 592 с.
11. Коваленко В.Н., Шуба Н.М., Шолохова Л.Б., Борткевич О.П. Ревматоидный артрит. Диагностика и лечение. — К.: Морион, 2001. — 272 с.
12. Михайлов Е.Е., Беневоленская Л.И., Аникин С.Г. Частота переломов проксимального отдела бедренной кости и дистального отдела предплечья среди городского населения России // Остеопороз и остеопатии. — 1999. — 1. — С. 18-20.
13. Насонова В.А., Бунчук Н.В. Ревматические болезни. — M.: Медицина, 1997. — С. 268-268.
14. Рекалов Д.Г., Борткевич О.П. Ранні інструментальні маркери ревматоїдного артриту як предиктори прогресування хвороби // Укр. мед. часопис. — 2011. — 4(84), VII/VIII. — С. 104-107.
15. Тер-Вартаньян С.Х., Яременко О.Б., Худина В.С. Локальная инъекционная терапия при поражениях суставов и периартикулярных тканей. — К.: Книга-плюс, 1997. — С. 51-53.
16. Терзов К.А., Масик О.М., Борткевич О.П. Роль ультразвукового дослідження в оцінці уражень колінних суглобів у хворих на ревматоїдний артрит // Український ревматологічний журнал. — 2006. — 1(23). — 57-61.
17. Alasaarela E., Takalo R., Tervonen O. et al. Sonography and MRI in the evaluation of painful arthritic shoulder // Br. J. Rheumatol. — 1997. — 36. — Р. 996-1000.
18. Alassaarela E., Suramo I., Tervonen O. et al. Evaluation of humeral head erosions in rheumatoid arthritis: a comparison of ultrasonography, magnetic resonance imaging, computed tomography and plain radiography // Br. J. Rheumatol. — 1998. — 37. — Р. 1152-1156.
19. Backhaus M., Burmester G.-R., Gerber T. et al. Guidelines for musculoskeletal ultrasound in rheumatology // Ann. Rheum. Dis. — 2001. — 60. — Р. 641-649.
20. Beltran J., Caudil J.L., Herman L.A. et al. Rheumatoid arthritis: MR imaging manifestations // Radiology. — 1998. — 165. — Р. 153-157.
21. Boers M., Kostense P.J., Verhoeven A.C., van der Linden S. Inflammation and damage in an individual joint predict futher damage in that joints in patients with early rheumatoid arthritis // Arthritis Rheum. — 2001. — 44. — Р. 2242-2246.
22. Breedveld F.C., Dijkmans B.A. Differential therapy in early and late stages of rheumatoid arthritis // Curr. Opin. Rheumatol. — 1996. — 8. — Р. 226-229.
23. EULAR: Working Party on Imaging in Rheumatology (2005). http://www.doctor33.it/eular/fr_references.asp
24. Hau M., Schultz H., Tony H.-P. et al. Evaluation of pannus and vascularization of the metacarpophalangeal and proximal interphalangeal joints in rheumatoid arthritis by high-resolution ultrasound (multidimensional linear array) // Arthritis & Rheumatism. — 1999. — 42(11). — Р. 2303-2308.
25. Kellgren J.H., Lawrence J.S. Radiological assessment of rheumatoid arthritis // Ann. Rheum. Dis. — 1957. — 16. — Р. 485-493.
26. Martinoli C., Bianchi S., Prato N. et al. US of the shoulder: non-rotator cuff disorders // Radiographics. — 2003. — 23(2). — Р. 381-401.
27. McGonagle D., Gibbon W., Emery P. Classification of inflammatory arthritis by enthesitis // Lancet. — 1998. — 352. — Р. 1137-1140.
28. Petersson C.J. Painful shoulders in patients with rheumatoid arthritis // Scand. J. Rheumatol. — 1986. — 15. — Р. 275-279.
29. Thompson P.W., Silman A.J., Kirwan J.R., Currey H.L.F. Articular indices of joint inflammation in rheumatoid arthritis: correlation with acute-phase response // Arthritis & Rheumatism. — 1987. — 30. — Р. 618-623.
30. Van Holsbeck M.T., Kolowich P.A., Eyler W.R. et al. US depiction of partial-thickness of the rotator cuff // Radiology. — 1995. — 197.— Р. 443-446.