Журнал «» 6(20) 2011
Вернуться к номеру
Контроль добового профілю артеріального тиску за допомогою нового блокатора рецепторів ангіотензину II олмесартану у хворих на гіпертонічну хворобу, що перебігає в межах метаболічного синдрому
Авторы: Мисниченко О.В., Коваль С.М., Інститут терапії ім. Л.Т. Малої НАМН України, м. Харків
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Версия для печати
Метою роботи було вивчення ефективності олмесартану у хворих на гіпертонічну хворобу (ГХ), що перебігає в межах метаболічного синдрому (МС), на підставі аналізу впливу цього препарату на показники добового моніторування артеріального тиску (АТ). Обстежено 54 хворі на ГХ 1–2-го ступеня з МС у віці 34–66 років (чоловіків — 24, жінок — 30). Встановлено, що олмесартан демонструє значну антигіпертензивну дозозалежну ефективність у вигляді монотерапії в даної категорії хворих, що належать до груп високого та дуже високого серцево-судинного ризику. Олмесартан вірогідно знижує середньодобові, середньоденні та середньонічні рівні і систолічного, і діастолічного АТ, навантаження тиском протягом усієї доби, варіабельність АТ та величину і швидкість дуже небезпечного у плані розвитку серцево-судинних ускладнень ранкового підйому АТ у цих хворих. Олмесартан нормалізує патологічний профіль АТ — non-dipper. Терапія олмесартаном не викликала негативних метаболічних змін і порушень функції нирок.
Гіпертонічна хвороба, метаболічний синдром, блокатор рецепторів ангіотензину ІІ, олмесартан, добовий профіль артеріального тиску.
Наприкінці XX століття з’явився принципово новий клас антигіпертензивних засобів — блокатори рецепторів ангіотензину ІІ (БРА ІІ), або сартани [8, 9, 22]. Концентрація уваги вчених на блокаді ефектів А ІІ обумовлена великою кількістю накопичених експериментальних та клінічних даних про ключову роль ренін-ангіотензинової системи (РАС), і в першу чергу А ІІ у становленні, прогресуванні гіпертонічної хвороби (ГХ), а також розвитку її тяжких ускладнень — серцевої недостатності (СН), хронічної ниркової недостатності, мозкового інсульту, інфаркту міокарда.
До відкриття БРА II використовували блокаду А ІІ шляхом пригнічення активності ангіотензинперетворюючого ферменту (АПФ) за допомогою інгібіторів АПФ (ІАПФ). Проте ІАПФ не здатні повністю блокувати синтез А ІІ. Крім того, у 10–12 % хворих, які приймають ІАПФ, виникає такий побічний ефект, як сухий кашель (перш за все за рахунок підвищення утворення брадикініну), що змушує припиняти терапію цими препаратами [4, 7]. БРА ІІ проявляють свою інгібіторну активність на рецепторному рівні — усі вони селективно блокують рецептори 1-го типу для А ІІ і таким чином найбільш повно пригнічують ефекти А ІІ незалежно від шляху його утворення. Однією з найважливіших властивостей препаратів цієї групи на відміну від інших препаратів першої лінії є мінімальна кількість побічних ефектів, порівнянна з плацебо, і в тому числі відсутність кашлю [7–9].
До сьогодні на ринку України було представлено шість БРА ІІ. За останній рік до клінічної практики увійшов новий представник цієї групи — олмесартан [1, 5]. По цілому ряду параметрів олмесартан є унікальним представником БРА ІІ. Олмесартан на відміну від усіх інших БРА ІІ зв’язується з двома сайтами рецепторів 1-го типу для А ІІ, що обумовлює його найбільш тривалу інгібуючу дію [6, 12]. Крім того, цей препарат (а також і інший представник БРА II кандесартан) проявляє найбільшу афінність до рецепторів 1-го типу для А ІІ серед препаратів групи сартанів. Олмесартан не взаємодіє з системою цитохрому Р450, що дає можливість його комбінування зі значною кількістю препаратів, які метаболізуються за допомогою цієї системи (варфарин, дигоксин, статини тощо) [1, 7, 10]. Олмесартан при пероральному застосуванні практично повністю всмоктується зі шлунково-кишкового тракту. Олмесартан проявляє дозозалежну дію, і його антигіпертензивна ефективність вірогідно вища за таку в деяких інших сартанів [7, 20, 21]. Олмесартан має виражені органопротекторні ефекти при ГХ — ренопротекторний і кардіопротекторний [1, 6, 7, 10, 21]. Ці ефекти в цілому притаманні сартанам. Важливими особливостями олмесатрану є його суттєвий антиатерогенний ефект і найбільш виражена серед інших сартанів протизапальна дія [5, 6, 10, 12, 20]. З урахуванням наведених даних новий сартан (олмесартан) викликає дуже великий науковий і практичний інтерес у плані його застосування для лікування хворих на ГХ із різними клінічними особливостями й варіантами перебігу та можливості більш ефективної профілактики серцево-судинних і ниркових ускладнень.
Одним із дуже поширених і прогностично несприятливих варіантів перебігу ГХ є її поєднання з МС. Для цієї категорії хворих притаманні значні патогенетичні і клінічні особливості [2, 4]. Лікування хворих на АГ в межах МС потребує диференційованого підходу до вибору антигіпертензивних препаратів, що з найбільшою вірогідністю можуть покращити прогноз захворювання.
У зв’язку з вищевикладеним метою даного дослідження було вивчення клінічної ефективності олмесартану у хворих на ГХ, що перебігає в межах МС, на підставі поглибленого аналізу впливу цього препарату на показники добового моніторування артеріального тиску (ДМАТ).
Матеріали та методи
Всього було обстежено 54 хворих на ГХ II стадії 1–2-го ступеня (м’яка та помірна форми) (за класифікацією Української асоціації кардіологів 2008 року) [3, 4] віком 34–66 років (середній вік становив 49 ± 3 роки). Чоловіків було 24, жінок — 30.
Серед обстежених хворих ГХ 1-го ступеня діагностована у 30 хворих (56 %), 2-го ступеня — у 24 хворих (44 %). Середня тривалість захворювання в групі хворих становила 9,7 ± 1,1 року. У 32 хворих (78 %) виявлена обтяжена спадковість за ГХ.
У всіх обстежених хворих ГХ перебігала на фоні МС. Наявність МС у хворих встановлювали відповідно до рекомендацій Української асоціації кардіологів (2008) при виявленні трьох і більше з наведених критеріїв:
— окружність талії (ОТ) > 94 см у чоловіків і ОТ > 80 см у жінок;
— сироваткові тригліцериди (ТГ) ≥ 1,7 ммоль/л;
— холестерин (ХС) ліпопротеїдів високої щільності (ЛПВЩ) < 1,03 ммоль/л у чоловіків і < 1,29 ммоль/л у жінок;
— артеріальний тиск (АТ) ≥ 130/85 мм рт.ст.;
— глюкоза плазми крові ≥ 5,6 ммоль/л.
У даному дослідженні у 39 (72 %) хворих був виявлений 4-компонентний МС та у 15 (28%) хворих — 5-компонентний МС.
В обстеженій групі хворих на ГХ із МС у 22 осіб (41 %) виявлена ішемічна хвороба серця (ІХС). Серед них у 16 (30%) хворих була діагностована стабільна стенокардія I–II функціональних класів.
СН зі збереженою систолічною функцією була діагностована у 20 хворих (37 %) (I функціонального класу — у 9 хворих (17 %), II функціонального класу — у 11 хворих (20 %).
Обстежені хворі були стратифіковані за ступенем ризику серцево-судинних ускладнень відповідно до рекомендацій Української асоціації кардіологів 2008 року [3, 4]. За ступенем указаного ризику ускладнень хворі розподілялись наступним чином: високий ризик виявлявся у 38 хворих (70 %), дуже високий ризик — у 16 хворих (30 %). Хворих із низьким та помірним ризиком серед обстежених осіб не виявлено.
У дослідження не включали хворих на симптоматичну АГ, хворих на цукровий діабет, із гострими запалювальними процесами, гострим коронарнимсиндромом, перенесеним інфарктом міокарда, стабільною стенокардію та СН високих градацій, захворюваннями нирок, печінки, крові.
Всім хворим проводили загальноприйняті клініко-лабораторні та інструментальні обстеження для діагностики стадії й форми ГХ. Вивчали показники ліпідного спектра сироватки крові: рівні загального ХС, ТГ, ХС ліпопротеїнів низької, дуже низької (ХС ЛПНЩ, ХС ЛПДНЩ) та ХС ЛПВЩ, вміст у сироватці крові глюкози натще ферментним засобом на фотометрі-аналізаторі Humareader N 2106 (Німеччина).
Морфофункціональні параметри лівого шлуночка оцінювали методом ехокардіографії на апараті ALOKA-SSD-280 (Японія) у режимі М-сканування за загальноприйнятою методикою (Н.М. Мухарлямов, Ю.Н. Беленков, 1974). Вивчались такі показники: кінцево-систолічний розмір (КСР), кінцево-діастолічний розмір (КДР), кінцево-систолічний об’єм (КСО), кінцево-діастолічний об’єм (КДО) лівого шлуночка (ЛШ), фракція вигнання (ФВ), фракція скорочення (ФС), середня швидкість скорочення волокон міокарда (V), товщина міжшлуночкової перегородки та задньої стінки (ТМШП та ТЗС) ЛШ. Індекс відносної товщини стінок (ВТС) ЛШ визначали за формулою ІВТС = (ТМШП + ТЗС ЛШ/КДР). Масу міокарда ЛШ (ММЛШ) розраховували за формулою: 1,04 х [(ТМШП + ТЗСЛШ + КДР)3 – (КДР)3] — 13,6 [11], індекс ММЛШ (ІММЛШ) визначали як відношення ММЛШ до площі поверхні тіла. За верхню межу норми ІММЛШ вважали 104 г/см2 для жінок та 117 г/см2 для чоловіків [11].
ДМАТ проводили за допомогою системи амбулаторного моніторування АТ (ABPM-4) фірми Meditech (Угорщина). Вивчали середньодобові, середньоденні, середньонічні САТ та ДАТ, варіабельність САТ і ДАТ за стандартом відхилення від середньої за добу (STD), ступінь зниження нічного САТ і ДАТ за добовим індексом (ДІ САТ, ДІ ДАТ). Інтерпретацію даних проводили з урахуванням існуючих рекомендацій [3, 4, 24].
Усі 54 хворі отримували олмесартан (препарат Кардосал) у вигляді монотерапії, одноразово на добу, вранці, у дозі 20 мг протягом 3 тижнів. При неефективності початкової дози її збільшували до 40 мг/добу з тривалістю прийому 5 тижнів. Терапію вважали ефективною при зниженні САТ менше 140 мм рт.ст., ДАТ — нижче 90 мм рт.ст. Тривалість лікування становила 8 тижнів.
Статистичну обробку даних проводили за допомогою програми Statistica 6,0. Дані наведені у вигляді M ± m. Відмінності між групами вважали вірогідними при р < 0,05.
Результати
У результаті дослідження встановлена висока антигіпертензивна ефективність монотерапії олмесартаном у добових дозах 20–40 мг у хворих на ГХ у поєднанні з МС. Так, виявлене вірогідне зниження середніх по групі рівнів САТ і ДАТ в обстежених хворих після завершення курсу терапії олмесартаном (табл. 1). Результати дослідження свідчили про те, що середнє зниження по групі хворих на ГХ із МС рівня САТ було 23 ± 2 %, рівня ДАТ — 14 ± 2 %.
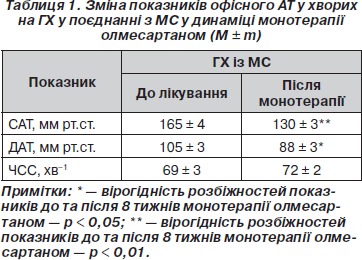
Встановлено, що монотерапія олмесартаном дозволила досягнути цільових рівнів офісного АТ в більшості обстежених хворих при добовій дозі як 40 мг, так і 20 мг. Зокрема, частота досягнення цільових рівнів офісного АТ у хворих при добовій дозі олмесартану 20 мг становила 61 %, при збільшенні добової дози до 40 мг — 76 %. При цьому не було встановлено вірогідної різниці в ефективності олмесартану залежно від статі, віку хворих, наявності спадкової схильності до ГХ та ступеня серцево-судинного ризику ускладнень. Однак треба відмітити певну особливість у вираженості антигіпертензивної дії препарату у хворих із великою тривалістю ГХ — понад 10 років (таких у дослідженні було 17 осіб). У таких хворих цільові рівні офісного АТ досягались тільки при добовій дозі олмесартану 40 мг.
Олмесартан добре переносився хворими на ГХ. Вже в перші дні прийому олмесартану хворі відзначали суттєве покращення самопочуття: значно зменшились головні болі, запаморочення, серцебиття, зменшувалась загальна слабкість, покращився сон. Зниження АТ не супроводжувалось розвитком рефлекторної тахікардії.
З метою деталізації особливостей та вираженості антигіпертензивної ефективності монотерапії олмесартаном у хворих на ГХ у поєднанні з МС у роботі було проведено ДМАТ у динаміці 8-тижневого лікування.
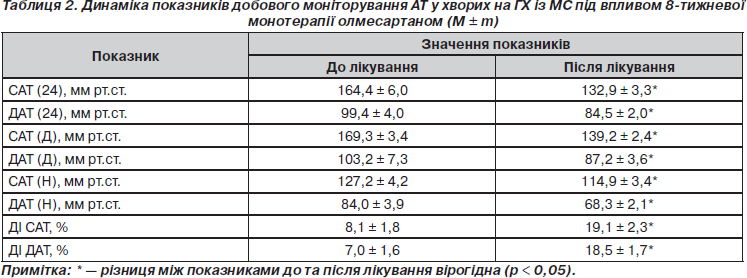
При аналізі даних ДМАТ у хворих на ГХ із МС після завершення курсу монотерапії олмесартаном у добових дозах 20–40 мг виявлено вірогідне зниження середньодобових, середньоденних та середньонічних САТ та ДАТ у цілому по групі (табл. 2). Цільові рівні середньодобових рівнів САТ і ДАТ під впливом монотерапії олмесартаном у добовій дозі 40 мг досягались у 72 % хворих при 8-тижневій терапії.
Встановлено, що за абсолютними значеннями зниження рівнів САТ було вірогідно вищим за ДАТ як у цілому за добу (d САТ –25, 4 ± 3,5 мм рт.ст., d ДАТ — 12, 4 ± 2,5 мм рт.ст., р < 0,05), так і за денні години (d САТ –28,6 ± 3,1 мм рт.ст., d ДАТ — 15,1 ± 2,3 мм рт.ст., р < 0,05), і за нічні (d САТ –12,0 ± 2,2 мм рт.ст., d ДАТ — 10,3 ± 2,0 мм рт.ст., р < 0,05). Крім того, наведені дані свідчать про те, що абсолютні середні значення зниження АТ (і САТ, і ДАТ) у денні години були вірогідно вищі за такі вночі.
Окремо треба відмітити зміни в ДМАТ у хворих на ГХ, які до початку лікування належали до групи циркадного ритму non-dipper (недостатнє зниження АТ в нічні часи). Терапія олмесартаном у таких хворих призводила до нормалізації порушень добового профілю в 91 % випадків і вірогідного підвищення добового індексу САТ і ДАТ, що свідчить про суттєве й вірогідне зниження нічних рівнів САТ і ДАТ під впливом олмесартану. Дані про вплив олмесартану на ДІ в цілому по групі хворих наведені в табл. 2.
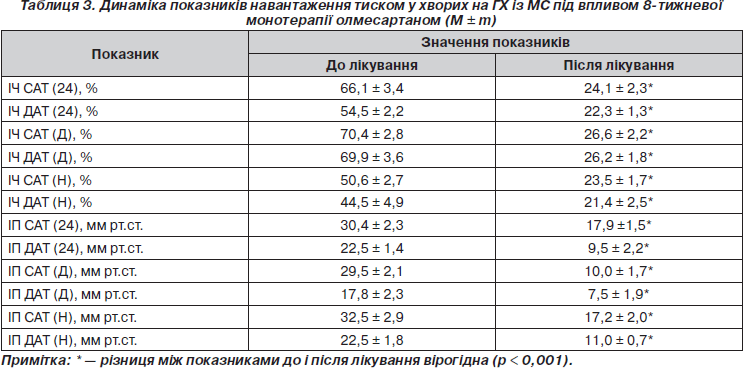
У результаті роботи встановлено, що лікування олмесартаном призвело до статистично значимого зменшення показників навантаження тиском у хворих на ГХ та МС. Було виявлено вірогідне зниження обох показників, що характеризують навантаження тиском, — індексу часу і нормованого індексу площі (табл. 3). Так, індекс часу САТ (24) зменшився на 36,2 ± 2,7 % (р < 0,001), індекс часу ДАТ (24) — на 31,2 ± 1,7 % (p < 0,001). Нормований індекс площі (ІП) САТ (24) і ДАТ (24) також вірогідно змінилися: d ІП CАТ (24) –12,5 ± 2,2 мм рт.ст., p < 0,001; d ІП ДАТ (24) –13,0 ± 1,5 мм рт.ст., p < 0,001.
Зниження показників навантаження тиском у хворих на ГХ, що перебігає на фоні МС, у динаміці монотерапії олмесартаном вказує не тільки на те, що цей препарат призводить до вірогідного зниження середніх значень САТ і ДАТ у цілому по групі хворих, але й нормалізує в першу чергу АТ у періоди його найбільшого підвищення або просто підвищення над рівнем нормального. При цьому такий вплив олмесартану простежується і в денні, і в нічні години.
Важливим показником ДМАТ, збільшення якого пов’язане з підвищенням ризику серцево-судинних катастроф, є збільшення ступеня вираженості ранкового підйому АТ. У проведеному дослідженні під впливом олмесартану ступінь ранкового підйому САТ зменшився з 36,4 ± 3,8 мм рт.ст. до 17,5 ± 3,2 мм рт.ст. (p < 0,001), ДАТ — з 30,7 ± 2,9 мм рт.ст. до 19,3 ± 3,0 мм рт.ст. (p < 0,01). При цьому відмічене і паралельне зниження швидкості ранкового підйому САТ з 14,7 ± 1,1 мм рт.ст. на годину до 8,5 ± 0,8 мм рт.ст. на годину (p < 0,001) і ДАТ — з 11,1 ± 1,0 мм рт.ст. на годину до 7,2 ± 0,9 мм рт.ст. на годину (p < 0,05). У цілому по групі зниження величини ранкового підвищення САТ і ДАТ до нормальних показників виявлено у 72 % хворих.
Ще одним показником, що може виявлятися при ДМАТ і значимо впливає на прогноз хворих, є величина варіабельності САТ і ДАТ за добу. У цілому ряді досліджень показано зростання ризику прогресування ГХ і ризику її ускладнень при підвищенні показника варіабельності АТ [4, 6, 19]. У даній роботі було встановлено вірогідне зниження варіабельності і САТ, і ДАТ під впливом тривалої терапії олмесартаном. Так, в обстежених хворих на ГХ із МС у цілому по групі в динаміці лікування олмесартаном показник варіабельності САТ вірогідно знизився з 18,1 ± 3,0 мм рт.ст. до 13,3 ± 2,1 мм рт.ст. (р < 0,05), а показник варіабельності ДАТ — з 16,3 ± 3,7 мм рт.ст. до 11,5 ± 2,8 мм рт.ст. (р < 0,05).
Під впливом монотерапії олмесартаном в обстежених хворих на ГХ у поєднанні з МС не було виявлено погіршення показників, що характеризують морфофункціональні параметри серця за даними ехокардіографії.
Олмесартан також не впливав негативно на параметри ліпідного та вуглеводного обмінів, на функцію нирок у хворих, які проходили дане дослідження.
Слід особливо відзначити, що під час 8-тижневої монотерапії олмесартаном не виявлено будь-яких побічних ефектів і жоден із хворих не відмовився від прийому препарату.
Таким чином, олмесартан проявляє суттєву антигіпертензивну ефективність у лікуванні хворих на ГХ у поєднанні з МС вже у вигляді монотерапії. Спостерігається дозозалежний ефект олмесартану в межах добових доз від 20 до 40 мг.
Треба відзначити, що обстежені хворі на ГХ із МС хоча й мали за показниками АТ 1–2-го ступеня (або м’яку та помірну АГ), все-таки належали до пацієнтів із високим і дуже високим серцево-судинним ризиком. Ці хворі вже мали множинні фактори ризику у вигляді МС, більше ніж третина з них мали ІХС у вигляді стабільної стенокардії I–II функціонального класу і СН I–II функціонального класу зі збереженою систолічною функцією, також більш ніж у третини хворих захворювання перебігало тривалий час — понад 10 років. Тобто обстежені пацієнти належали до однієї з найбільш поширених груп хворих на ГХ. У зв’язку з цим встановлені дані про достатню ефективність олмесартану навіть при монотерапії мають дуже суттєве практичне значення.
Отримані у проведеному досліджені дані про виражену ефективність олмесартану при м’якій та помірній ГХ, у тому числі і в поєднанні з метаболічними порушеннями, порівнянні з результатами ряду закордонних досліджень: OLMEPAS, The OlmeTelstudy, Oparil study, Brunner study, а також із результатами метааналізу, що включав 7 рандомізованих подвійних сліпих досліджень у США [6, 11, 14–16]. Крім того, у ряді закордонних порівняльних досліджень з іншими антигіпертензивними препаратами було виявлено, що олмесартан вірогідно більш ефективний, ніж бета-адреноблокатор атенолол, антагоністи кальцію амлодипін, фелодипін і нітрендипін, ІАПФ каптоприл та БРА II лозартан, кандесартан, валсартан і ірбесартан [13, 18, 19, 23]. З огляду на результати наведених досліджень отриманий у проведеній роботі досить виражений антигіпертензивний ефект монотерапії олмесартаном знаходить пояснення.
Важливу додаткову нову інформацію дають результати даного дослідження про виражений позитивний та нормалізуючий вплив олмесартану на показники ДМАТ. За отриманими даними, олмесартан вірогідно знижує середньодобові, середньоденні та середньонічні рівні і САТ, і ДАТ, виражено зменшує навантаження тиском протягом усієї доби, варіабельність АТ та гальмує величину дуже небезпечного в плані розвитку серцево-судинних ускладнень ранкового підйому АТ. У цілому олмесартан здатний нормалізовувати патологічні добові профілі АТ, зокрема один із найбільш небезпечних — профіль non-dipper.
Встановлені дані про значне й вірогідне зниження середніх добових, денних і нічних показників САТ і ДАТ, показників навантаження тиском у денні та нічні години підтверджують результати досліджень, які свідчать про тривалу 24-годинну дію цього препарату [17, 19]. Той факт, що олмесартан вірогідно більш виражено знижував середньоденні показники АТ і навантаження тиском теж у денні години порівняно з нічними, може бути обумовлений досягненням його максимальної антигіпертензивної дії через 6–8 годин після приймання [6, 7]. А треба зауважити, що у проведеному дослідженні олмесартан призначався одноразово на добу у всіх хворих в одну й ту саму годину — о 8-й годині ранку.
Виявлені дані щодо вірогідного зниження ступеня та вираженості ранкового підйому САТ і ДАТ під впливом олмесартану поряд з указаним вище вірогідним зниженням середньодобових показників АТ та навантаження тиском, напевне, ще більшою мірою демонструють вираженість тривалої 24-годинної антигіпертензивної активності цього представника БРА II [6, 19].
Важливе значення для можливості тривалої терапії олмесартаном мають виявлені в роботі відсутність рефлекторної тахікардії та дуже гарна переносимість препарату, практична відсутність побічних ефектів, відсутність негативного впливу на ліпідний спектр, рівні глікемії, пуринового обміну, функцію нирок.
Таким чином, результати проведеного дослідження підтверджують уже сформовані на підставі багатьох закордонних робіт великі перспективи олмесартану в довготривалому лікуванні хворих на ГХ із різними метаболічними факторами й різним серцево-судинним ризиком ускладнень без погіршення в цілому якості життя.
Висновки
Новий блокатор рецепторів А ІІ олмесартан демонструє значну антигіпертензивну ефективність у вигляді монотерапії у хворих на ГХ 1–2-го ступеня в поєднанні з МС, що при стратифікації їх серцево-судинного ризику належать до груп високого та дуже високого ризику.
Олмесартан проявляє виражену дозозалежну антигіпертензивну активність. Цільові рівні офісного АТ у групі хворих на ГХ 1–2-го ступеня з МС досягаються в 61 % при добовій дозі олмесартану 20 мг та в 76 % при добовій дозі 40 мг.
Олмесартан у хворих на ГХ 1–2-го ступеня в поєднанні з МС за даними ДМАТ вірогідно знижує середньодобові, середньоденні та середньонічні рівні САТ і ДАТ, показники навантаження тиском як для САТ, так і для ДАТ, нормалізує патологічний добовий профіль АТ — non-dipper. Цільові рівні середньодобових рівнів САТ і ДАТ під впливом монотерапії олмесартаном у добовій дозі 40 мг досягались у 72 % хворих при 8-тижневій терапії.
Застосування монотерапії олмесартаном у хворих на ГХ 1–2-го ступеня з МС у цілому по групі дозволило вірогідно знизити показники варіабельності САТ і ДАТ, а також зменшити величину та швидкість ранкового підвищення АТ у групі хворих із його надмірним підйомом.
Монотерапія олмесартаном у хворих на ГХ 1–2-го ступеня в поєднанні з МС не призводила до негативних змін у показниках ліпідного, вуглеводного та пуринового обмінів, не погіршувала функціональний стан нирок і супроводжувалась мінімальною частотою побічних ефектів.
1. Березин А.Е. Клиническая эффективность и безопасность применения олмесартана — нового антагониста рецепторов к ангиотензину II — у пациентов с артериальной гипертензией // Український медичний чисопис. — 2009. — № 3 (71), 5/6. — С. 1-6.
2. Митченко Е.И. Метаболический синдром, диабет и сердечно-сосудистые заболевания // Руководство по кардиологии / Под ред. В.Н. Коваленко — К.: МОРИОН, 2008. — С. 228-243.
3. Рекомендації Української асоціації кардіологів з профілактики та лікування артеріальної гіпертензії. Посібник до Національної програми профілактики і лікування артеріальної гіпертензії. — Київ, 2008. — 86 с.
4. Свищенко Е.П., Безродная Л.В. Эссенциальная артериальная гипертензия // Руководство по кардиологии / Под ред. В.Н. Коваленко — К.: МОРИОН, 2008. — С. 444-480.
5. Cиренко Ю.Н., Рековец О.Л. Роль олмесартана в лечении артериальной гипертензии // Артериальная гипертензия. — 2009. — № 2(4). — С. 48-58.
6. Brunner H.R., Stumpe K.O., Junuszewicz A. Antihypertensive efficacy of olmesartan medoxomil and candesartan cilexitil assessed by 24-hour ambulatory blood preasure monitoring in patients with essential hypertension // Clin. Drug. Invest. — 2003. — V. 23. — Р. 419-430.
7. Csajka C., Buclin T., Brunner H.R., Biollaz J. Pharmacokinetic — pharmacodynamic profile of angiotensin II receptor antagonists // Clin. Pharmacokinet. — 1997. — 32. — 1-29.
8. Dzau V.J., Mukoyama M., Pratt R.E. Molecular biology and angiotensin receptors: target for drug research? // J. Hypertens. — 1994. — 12. — S1-S5.
9. Goodfriend T.L., Elliott M.E., Catt K.J. Angiotensin receptors and their antagonists // N. Engl. J. Med. — 1996. — 334. — 1649-1654.
10. Laeis P., Puchler K. The pharmokinetic and metabolic profile of olmesartan medoxomil limits the risk of clinically relevant drug interaction // J. Hypertens. – 2001. — 19. — S21-32.
11. Mengden T., Ewald S., Kaufmann S. еt al. Telemonitoring of blood pressure self measuerment in the OLMETEL study // Blood Press. Monit. — 2004. — 9. — Р. 321-325.
12. Mizuno M., Sada T. Pharmocology of CS-866, a novel nonpeptide angiotensin antagonist II receptor antagonist // Eur. J. Pharmacol. — 1999. — 285. — 181-188.
13. Oparil S., Williams D., Chrisant S.G. et al. Comperetive efficacy of olmesartan, losartan, valsartan, and irbesartan in the control of essential hypertension // J. Clin. Hypertens. — 2001. — V. 3. — Р. 283-291.
14. Oparil S., Sylfani T. Role of angiotensin II receptor blocker as monotherapy in reaching blood pressure goals // Am. J. Hypertension. — 2005. — 18. — 287-294.
15. Puchler K., Laies P., Stumpe K. Blood pressure response, but not adverse event incidance, correlates with dose of angiotensin II antagonist // J. Hypertens. Suppl. — 2001. — V. 19. — Р. 41-48.
16. Scholze J., Ewald S. OLMEPAS — Study: Оlmesartan medoxomil for the treatment of hypertension under daily-practice condition — results of patients with seveare hypertension // J. Clin. Hypertens (Greenwich). — 2005. — 6. — 614-620.
17. Schwocho L., Masonson H. Pharmokinetics of CS-866, a new angiotensin II receptor blocker, in healthy subjects // J. Clin. — 2001. — 41. — 515-527.
18. Simons W.R. Comparative cost effectiveness of angiotensin II receptor blocker in a US managed care setting: olmesartan medoxomil compared with losartan, valsartan and irbesartan // Pharmacoeconomics. — 2003. — 21. — 61-74.
19. Smith D.H., Dubiel R. Use of 24-hour ABPM to assess antihypertensive efficacy: a comparison of olmesartan medoxomil, losartan, valsartan and irbesartan // Am. J. Cardiovasc. Drugs. — 2005. — 5. — 41-50.
20. Smith D.H. Comparison of angiotensin II receptor blocker in the treatment of essential hypertension // Drugs. — 2008. — V. 68. — Р. 1207-1245.
21. Smith D.H. Dose-response characteristics of olmesartan medoxomil and other angiotensin II receptor blocker // Am. J. Cardiovasc. Drugs. — 2007. — V. 7. — Р. 347-356.
22. Timmermans P.B., Wong P.C., Chiu A.T. et al. Angiotensin II receptors and angiotensin II receptor antagonists // Pharmacol. Rev. — 1993. — 45. — 205-251.
23. Williams P.A. A multi-centere, double-blind, efficacy, tolerebility and safety study of the oral angiotensin II antagonist olmesartan medoxomil versus captopril in patients with mild to moderete essential hypertension [abstract] // J. Hypertens. — 2001. — V. 19 (suppl. 2). — Р. 300.