Газета «Новости медицины и фармации» Артериальная гипертензия (229) 2007 (тематический номер)
Вернуться к номеру
Некоторые подходы к повышению приверженности к лечению при артериальной гипертензии
Авторы: И.Г. Березняков, Харьковская медицинская академия последипломного образования
Рубрики: Кардиология
Разделы: Справочник специалиста
Версия для печати
Эффективность лечебного вмешательства зависит не только от правильной и своевременной постановки диагноза и выбора оптимальной стратегии и тактики лечения. Немалую роль играет и точность соблюдения больным предписанного режима терапии — прежде всего медикаментозного. Для характеристики этого явления чаще всего используются термины «комплайентность» и «приверженность к лечению». Первый из них неоднократно пытались перевести на русский язык, но ни один из предложенных вариантов не был достаточно удачным. Недостатком термина «комплайентность» (дословно: выполнение, соблюдение [предписанного режима лечения], соответствие [действий пациента рекомендациям врача]), по мнению некоторых специалистов, является то обстоятельство, что он, во-первых, указывает на пассивное выполнение больным назначений врача и, во-вторых, на тот факт, что план лечения не был согласован врачом с пациентом [1].
Термин «приверженность к лечению» тоже далек от совершенства. Обычно с его помощью описывают долю от выписанных доз медикаментов, которые действительно были приняты пациентом за определенный промежуток времени. В ряде случаев трактовка этого термина охватывает также учет сведений о приеме (принимались ли ежедневно все выписанные таблетки или другие лекарственные формы для приема внутрь) и учет времени приема лекарств (принимались ли медикаменты в указанные промежутки времени).
В целом приверженность к предписанному режиму лечения определяется как склонность (или стремление) пациента следовать советам медработников. Представляется разумным рассматривать понятие «приверженность» как своего рода общий качественный термин, но для количественного анализа использовать 2 замещающих термина: 1) «комплайентность» и 2) «постоянство». Первый из них можно определить как степень соответствия между истинным режимом дозирования у конкретного пациента и предписанным режимом дозирования, второй — как время, прошедшее от принятия первой дозы до прекращения лечения [2].
Исполнение предписанного режима дозирования — процесс динамичный, изменяющийся с течением времени. Его нельзя адекватно охарактеризовать каким-либо одним числом, например долей предписанных доз, принятых за время наблюдения, или количеством дней (выраженным в процентах от продолжительности курса лечения), в течение которых больной принял все предписанное количество доз, либо средним интервалом времени между приемом очередных доз. Неразумно придумывать специальные пороговые величины, чтобы разделить больных на «приверженцев» и «неприверженцев», «комплайентных» и «некомплайентных» и т.д. Основная причина того, почему такое разделение не способно удовлетворить потребности практики, заключается в наличии широкого ряда специфичных для препарата, заболевания, лекарственной формы медикамента фармакодинамических параметров, которые определяют пороговые различия между достаточной и недостаточной экспозицией к медикаменту для достижения удовлетворительного терапевтического результата. Во многих работах, например, ссылаются на часто используемый, но никогда фармакометрически (т.е. с помощью фармакокинетики и фармакодинамики) не верифицированный критерий, согласно которому прием 80 % предписанных доз и более позволяет трактовать пациента как адекватно комплайентного. Например, если критерий 80 % применить к однократному приему в сутки комбинированного низкодозового перорального контрацептива, частота беременностей будет столь высока, что единственным выводом окажется признание неэффективности этого класса препаратов.
В целом приверженность к лечению обычно выше при острых состояниях. При хронических заболеваниях она значительно снижается спустя 6 месяцев лечения [3–5]. В рутинной клинической практике приверженность к лечению, как правило, ниже, чем во время рандомизированных клинических исследований (РКИ), хотя и тогда при хронических заболеваниях она может не превышать 48–73 % [3, 6, 7].
Клиническое и экономическое значение неприверженности к лечению
В недавнем метаанализе (21 РКИ (1970–2005 гг., 46 847 человек), включая 8 плацебо-контролируемых исследований (19 633 больных)) у постинфарктных больных, больных СПИДом, лиц с гиперхолестеринемией, сердечной недостаточностью, пациентов после трансплантации сердца, больных с сахарным диабетом, а также в группе лиц, у которых оценивали эффективность первичной профилактики сердечно-сосудистых заболеваний, была изучена связь между приверженностью к лечению и смертностью. Хорошая приверженность к приему препаратов сопровождалась снижением смертности по сравнению с плохой приверженностью к приему медикаментов: отношение шансов (ОШ) 0,56; 95% доверительный интервал (ДИ) 0,50–0,63 [8].
В США 33–69 % от числа всех госпитализаций, связанных с медикаментами, обусловлены плохой приверженностью к лечению, что обходится стране приблизительно в 100 млрд долларов в год [9–11].
Факторы, влияющие на приверженность к лечению
Вопреки распространенному мнению низкая приверженность к лечению не связана с возрастом, полом больного, семейным положением, образованием, уровнем доходов, социальным положением и даже стоимостью препарата или отсутствием необходимости платить за лекарство [12]. Другими словами, характер приверженности к лечению является индивидуальным качеством каждого конкретного пациента. Косвенные подтверждения этому были получены в ходе упомянутого выше метаанализа [8], в котором хорошая приверженность к приему плацебо сопровождалась снижением смертности по сравнению с плохой приверженностью к приему плацебо, причем отношение шансов и доверительный интервал оказались весьма близкими к значениям, установленным в группе активного лечения: ОШ 0,56; 95% ДИ 0,43–0,74. Более того, в 2 РКИ активное лечение оказалось опасным, и смертность в группе вмешательства была выше, чем в группе плацебо. Хорошая приверженность к лечению в этих двух исследованиях статистически значимо увеличивала риск смерти по сравнению с плохой приверженностью: ОШ 2,90, 95% ДИ 1,04–8,11. Авторы заключили, что, во-первых, наличие связи между хорошей приверженностью к приему плацебо и снижением смертности указывает на существование эффекта «здорового приверженца» и, во-вторых, хорошая приверженность к лекарственной терапии может быть суррогатным маркером «здорового поведения» (overall healthy behaviour) [8].
Попытки выяснить причины несоблюдения предписанного режима терапии у самих пациентов дают противоречивые результаты. Так, по данным одного из опросов, ведущей причиной является забывчивость (рис. 1). В то же время более четверти опрошенных вообще не смогли привести ни одного вразумительного объяснения [13].
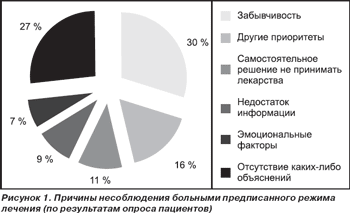
Тем не менее очертить круг причин, обусловливающих низкую приверженность к лечению, все же можно. Условно их можно разделить на: 1) связанные с врачом; 2) связанные с пациентом; 3) связанные с характером заболевания и назначенным лечением (табл. 1).

Методы повышения приверженности к лечению
В целом методы повышения приверженности к лечению можно объединить в 4 большие группы: 1) обучение пациентов; 2) улучшение схемы дозирования медикаментов; 3) улучшение взаимодействия между врачами и пациентами; 4) увеличение времени работы медицинских учреждений (включая вечернее время) и, следовательно, сокращение сроков ожидания больных в очереди [1]. Ниже будут рассмотрены возможности применения первых трех методов у больных с гипертонической болезнью. Обучение пациентов предполагает информирование их о нормальных величинах артериального давления (АД), разъяснение опасности повышенного АД и необходимости длительной терапии заболевания, вовлечение больных в образовательные программы по овладению навыками самоконтроля за величиной АД. К сожалению, результаты РКИ, в которых оценивалась эффективность образовательных вмешательств, направленных на пациентов, свидетельствуют об отсутствии значимого влияния на снижение АД [15, 16].
Улучшение схемы дозирования медикаментов включает в себя, прежде всего, уменьшение кратности приема лекарств в течение суток и упрощение инструкций по их применению [17, 18]. Авторы Кокрейновского обзора проанализировали 9 РКИ, в которых оценивалась эффективность упрощения режима дозирования в амбулаторном лечении больных с артериальной гипертензией. В 7 из них было установлено позитивное влияние данного вмешательства на приверженность к лечению. Относительное увеличение последней колебалось от 8 до 19,6 % [16]. При этом наибольшую роль играет уменьшение кратности приема лекарств в течение суток. Наивысшая приверженность к терапии отмечается в случаях приема медикаментов 1 раз в сутки, хотя различия в приверженности по сравнению с двукратным приемом в течение суток (в отличие от более частого), по данным обзоров клинических исследований, не достигали статистической значимости [7, 19]. Справедливости ради следует отметить, что превосходство однократного приема над двукратным с точки зрения приверженности к лечению не раз демонстрировалось в исследованиях у больных с артериальной гипертензией [20, 21].
Уменьшение кратности приема антигипертензивных препаратов в течение суток рассматривается как стратегически наиболее важный подход к повышению приверженности к лечению [16]. Достичь этого можно: 1) путем использования фиксированных комбинаций антигипертензивных средств; 2) путем применения лекарств с длительным периодом полувыведения, что позволяет дозировать их 1 раз в сутки; 3) путем создания и внедрения в клиническую практику лекарственных форм с постепенным высвобождением медикамента. Примерами успешного создания твердых лекарственных форм с постепенным высвобождением антигипертензивных средств являются ретардные формы антагонистов кальция нифедипина, дилтиазема и др.
В случаях, когда не удается добиться приемлемой приверженности к лечению, следует отдавать предпочтение так называемым снисходительным лекарствам, эффективность которых в меньшей степени страдает от пропуска или задержки приема очередной дозы. К таким медикаментам относят либо препараты с длительным периодом полувыведения (например, амлодипин, лизиноприл), либо средства, эффект которых не зависит от длительности периода полувыведения (например, тиазидные диуретики) [1].
Одним из путей улучшения взаимодействия между врачами и пациентами является переход от авторитарной модели поведения врача по отношению к больному к сотрудничеству с ним при обсуждении стратегии и тактики лечения [22]. Более того, когда возможно, следует поддерживать самостоятельное измерение АД и ведение дневника наблюдений самим пациентом [22, 23]. Тем не менее не стоит переоценивать эффективность подобного вмешательства. Самостоятельное измерение АД ассоциируется с весьма умеренным снижением диастолического АД (в среднем на 2 мм рт.ст., 95% ДИ –2,7… –1,4 мм рт.ст.) [15].
Дополнительные перспективы открывает индивидуализация лечения с участием самого больного. Предрасположенность к возникновению артериальной гипертензии носит полигенный мультифакториальный характер. Другими словами, у каждого конкретного пациента заболевание развивается в результате сложного взаимодействия комплекса генетических и средовых факторов. Поэтому предсказать, какой именно класс (или какие классы) антигипертензивных средств окажутся наиболее эффективными у данного больного, весьма затруднительно. Некоторые подсказки можно получить, если обратить внимание на расу и возраст пациента. В частности, у больных европеоидной расы в возрасте до 55 лет более эффективны ингибиторы ангиотензинпревращающего фермента (АПФ), блокаторы рецепторов к ангиотензину II 1-го типа и бета-адреноблокаторы, в то время как у лиц старше 55 лет предпочтение следует отдавать диуретикам и антагонистам кальция. У пациентов любого возраста — выходцев из Черной Африки артериальная гипертензия обычно низкоренинная, в связи с чем наиболее эффективными также оказываются диуретики и антагонисты кальция [24]. Однако ничто из сказанного не дает ответа на вопрос об оптимальном лечении каждого пациента.
Одним из путей преодоления указанных затруднений может быть ротация антигипертензивных препаратов. По сути, это пробное лечение представителями разных классов антигипертензивных средств в сопоставимых дозах на протяжении одинаковых промежутков времени с ежедневной регистрацией величины АД. Использовать этот метод можно при наличии нескольких условий: 1) согласия и желания больного; 2) самостоятельного измерения АД и ведения дневника наблюдений; 3) артериальной гипертензии не выше II (еще лучше — I) степени. Участие больного в определении оптимальных именно для него классов антигипертензивных средств повышает вероятность соблюдения предписанного режима лечения (как в ходе ротации, так и после ее завершения и подбора оптимальной терапии). Тем не менее эффективность подобного подхода с точки зрения приверженности к лечению еще предстоит изучить.
В практической деятельности врачам следует также преодолевать ошибочные представления, или мифы, укоренившиеся в общественном сознании. В словаре русского языка С.И. Ожегова приводится 2 толкования слова «миф»: 1) древнее народное сказание о легендарных героях, богах, о явлениях природы; 2) недостоверный рассказ, выдумка. Далее речь пойдет о представлениях, сформировавшихся на основании недостоверных или вовсе неверных фактов и/или умозаключений и усвоенных значительной частью населения Украины.
1. Осознанная или несознаваемая нелюбовь к «химии»
До сих пор во многих слоях общества негативно относятся к «химии», т.е. к лекарственным средствам, созданным синтетическим путем. Характерно, что недоверие бесконфликтно уживается с восхищением достижениями западноевропейской и североамериканской медицины. Тем не менее, выйдя за порог врачебного кабинета, некоторые пациенты отправляются не в аптеку, а за лекарственными травами. Фитотерапия как один из подходов к лечению, несомненно, имеет право на существование. К сожалению, эффективность лекарственных трав в лечении артериальной гипертензии никогда должным образом не изучалась. Если же брать объективные статистические показатели (продолжительность жизни, число инсультов и инфарктов миокарда на 100 тысяч населения и т.д.), то они неопровержимо свидетельствуют об эффективности именно медикаментозного лечения.
2. Убежденность в необходимости ежегодного курсового лечения артериальной гипертензии в стационаре
Другой распространенный миф — это убеждение, что гипертоническая болезнь лечится в стационаре. Пройдя ежегодный курс лечения в больнице, многие пациенты решают, что дело сделано, и прекращают прием медикаментов — до следующей госпитализации. Над преодолением этого стереотипа еще предстоит работать и работать.
3. Недоверие к препаратам для приема внутрь и переоценка возможностей медикаментов для парентерального применения
Этот миф тесно связан с предыдущим, ведь инъекционные препараты назначаются обычно в стационаре. Впрочем, переоценка возможностей средств для парентерального применения — отнюдь не прерогатива артериальной гипертензии. Со сходными проблемами приходится сталкиваться при назначении антибиотиков, глюкокортикоидов и многих других медикаментов.
Несомненно, при гипертонической болезни бывают случаи, когда необходима парентеральная терапия. Это неотложные ситуации, например гипертензивные кризы. В то же время лечение хронической стабильной гипертензии (даже при значительном повышении АД) должно проводиться лекарствами для приема внутрь.
4. «Аварийное реагирование»: эпизодический прием медикаментов, «когда болит голова» и в тому подобных случаях
Малосимптомность артериальной гипертензии у значительной части больных обусловливает эпизодичность приема антигипертензивных препаратов. Возобновление головных болей, головокружения, неприятных ощущений в области сердца многие пациенты расценивают как сигнал, свидетельствующий о необходимости приема медикаментов. После устранения жалоб прием лекарств, как правило, прекращается. При этом совершенно игнорируется тот факт, что АД нередко продолжает оставаться на повышенном уровне (либо быстро к нему возвращается) и, следовательно, сохраняется высокий риск сердечно-сосудистых катастроф.
5. Вера в «чудо-лекарства» (и ее последствия: разочарование в медикаментах, врачах и т.д.)
Одним из требований к современным антигипертензивным средствам является постепенное развитие лечебног о эффекта или, другими словами, мягкий и устойчивый контроль над величиной АД. Быстрое снижение, большой размах колебаний АД в течение суток рассматриваются как неблагоприятные факторы, свидетельствующие о далеко не оптимальном контроле. В глазах многих соотечественников достоинства современных препаратов превращаются в недостатки. Приобретая новое «чудодейственное» лекарство, значительная часть пациентов убеждена, что завтра, самое позднее послезавтра, проблема контроля над АД будет решена. Отсутствие немедленного эффекта вызывает разочарование в лекарстве и порождает поиски нового «чуда», новые разочарования в медикаментах, врачах и т.д. [25].
Среди других подходов к улучшению взаимодействия между врачом и пациентом следует упомянуть необходимость активного выявления нежелательных явлений (побочных эффектов) в ходе лекарственной терапии и письменных инструкций для больного (или лиц, ухаживающих за ним). Врачи склонны оценивать результаты антигипертензивной терапии по объективному показателю — достигнутому уровню АД. Система ценностей для больного выглядит иначе. Его больше заботит не величина АД, а собственное самочувствие. И если у него снижение АД будет сопровождаться появлением нежелательных явлений лекарственной терапии (приливами крови к лицу, учащенным сердцебиением, сухим кашлем, сонливостью и т.д.), то воспринимать результаты лечения он будет со знаком «минус». Отсюда рукой подать до частичного соблюдения врачебных рекомендаций или даже прекращения лечения.
Следует также учитывать вероятность непонимания или превратного истолкования больным инструкций врача. Это обстоятельство, к сожалению, часто игнорируется врачами. Для подавляющего большинства пациентов медицинские термины, в том числе названия медикаментов, — нечто чужеродное, сродни иностранному языку. Более того, далеко не все люди способны внятно и четко давать устные инструкции. Как, впрочем, далеко не все способны их адекватно воспринимать. Поэтому рекомендации по немедикаментозной и медикаментозной терапии следует давать письменно. Более того, пожилые люди, страдающие артериальной гипертензией, нередко имеют и другие заболевания, в том числе органические поражения головного мозга. В подобных случаях письменные инструкции по лечению следует давать не только пациентам, но и их родственникам либо лицам, ухаживающим за больными [25].
Заключение
Среди методов повышения приверженности к лечению у больных с артериальной гипертензией наиболее изучены обучение пациентов, улучшение схемы дозирования медикаментов и улучшение взаимодействия между врачами и пациентами.
Исследования эффективности образовательных программ, ориентированных на пациентов, не выявили значимого влияния подобных вмешательств на снижение АД.
Улучшение схемы дозирования медикаментов включает в себя, прежде всего, уменьшение кратности приема лекарств в течение суток и упрощение инструкций по их применению. Сократить количество приемов антигипертензивных средств можно путем использования фиксированных комбинаций антигипертензивных препаратов, применения лекарств с длительным периодом полувыведения, что позволяет дозировать их 1 раз в сутки, создания и внедрения в клиническую практику лекарственных форм с постепенным высвобождением медикамента. При невозможности добиться приемлемой приверженности к лечению следует отдавать предпочтение так называемым «снисходительным» лекарствам, эффективность которых в меньшей степени страдает от пропуска или задержки с приемом очередной дозы. К таким медикаментам относят препараты с длительным периодом полувыведения либо средства, эффект которых не зависит от длительности этого периода.
Среди путей улучшения взаимодействия между врачами и пациентами следует упомянуть переход от авторитарной модели поведения врача по отношению к больному к сотрудничеству с ним при обсуждении стратегии и тактики лечения. Когда возможно, следует поддерживать самостоятельное измерение АД и ведение дневника наблюдений самим пациентом. Определенные перспективы в плане улучшения взаимодействия между врачами и пациентами и повышения приверженности к лечению открывает индивидуализация терапии, разъяснение устоявшихся заблуждений, активное выявление нежелательных лекарственных явлений, представление рекомендаций в письменном виде.
1. Osterberg L., Blaschke T. Adherence to medication // N. Engl. J. Med. — 2005. — 353. — 487-97.
2. Vrijens B., Urquhart J. Patient adherence to prescribed antimicrobial drug dosing regimens // J. Antimicrob. Chemother. — 2005. — 55. — 616-27.
3. Jackevicius C.A., Mamdani M., Tu J.V. Adherence with statin therapy in elderly patients with and without acute coronary syndromes // JAMA. — 2002. — 288. — 462-7.
4. Cramer J., Rosenheck R., Kirk G. et al. Medication compliance feedback and monito ring in a clinical trial: predictors and outcomes // Value Health. — 2003. — 6. — 566-73.
5. Haynes R.B., McDonald H.P., Garg A.X. Helping patients follow prescribed treatment: clinical applications // JAMA. — 2002. — 288. — 2880-3.
6. Waeber B., Leonetti G., Kolloch R., McInnes G.T. Compliance with aspirin or placebo in the Hypertension Optimal Treatment (HOT) study // J. Hypertens. — 1999. — 17. — 1041-5.
7. Claxton A.J., Cramer J., Pierce C. A systematic review of the associations between dose regimens and medication compliance // Clin. Ther. — 2001. — 23. — 1296-310.
8. Simpson S.H., Eurich D.T., Majumdar S.R. et al. A meta-analysis of the association between adherence to drug therapy and mortality // BMJ. — 2006. — 333. — 15; doi:10.1136/bmj.38875.675486.55
9. McDonnell P.J., Jacobs M.R. Hospital admissions resulting from preventable adverse drug reactions // Ann. Pharmacother. — 2002. — 36. — 1331-6.
10. Senst B.L., Achusim L.E., Genest R.P. et al. Practical approach to determining costs and frequency of adverse drug events in a health care network // Am. J. Health Syst. Pharm. — 2001. — 58. — 1126-32.
11. Levy G., Zamacona M.K., Jusko W.J. Developing compliance instructions for drug labeling // Clin. Pharmacol. Ther. — 2000.— 68. — 586-91.
12. Kardas P.J. Patient compliance with antibiotic treatment for respiratory tract infections // J. Antimicrob. Chemother. — 2002. — 49. — 897-903.
13. Cramer J.A. Identifying and improving compliance patterns // J.A. Cramer, B. Spilker, eds. Patient compliance in medical practice and clinical trials. — New York: Raven Press, 1991. — 387-92.
14. Vander Stichele R. Measurement of patient compliance and the interpretation of randomized trials // Eur. J. Clin. Pharmacol. — 1991. — 41. — 27-35.
15. Fahey T., Schroeder K., Ebrahim S. Interventions used to improve control of blood pressure in patients with hypertension // The Cochrane Database of Systematic Reviews. — The Cochrane Collaboration: John Wiley and Sons, Ltd., 2006. — Issue 4.
16. Schroeder K., Fahey T., Ebrahim S. Interventions for improving adherence to treatment in patients with high blood pressure in ambulatory settings // The Cochrane Database of Systematic Reviews. — The Cochrane Collaboration: John Wiley and Sons, Ltd., 2006. — Issue 4.
17. Eisen S.A., Miller D.K., Woodward R.S., Spitznagel E., Przybeck T.R. The effect of prescribed daily dose frequency on patient medication compliance // Arch. Intern. Med. — 1990. — 150. — 1881-4.
18. Schroeder K., Fahey T., Ebrahim S. How can we improve adherence to blood pressure-lowering medication in ambulatory care? Systematic review of randomized controlled trials // Arch. Intern. Med. — 2004. — 164. — 722-32.
19. Greenberg R.N. Overview of patient compliance with medication dosing: a literature review // Clin. Therapeutics. — 1984. — 6. — 592-9.
20. Lee J.Y., Kusek J.W., Greene P.G. et al. Assessing medication adherence by pill count and electronic monitoring in the African American Study of Kidney Disease and Hypertension (AASK) Pilot Study // Am. J. Hypertens. — 1996. — 9. — 719-25.
21. Waeber B., Erne P., Saxenhofer H. et al. Use of drugs with more than 24-hour duration of action // J. Hypertens. — 1994. — 12 (Suppl. 8). — 67-71.
22. Feldman R., Bacher M., Campbell N., Drover A., Chockalingam A. Adherence to pharmacologic management of hypertension // Can. J. Public Health. — 1998. — 89. — I16-I18.
23. Vrijens B., Goetghebeur E. Comparing compliance patterns between randomized treatments // Control. Clin. Trials. — 1997. — 18. — 187-203.
24. National Collaborating Centre for Chronic Conditions. Hypertension: management of hypertension in adults in primary care: partial update. — London: Royal College of Physicians, 2006.
25. Березняков И.Г. Лечение артериальной гипертензии: почему мы терпим неудачи? // Артериальная гипертензия'99 / Под ред. И.Г. Березнякова. — Харьков: Константа, 1999. — 44-66.
