Газета «Новости медицины и фармации» 1-2 (442-443) 2013
Вернуться к номеру
Обґрунтування вибору тактики фармакотерапії гострих синуситів у дітей
Авторы: Леженко Г.О.1, Пашкова О.Є. 1, Пантюшенко Л.І. 2, 1 Запорізький державний медичний університет,
2 Запорізька обласна клінічна дитяча лікарня
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
 Синусит є поширеним захворюванням в амбулаторній педіатричній практиці, що достатньо часто зустрічається у всіх вікових групах дітей. За даними американських дослідників, 4,6 % всіх звернень до лікаря загальної практики припадає на частку синуситів. Щорічно кожна дитина хворіє 6–8 разів на гостру респіраторну вірусну інфекцію (ГРВІ). У 5–13 % випадків ГРВІ у дітей ускладнюється синуситом [11].
Синусит є поширеним захворюванням в амбулаторній педіатричній практиці, що достатньо часто зустрічається у всіх вікових групах дітей. За даними американських дослідників, 4,6 % всіх звернень до лікаря загальної практики припадає на частку синуситів. Щорічно кожна дитина хворіє 6–8 разів на гостру респіраторну вірусну інфекцію (ГРВІ). У 5–13 % випадків ГРВІ у дітей ускладнюється синуситом [11].
Антибактеріальна терапія при гострому й підгострому синуситі в дітей повинна бути направлена на ерадикацію збудника (відновлення стерильності синуса), запобігання розвитку ускладнень і переходу захворювання в хронічну форму. Вибір препарату в переважній більшості випадків проводиться емпірично, на основі даних про переважаючі збудники, їх резистентність в регіоні і з урахуванням тяжкості стану [10].
Сьогодні формування резистентності розглядається як одна з основних причин недостатньої ефективності антибіотикотерапії, що, у свою чергу, створює проблеми у виборі препаратів, призводить до зниження їх ефективності і сприяє збільшенню відсотка переходу в хронічний процес гострого бактерійного синуситу [6]. У той же час у разі відстроченої антибактеріальної терапії можливий розвиток орбітальних і внутрішньочерепних ускладнень, причому в педіатричній практиці вони зустрічаються частіше, ніж серед дорослих хворих [9].
На сьогодні основними збудниками гострого етмоїдиту і гаймориту є H.іnfluenzae, S.pneumoniae, і M.catarrhalis [2, 7].
Основним механізмом, що забезпечує резистентність H.influenzae до даних антибіотиків, є продукція bлактамаз — ферментів, що руйнують bлактамне кільце пеніцилінів. За даними зарубіжної літератури, майже всі штами H.influenzae є нечутливими до макролідів і азалідів. Ерадикація патогену при прийомі амоксициліну становила 38–63 %, прийом амоксициліну/клавуланату в дозі 45/6,4 мг/кг/добу був ефективніший — до 77 % ерадикації, а у вищій дозі (90/6,4 мг/кг/добу) — до 80–84 %. Резистентність H.influenzae до триметоприму/сульфаметоксазолу в ряді країн досягає 25 %, що не дозволяє розглядати препарат як засіб вибору. У той же час навіть одноразове введення цефтріаксону в дозі 50 мг/кг забезпечувало 100% рівень бактеріологічного лікування від H.іnfluenzae, доведена також висока ефективність проти даного збудника цефуроксиму аксетилу [8]. Таким чином, адекватність антибактеріальної терапії є дуже актуальним завданням.
На сьогодні на ринку представлений великий вибір антибактеріальних препаратів. Основним принципом емпіричної антибактеріальної терапії при гострому бактеріальному синуситі є активність проти найбільш вірогідних збудників захворювання з подальшою корекцією при отриманні результатів мікробіологічного дослідження. Неодмінними вимогами до антибактеріальних препаратів при лікуванні гострого синуситу в дітей є їх максимальна безпека, відсутність ототоксичного й інших небажаних ефектів. Крім того, антибіотик повинен бути активний щодо S.pneumoniae і Н.influenzae, зокрема резистентних штамів; добре проникати в слизову оболонку синусів із досягненням концентрації вище мінімальної пригнічуючої концентрації (МПК) для даного збудника.
Оптимальним препаратом для лікування гострих синуситів у дітей, що відповідає всім вищезазначеним вимогам, є антибіотик цефподоксиму проксетил (Цефодокс), що належить до групи цефалоспоринів ІІІ покоління [1, 3]. Цефподоксиму проксетил — проліки, що стають активними тільки в стінці тонкої кишки, де вони перетворюються на цефподоксим. Тому Цефодокс практично не впливає на флору кишечника, що дуже важливо для дітей, які схильні до розвитку дисбіозу кишечника. Вже через 2–3 години після перорального прийому Цефодоксу досягається максимальна концентрація препарату в сироватці крові. Тільки 18–23 % цефподоксиму зв’язується з білком. Цефподоксим практично не метаболізується і не екскретується з фекаліями [4]. Враховуючи широкий спектр дії цефподоксиму, його високу активність щодо грампозитивної та грамнегативної флори, бактерицидну дію та високий ступінь безпеки, Цефодокс доцільно застосовувати в лікуванні інфекцій лорорганів. Цефодокс швидко проникає у тканини, у тому числі мигдалини, легені й рідини організму, де концентрація Цефодоксу швидко досягає максимальних рівнів. У слизовій оболонці гайморових пазух концентрація цефподоксиму становить 0,34 мг/л, у тканині піднебінних мигдалин — 0,24 мг/л, у паренхімі легенів — 0,63 мг/л, у слизовій оболонці бронхів — 0,91 мг/л, у плевральній рідині — 1,84 мг/л, а в запальній рідині — 2,84 мг/л. Таким чином, концентрація Цефодоксу у тканинах значно перевищує МПК для більшості мікроорганізмів — збудників інфекцій лорорганів і дихальних шляхів. Приблизно 90 % цефподоксиму після прийому екскретується за 12 годин із сечею [4].
Результати проведеного нами бактеріологічного моніторингу 76 дітей, хворих на гострі синусити, показали, що серед основних збудників захворювання домінувала гемофільна паличка, що зустрічалася в 61 (80,3 %) пацієнта. Серед виявлених штамів збудника H.influenzae зустрічалася у 46 (60,5 %), H.haemolyticus — у 6 (7,9 %), H.parainfluenzae — у 5 (6,6 %) та H.parahaemolyticus — у 4 (5,3 %) хворих. Звертав на себе увагу той факт, що S.pneumoniae виступав етіологічним фактором захворювання лише у 9 (11,8 %) дітей із гострим захворюванням навколоносових пазух. Інші збудники зустрічалися значно рідше, тобто Moraxella catarhalis була виявлена у 3 (3,9 %) дітей, Klebsiella pneumonia — у 2 (2,6 %) і Proteus mirabilis — в 1 (1,3 %) хворого.
Аналіз антибіотикограм показав, що зазначені збудники найбільшу чутливість проявляли щодо цефалоспоринів ІІІ покоління на тлі помірної чутливості до бактерійної флори, що виділялася, у дітей із гострими синуситами, до захищених амінопеніцилінів. У частини дітей (25, або 32,9 %) також мала місце резистентність флори до азитроміцину.
Таким чином, одержані дані виступають свідченням, що призначення як емпіричної терапії цефалоспорину ІІІ покоління Цефодоксу в лікуванні гострих синуситів є доцільним та обґрунтованим.
Мета дослідження: оцінити ефективність перорального антибіотика з групи цефалоспоринів ІІІ покоління Цефодоксу при лікуванні гострих синуситів у дітей.
Матеріали і методи дослідження
Для досягнення поставленої мети було проведено комплексне обстеження і лікування 76 дітей із гострими бактеріальними синуситами віком від 7 до 16 років (середній вік пацієнтів становив 10,3 ± 1,2 року). Діагноз встановлювався на підставі діагностичних критеріїв гострого синуситу згідно з Протоколом лікування дітей, хворих на гострий і хронічний синуїт (Наказ МОЗ України № 181 від 21.04.2005 р.): гострий початок захворювання, підвищення температури тіла, млявість, швидка втомлюваність, зниження апетиту, порушення сну, головні і лицьові болі, утруднення носового дихання, виділення з носа, тривалий стійкий кашель, що посилюється після пробудження, набряклість слизової оболонки при риноскопії, слизисте, слизистогнійне або гнійне виділення під середньою носовою раковиною. Рентгенологічні дослідження були одними з вирішальних критеріїв діагностики синуситу. В окремих випадках для уточнення діагнозу проводилася комп’ютерна томографія навколоносових пазух. Обов’язковий комплекс обстеження включав дослідження загального аналізу крові, загального аналізу сечі, бактеріологічне дослідження патологічного виділення з носоглотки з визначенням чутливості до антибіотиків.
Всім пацієнтам призначався антибіотик цефподоксиму проксетил (Цефодокс) у віковому дозуванні (10 мг/кг маси тіла на добу на 2 прийоми, максимальна добова доза — 400 мг). Тривалість лікування становила 10 днів. За необхідності додатково призначалися судинозвужувальні й антигістамінні препарати.
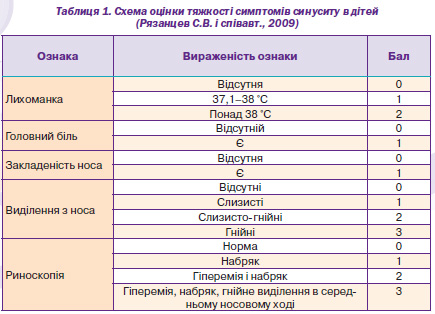
Клінічні ознаки оцінювалися до початку дослідження, на 5й і 11й день від початку терапії. Тяжкість симптомів оцінювалася за декількома параметрами: лихоманка, закладеність носа, виділення з носа, риноскопічна картина (табл. 1) [5].
Сума всіх балів становила загальний клінічний рахунок (ЗКР). Ступінь тяжкості розцінювався як тяжкий при рівні ЗКР понад 8 балів, середньотяжкий, якщо ЗКР становила до 8 балів.
Клінічна ефективність терапії оцінювалася як «значне поліпшення» при повному зникненні ознак захворювання (зниження ЗКР не менше ніж на 90 % або ЗКР на 11й день рівний 0); «поліпшення» — при частковому зникненні ознак захворювання без необхідності проведення подальшої антибактеріальної терапії (зниження ЗКР на 60 %); «без ефекту» — за відсутності позитивної динаміки (зниження ЗКР менше 60 %), що вимагає зміни антибактеріального препарату; «погіршення» — при прогресуванні ознак синуситу, що вимагають зміни антибактеріального препарату.
Результати дослідження і їх обговорення
До початку лікування більшість хворих (74 дитини — 97,4 %) скаржилися на закладеність носа, головний біль, підвищену стомлюваність, субфебрилітет. У 49 (64,5 %) пацієнтів спостерігалися слизисті виділення з носа, у 16 (21,1 %) — слизистогнійні і в 11 (14,5 %) дітей — гнійні. У частини хворих (47,4 %) батьки відзначали неприємний запах з рота у дитини. Риніт у 63 (82,9 %) дітей супроводжувався кашлем, що посилювався після сну. При пальпації і перкусії у 57 % пацієнтів відмічалася підвищена чутливість або болісність у ділянці передньої стінки верхньощелепної пазухи і/або передньої та нижніх стінок лобової пазухи. У всіх хворих діагноз синуситу був підтверджений при рентгенологічному дослідженні навколоносових пазух. За даними ЗКР у 55 (72,4 %) дітей захворювання розцінене як середньотяжке, а у 21 (27,6 %) пацієнта захворювання мало тяжкий перебіг. У клінічному аналізі крові в більшості дітей (66 пацієнтів — 86,8 %) у перший день дослідження спостерігалися незначні зміни у вигляді лейкоцитозу, зсуву лейкоцитарної формули вліво, збільшення ШОЕ.
Застосування Цефодоксу сприяло поліпшенню стану хворих починаючи з перших днів лікування: уже на 2–3й день прийому препарату нормалізувалася температура тіла, зникали головні болі, з 3–5го дня терапії поліпшувалося носове дихання, зменшувалися прояви кашлю.
На тлі лікування Цефодоксом спостерігалися значне зменшення ринореї і зміна характеру виділень з носа. На 5й день терапії в жодного хворого не було гнійного виділення з носа, слизистогнійні виділення зберігалися лише у 7 (9,2 %) хворих, зменшилася кількість дітей із серозними виділеннями з носа до 16 (21,1 %). У 53 (69,7 %) пацієнтів на 5й день терапії Цефодоксом виділення з носа були відсутні. Дані риноскопії на 5й день терапії також свідчили про позитивну динаміку: зменшилися гіперемія і набряклість слизової оболонки порожнини носа, а у 26 (34,2 %) пацієнтів риноскопічна картина відповідала нормі.
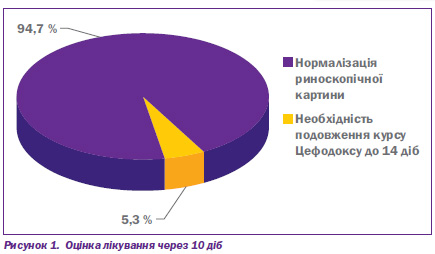
При обстеженні на 11й день від початку терапії у 72 дітей (94,7 %) риноскопічна картина нормалізувалася, виділення з носа відсутні й лише у 4 (5,3 %) спостерігалися слизисті виділення і зберігався помірний набряк слизової оболонки порожнини носа, яким було продовжено курс лікування до 14 днів із клінічним одужанням (рис. 1).
При лабораторному дослідженні на 11ту добу у всіх дітей нормалізувалися показники в аналізах периферичної крові.
Слід зазначити добру переносимість препарату Цефодокс, приємний смак та зручність у дозуванні. Побічних ефектів у хворих, які знаходилися під спостереженням, ми не помітили.
Висновки
1. Застосування цефалоспорину ІІІ покоління Цефодокс в комплексній терапії гострих синуситів у дітей показало високу ефективність препарату та його безпечність.
2. Цефалоспорин ІІІ покоління Цефодокс може застосовуватися як препарату вибору в терапії гострих запальних захворювань навколоносових пазух у дітей.
1. Дифференцированное применение антибактериальных препаратов в педиатрии (по материалам IX Всеукраинской научнопрактической конференции «Актуальные вопросы педиатрии») // Новости медицины и фармации. — 2007. — № 21–22. — С. 230231.
2. Егорова О.А. Синусит у детей: диагностика и антибактериальная терапия / О.А. Егорова, Е.И. Каманин // Consilium medicum. — 2003. — Том 05, № 6.
3. Новые перспективы использования пероральных цефалоспоринов в педиатрии. По материалам V Конгресса педиатров Украины, 15–17 октября, г. Киев // Здоров’я України. — 2008. — № 24/1. — С. 3637.
4. Опыт использования препарата «Цефодокс» в комплексной терапии гнойных синуситов у детей / В.В. Бережной, В.Г. Козачук, И.Б. Орлюк [и др.] // Современная педиатрия. — 2007. — № 3. — С. 8892.
5. Рязанцев С.В. Лечение острого гнойного синусита у детей макролидами / С.В. Рязанцев, В.И. Кочеровец, М.В. Молчанова // Педиатрия. — 2009. — № 3, приложение consilium medicum //http://medi.ru/doc/111602.htm>
6. Brook I. Chronic sinusitis in children and adultis: role of bacteria and antimicrobial management / I. Brook // Curr. Alleray Astma Rep. — 2005. — Vol. 5 (6). — P. 482490.
7. Leczenie ostrego bakteryjnego zapalenia zatok przynosowych Zalecenia Clinical Advisory Committee on Pediatric and Adult Sinusitis / I. Brook, W.M. Gooch III, S.G. Jenkins [et al.] // Medycyna Praktyczna Pediatria. — 2001. — № 2.
8. Leibovitz E. Haemophilus influenzae: A significant Pathogen in Acute Otitis Media / E. Leibovitz, M.R. Jacobs, R. Dagan // Pediatr. Infect. Dis J. — 2004. — Vol. 23 (12). — P. 11421152.
9. Oxford L.E. Complications of acute sinusitis in children / L.E. Oxford, J. McClay // Otolaryngol. Haed. Neck. Sura. — 2005. — Vol. 133 (1). — P. 3237.
10. Sinus and Allergy Health Partnership. Antimicrobial treatment guidelines for acute bacterial rhinosinusitis // Otolaryngology Head and Neck Surgery. — 2000. — Vol. 123. — P. 132.
11. Wald E.R. Sinusitis. Pediatric Infectious Diseases Principles and Practice / Ed. by H.B. Jenson, R.S. Baltimore. — 1st ed. — 2002. — V. 1. — P. 76070.

