Журнал «Медицина неотложных состояний» 2 (57) 2014
Вернуться к номеру
Детоксицирующие свойства препарата Реосорбилакт и его влияние на гемостаз
Авторы: Аваков В.Е., Сайипов Р.М., Давыдов Д.В., Бегматов С.Ж., Базаров А.Н. - Ташкентская медицинская академия, кафедра анестезиологии и реаниматологии, Республика Узбекистан
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Применение Реосорбилакта в виде внутривенных инфузий в комплексной терапии пациентов с гнойно-септическими заболеваниями, изолированными черепно-мозговыми травмами, пневмониями и операциями по поводу реконструкции внутренней сонной артерии оказывает выраженный детоксикационный эффект, который проявляется снижением концентрации молекул средней массы и продуктов перекисного окисления липидов. Быстро нормализовались показатели свертывающей системы крови, что свидетельствовало об улучшении реологии крови.
Застосування Реосорбілакту у вигляді внутрішньовенних інфузій у комплексній терапії пацiєнтiв iз гнійно-септичними захворюваннями, ізольованими черепно-мозковими травмами, пневмоніями та операціями з приводу реконструкції внутрішньої сонної артерії має виражений детоксикаційний ефект, який проявляється зниженням концентрації молекул середньої маси і продуктів перекисного окислення ліпідів. Швидко нормалізувалися показники системи згортання крові, що свідчило про поліпшення реології крові.
Application of Reosorbilact as an intravenous infusion in the combination treatment of patients with purulent-septic diseases, isolated traumatic brain injuries, pneumonias and operations for internal carotid artery reconstruction has a significant detoxifying effect, which manifests itself in the reduction of concentration of average-weight molecules and lipid peroxidation products. Parameters of blood coagulation system quickly returned to normal, indicating improvement of blood rheology.
детоксикация, реология, Реосорбилакт, молекулы средней массы, малоновый диальдегид.
детоксикація, реологія, Реосорбілакт, молекули середньої маси, малоновий дiальдегід.
detoxification, rheology, Reosorbilact, average-weight molecules, malondialdehyde.
Статья опубликована на с. 47-51
Инфузионно–детоксикационная терапия (ИДТ) в работе анестезиолога–реаниматолога является основополагающей для благоприятного исхода заболевания. Развитие хирургии, в частности так называемой большой хирургии, было бы невозможным без модернизации терапии сопровождения, в которой главенствующую роль играет ИДТ. В необходимости проведения ИДТ, конечно же, никто из врачей не сомневается, но вопрос «что использовать?» по–прежнему актуален.
Что же является главным для врача анестезиолога–реаниматолога при в выборе того или иного препарата? Основные направления инфузионной терапии:
— волюмокоррекция — восстановление адекватного объема циркулирующей крови (ОЦК) и нормализация ее состава при гиповолемии;
— гемореокоррекция — нормализация гомеостатических и реологических свойств крови;
— инфузионная регидратация — поддержание нормальной микро– и макроциркуляции (в частности, при клинически отчетливой дегидратации), нормализация электролитного баланса и кислотно–основного равновесия [9].
Общеизвестно, что главным недостатком кристаллоидов является их быстрое перераспределение из сосудистого русла в межклеточное пространство: 75–80 % введенного препарата через 1–2 ч после инфузии оказывается в интерстиции. В связи со столь непродолжительным волемическим эффектом для поддержания ОЦК при изолированном применении солевых растворов требуется введение большого объема растворов, что чревато риском развития отечного синдрома [8].
К компонентам крови относят свежезамороженную плазму (СЗП) и раствор альбумина. Общепризнано, что переливание СЗП в клинической практике проводится только с целью предотвращения или коррекции гемостатических нарушений, связанных с дефицитом факторов свертывания крови. Показания к трансфузии альбумина можно свести к необходимости коррекции дефицита общего белка и гипоальбуминемии. Кроме того, использование альбумина и СЗП ограничивается их высокой стоимостью, на порядок и более превышающей стоимость современных синтетических коллоидных плазмозаменителей [10].
Растворы на основе желатинов являются наименее токсичными, могут применяться у больных с патологией почек. Производные желатина увеличивают объем плазмы на 100 %, но этот эффект непродолжителен и составляет всего 3–4 ч [3].
При применении растворов гидроксиэтилкрахмала не отмечено повышения уровня гистамина, возникающего при прямом введении растворов желатина, не установлено появления реакций «антиген — антитело», характерных для растворов декстрана. Но в последнее время получены данные об отрицательном действии данных препаратов на систему гемостаза и высоком риске поражения почек, также следует учитывать их высокую стоимость [11].
Новые перспективы детоксикационной терапии наметились после создания оригинальных инфузионных препаратов на основе многоатомных спиртов, натрия лактата и электролитов, одним из которых является Реосорбилакт («Юрия–Фарм», Украина). Этот препарат с полифункциональным действием, обладая свойствами как кристаллоидов, так и коллоидов, нормализует несколько видов нарушений гомеостаза.
Реосорбилакт содержит сорбитол, основные катионы (Na+, К+, Са2+, Мg2+), анион Сl– и лактат-анион [7]. Благодаря гиперосмолярности Реосорбилакт вызывает поступление жидкости из межклеточного пространства в сосудистое русло, что способствует улучшению микроциркуляции и перфузии тканей [5]. Перемещение жидкости во внутрисосудистое русло сопровождается увеличением ОЦК. Благодаря мощному специфическому осмодиуретическому эффекту сорбитола, связанному с отсутствием у человека природных механизмов реабсорбции многоатомных спиртов в проксимальных почечных канальцах, отмечается выраженное диуретическое действие [4]. Кроме того, сорбитол, частично метаболизируясь до фруктозы, способствует нормализации углеводного и энергетического обмена, что особенно благоприятно сказывается на улучшении функционального состояния гепатоцитов, в которых восстанавливается депо гликогена. Пути обмена и утилизации сорбитола, фруктозы, глюкозы во многом похожи, но сорбитол обладает более выраженным антикетогенным свойством — он стимулирует окисление жирных кислот по некетогенному пути метаболизма и облегчает включение кетоновых тел в цикл Кребса, таким образом подтверждается ценность сорбитола как энергетического субстрата [1]. Сорбитол усиливает моторику кишечника за счет прямого действия на нервно-рецепторный аппарат кишечной стенки и усиления синтеза и секреции вилликинина, холецистокинина и витаминов группы В [6]. Лактат-анион, который содержится в препарате, способствует коррекции кислотно-основного равновесия плазмы, восстанавливает и стимулирует функции клеток ретикулоэндотелиальной системы печени и почек. Все вышеуказанные эффекты обусловливают спектр фармакологических свойств Реосорбилакта: противошоковое, энергетическое, детоксикационное, диуретическое, стимулирующее перистальтику кишечника действие, коррекцию метаболического ацидоза, коррекцию водно-солевого баланса [2].
Цель исследования: анализ детоксикационной способности препарата Реосорбилакт производства фармацевтической компании «Юрия-Фарм» (Украина) и его влияния на свертывающую систему.
Материал и методы
Обследовано 50 пациентов с гнойно-септическими заболеваниями, изолированными черепно-мозговыми травмами (ЧМТ), пневмониями и операциями по поводу реконструкции внутренней сонной артерии (ВСА) (табл. 1).
Подобная неоднородность исследуемых нами больных объясняется тем, что нас интересовал детоксицирующий эффект Реосорбилакта при различных токсических состояниях, вызванных инфекцией, травмой, гипоксией и гиперкапнией. Данные пациенты находились в отделениях хирургической реанимации № 1 и второй клиники Ташкентской медицинской академии с апреля по июнь 2013 года. У всех больных производилась оценка детоксицирующей функции препарата Реосорбилакт, а также его влияние на свертывающую систему.
Для суждения о степени выраженности интоксикации у всех больных нами использовалась экспрессная методика определения в крови и моче концентрации молекул средней массы (МСМ), которые, по мнению абсолютного большинства авторов, оказывают универсальный токсический эффект в результате их выраженного мембранотропного действия (Габриэлян Н.И. с соавт., 1985; Галактионов С.Г. с соавт., 1984; Огаи В.Ч., 1987).
Показатели МСМ в крови в норме составляют: при спектре 254 нм — 0,16–0,18 нмоль, при спектре 286 нм — 0,126–0,136 нмоль.
Показатели МСМ в моче в норме: при спектре 254 нм — 0,5–0,9 нмоль, при спектре 286 нм — 0,26–0,43 нмоль.
С этой же целью нами исследовался малоновый диальдегид (МДА) в крови, который образуется при перекисном окислении липидов (ПОЛ). Малоновый диальдегид является вторичным продуктом ПОЛ. Установлено, что в условиях гипоксии и при некоторых патологических состояниях, сопровождающихся гипоксией тканей, происходит накопление продуктов ПОЛ, в частности МДА (Осинская Л.Ф., 1980; Морозов А.В. и др., 1986).
Подсчет производился по методу Л.И. Андреевой и др. (1988). Показатель МДА в крови в норме составляет 2–3 нмоль/мл.
Показатель МДА в моче в норме — 6–9 нмоль/мл.
Сущность инфузионной подготовки заключалась в улучшении периферической гемоциркуляции и выведении токсинов из тканевых депо. Указанное можно рассматривать как процесс мобилизации токсинов.
Поставив задачу добиться наиболее эффективной мобилизации токсинов из тканевых депо в центральный кровоток, мы изучили уровень МСМ и МДА в венозной крови и в моче. Для более высокой достоверности исследования проводились на разных показателях длины волны спектрофотометра 254 и 286 нм.
Количество в/в введенного препарата — по 400 мл 2 раза в день со скоростью введения 40–60 капель в минуту.
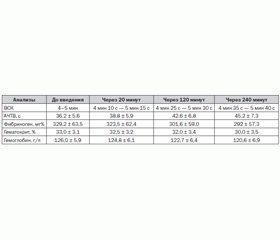
В представленных ниже табл. 2–5 показана динамика МСМ и МДА в крови и моче до в/в инфузии 400 мл Реосорбилакта и через 20, 120 и 240 минут после ее завершения.
Из табл. 3 нетрудно заметить, что после в/в инфузии Реосорбилакта в дозе 10–15 мл/кг массы тела пациентам с гнойно-септическими заболеваниями рост концентрации МСМ и МДА в плазме крови отмечался и по истечении 20 минут от момента окончания инфузии, затем концентрация МСМ и МДА снижалась в плазме крови в среднем на 22 % от исходного уровня. У больных с пневмониями, изолированными ЧМТ, хронической недостаточностью мозгового кровообращения (табл. 2, 4, 5) уже к 20-й минуте отмечалось постепенное снижение концентрации токсинов. Во всех исследуемых группах через 4 часа после инфузии Реосорбилакта концентрация МСМ и МДА в плазме крови снижалась в среднем на 65–70 %.
Данный феномен можно объяснить исходя из фармакодинамических свойств Реосорбилакта. Увеличивая объем плазмы, уменьшая вязкость крови, Реосорбилакт вызывает активизацию микрогемоциркуляции, размывание агрегатов форменных элементов крови, восстановление обмена между кровью и интерстицием во всех тканях организма, что закономерно приводит к вымыванию МСМ и МДА из микрогемоциркуляторного русла в центральный кровоток.
При параллельном исследовании МСМ и МДА в моче после инфузии Реосорбилакта через 6 часов концентрация МСМ и МДА достигала максимума, что свидетельствует об улучшении реологических свойств крови, вызванном инфузией Реосорбилакта и увеличении клубочковой фильтрации. Подтверждением указанного является рост концентрации МСМ и МДА в моче (табл. 6–9).
Выводы
1. После инфузии Реосорбилакта в дозе 10–15 мл/кг происходит значительное снижение содержания молекул средней массы и малонового диальдегида, что связано с эффектом гемодилюции и усилением экскреции их почками. Через 4 часа после инфузии Рео-сорбилакта отмечено снижение молекул средней массы на 14–40 % от исходного значения при разных заболеваниях, малонового диальдегида — на 36–72 %.
2. Реосорбилакт обладает выраженным дезинтоксикационным действием и может быть рекомендован как базовый препарат для снижения интоксикации при гнойно-септических заболеваниях, изолированных ЧМТ, пневмониях, в послеоперационном периоде после реконструкции ВСА.
3. При использовании Реосорбилакта быстро нормализовались показатели свертывающей системы крови, что свидетельствовало об улучшении реологии крови.
4. Учитывая полифункциональность Реосорбилакта, а именно наличие гемодинамического действия, выраженного дезинтоксикационного эффекта, улучшение микроциркуляции и реологии, корригирующее водно-солевой и кислотно-основный баланс, рекомендуется использовать его как универсальный раствор при различной хирургической патологии.
1. Барышев А.А. Гемодинамические плазмозаменители // Мир медицины. — 2001. — № 3–4. — С. 21–23.
2. Гаврисюк В.К., Гуменюк Н.И. Влияние реосорбилакта и реополиглюкина на состояние гемоконцентрации, вязкости крови и агрегационной способности тромбоцитов у больных с хроническим легочным сердцем // Кровообiг та гемостаз. — 2004. — № 2. — С. 39–40.
3. Габриэлян Н.И., Левицкий Э.Р., Дмитриев А.А. и др. Скрининговый метод определения средних молекул в биологических жидкостях // Метод. рекомендации. — М., 1985. — 17 с.
4. Гаврисюк В.К., Ячник А.И. Хроническое легочное сердце. — К., 1997. — 96 с.
5. Гуменюк Н.И., Лишневская В.Ю. Влияние реосорбилакта на реологические свойства крови у больных ишемической болезнью сердца и хроническим обструктивным бронхитом // Украинский пульмонологический журнал. — 2003. — № 3. — С. 38–40.
6. Молчанов И.В., Косаченко В.М., Горбачевский Ю.В. Современные методы применения коллоидных растворов в инфузионно-трансфузионной терапии // Вестник службы крови. — 1999. — С. 35–40.
7. Когония М.З., Пастернак Г.И., Ткачева М.Ю. Опыт применения отечественных препаратов реосорбилакт и сорбилакт в комплексном лечении больных с острым панкреатитом в условиях отделения интенсивной терапии // Украинский химиотерапевтический журнал. — 2008. — № 1–2 (22). — С. 172–175.
8. Dintenfass L., Julian D.G., Miller G.E. Viscosity of blood in normal subjects and in patients suffering from coronary occlusion and arterial thrombosis // Am. Heart J. — 1986. — Vol. 111. — P. 587–600.
9. Dormandy J.A., Edelman J.B. High blood viscosity an aetiological factor in venous thrombosis // Brit. J. Surg. — 1973. — Vol. 60, № 3. — P. 187–190.
10. Dormandy J.A. Clinical evidence of link between haemorheology and thrombosis // Hemostasis. — 1982. — Vol. 12, № 1. — P. 168–170.
11. Haljamäe H., Dahlqvist M., Walentin F. Artificial colloid in clinical practice: pros and cons // Clin. Anaesthesiol. — 1997. — Vol. 1. — P. 49–79.
12. Simone G., Devereux R.B., Chien S. et al. Relation of blood viscosity to demographic and physiologic variables and to cardiovascular risk factors in apparently normal adults // Circulation. — 1990. — Vol. 81, № 1. — P. 107–117.

/48/48.jpg)
/49/49.jpg)
/49/49_2.jpg)
/50/50.jpg)