Журнал «Медицина неотложных состояний» 2 (57) 2014
Вернуться к номеру
Динаміка рівня альдостерону у хворих на хронічну серцеву недостатність зі збереженою фракцією викиду під впливом лікування
Авторы: Курята О.В., Кушнір Ю.С. - ДЗ «Дніпропетровська медична академія», Кафедра госпітальної терапії № 1 та профпатології
Рубрики: Медицина неотложных состояний, Кардиология
Разделы: Клинические исследования
Версия для печати
Метою роботи було визначити динаміку рівня альдостерону за умов використання петльових діуретиків у хворих на хронічну серцеву недостатність (ХСН) зі збереженою систолічною функцією лівого шлуночка, обумовлену ішемічною хворобою серця, з урахуванням маси тіла. У дослідження залучені 42 хворі (чоловіків — 29, жінок — 13) віком від 51 до 75 років (середній вік — 68,40 ± 1,17 року) із ХСН ІІ–ІІІ функціонального класу зі збереженою фракцією викиду лівого шлуночка (понад 45 %) з ознаками затримки рідини. Всі хворі були розподілені на дві групи. Першу групу становили 26 хворих на ХСН, які як діуретик отримували торасемід (препарат Торсид, компанія «Фармак», Україна), другу — 16 пацієнтів, яким було призначено фуросемід. Окрім діуретиків усі хворі отримували стандартну терапію. Хворим на початку дослідження та через 14 днів додатково визначали кількісні рівні альдостерону та мікроальбумінурії. Встановлено, що рівень альдостерону у хворих на ХСН зі збереженою фракцією викиду залежить від маси тіла. Використання фуросеміду обумовлювало підвищення рівня альдостерону, проте на тлі прийому торасеміду рівень альдостерону знижувався. Максимальний негативний вплив зареєстровано у хворих з ожирінням.
Целью работы было определить динамику уровня альдостерона при использовании петлевых диуретиков у больных с хронической сердечной недостаточностью (ХСН) с сохраненной систолической функцией левого желудочка, обусловленной ишемической болезнью сердца, учитывая массу тела. В исследование было включено 42 больных (мужчин — 29, женщин — 13) в возрасте от 51 до 75 лет (средний возраст — 68,40 ± 1,17 года) с ХСН ІІ–ІІІ функционального класса с сохраненной фракцией выброса левого желудочка (больше 45 %) с признаками задержки жидкости. Все больные были разделены на две группы. Первую группу составили 26 больных с ХСН, которые в качестве диуретика получали торасемид (препарат Торсид компании «Фармак», Украина), вторую — 16 пациентов, которым был назначен фуросемид. Кроме диуретиков все больные получали стандартную терапию. Больным в начале исследования и через 14 дней определяли количественные уровни альдостерона и микроальбуминурии. Установлено, что уровень альдостерона у больных с ХСН и сохраненной фракцией выброса зависит от массы тела. Использование фуросемида обусловливало повышение уровня альдостерона, однако на фоне приема торасемида уровень альдостерона снижался. Максимально негативное влияние зарегистрировано у больных с ожирением.
The aim of the study was to determine the dynamics of aldosterone level when using loop diuretics in patients with chronic heart failure (CHF) and preserved left ventricular ejection fraction conditioned by coronary heart disease, taking into account the body mass. The study included 42 patients (29 males, 13 females) aged 51 to 75 years (mean age 68.40 ± 1.17 years) with CHF II–III functional class with preserved left ventricular ejection fraction (more than 45 %) with signs of fluid retention. All patients were divided into two groups. The first group included 26 patients with CHF, who received torasemid as a diuretic (Torsid, manufactured by Farmak, Ukraine), the second one — 16 patients, administered with furosemide. In addition to diuretics all patients received standard therapy. At baseline and in 14 days we defined in patients quantitative levels of aldosterone and microalbuminuria. It is found that the aldosterone level in patients with CHF and preserved ejection fraction depends on the body mass. The use of furosemide сaused the increase of aldosterone level, however, on the background of torasemide administration, aldosterone level decreased. The maximum negative impact was registered in patients with obesity.
хронічна серцева недостатність, збережена фракція викиду, альдостерон, петльові діуретики.
хроническая сердечная недостаточность, сохраненная фракция выброса, альдостерон, петлевые диуретики.
chronic heart failure, preserved ejection fraction, aldosterone, loop diuretics.
Статья опубликована на с. 57-62
Незважаючи на досягнення сучасної медицини, поширеність хронічної серцевої недостатності (ХСН) не тільки не знижується, але й продовжує зростати [2, 4]. Дослідження останніх років свідчать про збільшення кількості хворих із симптомами серцевої недостатності при фракції викиду (ФВ) лівого шлуночка ≥ 45 % [6, 22]. На жаль, на сучасному етапі узгодженого погляду на лікування цієї категорії хворих не розроблено. Дослідження CHARM–PRESERVED, I–PRESERVED, PEP–CHF завершені, але не продемонстрували значного впливу на кінцеві точки [11, 20, 21, 24].
Важливу роль у розвитку та прогресуванні ХСН має ожиріння [2], але результати досліджень не є однозначними. За літературними даними, існує так званий «парадокс ожиріння», при якому смертність у хворих із нормальною масою тіла вища, ніж у хворих із надлишковою вагою та ожирінням [19].
З накопиченням даних щодо патогенезу ХСН змінюються парадигми ведення таких хворих. В основу лікування включено інгібітори ангіотензинперетворюючого ферменту (АПФ), бета-блокатори, блокатори мінералокортикоїдних рецепторів та при незначних ознаках застою — діуретична терапія. Згідно з рекомендаціями Європейської асоціації кардіологів (2012), діуретики можуть бути використані за необхідності для полегшення ознак та симптомів затримки рідини незалежно від показника ФВ, але не показані для зниження ризику госпіталізацій та смерті (клас І, рівень В) [18]. Згідно з даними Американської асоціації серця (2006–2009), діуретики рекомендують призначати за наявності симптомів затримки рідини (ортопное, симетричні набряки, посилення задухи, пульсація яремних вен, гепатомегалія та симетричні вологі хрипи у легенях) тривало та безперервно [9].
За даними літератури, діуретична терапія супроводжується збільшенням активності ангіотензину ІІ (А ІІ) та альдостерону [1, 8, 17]. Неодноразово продемонстровано, що високий плазмений рівень альдостерону ініціює розвиток фіброзу та сприяє накопиченню колагену [3, 4]. Для запобігання гіпертрофії лівого шлуночка та стимуляції її регресії обов’язковою є старт-терапія інгібіторами АПФ або блокаторами рецепторів А ІІ. Однак вони тільки транзиторно пригнічують продукцію альдостерону, плазмений вміст якого у хворих із ХСН збільшено на 40 % навіть на тлі постійної терапії інгібіторами АПФ. Цей феномен отримав назву «вислизування альдостерону» та значно обмежує терапевтичний ефект інгібіторів ренін-ангіотензинової системи (РАС) [3].
До останнього часу серед петльових діуретиків здебільшого використовували фуросемід. У даний час накопичуються дані щодо його негативного впливу на рівень гормональної активності в нирках, на швидкість клубочкової фільтрації (ШКФ) на тлі значного коливання його біодоступності залежно від рівня білка в плазмі та сечі [8].
Становить інтерес здатність торасеміду позитивно впливати на РАС [1, 8]. З іншого боку, в експериментальних дослідженнях встановлено, що торасемід блокує вазоспазм і знижує рівень альдостерону в результаті впливу на рівень карбокситермінальної протеїнкінази та зменшення процесу депонування колагену [4]. При цьому позитивний ефект торасеміду щодо альдостерону є особливо важливим, оскільки згідно з сучасними уявленнями альдостерону відводиться ключова роль у прогресуванні як діастолічної, так і систолічної дисфункції серця [3]. На тлі прийому торасеміду відбувається зниження депонування колагену в міокарді та індексу фіброзу міокарда на 30 % (Lopez B. et al., 2004) [17].
Мета роботи — визначити динаміку рівня альдостерону за умов використання петльових діуретиків у хворих на хронічну серцеву недостатність зі збереженою фракцією викиду, обумовлену ішемічною хворобою серця (ІХС), з урахуванням маси тіла.
Матеріали та методи дослідження
У дослідження залучені 42 хворі (чоловіків — 29, жінок — 13) у віці від 51 до 75 років (середній вік — 68,40 ± 1,17 року) із ХСН ІІ–ІІІ функціонального класу (ФК) згідно з класифікацією Нью-Йоркської асоціації серця (NYHA), обумовленою ішемічною хворобою, зі збереженою систолічною функцією лівого шлуночка (ФВ понад 45 %) з ознаками затримки рідини.
Діагностику ХСН проводили згідно з Наказом МОЗ України № 436 від 03.07.06 р., рекомендаціями Української асоціації кардіологів та Європейського товариства кардіологів [5, 7, 18]. ХСН визначали за наявності об’єктивних та суб’єктивних ознак, притаманних цьому клінічному синдрому, проводили збір анамнестичних даних, фізикальне обстеження з використанням лабораторно-інструментальних методів дослідження.
Критерії включення: наявність ХСН ІІ–ІІІ функціонального класу, обумовлена ІХС; ФВ ≥ 45 %; індекс маси тіла (ІМТ) ≥ 18,5 < 40 кг/м2; інформована згода хворого.
Критерії виключення: гостра серцева недостатність, інфаркт міокарда та порушення мозкового кровообігу в анамнезі до 6 місяців, гострі порушення ритму, що обумовлюють порушення гемодинаміки, фракція викиду менше 45 %, ХСН І, ІV функціонального класу, ожиріння ІІІ–ІV ступеня, гіпотиреоз, швидкість клубочкової фільтрації ≤ 60 мл/хв/1,73 м2, захворювання крові.
Стенокардію діагностовано у 31 (73,8 %) хворого, у всіх 42 (100,0 %) хворих — артеріальна гіпертензія, у тому числі у 26 (61,9 %) — ІІ стадії, у 16 (38,1 %) — ІІІ стадії; 11 пацієнтів (26,2 %) мали в анамнезі (більше півроку) інфаркт міокарда, 5 (11,9 %) — порушення мозкового кровообігу. При обчисленні ІМТ у хворих із ХСН виявлено 18 хворих (42,9 %) з ожирінням І–ІІ ступеня (ІМТ 30,0–39,9 кг/м2), 14 (33,3 %) — з підвищеним ІМТ (25,0–29,9 кг/м2) та 10 (23,8 %) — з нормальним ІМТ (18,5–24,9 кг/м2). Всі пацієнти отримували базисну терапію відповідно до стандартів лікування хворих на ХСН (Наказ МОЗ України від 03.07.2006 р. № 436): 41 хворий (97,6 %) — інгібітори АПФ, 28 (66,7 %) — b-адреноблокатори, 31 (73,8 %) — статини, 16 (38,1 %) — нітрати, 4 (9,5 %) — антагоністи кальцію, антагоністи альдостерону — 9 (21,4 %).
Всі обстежені хворі на ХСН, які потребували призначення діуретиків, випадковим чином були розподілені на дві групи. Першу групу становили 26 хворих на ХСН, які як діуретик отримували торасемід (препарат Торсид компанії «Фармак», Україна), другу — 16 пацієнтів, яким було призначено фуросемід. Окрім діуретиків усі хворі отримували стандартну терапію ХСН, порівнянну в обох групах. Оцінка клінічної ефективності лікування та динаміки альдостерону проводилась через 10–14 днів. Середні дози для обох препаратів були порівнянні і становили 15,0 ± 1,8 мг для торасеміду та 53,8 ± 5,4 мг для фуросеміду (співвідношення середніх доз торасеміду та фуросеміду приблизно 1 : 3).
Для клінічної оцінки функції нирок визначали рівень креатиніну в сироватці крові та обчислювали швидкість клубочкової фільтрації за формулою Cocroft — Gault або MDRD (за наявності ожиріння). Визначення ШКФ за формулою Cocroft — Gault проводилось згідно з рекомендаціями Американської національної федерації нирок [16]. Визначення мікроальбумінурії (МАУ) проводилося імунотурбодиметричним методом із використанням реактиву I.S.E. S.r.l. (Італія). Вміст альбуміну оцінювався в першій порції ранкової сечі. Нормальні значення знаходились у діапазоні 0–30 мг/л.
Хворим на початку дослідження та через 14 днів визначали кількісний рівень альдостерону методом імуноферментного аналізу в сироватці крові за допомогою наборів реактивів фірми DRG (Німеччина). Для цього вранці натщесерце хворим проводився забір 5 мл крові в положенні лежачи у стані спокою не менше ніж 2 години, потім зразок крові центрифугували та заморожували при t –20 °С.
Для статистичного аналізу даних використовували ліцензійну програму Statistica 6.1. Первинна обробка отриманих даних проводилася методами описової статистики з представленням кількісних даних у вигляді середньої арифметичної (М), її стандартної похибки (± m), 95% довірчого інтервалу (95% СІ). Враховуючи невелику кількість спостережень, а також відхилення від нормального закону розподілу даних в окремих групах та на різних етапах спостереження, для порівняння використовували непараметричні методи: для середніх показників — Т-критерій Вілкоксона (у динаміці), U-критерій Манна — Уїтні (між групами), для відносних показників — критерій хі-квадрат Пірсона (x2). Для оцінки взаємозв’язку між ознаками виконувався кореляційний аналіз із розрахунком коефіцієнтів рангової кореляції Спірмена (r). Критичне значення рівня значимості (р) приймалося ≤ 0,05.
Результати дослідження
За основними характеристиками досліджені хворі на ХСН вірогідно не відрізнялись між собою (табл. 1).
У початковому стані ХСН ІІ ФК (NYHA) виявлено у 30,8 % пацієнтів І групи та у 37,5 % ІІ групи; ІІІ ФК (NYHA) —у 69,2 та 62,5 % відповідно (р = 0,653 між групами). За час дослідження на тлі терапії в обох групах встановлена вірогідна позитивна динаміка ФК. Так, у І групі ФК у середньому зменшився з 2,69 ± 0,09 до 2,31 ± 0,12 (р = 0,005), у ІІ групі — з 2,63 ± 0,13 до 2,25 ± 0,14 (р = 0,028) (рис. 1), при цьому різниця між порівнюваними групами не є вірогідною (р = 0,723). Позитивна динаміка ФК асоціювалась із покращенням самопочуття у хворих. Так, у першій групі скарги на загальну слабкість зменшились на 46,2 %; задишку — на 61,5 %; набряки нижніх кінцівок — на 92,3 %; болі в ділянці серця — на 19,2 %; у другій групі — на 37,5; 62,5; 87,5; 12,5 % відповідно.
/59/59.jpg)
При виконанні тесту з 6–хвилинною ходьбою в обох групах було виявлено вірогідне підвищення толерантності до фізичного навантаження при певній перевазі за умов використання торасеміду (препарат Торсид компанії «Фармак», Україна) (рис. 2).
/60/60.jpg)
У групі з торасемідом збільшення середньої дистанції при виконанні проби з 6-хвилинною ходьбою становило 17,2 ± 2,6 %, у групі з фуросемідом — 9,6 ± 1,4 % (р = 0,03 між групами).
На тлі терапії як фуросемідом, так і торасемідом спостерігалась позитивна динаміка зменшення показників систолічного та діастолічного артеріального тиску (р < 0,05), при цьому між групами вірогідної різниці не виявлено (р > 0,05).
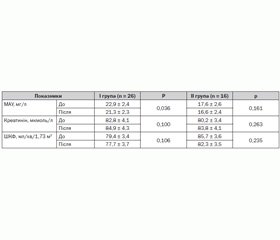
Мікроальбумінурію виявлено в 6 з 42 хворих (14,3 %). За час лікування рівень МАУ знижувався в обох групах, але вірогідно тільки в групі з торасемідом (р = 0,036) (табл. 2). Вірогідної динаміки креатиніну та ШКФ за період спостереження не виявлено.
Встановлено, що петльові діуретики по-різному впливають на рівень альдостерону (табл. 3). Так, у групі фуросеміду встановлено підвищення альдостерону на 8,4 %, що може бути оцінено як негативний вплив. У той же час у групі торасеміду такого впливу не виявлено, а, навпаки, після лікування зареєстровано певне зниження рівня альдостерону (у середньому на 2,3 %) (р < 0,001 при порівнянні між групами). Аналіз динаміки концентрації альдостерону на індивідуальному рівні показав її зниження у 16 з 25 хворих І групи (64,0 %), і в жодного хворого з ІІ групи (р < 0,001) зменшення показника не було.
За результатами кореляційного аналізу встановлено тісний взаємозв’язок між рівнем альдостерону у хворих із ХСН та ІМТ як на початку дослідження (коефіцієнт кореляції r = 0,91; p < 0,001), так і під впливом терапії (r = 0,88; p < 0,001 — у І групі і r = 0,96; p < 0,001 — у ІІ групі). З урахуванням цього було проаналізовано динаміку показників альдостерону в підгрупах хворих із нормальною або підвищеною масою тіла та з ожирінням І–ІІ ступеня при прийомі різних діуретиків (табл. 4).
Встановлено, що початковий рівень альдостерону у хворих із ХСН та ожирінням І–ІІ ступеня майже вдвічі перевищував такий показник у хворих із нормальною або надлишковою масою тіла — 842,4 ± 32,6 пг/мл проти 476,3 ± 23,2 пг/мл (p < 0,001).
За період спостереження в обох групах торасеміду та фуросеміду відзначалось зниження маси тіла на 1,44 ± 0,12 кг (1,68 ± 0,12 % від початкової маси тіла) та 1,63 ± 0,17 кг (1,77 ± 0,17 %) відповідно (р > 0,40 при всіх порівняннях між групами за критерієм Манна — Уїтні). При цьому відсоток зниження маси тіла від початкового рівня вірогідно не залежав від ІМТ та обраного діуретика.
Рівень альдостерону за обраний термін лікування торасемідом знизився в середньому на 4,4 % (р = 0,007) у хворих із нормальною або підвищеною масою тіла і практично не змінився в пацієнтів з ожирінням (р = 0,878) (табл. 4). Аналіз динаміки показника на індивідуальному рівні показав його зниження у 12 з 15 хворих з нормальним або підвищеним ІМТ (80,0 %) і лише в 4 із 10 хворих (40,0 %) з ожирінням (р = 0,041 за критерієм x2). На тлі терапії фуросемідом концентрація альдостерону вірогідно підвищувалась в обох підгрупах (р = 0,012), але більш інтенсивно у хворих з ожирінням.
Обговорення результатів
Результати багатоцентрового дослідження TORIC, у якому порівнювався фуросемід із торасемідом у хворих із клінічно вираженою серцевою недостатністю, продемонстрували переваги торасеміду не тільки щодо покращення клініко-функціонального стану, але також щодо його впливу на смертність хворих та профілактику кардіоваскулярних ускладнень [10, 14].
Низка досліджень свідчать, що на відміну від фуросеміду торасемід зменшує продукцію альдостерону, а також попереджує його зв’язування з відповідними рецепторами, у тому числі локально на рівні кардіоміоцитів [4, 17]. Метою нашої роботи було порівняти вплив торасеміду на клінічний стан, а також вивчити його можливі додаткові властивості впливати на рівень альдостерону, можливо, з урахуванням маси тіла. Вплив торасеміду на рівень альдостерону може бути важливим напрямком тривалого лікування хворих із ХСН. Адже в плацебо-контрольованому дослідженні TOPCAT показано, що альдостерон та обумовлена ним активація мінералокортикоїдних рецепторів викликають виникнення та прогресування міокардіального та судинного фіброзу [23]. Згідно з висновками рандомізованих клінічних досліджень RALES, EPHESUS та EMPHASIS, антагоністи мінералокортикоїдних рецепторів (спіронолактон, еплеренон) знижують загальну смертність та частоту госпіталізацій у пацієнтів із ХСН [4]. Проте ці дослідження стосуються лише хворих із ХСН та систолічною дисфункцією лівого шлуночка, у той час як при збереженій фракції викиду дані відсутні, хоча питома вага у структурі ХСН таких хворих є досить високою. До того ж не враховувалось можливе значення маси тіла хворих.
Хворі на ХСН досить часто потребують діуретичної терапії з метою попередження ретенції рідини, тому диференційний вибір петльового діуретика є важливим для профілактики ускладнень та представляє перспективний напрямок.
Певним обмеженням нашого дослідження є те, що рівень креатиніну досліджувався лише в плазмі та обраний гострофазовий термін лікування (10–14 днів). За літературними даними, при вживанні петльових діуретиків спочатку спостерігається приріст креатиніну переважно в сечі, а з 5–7-ї доби в плазмі [13]. Тому пролонгація дослідження в більш віддаленому періоді може бути перспективною.
Висновки
1. У хворих на ХСН зі збереженою фракцією викиду рівень альдостерону залежить від маси тіла.
2. Використання фуросеміду у даної категорії хворих обумовлювало підвищення рівня альдостерону, проте на тлі прийому торасеміду рівень альдостерону знижувався. Максимальний негативний вплив зареєстровано у хворих з ожирінням.
3. При клінічній порівнянності петльових діуретиків та впливу на рівень креатиніну торасемід мав перевагу щодо рівня мікроальбумінурії.
1. Гендлин Г.Е. Современная диуретическая терапия пациентов с хронической сердечной недостаточностью / Г.Е. Гендлин, Е.Е. Рязанцева // Клиническая фармакология. — 2012. — № 1.
2. Горбась І.М. Епідеміологічні аспекти хронічної серцевої недостатності у дорослого населення України / І.М. Горбась, Л.Г. Воронков // Український кардіологічний журнал. — 2008. — № 7.
3. Коваленко В.Н. Сердечно-сосудистые заболевания и ренин–ангиотензиновая система / В.Н. Коваленко, Т.В. Талаева, В.В. Братусь — К.: Морион, 2013. — С. 232.
4. Применение диуретиков при лечении больных с ХСН / Материалы международной конференции с участием профессора Л.Г. Воронкова и профессора Г.П. Арутюнова // Серцева недостатність. — 2013. — № 3. — С. 79–85.
5. Про затвердження протоколів надання медичної допомоги за спеціальністю «Кардіологія». Наказ МОЗ України від 03.07.2006 № 436. — Режим доступу: www.moz.gov.ua
6. Распространенность хронической сердечной недостаточности в Европейской части Российской Федерации — данные ЭПОХА-ХСН / И.В. Фомин, Ю.Н. Беленков, В.Ю. Мареев [и др.] // Сердечная недостаточность. — 2006. — Т. 7, № 3. — С. 112–115.
7. Рекомендації Асоціації кардіологів України з лікування хронічної серцевої недостатності у дорослих (перегляд 2011) / Л.Г. Воронков, К.М. Амосова, А.Е. Багрій [та ін.] // Серцева недостатність. — 2011. — № 1. — С. 101–116.
8. Целуйко В. И. Диуретики при сердечной недостаточности: знакомые незнакомцы / В.И. Целуйко // Здоров’я України. — 2011. — Додаток № 1. — С. 64–65.
9. 2009 Focused Update: ACCF/AHA Guidelines for the Diagnosis and Management of Heart Failure in Adults // Circulation. — 2009. — Vol. 119. — P. 1977–2016.
10. Ahmed Ali. Heart failure, chronic diuretic use, and increase in mortality and hospitalization: an observational study using propensity score methods / Ali Ahmad, Robert C. Bourge // European Heart Journal — 2006. — Vol. 27 (12). — P. 1431–1439.
11. Association between use of renin angiotensin system antagonists and mortality in patients with heart failure and preserved ejection fraction / L.H. Lund, L. Benson, U. Dahlstrom, M. Edner // JAMA. — 2012. — Vol. 308. — P. 2108–2117.
12. Borlaug B.A. Heart failure with preserved ejection fraction: pathophysiology, diagnosis, and treatment / B.A. Borlaug, W.J. Paulus // Eur. Heart J. — 2011. — Vol. 32. — P. 670–679.
13. Clinical outcome of renal tubular damage in chronic heart failure. Kevin Damman, Serge Masson, Hans L. Hillege, Aldo P. Maggioni, Adriaan A. Voors [et al.] // Eur. Heart J. — 2011. — Vol. 32 (21). — P. 2705–2712.
14. Cosin Juan. Torasemide in chronic heart failure: results of the TORIC study / Juan Cosín, Javier Díez // European Journal of Heart Failure — 2002. — Vol. 4 (4). — Р. 507–513.
15. Definition and classification of chronic kidney disease: a position statement from Kidney Disease: Improving Global Outcomes (KDIGO) / A.S. Levey, K.U. Eckardt, Y. Tsukamoto [et al.] // Kidney Int. — 2005. — Vol. 67. — P. 2089–2100.
16. Dirk J. van Veldhuisen. Pharmacological treatment of heart failure with preserved ejection fraction: a glimpse of light at the end of the tunnel? / Dirk J. van Veldhuisen, and John J.V. McMurray // European Journal of Heart Failure. — 2013. — Vol. 15 (1). — P. 5–8.
17. Effects of loop diuretics on myocardial fibrosis and collagen type I turnover in chronic heart failure / B. Lopez, R. Querejrta, A. Gonzalez [et al.] // J. Am. Coll. Cardiol. — 2004. — Vol. 43 (11). — P. 2028–2035.
18. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012 // Eur. Heart J. — 2012. — Vol. 33. — P. 1787–1847.
19. Haehling S. Anker Revisiting the obesity paradox in heart failure: new insights? / S. Haehling, W. Doehner // Eur. J. Heart Fail. — 2011. — Vol. 13 (2). — P. 130–132.
20. Heart failure with preserved ejection fraction: clinical characteristics of 4133 patients enrolled in the I–PRESERVE trial / J.J. McMurray, P.E. Carson, M. Komajda, R. McKelvie [ et al.] // European Journal of Heart Fail. — 2008. — Vol. 10. — P. 149–156.
21. Irbesartan in patients with heart failure and preserved ejection fraction / B.M. Massie, P.E. Carson, J.J. McMurray [et al.] // N. Engl. J. Med. — 2008. — № 4. — Р. 359.
22. Prognosis of heart failure with preserved ejection fraction: a 5 year prospective population–based study / C. Tribouilloy, D. Rusinaru [et al.] // Eur. Heart J. — 2008. — Vol. 28, № 3. — P. 339–347.
23. Sanderson J.E. Heart failure with a normal ejection fraction / J.E. Sanderson // Heart. — 2007. — Vol. 93. — P. 155–158.

/59/59_2.jpg)
/60/60_2.jpg)
/61/61.jpg)