Журнал «Neoplasm» 1(13) 2014
Вернуться к номеру
Неоадъювантная химиолучевая терапия резектабельного рака прямой кишки дистальных локализаций
Авторы: Думанский Ю.В., Башеев В.Х., Бондаренко Н.В., Золотухин С.Э., Совпель И.В. - Донецкий областной противоопухолевый центр; Донецкий национальный медицинский университет им. М. Горького
Рубрики: Онкология
Разделы: Клинические исследования
Версия для печати
В Донецком областном противоопухолевом центре разработан способ комбинированного неоадъювантного лечения резектабельного рака прямой кишки, который состоит в предоперационном крупнофракционном интенсивном облучении на фоне эндолимфатической химиотерапии 5-фторурацилом и последующем хирургическом лечении в течение 48 ч. В контрольные подгруппы вошли пациенты, получившие неоадъювантный курс внутривенной химиолучевой терапии или только курс лучевой терапии. Оценка состава исследуемых и контрольных групп больных показала их полную идентичность по основным прогностическим признакам. Послеоперационные осложнения отмечены у 8 (12,5 %) пациентов в исследуемой группе и у 10 (15,87 %) и 13 (14,29 %) — в контрольных подгруппах. Показатели 5-летней выживаемости в исследуемой группе составили 73,5 ± 6,3 %, в контрольных подгруппах — 64,6 ± 5,8 % и 64,4 ± 6,8 %. Частота местного рецидивирования в исследуемой группе составила 6,2 ± 3,0 %, а частота отдаленного метастазирования — 15,6 ± 4,5 %.
In Donetsk regional antitumor center, the method of combined neoadjuvant treatment of resectable rectal cancer was developed, it consists in preoperative large-fraction intensive irradiation on the background of endolymphatic 5-fluorouracil chemotherapy and followed surgical treatment within 48 hours. The control subgroups consisted of patients who received neoadjuvant course of intravenous chemoradiotherapy or just a course of radiotherapy. Assessment of the study and control groups of patients showed their complete identity by the main prognostic features. Postoperative complications were observed in 8 (12.5 %) patients from the study and in 10 (15.87 %) and 13 (14.29 %) — in the control subgroups. 5-year survival rate in the study group was 73.5 ± 6.3 %, in the control subgroups — 64.6 ± 5.8 % and 64.4 ± 6.8 %. The local recurrence rate in the study group was 6.2 ± 3.0 %, and the incidence of distant metastases — 15.6 ± 4.5 %.
У Донецькому обласному протипухлинному центрі розроблений спосіб комбінованого неоад’ювантного лікування резектабельного раку прямої кишки, що полягає в передопераційному великофракційному інтенсивному опроміненні на фоні ендолімфатичної хіміотерапії 5-фторурацилом і наступному хірургічному лікуванні протягом 48 год. У контрольні підгрупи ввійшли пацієнти, що одержали неоад’ювантний курс внутрішньовенної хіміопроменевої терапії або тільки курс променевої терапії. Оцінка складу досліджуваних і контрольних груп хворих показала їхню повну ідентичність за основними прогностичними ознаками. Післяопераційні ускладнення відзначені у 8 (12,5 %) пацієнтів у досліджуваній групі й в 10 (15,87 %) і 13 (14,29 %) — у контрольних підгрупах. Показники 5-річної виживаності в досліджуваній групі склали 73,5 ± 6,3 %, у контрольних підгрупах — 64,6 ± 5,8 % і 64,4 ± 6,8 %. Частота місцевого рецидивування в досліджуваній групі склала 6,2 ± 3,0 %, а частота віддаленого метастазування — 15,6 ± 4,5 %.
рак прямой кишки, предоперационная лучевая терапия, эндолимфатическая химиотерапия, отдаленные результаты лечения.
rectal cancer, preoperative radiotherapy, endolymphatic chemotherapy, long-term results.
рак прямої кишки, передопераційна променева терапія, ендолімфатична хіміотерапія, віддалені результати лікування.
Статья опубликована на с. 13-19
Анализ публикаций последних лет свидетельствует о росте заболеваемости колоректальным раком во всем мире. Рак прямой кишки, составляя 2–10 % всех злокачественных новообразований, 25–30 % опухолей желудочно-кишечного тракта и 40–45 % колоректального рака, по темпам прироста вышел на первое место в большинстве развитых стран. Заболеваемость больных раком прямой кишки в Украине в 2010 году составила 20,4 на 100 000 населения, что значительно выше по сравнению с 2000 годом, когда заболеваемость злокачественными новообразованиями составляла 16,6 на 100 000 населения [1, 2].
На сегодняшний день безусловным и единственным методом, позволяющим надеяться на радикальное излечение, независимо от формы течения и распространенности опухолевого процесса, остается хирургический. По данным большинства исследователей, несмотря на совершенствование оперативной техники, отдаленные результаты после чисто хирургического лечения остаются на одном уровне в течение уже многих десятилетий, 5–летняя выживаемость составляет в среднем 55–60 % [3–5]. В связи с этим одной из приоритетных задач развития онкопроктологии на современном этапе является разработка и внедрение в клиническую практику новых протоколов комбинированного и комплексного лечения рака прямой кишки, направленных на дополнение хирургического метода химиолучевой терапией.
Имеющиеся в литературе статистические данные свидетельствуют о недостаточной эффективности современных способов комбинированного лечения резектабельного рака прямой кишки, не позволяющих существенно улучшить отдаленные результаты. На сегодняшний день основные усилия направлены на совершенствование неоадъювантных методов предоперационного воздействия на опухолевый процесс с целью повышения абластики радикального хирургического вмешательства. В то же время изучение опубликованных на сегодняшний день результатов проведенных исследований эффективности предоперационной лучевой терапии (ЛТ) в лечении рака прямой кишки не показало значительного прогресса в улучшении отдаленных результатов, в том числе при сочетании лучевого лечения с традиционными методами химиотерапии. Предоперационная лучевая терапия достоверно снижает частоту местного возврата заболевания, однако не влияет на частоту отдаленного метастазирования и, соответственно, на продолжительность жизни пациентов. Лишь в отдельных сообщениях приводятся данные, свидетельствующие о повышении 5-летней выживаемости на несколько процентов либо об увеличении только безрецидивной выживаемости [2, 6, 7]. Огромное разнообразие методик предоперационной ЛТ, различия в дозах и схемах их дробления, объемах облучения, а также интервалах между окончанием ЛТ и оперативным вмешательством приводят к значительным различиям в результатах и затрудняют их интерпретацию [8, 9].
Цель работы. Улучшение отдаленных результатов лечения резектабельного рака прямой кишки дистальных локализаций за счет оптимизации схемы предоперационной химиолучевой терапии.
Материалы и методы исследования
Теоретическим обоснованием предложенного в Донецком областном противоопухолевом центре нового неоадъювантного способа предоперационного воздействия, заключающегося в дополнении предоперационного интенсивного облучения эндолимфатической химиотерапией, стали исследования фармакокинетики и фармакодинамики при эндолимфатическом введении 5-фторурацила. Результаты этих исследований показали более длительную и высокую терапевтическую концентрацию в крови лекарственного вещества, объясняющую высокую эффективность лечения злокачественных опухолей [8, 10, 11] (рис. 1).
Суть метода заключается в следующем (Патент України на корисну модель № 63036 от 26.02.2011 г.). За 24 часа до начала облучения выполняют катетеризацию лимфатического сосуда на бедре. Инфузию 5-фторурацила начинают за 24 часа до начала облучения и в последующем проводят ежедневно в течение 5 дней, разовая доза обычно не превышает 425 мг/м2, суммарная — 5 граммов. С целью модуляции эффекта введение 5-фторурацила дополнялось внутривенным введением лейковoрина в дозировке 60 мг/сут. В нашем исследовании лучевую терапию проводили методом подвижного интенсивного ежедневного облучения разовой очаговой дозой 5 Гр до суммарной дозы 25 Гр. После окончания предоперационной терапии в течение 48 ч выполняли хирургическое вмешательство в объеме брюшноанальной резекции прямой кишки.
В исследование эффективности разработанного предоперационного неоадъювантного способа лечения рака прямой кишки с использованием эндолимфатической химиотерапии на фоне интенсивного лучевого лечения включены 64 первичных пациента с резектабельным раком прямой кишки (группа ИКЛТ + э/л ХТ). Критериями включения явились следующие. Локализация опухоли соответствовала 3–9 см от ануса (ниже уровня тазовой брюшины и без вовлечения структур тазового дна), что характерно для более 60 % больных со злокачественным поражением прямой кишки. Возрастная категория до 70 лет, без тяжелой сопутствующей патологии и осложненного течения, что позволяет исключить влияние последних на выбор тактики специального лечения. Все пациенты получили комбинированное лечение на базе проктологического отделения ДОПЦ в период с 2004 по 2009 г. С учетом того, что повсеместно распространенными и рекомендуемыми методами неоадъювантного лечения рака прямой кишки являются как только лучевая терапия, так и комбинация лучевой терапии и химиотерапии, контрольная группа была разделена на 2 подгруппы сравнения. В первую подгруппу вошли 63 больных резектабельным раком прямой кишки с аналогичными параметрами включения в исследование, получивших стандартный неоадъювантный предоперационный курс крупнофракционного облучения по интенсивной программе на фоне внутривенной химиотерапии (группа ИКЛТ + в/в ХТ). Во вторую контрольную подгруппу сравнения вошел 91 пациент, получивший в предоперационном периоде только крупнофракционный курс лучевой терапии (группа ИКЛТ). После проведенного неоадъювантного лечения пациенты контрольных и исследуемой групп были оперированы в радикальном объеме в течение 48 часов.
Результаты и их обсуждение
Оценка состава исследуемой и контрольных групп показала их полную идентичность по основным прогностическим признакам.
Интраоперационные осложнения, а именно перфорации опухоли или стенки кишки на этапе мобилизации, в группе, получившей ИКЛТ + э/л ХТ, возникли в 1 (1,6 %) случае. В группе, получившей ИКЛТ + в/в ХТ, данные осложнения наблюдались в 4 (6,3 %) случаях. В группе, получившей ИКЛТ, — в 2 (2,2 %) случаях. В 1 (0,5 %) случае в группе, получившей ИКЛТ, на этапе мобилизации прямой кишки произошло кровотечение из пресакральных вен, которое не носило тяжелого характера и было остановлено с помощью электросварочного комплекса и тампонирования полости малого таза марлевым тампоном. Послеоперационные осложнения суммарно по 3 группам отмечены в 31 (14,2 %) случае. В исследуемой группе, получившей ИКЛТ + э/л ХТ, послеоперационные осложнения отмечены в 8 (12,5 %) случаях, в группах сравнения, где проведены ИКЛТ + в/в ХТ и ИКЛТ, послеоперационные осложнения отмечены в 10 (15,9 %) и 13 (14,3 %) случаях соответственно. Основной удельный вес в исследуемой и контрольной группах в целом пришелся на гнойно-септические процессы — 14 (6,4 %). Наиболее частое осложнение после выполнения тотальной мезоректумэктомии — развитие абсцесса в малом тазу. Данное осложнение возникло в 3 (4,7 %) случаях в группе, получившей ИКЛТ + э/л ХТ. В группах, получивших ИКЛТ + в/в ХТ и ИКЛТ, абсцедирование в малом тазу было отмечено в 3 (4,8 %) и 4 (4,4 %) случаях соответственно суммарно в структуре всех осложнений. Некроз низведенной кишки развился в целом по 3 группам у 10 (4,6 %) пациентов. Некроз низведенной кишки в группе, получившей ИКЛТ + э/л ХТ, развился в 3 (4,7 %) случаях. На некрозы низведенной кишки в группах сравнения, где была проведена ИКЛТ + в/в ХТ и ИКЛТ, пришлось по 3 и 4 наблюдения — соответственно 4,9 и 4,1 %. Во всех случаях некроза низведенной кишки были предприняты повторные оперативные вмешательства. В нашем исследовании зафиксирован 1 (1,1 %) летальный исход в группе, получившей ИКЛТ. В целом по 3 группам послеоперационная летальность составила 0,5 %.
Таким образом, частота и характер послеоперационных осложнений существенно не отличались не только в группах, но и в сравнении с данными литературы, что позволило характеризовать разработанный способ неоадъювантного химиолучевого лечения как не ухудшающий непосредственные показатели [3, 5, 11].
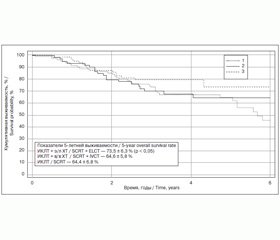
Результаты изучения выживаемости в исследуемой и группах сравнения представлены на рис. 2.
Изучение 5-летней выживаемости по группам продемонстрировало преимущество разработанного способа неоадъювантного предоперационного воздействия с использованием эндолимфатической химиотерапии и интенсивного крупнофракционного облучения перед традиционной внутривенной химиолучевой терапией и только лучевой терапией. Применение предоперационного крупнофракционного облучения на фоне эндолимфатической химио–терапии позволило увеличить показатель 5-летней выживаемости до 73,5 ± 6,3 % в сравнении с группами контроля, получившими ИКЛТ + в/в ХТ и ИКЛТ, где 5-летняя выживаемость составила 64,6 ± 5,8 % и 64,4 ± 6,8 % соответственно (р < 0,05).
Частота местного рецидивирования и отдаленного метастазирования в исследуемой и контрольных группах представлена на рис. 3.
Частота местного рецидивирования в исследуемой группе составила 6,20 %, а частота отдаленного метастазирования — до 15,60 %. В группах сравнения, получивших ИКЛТ и ИКЛТ + в/в ХТ, местный рецидив возник в 9 (9,89 %) и 7 (11,11 %) случаях соответственно, а отдаленные метастазы образовались у 14 (22,22 %) и 20 (21,98 %) пациентов соответственно. При изучении показателя 5-летней выживаемости в зависимости от стадии опухолевого процесса либо в зависимости от локализации опухоли в прямой кишке достоверных отличий между контрольными и исследуемой группами не обнаружено.
К 12 месяцам от момента операции нормализация функции толстой кишки и удерживающего аппарата прямой кишки отмечена практически в равной степени у большинства больных во всех трех подгруппах с общим результатом 74,6 %. При оценке функции удерживающего аппарата аноректума с использованием Wexner score показатели анальной континенции не отличались в исследуемой и контрольных группах, а в целом по трем группам данный показатель составил 10,6 ± 2,2 балла. Субъективно все больные были удовлетворены функциональными результатами операции.
Выводы
Применяемый метод предоперационного лечения с использованием эндолимфатической химиотерапии и крупнофракционного интенсивного облучения при комбинированном лечении резектабельного рака прямой кишки не влияет на частоту интра- и послеоперационных осложнений и увеличивает показатели 5-летней выживаемости в сравнении с традиционными способами неоадъювантной терапии резектабельного рака прямой кишки.
Neoadjuvant Chemoradiotherapy for Resectable Rectal Cancer of Distal Locations
Analysis of publications in recent years shows worldwide morbidity growth of colorectal cancer. Rectal cancer makes 2–10 % among all malignant tumors, 25–30 % among tumors of the gastrointestinal tract and 40–45 % of colorectal cancer and takes the first place in the most developed countries in temp of growth. The incidence of rectal cancer patients in Ukraine in 2010 was 20.4 per 100 000 population, which is significantly higher compared to 2000, when the incidence of malignant tumors was 16.6 [1, 2]
For today standard the only method that can give a hope for a radical cure, regardless of flowing and dissemination of the tumor process remains surgical. According to majority of researchers, despite the improvement of surgical technique, long-term results after surgical treatment remains purely on the same level for many years, the 5-year survival rate is 60 % on the average [3–5]. In this connection, one of the development priorities of onсoproctology at the present stage is the development and introduction into clinical practice new protocols of combined treatment of rectal cancer, aimed to supplement the surgical method by chemoradio-therapy.
Available in the literature statistical data shows insuffiсient effectiveness of modern methods of combined treatment of resectable rectal cancer that cannot significantly improve long-term results. For today the main efforts are directed on improving the methods of preoperative neoadjuvant effect on the tumor process in order to improve the ablastic of radical surgery. At the same time, published by far results of studies in efficiency of preoperative radiotherapy in the treatment of rectal cancer did not show significant progress in improving of long-term results, including a combination of radiation therapy with traditional methods of chemotherapy. Preoperative radiotherapy significantly reduce the incidence of local recurrence rate, however, has no effect on frequency of distant metastasis and consequently the length of patients life. Only in some publications are given the evidence of increasing 5-year survival rate on a few percent, or only increasing of disease-free survival [2, 6, 7]. A huge variety of methods of preoperative radiotherapy, differences in doses and schemes of their conduction, volumes of radiation fields and also the intervals between the end of radiotherapy and surgical treatment lead to significant differences in the results and make difficulties in its interpretation [8, 9].
Purpose of the work. Іmproving long-term results of treatment of resectable rectal cancer distal locations due to optimization scheme of preoperative chemoradiotherapy.
Materials and Methods of the Study
Studies of pharmacokinetics and pharmacodynamics during the endolymphatic administration of 5-fluorouracil were the theoretical substantiation of the suggested in Donetsk regional antitumor center new neoadjuvant therapy of resectable rectal cancer that assume to supplement the preoperative short course radiotherapy with endolymphatic chemotherapy. Results of these studies revealed more prolonged and higher therapeutic concentrations of the drug substance in blood that explain the high efficiency in the treatment of malignant tumors [8, 10, 11] (see Fig. 1). The essence of the method is following («Patent of Ukraine № 63036 dated 26.02.2011»). 24 hours before the beginning of radiotherapy the lymphatic vessel catheterization is performed on the thigh. 5-FU infusion begins 24 hours before radiotherapy and subsequently performed daily for 5 days, a single daily dose is 425 mg/m2. In order to modulate the effect of 5-FU administration it was supplemented with leucovorin intravenous in dose of 60 mg per day. In our study radiotherapy was performed by the mobile intensive daily radiation in dose of 5 Gy to achieve the total dose of 25 Gy. The surgery performed within 48 hours after the end of preoperative chemoradiotherapy.
64 patients with primary resectable rectal cancer were included in the study to assess the effectiveness of developed neoadjuvant method, which included treating rectal cancer with short course radiation therapy and supplemented with endolymphatic chemotherapy (group SCRT + ELCT). Inclusion criteria were following. Localization of the tumor 3–9 cm from the perianal skin (below the pelvic peritoneum and without the involvement of the pelvic structures and muscles, without transition on anal canal). Age category up to 70 years without severe comorbidity and complicated clinical course, which allows eliminating the influence of the lasts on the choice of tactics of special treatment. All patients received combined treatment on the basis of department colorectal surgery Donetsk regional antitumor center from 2004 to 2009 years. Considering that widespreaded and recommended methods of neoadjuvant treatment of rectal cancer are radiotherapy alone and the combination of radiotherapy and chemotherapy, the control group divided in two comparison subgroups. The first subgroup included 63 patients with resectable rectal cancer, who received standard neoadjuvant short course of radiotherapy on the background of intravenous chemotherapy (group SCRT+ + IVCT). The second control subgroup included 91 patients who received only preoperative short course radiation therapy (group SCRT). After performed neoadjuvant treatment, patients of control and study groups underwent radical surgical treatment within 48 hours. Surgical operations that performed to the patients were intersphincter and low anterior resections.
Results and Their Discussion
Evaluation of the study and control groups of the patients showed their complete identity in the main prognostic features.
Intraoperative complications, namely, perforation of the tumor or bowel wall during mobilization in the group SCRT + ELCT appeared in 1 (1.6 %) cases. In the SCRT + IVCT group this complication occurred in 4 (6.3 %) cases. In the group SCRT this complication occurred in 2 (2.2 %) cases. In 1 (0.5 %) case in the group that received SCRT during mobilization of the rectum there was a bleeding from presacral vein plexus, which was not of a heavy nature and was stopped with electric welding complex and tamponing the pelvic cavity with a gauze pad. Postoperative complications in total 3 groups noted in 31 (14.2 %) patient. In the study group, where patients received SCRT + ELCT postoperative complications were noted in 8 (12.5 %) cases, in the comparison groups where patients received SCRT + IVCT and SCRT postoperative complications were noted in 10 (15.9 %) and 13 (14.3 %) cases, respectively. The main share in the study and control groups in general fell on purulent inflammatory processes was in 14 (6.4 %) cases. The most common complication after total mesorectumectomy was a development of an abscess in the pelvis. This complication occurred in 3 (4.7 %) patients in the group received SCRT + ELCT. In the groups that received SCRT + IVCT and SCRT abscess in the pelvis was noted in 3 (4.8 %) and 4 (4.4 %) cases, respectively in the total structure of all complications. Necrosis of bring down bowel developed in the whole 3 groups in 10 (4.6 %) patients. Necrosis of the bowel in the group that received SCRT + ELCT developed in 3 (4.7 %) cases. Bowel necrosis in the comparison groups SCRT + IVCT and SCRT occurred in 3 and 4 cases — 4.9 % and 4.1 % respectively. In all cases, necrosis of bowel were underwent reoperation. In our study noted 1 (1.1 %) case of death in the group that received SCRT. Cause of death was pulmonary thromboembolism. In general, in three groups postoperative mortality was 0.5 %.
Thus, the frequency and character of postoperative complications were not significantly different not only between groups, but also in comparison to the literature which allowed us to characterize the developed method of neoadjuvant chemoradiotherapy as not worsening intraoperative and postoperative complications [3, 5, 11].
5-year overall survival in the study and control groups presented in Figure 2.
Studying 5-year survival demonstrated benefit of developed method neoadjuvant treatment with using short course radiotherapy supplied with endolymphatic chemotherapy compared to neoadjuvant short course of radiotherapy on the background of intravenous chemotherapy and short course of radiotherapy alone. The use of preoperative short course radiotherapy supplied with endolymphatic chemotherapy allowed increasing 5-year overall survival rate up to 73.5 ± 6.3 % in comparison with control groups that received neoadjuvant short course of radiotherapy on the background of intravenous chemotherapy and short course of radiotherapy alone, where 5–year overall survival rate was 64.4 ± 6.8 % and 64.6 ± 5.8 % respectively (p < 0.05).
The frequency of local recurrence rate and distant metastases in the study and control groups presented in figure 3.
The frequency of local recurrence rate in the study group which received SCRT + ELCT occurred in 6.20 % and the frequency of distant metastases was in 15.60 % cases. In the comparison group which received SCRT + IVCT and SCRT local recurrence rate occurred in 9 (9.89 %) and 7 (11.11 %) cases respectively, and the frequency of distant metastases occurred in 14 (22.22 %) and 20 (21.98 %) patients respectively. There is no significant difference in 5-year survival rate according to tumor stage or depending on localization of the tumor in the rectum between the control and study groups were found.
By 12 months from the time of surgery normalization function of the colon and anal continence marked almost equally in the majority of patients in all three subgroups with the overall result of 74.6 %. In assessing the function of the anal continence by using Wexner score scale anal continence did not differ between the study and control groups, and in general in three groups, this sign was 10.6 ± 2.2 points. Subjectively, all patients were satisfied by functional results of the operation.
Conclusions
The applied method of preoperative combined treatment resectable rectal cancer which consists of short course radiation therapy supplied with endolymphatic chemotherapy does not affect the frequency of intra- and postoperative complications and increase 5-year survival rate compared with the traditional methods of neoadjuvant therapy of resectable rectal cancer.
1. Бюллетень канцер-реестра Украины № 13. — К., 2012.
2. Вибрані лекції з клінічної онкології / За заг. ред. Г.В. Бондаря. — Луганськ: ВАТ «Луганська обласна друкарня», 2009. — 559 с.
3. Башеєв В.Х. Оптимізація тактики лікування раку нижньоампулярного відділу прямої кишки: Автореф. дис… д-ра мед. наук: 14.01.07 / Дон. держ. мед. університет. — Донецьк, 2003. — 32 с.
4. Бондарь Г.В., Башеев В.Х. Тенденции развития хирургии рака прямой кишки // Материалы II съезда онкологов стран СНГ. — К., 2000. — № 711.
5. Кикоть В.А. Пути повышения эффективности лечения рака прямой кишки: Автореф. дис… д-ра мед. наук. — К.,1989. — 29 с
6. An interval > 7 weeks between neoadjuvant theapy and surgery improves pathologic complete response and disease-free survival in patients with locally advanced rectal cancer / H. Tulchinsky, E. Shmuell, A. Giger et al. // Ann. Surg. Oncol. — 2008. — Vol. 15. — P. 2661-2667.
7. Neoadjuvant vs adjuvant pelvic radiotherapy for locally advanced rectal cancer: Which is superior? / S. Popek, V. Tsikitis // World J. Gastroenterology. — 2011. — Vol. 17 (7). — P. 848-854.
8. Забудкин А.Ф., Попович Ю.А. Оценка эффективности и токсичности 5-фторурацила при различных способах введения больным с распространенным раком желудка // Архив клинич. и эксперим. медицины. — 2000. — Т. 9, № 4. — С. 483-486.
9. Ceelen W.P. Preoperative chemoradiation versus radiation alone for stage II and III resectable rectal cancer (Review) / W.P. Ceelen, van Nieuwenhov, K. Fierens // Cochrane Database Syst. Rev. — 2009. — Vol. 1. — CD006041.
10. Применение эндолимфатической терапии путем катетеризации лимфатических сосудов бедра в комплексе лечения онкологических заболеваний / Ю.И. Яковец, А.Г. Гончар, А.В. Борота и др. // Клiнічна хiрургiя. — 2001. — № 2. — С. 30-32.
11. Борота О.В. Ендолімфатична антибактеріальна терапія у одноетапному хірургічному лікуванні хворих з загальними ускладненнями раку ободової кишки: Автореф. дис... канд. мед. наук: 14.00.14 / Дон. держ. мед. університет. — Донецьк, 1994. — 22 с.

/15/15.jpg)
/17/17.jpg)
/18/18.jpg)