Журнал «Медицина неотложных состояний» 3 (58) 2014
Вернуться к номеру
Гемодинамические эффекты акупана и нефопама в свете профилактики и коррекции артериальной гипотензии и брадикардии, обусловленных симпатическим блоком при спинномозговой анестезии
Авторы: Малеев С.Б. - Анестезиологическое отделение городской больницы им. Ленина, г. Славянск; Малеева Е.С. - Харьковский национальный медицинский университет
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
В вводной части статьи обращено внимание на возрастающую популярность и актуальность спинномозговой анестезии в различных областях хирургии, травматологии, ортопедии, урологии благодаря высокой эффективности, надежной антиноцицептивной защите, простоте выполнения, низким материальным затратам, возможности проведения анестезии или с использованием поверхностной седации, или без нее. Это свойство нейроаксиальных методов анестезии особенно важно в ургентной анестезиологии, так как позволяет сохранять естественную протекцию верхних дыхательных путей, делая анестезиологическое пособие более безопасным. Несмотря на перечисленные достоинства спинномозговой анестезии, указано на негативные моменты, обусловленные симпатическим блоком при нейроаксиальных методах обезболивания. Такими нежелательными, а порой и потенциально опасными факторами являются избыточная артериальная гипотензия и брадикардия, что требует коррекции в периоперационном периоде. Высказано предположение о возможности использовать холинолитические и симпатомиметические свойства акупана (нефопама) для профилактики и нивелирования вышеуказанных последствий симпатического блока.
Материалы и методы. Проведено исследование на основе личного опыта автора этой статьи, для чего взяты идентичные группы взрослых пациентов, подвергшихся оперативному вмешательству по поводу острого аппендицита, паховой и пупочной грыж как в плановом, так и в ургентном порядке в условиях спинномозговой анестезии в 2010–2012 годах. Пациентам исследуемой группы (n = 27) за 15–20 минут до выполнения спинномозговой анестезии внутримышечно вводился нефопам или акупан 20 мг. Больным контрольной группы (n = 28) препарат не вводился. Исследовались систолическое артериальное давление, пульс, начало и скорость введения альфа-адреномиметика мезатона, потребность в коррекции брадикардии атропином.
Результаты исследования. В исследуемой группе у троих пациентов мужского пола (11,1 %) и одной женщины (3,7 %) введение вазопрессора не потребовалось. В контрольной группе без фармакологической коррекции симпатического блока не обошелся ни один пациент. В первой группе введение мезатона было начато с 8–20-й минуты после индукции спинномозговой анестезии. Во второй группе потребовалось гораздо более раннее введение вазопрессора (2–8-я минуты). Скорость введения мезатона была значительно ниже у пациентов исследуемой группы (3,9 ± 1,7 мкг/мин), чем у больных контрольной группы (16,1 ± 4,0 мкг/мин). Частота сердечных сокращений была более стабильной у больных первой группы (62–94 в 1 минуту). Во второй группе брадикардия (ЧСС менее 60 в минуту), обусловленная симпатическим блоком и потенцированная рефлекторным отрицательным хронотропным воздействием мезатона, потребовала повторных введений атропина у 19 (67,9 %) оперируемых.
Выводы. Таким образом, предшествующее спинальной анестезии введение акупана (нефопама) оказывает явный и клинически значимый антигипотензивный и положительный хронотропный эффекты при симпатическом блоке, индуцированном спинальной анестезией. Это позволяет рекомендовать его не только для профилактики периоперационной дрожи, но и для снижения гипотензивного и брадиаритмического эффектов нейроаксиальной анестезии.
У вступній частині статті звернуто увагу на зростаючу популярність і актуальність спинномозкової анестезії в різних галузях хірургії, травматології, ортопедії, урології завдяки високій ефективності, надійному антиноцицептивному захисту, простоті виконання, низьким матеріальним витратам, можливості проведення анестезії або з використанням поверхневої седації, або без неї. Ця властивість нейроаксіальних методів анестезії особливо важлива в ургентній анестезіології, оскільки дозволяє зберігати природну протекцію верхніх дихальних шляхів, роблячи анестезіологічний засіб більш безпечним. Незважаючи на перераховані достоїнства спинномозкової анестезії, вказано на негативні моменти, обумовлені симпатичним блоком при нейроаксіальних методах знеболювання. Такими небажаними, а часом і потенційно небезпечними факторами є надлишкова артеріальна гіпотензія та брадикардія, що вимагає корекції в періопераційному періоді. Висловлено припущення про можливість використовувати холінолітичні та симпатоміметичні властивості акупану (нефопаму) для профілактики та нівелювання вищевказаних наслідків симпатичного блоку.
Матеріали та методи. Проведено дослідження на основі особистого досвіду автора цієї статті, для чого були взяті ідентичні групи дорослих пацієнтів, які зазнали оперативні втручання з приводу гострого апендициту, пахової та пупкової кил як в плановому, так і в ургентному порядку в умовах спинномозкової анестезії в 2010–2012 роках. Пацієнтам досліджуваної групи (n = 27) за 15–20 хвилин до виконання спинномозкової анестезії внутрішньом’язово вводився нефопам або акупан 20 мг. Хворим контрольної групи (n = 28) препарат не вводився. Досліджувалися систолічний артеріальний тиск, пульс, початок і швидкість введення альфа-адреноміметика мезатону, потреба в корекції брадикардії атропіном.
Результати дослідження. У досліджуваній групі у трьох пацієнтів чоловічої статі (11,1 %) і однієї жінки (3,7 %) у введенні вазопресорів не було потреби. У контрольній групі без фармакологічної корекції симпатичного блоку не обійшовся жоден пацієнт. У першій групі введення мезатону було розпочато з 8–20-ї хвилини після індукції спинномозкової анестезії. У другій групі знадобилося значно більш раннє введення вазопресорів (2-га — 8-ма хвилини). Швидкість введення мезатону була значно нижчою в пацієнтів досліджуваної групи (3,9 ± 1,7 мкг/хв), ніж у хворих контрольної групи (16,1 ± 4,0 мкг/хв). Частота серцевих скорочень була більш стабільною у хворих першої групи (62–94 за 1 хвилину). У другій групі брадикардія (ЧСС менше від 60 за 1 хвилину), що обумовлена симпатичним блоком і потенційована рефлекторним негативним хронотропним впливом мезатону, потребувала повторні введення атропіну в 19 (67,9 %) оперованих.
Висновки. Таким чином, попереднє спінальній анестезії введення акупану (нефопаму) надає явний і клінічно вагомий антигіпотензивний і позитивний хронотропний ефекти при симпатичному блоці, індукованому спінальною анестезією. Це дозволяє рекомендувати його не тільки для профілактики періопераційного тремтіння, але й для зниження гіпотензивного та брадіаритмічного ефектів нейроаксіальної анестезії.
The introduction of the article drew attention to the increasing popularity and relevance of spinal anesthesia in the various fields of surgery, traumatology, orthopedics, urology due to high efficiency, reliable antinociceptive protection, ease of implementation, low material costs, the possibility of using anesthesia with anxiolysis, or without it. This property of neuraxial anesthesia techniques is especially important in emergency anesthesiology, as it allows preserve the natural protection of the upper respiratory tract, making anaesthetic support more safe. Despite these advantages of spinal anesthesia, there is indicated on the negative aspects arising from sympathetic block for neuraxial techniques of anesthesia. Such undesirable, and sometimes potentially dangerous factors are excessive hypotension and bradycardia, which requires correction in the perioperative period. Suggested the possibility of using cholinolytic and sympathomimetic properties of acupan (nefopam) for the prevention and leveling the above effects of sympathetic block.
Materials and Methods. A study based on personal experience of the author of this article, for what there are taken identical groups of adult patients underwent surgery for acute appendicitis, inguinal and umbilical hernias, both planned and in urgent procedure under spinal anesthesia, in 2010–2012. Patients of the study group (n = 27) 15–20 minutes before performing spinal anesthesia we administered intramuscularly nefopam or acupan 20 mg. Patients from control group (n = 28) didn’t receive the drug. We investigated systolic blood pressure, pulse, initiation and the rate of infusion of alpha-adrenergic agonist mezaton, need for correction of bradycardia with atropine.
Results of the Study. In the study group three male patients (11.1 %) and one woman (3.7 %) did not require vasopressor infusion. In the control group pharmacological correction of sympathetic block was necessary to all patients. In the first group mezaton infusion began from 8–20th minute after induction of spinal anesthesia. The second group needed much more early infusion of vasopressor (2nd — 8th minute). Rate of mezaton administration was significantly lower in patients of the study group (3.9 ± 1.7 mcg/min)
than in control patients (16.1 ± 4.0 mcg/min). Heart rate was more stable in patients of the first group (62–94 per 1 minute). In the second group bradycardia (heart rate less than 60 per 1 minute) caused by sympathetic block and potentiated by reflex negative chronotropic influence of mezaton, required repeated injections of atropine in 19 (67.9 %) patients.
Conclusions. Thus, the administration of acupan (nefopam) before spinal anesthesia provides a clear and clinically significant antihypotensive and positive chronotropic effects in the sympathetic block induced by spinal anesthesia. It enables to recommend it not only for the prevention of perioperative shivering, but also to reduce the hypotensive and bradiaritmic effects of neuraxial anesthesia.
акупан, нефопам, спинномозговая анестезия, артериальная гипотензия, брадикардия, симпатический блок.
акупан, нефопам, спинномозкова анестезія, артеріальна гіпотензія, брадикардія, симпатичний блок.
acupan, nefopam, spinal anesthesia, arterial hypotension, bradycardia, sympathetic block.
Статья опубликована на с. 65-68
Цель исследования: снижение гипотензивного и брадиаритмического эффектов нейроаксиальной анестезии путем предоперационного введения нефопама (акупана).
Популярность спинномозговой анестезии в различных областях травматологии, ортопедии, урологии и хирургии как в моноварианте, так и в сочетании с компонентами общей анестезии обусловлена высокой эффективностью, надежной антиноцицептивной защитой, простотой выполнения и низкими материальными затратами. В большинстве случаев возможно проведение анестезии или с использованием поверхностной седации, или без нее. Это свойство нейроаксиальных методов анестезии особенно важно в ургентной анестезиологии, так как позволяет сохранять естественную протекцию верхних дыхательных путей.
Обладая значительным количеством полезных свойств, спинномозговой анестезии присущи некоторые негативные моменты, которые приходится предупреждать и корригировать в периоперационном периоде. Одним из них является вызванная симпатическим блоком артериальная гипотензия, степень выраженности которой зависит от волемической компенсации больного, уровня распространения симпатического блока в ростральном направлении, возраста, компенсаторных возможностей конкретного пациента. Брадикардия различной степени выраженности является следующим нежелательным, а зачастую и потенциально опасным феноменом, обусловленным обратимой симпатической денервацией при спинномозговой анестезии. Клиническим парадоксом в данной ситуации является потенцирование отрицательного хронотропного эффекта мезатоном, традиционно применяемым в Украине для профилактики и коррекции артериальной гипотензии при нейроаксиальной анестезии.
Относительно недавно на фармацевтическом рынке Украины появился нефопам (3,4,5,6-тетрагидро-5-метил-1-фенил-1Н-2,5-бензоксазоцина гидрохлорид) производства Eipico (Египет) и немного позже — акупан производства Biocodex (Франция). При ознакомлении с инструкцией к нефопаму привлекли внимание такие свойства препарата, как профилактировать и купировать озноб. Сталкиваясь в повседневной практике с развитием дрожи при проведении спинномозговой анестезии, автор статьи на основе личного опыта провел работу по изучению способности нефопама предупреждать и купировать периоперационную дрожь при спинномозговой анестезии, что нашло последующее отражение на страницах этого уважаемого периодического издания (№ 4(29), 2010).
В ранее напечатанной статье обращается внимание на свойство нефопама влиять на гемодинамику, повышая артериальное давление. Принято решение исследовать и использовать это свойство препарата для профилактики и снижения выраженности артериальной гипотензии и брадикардии, вызванных симпатическим блоком при спинальной анестезии.
Материалы и методы
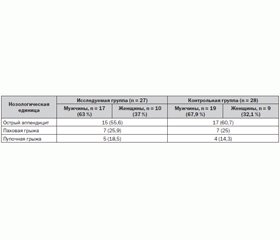
Проведено исследование на основе личного опыта автора этой статьи. Взяты идентичные группы взрослых пациентов, подвергшихся оперативному вмешательству по поводу острого аппендицита, паховой и пупочной грыж как в плановом, так и в ургентном порядке в условиях спинномозговой анестезии. Намеренно отобраны оперативные вмешательства, требующие примерно один уровень нейроаксиального блока и, как правило, не сопровождающиеся клинически значимой кровопотерей. В исследуемую группу вошли 27 пациентов (17 мужчин (63 %), 10 женщин (37 %)), подвергшихся плановому или ургентному оперативному вмешательству в 2010–2012 годах по поводу острого аппендицита — 15 (55,6 %), паховой грыжи — 7 (25,9 %), пупочной грыжи — 5 (18,5 %) чел. Контрольная группа состояла из 28 больных (19 мужчин (67,9 %), 9 женщин (32,1 %)), прооперированных в 2010–2012 годах по поводу острого аппендицита — 17 (60,7 %), паховой грыжи — 7 (25 %), пупочной грыжи — 4 (14,3 %) (табл. 1).
Все больные обеих групп были без клинических и анамнестических проявлений гиповолемии и водно-электролитных нарушений. Возраст пациентов: 19–45 лет в основной группе и 21–43 года — в контрольной. В обеих группах оперируемые были без сопутствующей соматической патологии, что соответствовало ASA-I и ASA-IE. Исходное систолическое АД при поступлении в операционную: 124–141 мм рт.ст. в исследуемой и 121–145 мм рт.ст. в контрольной группе, пульс — соответственно 92–104 и 92–108 ударов в 1 минуту. Следовательно, пациенты из обеих групп достоверно не различались по полу, возрасту, характеру и степени тяжести заболеваний, показателям гемодинамики, что свидетельствует о репрезентативности выборки.
Перед спинномозговой анестезией осуществлялась преинфузия раствором NaCl 0,9% в объеме 400,0 мл. В положении больного на ипсилатеральном зоне оперативного вмешательства боку с опущенным головным концом после пункции субарахноидального пространства иглой с острием типа Quincke 26G в промежутках L3-L4-L5 интратекально вводился заблаговременно подогретый маркаин спинал хэви 0,5% (AstraZeneca) в количестве 15–20 мг. Пункция субарахноидального пространства у всех больных была выполнена без технических сложностей. Верхний уровень сенсорного блока, учитывая возможные пределы хирургического вмешательства, устанавливали на уровне пятого-седьмого торакальных сегментов и корригировали временем и степенью наклона операционного стола. Всем больным инфузия проводилась подогретыми кристаллоидами. Характер и объем инфузионной терапии — без существенных различий в обеих группах (10–15 мл/кг/ч). При поступлении в операционную за 15–20 мин до выполнения спинномозговой анестезии больным основной группы однократно внутримышечно вводился нефопам или акупан 20 мг, без какого–либо предпочтения конкретному препарату. Пациентам контрольной группы акупан (нефопам) не вводился. Девиации гемодинамики вследствие развития симпатического блока корригировались внутривенной инфузией мезатона. Брадикардия с ЧСС менее 60 ударов в минуту купировалась болюсными введениями атропина в дозе 0,5 мг. Длительность оперативного вмешательства: от 30 до 105 минут в основной группе и от 25 до 95 минут — в контрольной. Проводился контроль пульса и артериального давления, измеряемых неинвазивно мониторами Utas UM-300 и Mediana YM-6000 до анестезии и каждые 2 минуты после интратекального введения местного анестетика. Артериальное давление удерживалось в пределах ± 20 % от исходного. Практически введение мезатона начиналось при снижении систолического артериального давления ниже 100–105 мм рт.ст. Оценивалась стабилизация гемодинамики при симпатическом блоке, вызванном спинномозговой анестезией. Регистрировались начало и скорость инфузии мезатона, необходимые для стабилизации гемодинамики, депрессированной симпатическим блоком.
Результаты исследования
В исследуемой группе у троих пациентов мужского пола (11,1 %) и одной женщины (3,7 %) введение вазопрессора не потребовалось. В контрольной группе без фармакологической коррекции симпатического блока не обошелся ни один пациент. Развитие гипотензии у больных исследуемой группы было значительно более мягким и не столь стремительным, что вызывало ассоциации с плавным развитием симпатического блока при эпидуральной анестезии. В первой группе введение мезатона было начато с 8–20-й минуты после индукции спинномозговой анестезии. Во второй группе потребовалось гораздо более раннее введение вазопрессора — 2–8-я минута. Скорость введения мезатона была значительно ниже у пациентов исследуемой группы (3,9 ± 1,7 мкг/мин), чем у больных контрольной группы (16,1 ± 4,0 мкг/мин). Частота сердечных сокращений была более стабильной у больных первой группы (62–94 в 1 минуту), что обусловлено холинолитическими и симпатомиметическими свойствами акупана. Во второй группе брадикардия (ЧСС менее 60 в 1 минуту), обусловленная симпатическим блоком и потенцированная рефлекторным отрицательным хронотропным воздействием мезатона, потребовала повторных введений атропина у 19 (67,9 %) оперируемых. Дрожь в периоперационном периоде в исследуемой группе не зарегистрирована ни у одного пациента. В контрольной группе отмечена констатация этого клинического феномена у 17 (60,7 %) чел.
Выводы
Таким образом, предшествующее спинальной анестезии введение акупана (нефопама) оказывает явный и клинически значимый антигипотензивный и положительный хронотропный эффекты при симпатическом блоке, индуцированном спинальной анестезией. Это позволяет рекомендовать его не только для профилактики периоперационной дрожи, но и для снижения гипотензивного и брадиаритмического эффектов нейроаксиальной анестезии. Считаем своим долгом предостеречь от неосторожного введения нефопама на фоне начатой инфузии мезатона. У двоих больных, не вошедших в данное исследование, введение препарата на фоне введения вазопрессора привело к значительной и стойкой артериальной гипертензии, которая сохранялась после прекращения инфузии мезатона.
1. Агаджанян А.Н., Тель Л.З., Циркин В.И., Чеснокова С.А. Физиология человека // Медицинская книга. — Н. Новгород: НГМА, 2001. — 526 с.
2. Андрющенко В.П., Маглеваный В.А., КуновскийВ.В. Акупан®: принципиально новый подход к купированию острого болевого синдрома // Медицина неотложных состояний. — 2013. — 2(49).
3. Климчук Л.В. Опыт применения Акупана для профилактики послеоперационной дрожи после хирургических вмешательств в онкологии // Медицина неотложных состояний. — 2013. — № 2(49).
4. Компендиум 2006 г. Лекарственные препараты / Под ред. В.Н. Коваленко, А.П. Викторова. — К.: Морион, 2006. — 2270 с.
5. Малеев С.Б. Решение проблемы периоперационной дрожи, индуцированной спинномозговой анестезией // Медицина неотложных состояний. — 2010. — № 4(29).
6. Малрой М. Местная анестезия. — М.: Бином. Лаборатория знаний, 2003.
7. Мельник В.М., Ложкин В.В. Многолетний опыт применения нефопама в анестезиологической практике ГВМКЦ «Главный военный клинический госпиталь» МО Украины // Медицина неотложных состояний. — 2013. — № 5(52).
8. Пасечников С.П., Никитин О.Д., Малолетний Л.Н. Сравнительная оценка эффективности послеоперационного обезболивания морфином и Акупаном в урологической практике // Медицина неотложных состояний. — 2013. — № 1(48).
9. Шраменко Е.К., Ермилов Г.И., Смирнова Н.Н., Кононов А.В., Базун М.И. Применение уникального аналгетика нефопам в анестезиологии, интенсивной терапии и на догоспитальном этапе // Украинский журнал экстремальной медицины им. Г.О. Можаева. — 2008. — № 1.
10. Черний В.И., Коваленко В.Л. Акупан и спинальные анестезии // Медицина неотложных состояний. — 2011. — № 3–8(38–39).
11. Черний В.И., Ермилов Г.И., Колганова Е.А., Егоров А.А. Применение мультимодальной аналгезии с использованием Акупана, дексалгина и налбуфина в периоперационном периоде // Медицина неотложных состояний. — 2011. — № 6(37).
12. De Witte J., Sessler D.I. Perioperative Shivering: Physiology and Pharmacology // Anesthesiology. — Feb. 2002. — Vol. 96, Issue 2. — Р. 467–484.

/66/66.jpg)