Журнал «Медицина неотложных состояний» 3 (58) 2014
Вернуться к номеру
Профилактика и лечение острого повреждения почек, вызванного рабдомиолизом различного генеза
Авторы: Шраменко Е.К., Черний В.И., Прокопенко Б.Б. - Донецкий национальный медицинский университет им. М. Горького; Донецкое областное клиническое территориальное медицинское объединение
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Проанализированы результаты лечения 47 больных с травматическим и нетравматическим рабдомиолизом. Все пациенты были разделены на 2 группы: в 1-й осуществляли гемодилюцию и раннее ощелачивание плазмы, во 2-й группе такую терапию не проводили. В 1-й группе результаты лечения оказались лучше, летальность — ниже.
Проаналізовано результати лікування 47 хворих із травматичним і нетравматичним рабдоміолізом. Усі пацієнти були розподілені на 2 групи: у 1-й виконували гемодилюцію й раннє облуговування плазми, у 2-й групi таку терапiю не проводили. У 1-й групі результати лікування виявилися кращими, летальність — нижчою.
The treatment outcomes of 47 patients with traumatic and non-traumatic rhabdomyolysis were analyzed. All patients were divided into group: in the 1st one there were carried out hemodilution and early plasma alkalinization, in the 2nd one such therapy wasn’t done. In 1st group the treatment outcomes were better, mortality — lower.
рабдомиолиз, острое повреждение почек, нефропротекция, интенсивная терапия.
рабдоміоліз, гостре пошкодження нирок, нефропротекцiя, інтенсивна терапія.
rhabdomyolysis, acute kidney injury, nephroprotection, intensive therapy.
Статья опубликована на с. 76-79
Актуальность
Рабдомиолиз (РМ) — разрушение поперечнополосатой мускулатуры различного происхождения, все чаще выявляется в отделениях интенсивной терапии. Летальность остается высокой, до 40 %, особенно при присоединении острого повреждения почек (ОПП), требующего диализного лечения. Наиболее частыми причинами разрушения миоцитов, приводящими к развитию миоренального синдрома, являются травматические и токсические [1]. К травматическим причинам относятся: синдром длительного сдавления (СДС), который подразделяется на синдром длительного раздавливания (СДР) и синдром позиционного сдавления (СПС); синдром включения (реперфузионное повреждение) после окклюзии или гипоперфузии мышечных сосудов, чрезмерные мышечные нагрузки (тяжелая физическая нагрузка, судорожный синдром и др.). Токсические причины рабдомиолиза: передозировка лекарственных препаратов (статины, анаболические стероиды, амфетамины, корень солодки, фибраты) и некоторые яды змей и насекомых. Нетравматический РМ имеет свои особенности: развивается сравнительно медленно, отмечается боль и выраженная слабость во всех мышцах тела, вплоть до парезов, что иногда расценивается как острая демиелинизирующая полинейропатия, нередко сочетается с печеночной недостаточностью. РМ усугубляется в условиях гипертермии. Часто наблюдается сочетание травматических, токсических причин и гипертермии тела или повышения температуры окружающей среды.
В формировании ОПП при РМ наряду с другими факторами существенное значение имеют такие, как плазмопотеря в поврежденные участки тела, быстрое снижение объема циркулирующей крови и быстрое поступление в кровоток продуктов мышечного распада (миоглобин, креатинкиназа, калий, лизосомальные ферменты) и нарушенного метаболизма клеток (молочная, пировиноградная кислота, полипептиды и др.). Проведение гемодилюции и ощелачивания плазмы и мочи предусматривает устранение ведущих факторов развития ОПП и предотвращение формирования при миоглобинурии в кислой среде мочи нерастворимого осадка, обтурирующего просвет почечных канальцев. Однако исследования, посвященные данному вопросу, носят достаточно противоречивый характер. Авторы высказываются как в пользу [5, 6], так и против ощелачивания плазмы крови [3, 4].
Цель исследования: оценить возможности нефропротекции при остром повреждении почек, вызванном рабдомиолизом различного происхождения.
Материал и методы
За последние 5 лет в реанимационном центре ДОКТМО наблюдали 47 пациентов (все мужчины) в возрасте 36,8 ± 3,1 года с РМ различного происхождения. Из них 5 чел. — с СДР, 33 — с СПС, 2 — с синдромом включения после ранения бедренной артерии и нижней полой вены (табл. 1), 7 пациентов с рабдомиолизом вследствие сочетания приема лекарственных препаратов, тяжелой физический нагрузки и гипертермии. Шесть из них были спортс–менами или шахтерами. Три пациента принимали статины в связи с гиперлипидемией в дозировке, превышающей терапевтическую, 3 — анаболические стероиды, 1 — амфетамины. Таким образом, можно выделить пациентов с травматическим (40) и нетравматическим (7) РМ. Деление условно, так как нередко имело место сочетание факторов.
Всем больным выполнялись общеклинические, биохимические исследования, ЭКГ, УЗИ органов брюшной полости и забрюшинного пространства, части из них — ЭхоКГ и компьютерная томография. Дополнительно всем пациентам было проведено допплеровское сканирование сосудов почек в динамике с целью сравнительной оценки нарушений почечного кровотока. С учетом анамнеза, клинико-лабораторных данных, состояния гемодинамики почек назначали ренопротективную терапию [2]. Гемодиализное лечение проводилось на аппаратах АК-90, АК-200 (Gambro), Tina (Baxter), Innova (Gambro). Диализаторы — Alwal GFE, GFS, Poluflux (Gambro), F-5 (Fresenius). При необходимости гемодиализ сочетали с плазмаферезом, экстракорпоральной антибиотикотерапией, ультрафиолетовым облучением крови. Сосудистый доступ обеспечивали формированием артериовенозного шунта на предплечье или установкой двухходового катетера в центральный сосуд. Антикоагуляцию проводили нефракционированным или низкомолекулярным гепарином.
Все больные, независимо от причины РМ, были разделены на 2 группы. 1-я группа — 20 больных, которым проводилась ранняя гемодилюция, ощелачивание плазмы и стимуляция диуреза (первые часы, сутки от развития РМ); 2-я группа — 27 больных, которым в раннем периоде по разным причинам (позднее поступление, неустановленный диагноз и др.) такая терапия не осуществлялась. В этой группе троим пациентам выполнены лампасные разрезы, двум — фасциотомия. В остальном терапия была идентичной.
Объем гемодилюции зависел от величины зоны повреждения, степени сгущения крови и составлял 35–40 мл/кг массы тела в сутки и более с учетом скорости и объема диуреза. Гемодилюцию выполняли кристаллоидными растворами: внутривенно быстро вводили 0,9% раствор хлорида натрия, раствор Фокса, Рингера. С целью ощелачивания плазмы и мочи применяли: 4,2% раствор соды-буфер 100–200 мл дважды в сутки; 4% раствор натрия гидрокарбоната в объеме 150–400 мл/сут (а не 1,5–2 л, как указывается в ряде источников); а также трисоль 400–600 мл/сут. После проведенной инфузионной терапии внутривенно струйно вводили салуретики (фуросемид, торасемид) — 20–40 мг/сут. В состав инфузионной терапии включали также: 10% раствор глюкозы 200–400 мл/сут; реосорбилакт 200 мл/сут. Каждому больному было выполнено от 2 до 6 инфузий раствора гидрокарбоната натрия на протяжении трех суток. В случае стойкой олигурии (0,3 мл/кг/ч и менее) в течение 24 часов введение прекращали.
Для оценки эффективности проводимой терапии в группах сравнивали: длительность стадии олигоанурии, необходимость проведения заместительной почечной терапии, количество гемодиализов, присоединение полиорганных нарушений, исход.
Результаты и их обсуждение
Все пациенты хорошо переносили инфузии растворов гидрокарбоната натрия, при этом на третьи сутки коррекция дефицита оснований сопровождалась нормализацией рН крови и мочи. Темно-коричневая при поступлении, окраска мочи менялась на светло-соломенный цвет. В то же время инфузия раствора сода-буфер в течение 3 дней не приводила к гипернатриемии и предотвращала прогрессирование гиперкалиемии.
Уровень креатинкиназы на 3-и — 5-е сутки заболевания был высоким и сопоставимым в обеих группах (2907,7 ± 364,9 и 2865,4; р > 0,05). Уровень калия плазмы (5,28 ± 0,15 ммоль/л и 6,07 ± 0,11 ммоль/л), мочевины (22,11 ± 0,97 ммоль/л и 31,22 ± 1,10 ммоль/л) и креатинина (372,94 ± 15,65 мкмоль/л и 730,06 ± 28,54 мкмоль/л) был выше во второй группе (р < 0,05). Функциональное состояние почек оценивалось также по показателям артериального почечного кровотока. На 3-и — 5-е сутки у всех пациентов отмечены гемодинамически значимые нарушения кровотока в почках, которые проявлялись снижением линейных скоростей и повышением индекса резистентности в основном стволе почечных артерий. Максимальная систолическая скорость кровотока (Vps) в 1-й и 2-й группах достоверно не отличалась. Если в контрольной группе этот показатель составил 73,0 ± 4,2 см/с, то в 1-й и 2-й группах — соответственно 49,95 ± 0,67 см/с и 51,33 ± 0,86 см/с (р > 0,05). В то же время индекс резистентности (RI) был выше во второй группе (0,79 ± 0,01 и 0,82 ± 0,01; р < 0,05), что свидетельствовало о более тяжелом течении ОПП. В контрольной группе RI составил 0,62 ± 0,05.
На 5–7-е сутки от начала заболевания 8 пациентам из 1-й группы и 15 — из 2-й группы в связи с олигурией, гиперкалиемией, гиперазотемией, энцефалопатией, гастроэнтеропатией было начато лечение гемодиализом. Количество сеансов гемодиализа на одного больного в 1-й группе составило 3,8 ± 0,3, во второй — 8,8 ± 0,4 (р < 0,05).
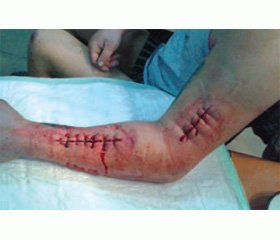
В группе пациентов, в которой проводили раннюю гемодилюцию и ощелачивание плазмы, наблюдали следующие осложнения: дыхательную недостаточность — у 3 чел., желудочно-кишечное кровотечение — у 2, тяжелый гипертензионный синдром — у 2. Во 2-й группе: присоединение гнойно-септических осложнений — у 8 пациентов, дыхательная недостаточность — у 5, кровотечения различной локализации — у 6, в том числе из лампасных разрезов (рис. 1, 2); повторные эпизоды жизнеопасной гиперкалиемии (более 7,5 ммоль/л), требующие проведения ургентного гемодиализа, с соответствующими изменениями на ЭКГ — у двух больных.
Восстановление диуреза в 1-й группе наблюдалось на 7–15-е сутки, во второй — на 15–30-е сутки, в среднем на 9,4 ± 0,7 сут и 21,7 ± 1,2 сут соответственно (р < 0,05). Показатели артериального кровотока быстрее восстановились в 1-й группе. Vps повысилась до 59,6 ± 0,2 см/с и 57,90 ± 0,15 см/с соответственно. RI снизился до 0,65 ± 0,02 в 1-й группе и до 0,69 ± 0,03 — во второй. В 1-й группе умер 1 пациент, во второй — 4 (двум из них выполнены лампасные разрезы).
Вышеизложенное доказывает, что эффективность лечения оказалась выше в 1-й группе, в которой выполнялось раннее ощелачивание плазмы. Таким образом, одним из основных принципов первичной нефропротекции при РМ любого происхождения является как можно более ранняя гемодилюция, ощелачивание плазмы и стимуляция диуреза малыми дозами салуретиков. Однако нефропротективные мероприятия при РМ не ограничиваются только этим. Учитывая патогенез РМ, первичная медикаментозная нефропротекция при травматическом рабдомиолизе предусматривает адекватное обезболивание, улучшение реологических свойств крови, коррекцию гемодинамических нарушений, дыхательных расстройств, стимуляцию деятельности желудочно-кишечного тракта, при нетравматическом РМ — включение в комплекс лечения гепатопротекторов. Немедикаментозная нефропротекция при травматическом РМ заключается в иммобилизации поврежденных участков туловища и в удалении, по возможности, источника интоксикации. Выполнение лампасных разрезов не предупреждает развитие тяжелой формы ОПП, усугубляет плазмопотерю, анемию, боль, способствует присоединению инфекционных –осложнений и, таким образом, не является нефропротективным мероприятием. Немедикаментозная нефропротекция в группе нетравматического рабдомиолиза — ограничение физической нагрузки. Вторичная нефропротекция предусматривает проведение лечебных мероприятий на 3-и — 5-е и более сутки олигоанурии, когда повреждение почечных канальцев уже произошло, и включает в себя коррекцию нарушений, усугубляющих и поддерживающих дистрофию и некроз эпителия проксимального отдела канальцев: лечение инфекционных осложнений (антибиотикотерапия и др.), коррекцию гипертензионного синдрома, анемии и геморрагических осложнений; проведение гемодиализа и ультрафильтрации; при необходимости — выполнение плазмафереза, экстракорпоральной антибиотикотерапии, ультрафиолетового облучения крови.
Выводы
1. Ранняя гемодилюция и ощелачивание плазмы при РМ любого происхождения являются эффективными и безопасными методами нефропротекции, так как способствуют укорочению длительности стадии олигоанурии, снижают потребность в диализном лечении и улучшают исход острого повреждения почек.
2. Нефропротекция при РМ должна включать адекватное обезболивание, улучшение реологических свойств крови, коррекцию гемодинамических нарушений, дыхательных расстройств, стимуляцию деятельности желудочно-кишечного тракта, проведение эфферентных методов.
3. Выполнение лампасных разрезов на поврежденных участках тела не является нефропротективным мероприятием.
1. Миронов Л.Л. Рабдомиолиз // Медицина неотложных состояний. — 2006. — № 6(7). — С. 7-14.
2. Шраменко Е.К., Кузнецова И.В., Шкарбун Л.И., Логвиненко Л.В., Прокопенко Б.Б. Патогенетическое обоснование тактики ренопротекции у больных с острой почечной недостаточностью // Біль, знеболювання і інтенсивна терапія. — 2010. — № 2(д). — С. 287-289.
3. Brown C.V., Rhee P., Chan L., Evans K., Demetriades D., Velmahos G.C. Preventing renal failure in patients with rhabdomyolysis: do bicarbonate and mannitol make a difference? // J. Trauma. — 2004. — 56. — 1191-1196.
4. Powell-Tuck J., Gosling P., Lobo D.N. et al. British Consensus Guidelines on Intravenous Fluid Therapy for Adult Surgical Patients. GIFTASUP. 7 March 2011.
5. Vanholder R., Sever M.S., Erek E., Lameire N. Rhabdomyolysis // J. Am. Soc. Nephrol. — 2000. — 11. — 1553-1561.
6. Bosch X., Poch E., Grau J.M. Rhabdomyolysis and Acute Kidney Injury // New England Journal Med. — 2009. — 13. — 62-67.

/77/77.jpg)
/78/78.jpg)