Журнал «Травма» Том 15, №3, 2014
Вернуться к номеру
Риск развития местного гипертензионного ишемического синдрома при травме
Авторы: Страфун С.С. - ГУ «Институт травматологии и ортопедии НАМН Украины», г. Киев; Ткач А.В. - ГУ «Крымский государственный медицинский университет им. С.И. Георгиевского», г. Симферополь; Страфун А.С. - ГУ «Институт травматологии и ортопедии НАМН Украины», г. Киев; Салий А.П. - ГУ «Крымский государственный медицинский университет им. С.И. Георгиевского», г. Симферополь;
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
По различным данным, при травмах местный гипертензионный ишемический синдром (МГИС) развивается в 20 % случаев. Однако переход МГИС в ишемическую контрактуру Фолькмана минимален. Наиболее часто исходом данного синдрома становится нарушение функции и снижение силы конечности, замедленное сращение переломов. Эти проявления обусловлены выраженным рубцово-фиброзным перерождением, а при более выраженном процессе отмечается несращение переломов.
На основании анализа верифицированного МГИС у 230 пациентов мы создали балльную систему оценки прогноза развития и течения данного состояния.
На основании ранжирования прогностических факторов разработаны алгоритмы диагностики компартмент-синдрома для травматически поврежденного и удлиняемого сегмента конечности, которые позволяют разработать дифференцированную тактику лечения и избежать развития тяжелых ишемических изменений тканей у 89 % таких пациентов.
За різними даними, при травмах місцевий гіпертензійний ішемічний синдром (МГІС) розвивається в 20 % випадків. Однак перехід МГІС в ішемічну контрактуру Фолькмана мінімальний. Найчастіше результатом даного синдрому стає порушення функції і зниження сили кінцівки, уповільнене зрощення переломів. Ці прояви зумовлені вираженим рубцево-фіброзним переродженням, а при більш вираженому процесі відмічається незрощення переломів.
На підставі аналізу верифікованого МГІС у 230 пацієнтів ми створили бальну систему оцінки прогнозу розвитку і перебігу даного стану.
На підставі ранжування прогностичних чинників розроблені алгоритми діагностики компартмент-синдрому для травматично ушкодженого і подовжуваного сегмента кінцівки, що дозволяють розробити диференційовану тактику лікування та уникнути розвитку тяжких ішемічних змін тканин у 89 % таких пацієнтів.
According to various reports, in traumas local hypertensive ischemic syndrome (LHIS) develops in 20 % of cases. However, LHIS transformation into ischemic Volkmann’s contracture is minimal. Most often the outcome of this syndrome is impaired function and reduced limb strength, delayed fracture healing. These manifestations are due to severe scar-fibrous degeneration, and nonunions are being detected in more severe process.
Based on the analysis of the verified LHIS in 230 patients, we have created a scoring system tp evaluate the prognosis for development and course of this condition.
On the basis of prognostic factors ranking we developed algorithms to diagnose compartment syndrome for traumatically injured and lengthen limb segment, which allow to develop a differentiated treatment strategy and to avoid the development of severe ischemic tissue changes in 89 % of these patients.
диагностика, отек, ишемия.
діагностика, набряк, ішемія.
diagnosis, edema, ischemia.
Статья опубликована на с. 5-10
Введение
По различным данным, при травмах местный гипертензионный ишемический синдром (МГИС) развивается в 20 % случаев. Однако переход МГИС в ишемическую контрактуру Фолькмана минимален. Наиболее часто исходом данного синдрома становится нарушение функции и снижение силы конечности, замедленное сращение переломов. Эти проявления обусловлены выраженным рубцово-фиброзным перерождением, а при более выраженном процессе отмечается несращение переломов [2].
Материалы и методы
На основании анализа верифицированного МГИС у 230 пациентов мы создали балльную систему оценки прогноза развития и течения данного состояния.
Оценка сроков развития МГИС по этиологическому фактору позволяет сделать вывод о прогностической значимости параметра «этиология травмы» для прогнозирования компартмент-синдрома. Проведенный сравнительный анализ травм ожоговой этиологии (83 пациента) и прочих травм показал наличие статистически значимых различий в сроках развития МГИС (p < 0,001). При ожоговых поражениях и электротравме средние сроки развития МГИС составляют 1,3 ± 1,0 дня. При травмах другой этиологии сроки увеличиваются до 4,03 ± 3,20 дня (F = 49,9; p = 0,0001), что свидетельствует о статистически значимой зависимости сроков развития МГИС от этиологии травмы.
В настоящее время существует три активно используемые, разработанные по определенным клиническим аспектам формализованные системы диагностики и принятия решений в различных областях медицины.
Наличие в практическом арсенале врачей-травматологов системы мониторинга (аэроионный компьютерный комплекс) и прогнозирования тяжести патологии и вероятного характера ее течения может существенно улучшить качество медицинской помощи, диагностики, повысить ее медицинскую и экономическую эффективность.
В научной практике существуют различные подходы к прогнозированию и диагностике патологических процессов. По нашему мнению, методология вероятностного анализа, представленная в монографии Е.В. Гублера «Вычислительные методы анализа и распознавания патологических процессов», является наиболее оптимальной для использования и заключается в определении вероятности возможных диагнозов или развития определенных патологических процессов. Решение данной задачи базируется на использовании байесовских алгоритмов. Используя данный методический подход, мы можем оценить вероятность развития МГИС по комплексу клинических характеристик пациента.
Реализация настоящей модели требует использования информативных критериев. Для построения прогностической модели нами не использовались параметры с низким уровнем информативности (информационной меры Кульбака).
Оценка информативности признаков проводилась по формуле:
P(xj /A1) P(xj /A1) – P(xj /A2)
J(x) = 100 lg _________ • ________________,
P(xj /A2) 2
где J(x) — информационная ценность признака;
P(xj /A1) — условная вероятность информационной группы j признака х в группе больных с наличием МГИС (А1);
P(xj /A2) — условная вероятность информационной группы j признака х в контрольной группе А2.
Группы высокой вероятности прогноза тяжелых форм МГИС формировались на основе расчета прогностических коэффициентов (ПК) каждого из параметров клинических характеристик. Расчеты проведены по разработанной А.А. Генкиным и Е.В. Гублером методике неоднородной последовательной процедуры, основанной на последовательном анализе Вальда.
P(xj /A1)
ПК(xj ) = 100 lg ________,
P(xj /A2)
где ПК(xj) — прогностический коэффициент для определенного значения диагностического параметра.
Контрольная группа формировалась динамически для каждого изучаемого параметра. Контролем были больные с МГИС, которые не имели оцениваемых клинических характеристик. Например, оценка развития МГИС у больных с ожоговой травмой проводилась с использованием контрольной группы, в которой были больные, не имеющие данной характеристики (другие виды поражений).
Анализ прогностических групп проводился путем определения суммы отдельных прогностических коэффициентов, при вероятности пропуска группы высокого прогноза на уровне не более р < 0,05 (ошибка первого рода — a) и ложного отнесения группы минимального прогноза в группу высокого — не более p = 0,1 (ошибка второго рода — a). Пороговые значения прогностических коэффициентов при вышеуказанных уровнях ошибок составляют от –120 до 100. При достижении верхнего порога оцениваемый больной может быть отнесен к контингенту высокой вероятности тяжелой формы МГИС, а при достижении нижнего — минимальной прогностической вероятности тяжелых патологических изменений.
Диапазон между пороговыми значениями пропорционально разделен на 3 части: от –120,0 до –50 (группа сниженного риска), от –49,9 до +30 (группа среднего риска (вероятности)) и от +30,1 до +100 (группа повышенного риска), что дает возможность формировать группы с промежуточными состояниями и более дифференцированно подходить к планированию лечебной тактики.
Результаты и их обсуждение
Ценность использованной методологии обусловлена ее простотой и возможностью многоэтапного применения в течение любого из периодов лечения. Данная диагностическая модель является существенным дополнением к системе клинической диагностики МГИС. Результаты расчетов прогностических коэффициентов приведены в табл. 1.
Комбинированное использование прогностических коэффициентов, отвечающих определенным диапазонам диагностических результатов, позволяет нам, с одной стороны, несколько формализовать диагностические критерии и вместе с тем оценить их прогностическую ценность для определенной категории больных.
Методика прогнозирования предусматривает определение суммы прогностических коэффициентов по отдельным диагностическим параметрам. Так, например, если у больного 55 лет (ПК = –21) ожоговая этиология травмы (ПК = +52), АД ниже 120 мм рт.ст. (или шок) (ПК = +22), 1 локализация (ПК = –17), срок обращения за помощью 2 часа (ПК = +4), без повреждений магистральных сосудов (ПК = –25), уровень подфасциального давления 25 (ПК = +8). При этом суммарное значение ПК = –21 + 52 + 22 – 17 + 4 – 25 + 8 = 23, что соответствует группе среднего риска развития МГИС. Детальное обследование больного, с оценкой аэроионных проб и других показателей, позволяет более точно дифференцировать характер процесса и его прогноз с возможным переходом пациента как в группу сниженного риска, так и в группу повышенного и высокого риска.
Наиболее неблагоприятными прогностическими признаками являются: ожоговая травма (ПК = +52), электротравма (ПК = +45), длительное использование кровоостанавливающих жгутов (более 4 часов) (ПК = +40), повреждение магистральных сосудов без восстановления более 6 часов (ПК = +47), повышение NH3 (ПК = +36). Наличие указанных признаков формирует повышенный или высокий риск развития МГИС даже без учета других клинических характеристик больных.
Коэффициенты информативности являются вспомогательными параметрами прогностической модели и дают возможность оценить информационную ценность отдельных клинических характеристик. Но при этом меньшие коэффициенты информативности отдельных признаков не исключают необходимости их комплексного использования.
Как показывает данный анализ, при своевременно проведенной диагностике и своевременно начатом консервативном лечении отмечается МГИС легкой и средней степени, патологический процесс завершается на стадии обратимых нарушений кровообращения, не переходя в дальнейшие этапы развития (2-я стадия — необратимых нарушений кровоснабжения при МГИС, ишемическая контрактура Фолькмана, острый период; 3-я стадия — ишемическая контрактура Фолькмана, реактивно-восстановительный период; 4-я стадия — ишемическая контрактура Фолькмана, резидуальный период).
Таким образом, ранняя диагностика и безотлагательно начатое лечение не по имеющимся клиническим показаниям, а по прогностическим данным (при балльной оценке) позволяет проводить профилактику компартмент-синдрома или начинать лечение в фазе обратимого расстройства кровоснабжения, без формирования фиброзно-рубцового перерождения мягких тканей и неврологических дефицитов. Также балльная оценка позволяет делать прогноз не только развития патологического процесса, но и тяжести его течения.
Так, при анализе клинического течения у 83 пациентов с ожогами, вызванными электротравмой, или циркулярными ожогами, занимающими 2/3 и более диаметра сегмента, вызванными другими травмирующими агентами (тепловые, химические), развивалась тяжелая степень МГИС в 100 % случаев. Поэтому мы оценили данное состояние в +52 балла.
Высокоэнергетическая травма наблюдалась у наших пациентов в 28,45 % случаев (70 пациентов), поэтому риск при высокоэнергетической травме мы расценили как высокий, в балльном эквиваленте: перелом типа А — –27 баллов, типа В — +2 балла, типа С — +31 балл.
Наличие шокового состояния, наблюдающегося у 15 пациентов (6,07 %), было определено нами в +22 балла риска развития МГИС, при давлении от 120 до 140 мм рт.ст. риск снижался до –15 баллов, при давлении > 140 мм рт.ст. до –5 баллов.
В некоторых клинических случаях (7 случаев — 2,85 %) наблюдалась патология двух конечностей. Риск развития МГИС оценен нами в +4 балла в связи с рефлекторным выключением «мышечного насоса» с обеих сторон. При наличии повреждения обоих сегментов одной конечности, на наш взгляд, резко повышается риск развития МГИС, статистически верифицирован как +9 баллов. Доля такой патологии в наших наблюдениях составляет: 7 пациентов (2,85 %) с наличием переломов и 73 (29,67 %) — с наличием электротравмы, риск развития МГИС равен 100 баллам.
Важна и локализация — место перелома для определения степени риска развития МГИС. Практически все больные с наличием переломов имели следующую их локализацию: дистальный метаэпифиз плеча, перелом обеих костей предплечья, проксимальный метаэпифиз большеберцовой кости, переломы лодыжек с наличием вывиха стопы, множественные переломы костей стопы. Для риска развития МГИС повреждения данной локализации получили +7 баллов. Риск развития МГИС в послеоперационном периоде оценен нами в +3 балла — при синтезе обеих костей предплечья или голени накостными фиксаторами.
Важным фактором является длительность времени, через которое пациент обратился после травмы: обращение до 1 ч — –22 балла, от 1 до 6 ч — +4 балла, от 7 до 24 ч — +16 баллов, более суток — +26 баллов. При пребывании пациента на месте происшествия в холодное время года от 1 до 3 часов добавляется 1 балл, при пребывании более 3 ч — 7 баллов.
Использование кровоостанавливающих жгутов (на этапе догоспитальной помощи или интраоперационно) было у 17 пациентов (6,91 %), риск развития МГИС оценивался в –12 баллов при соблюдении сроков их применения. При увеличении времени применения жгута до 4 часов риск оценивался в +14 баллов, при увеличении данного срока — +40 баллов.
Отсутствие адекватной транспортной иммобилизации — +16 баллов. При попытках пациента выполнить функциональную нагрузку на поврежденную конечность дополнительно добавляется 15 баллов.
Немаловажным фактором, который оценен нами в +32 балла, является осложненный перелом с повреждением магистральных сосудов, наличие синдрома длительного сдавления конечности или кратковременное сдавление с наличием нескольких переломов сегмента (обычно в нашей практике это были стопа и кисть). Наличие только повреждения магистральных сосудов не всегда приводило к развитию МГИС, зависело от локализации, анатомических особенностей пациента (наличие коллатералей), сроков от времени повреждения до восстановления кровообращения. При восстановлении кровоснабжения в первые 2 ч — –8 баллов, 2–6 часов — +6 баллов, при увеличении времени прогноз ухудшается до +47 баллов.
По уровню подфасциального давления прогноз развития компартмент-синдрома распределен следующим образом: при тканевом давлении до 20 мм рт.ст. — –22 балла, 20–30 мм рт.ст. — +8 баллов, при давлении свыше 30 мм рт.ст. — +27 баллов.
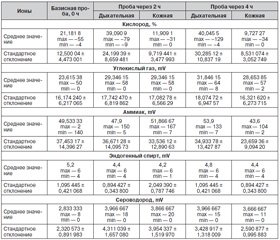
По данным аэроионных проб также можно определить наличие МГИС и степень тяжести проявления — на основании сравнения средних значений показателей ионов (M ± m), представленных в табл. 2.
Видно, что повышение уровня углекислого газа, аммиака, сероводорода и снижение уровня ионов кислорода, эндогенного спирта позволяют прогнозировать развитие компартмент-синдрома. Это дает возможность оценить каждый показатель аэроионных проб. Вариант нормы соответствует –34 баллам, повышение СО2 — +5 баллов, повышение H2S — +9 баллов, повышение NH3 — +65 баллов, снижение O2 — +12 баллов. Причем вся данная группа ионов позволяет судить о наличии компартмент-синдрома. Кроме того, в прогностическом плане течения МГИС повышение уровня аммиака (азотистые соединения) говорит о наличии второй фазы развития — необратимой в связи с деструкцией тканей, оценивается в +66 баллов.
Выводы
1. При термической травме конечности — циркулярных ожогах IIIb и IV ст. или ожогах, занимающих 2/3 окружности сегмента, и электротравме открытая лечебно-профилактическая декомпрессия показана во всех случаях, независимо от показателей подфасциального давления.
2. На основе вероятностного анализа разработана система прогнозирования развития компартмент-синдрома. Комбинированное использование прогностических коэффициентов, отвечающих определенным диапазонам диагностических результатов, позволяет количественно рассчитать степени риска развития компартмент-синдрома. Полученные результаты свидетельствуют о том, что статистически значимое повышение риска развития МГИС сопровождается снижением уровня кислорода < 17,3 % (относительный риск 7,37; р < 0,01), снижением уровня углекислого газа < 0,043 mV (относительный риск 4,05; р < 0,01), а также повышением уровня аммиака выше 0,423 mV (относительный риск 8,78; р < 0,01).
3. На основании ранжирования прогностических факторов разработаны алгоритмы диагностики компартмент-синдрома для травматически поврежденного и удлиняемого сегмента конечности, которые позволяют разработать дифференцированную тактику лечения и избежать развития тяжелых ишемических изменений тканей у 89 % таких пациентов.
1. Лябах А.П., Страфун С.С, Лєсков В.Г. Сучасна клінічна діагностика ішемічних контрактур стопи: Метод. рек. — К., 2001. — 12 с.
2. Профілактика, діагностика та лікування ішемічних контрактур кисті та стопи / Страфун С.С., Бруско А.Т., Лябах А.П., Лєсков В.Г., Тимошенко С.В. — К.: Стилос, 2007. — 264 с.
3. Страфун С.С. Профілактика, діагностика та лікування ішемічних контрактур кисті та стопи / С.С. Страфун // Вістник ортоп. та протезув. — 2002. — № 2. — С. 85-88.
4. Страфун С.С. Сравнительные способы диагностики местного гипертензионно-ишемического синдрома / С.С. Страфун, А.В. Ткач, Ю.И. Решетилов, С.Н. Дмитриева // Травма. — 2009. — Т. 10, № 2. — С. 226-229.
5. Ткач А.В. Способы диагностики местного гипертензионно-ишемического синдрома у пациентов с ожогами конечностей / А.В. Ткач // Таврический медико-биологический вестник. — 2012. — Т. 15, № 1. — С. 245-247.

/7/7.jpg)
/9/9.jpg)