Журнал «Здоровье ребенка» 4 (55) 2014
Вернуться к номеру
Ферментотерапія в педіатрії: доцільність і виваженість підходів до її проведення
Авторы: Банадига Н.В. - ВДНЗ «Тернопільський державний медичний університет ім. І.Я. Горбачевського МОЗ України»
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
У статті розглядається роль ферментів у процесі травлення, а також приділяється увага проблемі зовнішньосекреторної недостатності підшлункової залози. Дані характеристика ферментних препаратів, рекомендації щодо їх раціонального застосування.
В статье рассматривается роль ферментов в процессе пищеварения, а также уделяется внимание проблеме внешнесекреторной недостаточности поджелудочной железы. Даны характеристика ферментных препаратов, рекомендации относительно их рационального применения.
The article considered the role of enzymes in the digestive process, and attention is paid to the problem of exocrine pancreatic insufficiency. Characteristics of enzyme preparations, recommendations for their rational use are given.
підшлункова залоза, недостатність, ферментні препарати.
поджелудочная железа, недостаточность, ферментные препараты.
pancreas, insufficiency, enzyme preparations.
Статья опубликована на с. 102-107
В останні два десятиліття реєструється помітне погіршення показників здоров’я дітей, зросла частка хронічної патології, серед якої чільне місце займає гастроентерологічна [1, 4, 7, 11]. Незважаючи на добрі напрацювання діагностичного алгоритму, запровадження уніфікованих протоколів лікування захворювань органів травлення, залишаються не вирішеними проблеми поліпрагмазії та недостатньої ефективності медикаментозної терапії. Реальні труднощі обумовлені тим, що згаданій патології на сучасному етапі притаманні феномени синтропії, рання маніфестація, рецидивуючий перебіг. Поряд із цим зростає важливість корекції порушеної функції суміжних органів, зокрема зовнішньосекреторної функції підшлункової залози (ПЗ) [3, 6]. З огляду на важливість адекватного нутритивного забезпечення для динамічного, гармонійного розвитку дитини потрібні кваліфікований підхід до лікування основного захворювання та цілеспрямоване усунення функціональних порушень із боку суміжних органів. Водночас у дитячому віці переважають функціональні ураження або вони мають місце в дебюті захворювання [2, 4], що обумовлює доцільність використання замісної (ферментної) терапії. Підшлункова залоза — центральна залоза травлення, відрізняється від інших органів множинністю функцій. Вона здатна виробляти панкреатичний сік (суміш різних ензимів), що є проявом її зовнішньосекреторної діяльності, і гормони внутрішньої секреції (інсулін, глюкагон, калікреїн), що регулюють обмінні процеси, які впливають на стан мікроциркуляторного русла багатьох органів і систем, у тому числі слизової оболонки органів травлення, у першу чергу шлунка і дванадцятипалої кишки. У зв’язку з цим у гастроентерології доволі часто проводять корекцію процесів мальабсорбції та мальдигестії із застосуванням препаратів на основі ферментів ПЗ.
У педіатричній практиці ферментні препарати (ФП) набули широкого застосування, цьому є об’єктивні передумови. У дітей раннього віку спостерігається низька функціональна активність травного каналу загалом і ПЗ зокрема. Окремо слід сказати про функціональну незрілість ПЗ у дітей, що визначається не лише пізнім стартом екзокринної функції ПЗ на першому році життя дитини, а й анатомічними особливостями залози. Зокрема, багата васкуляризація ПЗ, добрий розвиток сполучнотканинного каркаса за умов будь–яких патологічних впливів сприяють легкому виникненню набряку, що зумовлює порушення відтоку секрету, підвищення внутрішньопротокового тиску. Повертаючись до особливостей функціонування екзокринної частини ПЗ у ранньому віці, доречно наголосити на певних пристосувальних механізмах, що покликані забезпечити еволюційне дозрівання секреторного апарату залози. Насамперед це стосується ролі раннього та тривалого грудного вигодовування, компоненти якого, незважаючи на низьку ферментативну активність залоз травної системи, добре засвоюються, оскільки молоко містить достатньо високу кількість ферментів (ліпаза, амілаза, пепсин, трипсин). Цим забезпечуються комфортні умови фізіологічного дозрівання екзокринної активності ПЗ, а введення страв прикорму — стимул до прискорення темпів становлення травної функції. Тобто такий характер харчування — запорука фізіологічних темпів постнатального розвитку ферментативних систем. Однак у випадку штучного вигодовування (навіть за умови раціонального) може виникати транзиторна екзокринна недостатність, обумовлена фізіологічною незрілістю ПЗ.
Лікар–педіатр при спостереженні за дитиною враховує також особливості становлення екзокринної функції ПЗ. У малюків перших 6 місяців життя є дефіцит амілази, що обумовлює зниження можливостей засвоєння крохмалю. Протягом першого року життя активність і секреція панкреатичних ферментів динамічно зростають. Так, активність амілази сягає свого максимуму у дев’ятимісячному віці. Окрім того, у постнатальному періоді ацинарна частина ПЗ зазнає інтенсивного розвитку — у віці до 3 років та в період статевого дозрівання. Останнє потребує врахування при плануванні дієтичних рекомендацій дітям цих двох груп. Водночас ПЗ має суттєві компенсаторні можливості в дитячому віці, а також може адаптуватися до особливостей харчування. Під останнім слід розуміти, що тривале одноманітне (чи часто повторюване) харчування обумовлює зміну характеру секреції ПЗ у відповідь на харчовий стимул (переважання жирів чи вуглеводів або білків), однак таке пристосування за тривалістю та ефективністю буде в кожного пацієнта індивідуальним, що визначається функціональним станом травної системи загалом і значенням спадковості зокрема.
Травлення є складним багатоступінчастим процесом, що забезпечує організм дитини необхідними нутрієнтами для динамічного й гармонійного розвитку. Перші етапи засвоєння їжі розпочинаються в ротовій порожнині (хімічна (амілаза слини) та механічна обробка). Просуваючись по травному каналу, їжа зазнає наступного й повного гідролізу та всмоктування. Загалом виділяють три основні послідовні етапи:
1) порожнинне травлення — формування харчового хімусу й гідроліз харчових компонентів до оліго– і мономерів, у якому провідну роль відіграють ферменти підшлункової залози;
2) мембранне травлення, що відбувається на зовнішній мембрані ентероцитів за участю кишкових гідролаз і фіксованих на нутрієнтах панкреатичних ферментів та забезпечує кінцевий гідроліз компонентів їжі;
3) процеси всмоктування.
При цьому провідну роль відіграє саме порожнинне травлення, що, у свою чергу, залежне насамперед від кількості й активності ферментів підшлункової залози. Однак порушення порожнинного травлення може бути спричинене не лише патологією ПЗ, а й ураженням інших органів, зокрема печінки, жовчовивідних шляхів, дванадцятипалої кишки, у якій об’єднуються основні шляхи — шлунковий, печінковий, панкреатичний, і тонкої кишки, що дає можливість регулювати секреторну, моторну й евакуаторну діяльність органів травлення. Вищевикладене доводить єдність функціонування органів, пов’язаних анатомічно із дванадцятипалою кишкою.
Гідроліз білкових компонентів їжі здійснюється протеолітичними ферментами (трипсин, хімотрипсин, еластаза, карбоксипептидаза), що синтезуються підшлунковою залозою в неактивному стані, а у просвіті дванадцятипалої кишки (за наявності ентерокінази й оптимального pH) активуються. При значенні pH 5–7 кишкова ентерокіназа переводить неактивний трипсиноген в активний трипсин, запускаючи механізм активації інших протеолітичних ферментів.
Гідроліз вуглеводів (крохмаль, глікоген) здійснюється амілазою до дисахаридів і глюкози. Жири в присутності жовчі розщеплюються панкреатичною ліпазою до ди– і моногліцеридів, жирних кислот, гліцерину.
Важливе клінічне значення має та обставина, що дія панкреатичних ферментів зменшується в міру просування харчової грудки від дванадцятипалої до термінальних відділів клубової кишки. Слід пам’ятати, що лише невелика кількість активної ліпази досягає порожнистої кишки, а протеази є більш стійкими, приблизно 30–45 % їх активності спостерігається в термінальних відділах тонкої кишки. Саме цим пояснюється той факт, що клінічні прояви панкреатичної недостатності першочергово пов’язані з порушенням процесів травлення жирів, лише згодом — білків і вуглеводів. Згідно з рекомендаціями Австралійського клубу панкреатологів [11], екзокринна недостатність ПЗ проявляється тоді, коли кількість ферментів, виділених у просвіт дванадцятипалої кишки у відповідь на стимуляцію їжею, недостатня для забезпечення фізіологічних процесів травлення.
Причини зовнішньосекреторної недостатності ПЗ:
— ураження залози із зменшенням функціонуючої паренхіми;
— зниження pH < 5,5 у дванадцятипалій кишці (інактивація кишкової ентерокінази і панкреатичних ферментів);
— моторна дисфункція дванадцятипалої кишки;
— надмірний бактерійний ріст у тонкій кишці (руйнування ферментів);
— дефіцит жовчі та ентерокінази.
Патологія ПЗ (здебільшого хронічна) супроводжується зменшенням маси функціонуючої паренхіми, що обумовлює недостатність її екзокринної функції. Остання полягає у зниженні секреції ферментів, що забезпечують гідроліз жирів (ліпаза, коліпаза, фосфоліпаза А), білків (трипсин, хімотрипсин, еластаза, карбоксипептидаза А, В), вуглеводів (амілаза), синтез бікарбонатів. Потрібно розуміти, що типові клінічні прояви (стеаторея) з’являються за умови ураження 90 % маси ПЗ і більше. Складності діагностики полягають і в тому, що донедавна не були сформульовані світові стандарти діагностики хронічного панкреатиту та екзокринної недостатності ПЗ [11].
Панкреатична недостатність може мати первинний або вторинний характер, останній частіше зустрічається саме в дітей. Серед причин екзокринної недостатності виділяють первинні (вроджені аномалії, спадкові захворювання, пухлини ПЗ) та вторинні (перенесені захворювання, патологія травної системи, порушення моторики кишечника, функціональна незрілість ПЗ, аліментарні фактори, харчова алергія). Первинну панкреатичну недостатність виділяють в основному в дітей із муковісцидозом — 85–90 % випадків. За потреби корекції екзокринної недостатності підшлункової залози провідну роль відіграє компенсація дефіциту ферментів, що забезпечують гідроліз жирів (ліпази) [3, 7, 9].
Раніше зазначалося, що в дітей частіше спостерігається вторинна панкреатична недостатність, яка значною мірою обумовлена патологією гепатобіліарної зони. Зокрема, порушення процесів жовчоутворення й виділення обумовлює порушення моторно–евакуаторної функції жовчного міхура, емульгації жирів. Останнє спричиняє зниження панкреатичної ліпази.
Вторинна панкреатична недостатність виникає також на фоні тяжких захворювань кишечника (виразковий коліт, хвороба Крона, целіакія), коли порушення панкреатичних ферментів викликане зменшенням продукції холецистокініну, секретину, ентерокінази клітинами тонкої кишки. Останнім часом значна увага приділяється екзокринній недостатності ПЗ у дітей з алергічними захворюваннями (атопічний дерматит, харчова алергія), а її корекція покращує ефективність лікувальних заходів.
У практичній діяльності педіатра, сімейного лікаря, лікаря–інфекціоніста значне місце займає ведення дітей із гострими кишковими інфекціями. У цій ситуації логічним є питання потреби, доцільності застосування ФП. За умов інфекційно–запального ураження кишечника існують реальні передумови виникнення транзиторної ферментативної (у тому числі панкреатичної) недостатності.
Клінічними проявами порушення екзокринної недостатності підшлункової залози є болі в животі, зміна (частіше втрата) апетиту, нудота, бурчання в животі, метеоризм, зміни частоти випорожнень (діарея, запори) та їх характеру (неперетравлені рештки, стеаторея, креаторея). Однак вищезазначені симптоми не є специфічними, тому лікар порівнює клінічні ознаки та шукає типові симптомокомплекси. Зокрема, біль при панкреатичній недостатності локалізується в епігастрії, лівому підребер’ї, може мати оперізуючий характер, іррадіювати під лопатку, в плече. Болі мають постійний або нападоподібний характер, провокуються прийомом жирної їжі, переїданням. Біль при ураженні ПЗ погано купірується анальгетиками, посилюється при застосуванні тепла, зменшується при використанні холоду. Інтенсивні болі змушують дитину займати вимушене положення. Окрім того, болі супроводжуються здуттям живота, бурчанням, симптомами диспепсії. Характерними є рідкі випорожнення, у великій кількості, пінистого характеру, світло–жовтого кольору, сального вигляду.
Для точної ідентифікації панкреатичної недостатності необхідно застосувати складний та великий за обсягом алгоритм, що передбачає використання лабораторних та інструментальних методів. Найбільш доступним та до певної міри показовим є копрологічне дослідження. Стосовно інформативності змін, виявлених при копрологічному дослідженні, слід зауважити:
— велика кількість м’язових волокон є свідченням зниженої активності протеолітичних ферментів (шлунка і підшлункової залози);
— велика кількість нейтрального жиру — свідчення зниження ліполітичної активності ферментів підшлункової залози;
— велика кількість жовчних кислот говорить про зменшення жовчі;
— велика кількість солей жирних кислот (мила) з’являється внаслідок зниження протеолітичної активності тонкої кишки;
— велика кількість крохмалю та йодофільної флори свідчить про зниження амілолітичної активності.
Більш точним непрямим, але дорогим методом є ліпідограма калу. Певну діагностичну цінність мають провокаційні тести, що не можуть бути широко запровадженими в педіатричну практику. Сучасним та високоінформативним методом оцінки екзокринної функції ПЗ вважають визначення в калі еластази–1 [3, 10, 12]. Важливим є й те, що на результати не впливають характер харчування чи вживання ФП. Водночас цим методом неможливо визначити наявність відносної панкреатичної недостатності (показники фекальної еластази в межах норми), для цього потрібне зіставлення їх з клінічними ознаками та результатами провокаційних тестів.
Узагальнюючи клінічний досвід застосування ФП, слід відзначити, що приводом до їх призначення є:
— порушення процесів порожнинного травлення;
— порушення процесів травлення на рівні шлунка;
— порушення моторики верхніх відділів травного каналу;
— захворювання підшлункової залози, у тому числі синдром панкреатичного болю, що супроводжуються порушенням зовнішньосекреторної функції;
— захворювання жовчного міхура, шлунка, кишечника.
Корекція порушень травної функції ПЗ передбачає насамперед раціональну терапію основного захворювання, що й обумовило виникнення панкреатичної недостатності. Провідну роль у лікуванні цих захворювань відіграє дієтотерапія, характер якої визначається основним захворюванням. Не можна не звертати увагу на те, що дитина на відміну від дорослого продовжує рости й розвиватися, а тому потребує не лише пластичного матеріалу (білки), а й енергії (жири, вуглеводи). Ця проблема на сучасному етапі адекватно вирішується. Завдяки наявним високоефективним ФП замісна терапія не вимагає зменшення споживання жирів дитиною, потрібен індивідуальний підхід до вибору оптимальної дози замісної терапії. Це дає можливість забезпечити пацієнту максимально необхідний нутритивний статус, що має вирішальне значення для організму, який продовжує рости та вдосконалюватися.
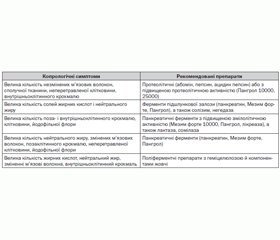
Однією з клінічних передумов до призначення ФП є також результати копрологічного дослідження (табл. 1).
Говорячи про роль ферментної терапії в лікуванні гострих кишкових інфекцій, слід пам’ятати, що ФП призначають у разі:
— купірування в дитини проявів токсикозу з ек–сикозом ІІ–ІІІ ступеня, інфекційно–токсичного шоку, нейротоксикозу;
— супутньої патології травної системи;
— розширення складу дієти при стабільному стані пацієнта;
— клінічних (метеоризм, диспепсія, густо обкладений язик) і копрологічних (неперетравлені рештки їжі) ознак порушення травлення (табл. 1).
Протипоказання до застосування ФП при гострих кишкових інфекціях:
— гострий період захворювання (ФП на основі панкреатиту із компонентами жовчі). Оскільки компоненти жовчі стимулюють моторику кишечника, жовчного міхура, збільшують осмотичний тиск хімуса, що обтяжує діарейний синдром;
— при секреторній, інвазивній діареї в перші 2–3 доби з моменту захворювання, при посиленій перистальтиці кишечника. У разі ротавірусної інфекції ФП в початковому періоді не призначають.
Раціональне застосування ФП передбачає обов’язкове врахування таких моментів:
— препарат тваринного чи рослинного походження;
— уміст ферментів, насамперед активність ліпази;
— форма випуску (порошок, таблетки, капсули), якій властива кислотостійкість, щоб запобігти інактивації панкреатичних ферментів;
— швидке вивільнення ферментів у просвіті дванадцятипалої кишки при значеннях рН 5–7;
— добра переносимість, відсутність побічних ефектів;
— регламентація прийому відповідно до прийомів їжі;
— тривалість застосування.
Лікар обирає один із відомих ФП:
— екстракти слизової оболонки шлунка (абомін, ацидин–пепсин);
— панкреатичні ферменти, що об’єднують амілазу, ліпазу, трипсин (панкреатин, Мезим форте, Пангрол);
— ферменти рослинного походження, що містять папаїн, грибкову амілазу, протеазу, ліпазу тощо;
— комбіновані ФП — панкреатин у поєднанні з компонентами жовчі, геміцелюлози;
— комбіновані ФП — поєднання панкреатину з рослинними ензимами, вітамінами;
— дисахаридази.
З позицій власного досвіду та узагальнюючи офіційно оприлюднені дані клінічних досліджень, перевагу надаємо препаратам на основі панкреатину (містять ліпазу, амілазу, протеази), зокрема тваринного походження. Ці ФП вважають універсальними, такими, що не впливають на функції шлунка, печінки, моторику кишечника й біліарної системи. Водночас вони забезпечують достатню концентрацію ферментів та усувають комплекс клінічних симптомів (нудота, бурчання, метеоризм, неперетравлені рештки у калі, стеаторея). Сучасні препарати панкреатину можна успішно використовувати в дітей різних вікових груп [3, 8, 11].
Саме з цих міркувань заслуговують на увагу препарати панкреатину Мезим і Пангрол (табл. 2) виробництва німецької компанії «Берлін–Хемі», що призначають для корекції панкреатичної недостатності та транзиторних порушень зовнішньосекреторної функції ПЗ. Зокрема, препарат Мезим 10000 містить свинячий панкреатин у концентрації 10000 ОД ліпази, 7500 ОД амілази, 375 ОД протеаз. На відміну від креону Мезим форте (табл. 2), що містить 4200 ОД амілази, 3500 ОД ліпази і 250 ОД протеаз, частіше призначається для корекції короткочасних і незначних дисфункцій підшлункової залози. Таблетка Мезим форте вкрита спеціальною кислотостійкою оболонкою, що захищає компоненти препарату від агресивного впливу кислого середовища шлунка й забезпечує особливу фармакодинаміку (активація ферментів у проксимальних відділах дванадцятипалої кишки, неподалік від виходу протоку ПЗ). Панкреатична ліпаза (свиняча), що міститься в препараті Мезим форте 10000, схожа за механізмом дії на людську ліпазу.
У педіатричній практиці добре зарекомендував себе ФП Пангрол, особливо у формі капсул (з умістом 10000 або 25000 ліпази), що є двошаровим препаратом: укритий кишковорозчинною оболонкою, містить мікротаблетки, які діють лише в просвіті дванадцятипалої кишки. На відміну від міні–мікросферичних ферментів технологія виробництва мікротаблеток Пангролу вигідно відрізняється відсутністю фталатів, що дуже важливо (із міркувань безпеки) в дитячому віці та при вагітності. При рН дуоденального вмісту понад 5,5 оболонки розчиняються, при цьому практично відтворюються фізіологічні процеси травлення, коли панкреатичний сік виділяється порціями при періодичному надходженні їжі зі шлунка. Застосування Пангролу 20000 передбачає комплексне вирішення проблем, пов’язаних із порушенням зовнішньосекреторної функції ПЗ (купірування явищ метеоризму, бурчання в животі), завдяки вмісту симетикону.
У клінічній практиці часто зустрічаються розлади функціональної діяльності ПЗ, що супроводжують різні захворювання верхніх відділів травного каналу або зустрічаються при погрішностях в їжі, переїданні. Дітей можуть турбувати нудота, нездужання, тяжкість у животі, короткочасні ниючі або тиснучі болі навколо пупка, спостерігається короткочасне розм’якшення калу після переїдання або прийому незвичної, нової їжі. Особливо часто це зустрічається під час відпочинку, далеко від звичайних місць проживання. Однак при клінічному й лабораторному обстеженні виражених патологічних змін, як правило, не визначається. Саме в цих випадках і необхідне застосування слабоактивних панкреатичних ензимів (Мезим форте, панкреатин).
Більшість фахівців у галузі гастроентерології, панкреатології дотримуються думки, що форма випуску ФП теж має вирішальне значення у проведенні ефективної терапії. Зокрема, із метою купірування панкреатичного болю доцільним є використання класичних форм панкреатину (таблетки), а не капсул. Оскільки при зниженні вироблення бікарбонатів ПЗ відбувається ідентифікація вмісту верхніх відділів дванадцятипалої кишки, то в кислому середовищі вивільнення захищених ентеросолюбною оболонкою ферментів не відбувається і концентрація протеаз не підвищується. Відповідно, через рилізинг–систему не задіяний механізм зворотного зв’язку з наступним зменшенням вироблення ендогенних ферментів ПЗ, а тому це не забезпечує функціональний спокій залози.
Результати ряду досліджень свідчать про високу клінічну ефективність таблетованих препаратів панкреатину (Мезим 10000, Пангрол 20000) у лікуванні больових форм ураження ПЗ та недостатню ефективність капсульованих форм, у яких гранули панкреатину вкриті ентеросолюбною оболонкою. Больовий компонент при ураженні підшлункової залози обумовлений здебільшого зростанням внутрішньопротокового тиску та підвищеною секрецією залози. За цих обставин провідну роль відіграє вміст у ФП протеаз; вони забезпечують відносний спокій підшлункової залози і зменшують вираженість больових відчуттів завдяки тому, що блокують панкреатичну секрецію у відповідь на руйнування секретину та холецистокініну у просвіті дванадцятипалої кишки.
ФП у формі капсул високоефективні при використанні з метою компенсації панкреатичної недостатності. Водночас застосування таблетованих форм (Мезим, Пангрол) панкреатину також є виправданим, і з доведеною клінічною ефективністю у випадку нетяжких порушень зовнішньосекреторної функції ПЗ. Аналізуючи дані численних публікацій із приводу порівняльного застосування класичних таблеток панкреатиту (Мезим 10000) із кислотостійкою оболонкою й капсул, у яких панкреатин укритий кишковорозчинною оболонкою, у випадку хронічного панкреатиту із зовнішньосекреторною недостатністю, дійшли висновку, що у подоланні панкреатичної недостатності їх ефективність ідентична [7, 8]. Проте при вираженому панкреатичному болю перевага надається таблетованим формам панкреатину.
Загальновідомо, що вибирають ФП, укриті кислотостійкою оболонкою, в іншому випадку в просвіті шлунка руйнується до 80 % активності ліпази. Водночас важливим є оптимальне співвідношення вмісту ліпази і протеаз. Якщо вміст останніх високий, то, цілком ймовірно, буде прискорення механізмів інактивації ліпази.
Із метою корекції екзокринної недостатності підшлункової залози не використовують ФП, що містять компоненти жовчі. Останні чинять холеретичний і холекінетичний ефект, активують моторну функцію й підвищують осмотичний тиск у кишечнику, посилюють діарею.
Дозування ФП слід здійснювати відповідно до маси тіла дитини та глибини порушень процесів травлення [3, 6]. Доза під час лікування здебільшого зазнає корекції з огляду на самопочуття дитини, наявність апетиту, купірування розладів травлення, тобто під контролем копрограми й динаміки маси тіла. Поява на тлі ферментотерапії запорів не є свідченням недоліків капсульної форми препарату. Насамперед це може бути зумовлене застосуванням надто високих доз (за ліпазою) ФП.
Дозу Пангролу, як і будь–якого іншого ферментного препарату, розраховують за вмістом ліпази. Слід розпочинати з 1000 ОД ліпази на 1 кг маси тіла на добу. За відсутності ефекту дозу препарату поступово збільшують під контролем копрограми, доводячи до 4000–5000 ОД на 1 кг маси тіла на добу, при тяжкій екзокринній недостатності ПЗ доза не повинна перевищувати 15000 ОД на 1 кг маси тіла на добу. Добову дозу препарату рівномірно розподіляють на кількість прийомів їжі за день.
Важливе значення має правильна регламентація прийому ФП відповідно до вживання їжі. За умови прийому препарату до чи після їжі виникають дві патологічні ситуації: передчасне або запізніле вивільнення ферментів у просвіті дванадцятипалої кишки, що лише поглиблює прояви екзокринної недостатності. ФП у формі капсул із міні–мікросферами або міні–мікротаблетками слід приймати під час їжі, що забезпечує високу активність гідролітичних процесів.
Тривалість використання ФП у кожному випадку буде індивідуальною та визначатиметься моментом досягнення компенсації панкреатичної недостатності (нормалізація випорожнень: зникнення неперетравлених домішок, стеатореї, креатореї, позитивна динаміка маси тіла, лабораторних показників).
Недостатня ефективність замісної терапії ФП може бути обумовлена групою причин: недотримання регламентованого прийому препарату; неточність діагностичного алгоритму; неадекватна терапія основного захворювання (у випадку екзокринної недостатності вторинного генезу замісна терапія є лише компонентом комплексної терапії). Вищезгадане обумовлює необхідність відстежити ефективність із корекцією дози, тривалості застосування ФП у кожної дитини.
Побічна дія ФП на основі панкреатину: можливі алергічні реакції, рідко — діарея або запор, нудота, дискомфорт у животі. Препаратам притаманна добра переносимість та нечасті побічні ефекти.
Застереження. У сечі хворих, які тривало застосовують високі дози панкреатичних ферментів, може спостерігатися підвищений уміст сечової кислоти, що сприяє преципітації сечової кислоти в канальцевому апараті нирки, створюючи передумови для розвитку дисметаболічної нефропатії і сечокам’яної хвороби.
При застосуванні препаратів панкреатину спостерігається зниження всмоктування фолієвої кислоти і заліза. Тому при тривалому застосуванні ФП рекомендується контролювати їх рівень в крові, при потребі призначати препарати заліза і фолієвої кислоти.
Таким чином, застосування препаратів панкреатину в педіатрії має реальні передумови й потребує від лікаря чітких дій у виборі препарату, дози, регламентації прийому та відстеження ефективності замісної терапії в кожному конкретному випадку.
1. Банадига Н.В. Діагностика та корекція порушень зовнішньосекреторної функції підшлункової залози у дітей / Н.В. Банадига, О.М. Дутчак // Современная педиатрия. — 2006. — № 1. — С. 82–84.
2. Банадига Н.В. Особливості діагностики стану підшлункової залози в дітей із патологією гепатобіліарної зони / Н.В. Банадига, О.М. Дутчак // Клінічна та експериментальна патологія. — 2006. — Т. V, № 3. — С. 9–11.
3. Банадига Н.В. Панкреатична недостатність у дітей з патологією травної системи / Н.В. Банадига, О.М. Дутчак, І.О. Рогальський та інші // Современная педиатрия. — 2011. — № 3. — С. 155–118.
4. Белоусов Ю.В. Заболевания поджелудочной железы у детей: панкреатит или панкреатопатия? // Здоров’я України. — 2004. — № 96.
5. Губергриц Н.Б. Возможности лабораторной диагностики заболеваний поджелудочной железы // Экспериментальная и клиническая гастроэнтерология. — 2008. — № 7. — С. 93–101.
6. Захарова И.Н., Коровина Н.А., Малова Н.Е. Экзокринная недостаточность поджелудочной железы // Міжнар. ендокринол. журнал. — 2009. — Т. 22, № 4.
7. Нагорная Н.В., Лимаренко М.П. Внешнесекреторная функция поджелудочной железы и методы ее оценки // Здоровье ребенка. — 2012. — № 8(43). — С. 76–81.
8. Шифрин О.С. Ферментные препараты в лечении внешнесекреторной недостаточности поджелудочной железы // Сonsilium Medicum Ukraina. — 2008. — № 1.
9. Kamath B.M., Piccoli D.A., Magee J.C., Sokol R.J. Pancreatic insufficiency is not a prevalent problem in Alagille syndrome // J. Pediatr. Gastroenterol. Nutr. — 2012 May 18.
10. Leeds J.S., Oppong K., Sanders D.S. The role of fecal elastase–1 in detecting exocrine pancreatic disease // Nat. Rev. Gastroenterol. Hepatol. — 2011. — Vol. 8, № 7. — P. 405–415.
11. Manadement of pancreatic exocrine insufficiency; Australasian Pancreatic Club reccomendations / J. Toouli, A.V. BianKin, M.R. Oliver et al. // MIA. — 2010. — Vol. 193, № 8. — P. 461–467.
12. Wali P.D., Loveridge–Lenza B., Horvath K. Comparison of fecal elastase 1 and pancreatic function testing in children // J. Pediatr. Gastroenterol. Nutr. — 2012. — Vol. 54, № 7. — P. 277–280.

/105/105.jpg)
/106/106.jpg)