Международный эндокринологический журнал 4 (60) 2014
Вернуться к номеру
Порівняльна оцінка ефективності препарату Еспа-карб у лікуванні хворих із гіпертиреозом
Авторы: Паньків В.І. - Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, м. Київ
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
У статті розглядаються підходи до консервативного лікування хворих на дифузний токсичний зоб (ДТЗ). Мета дослідження — оцінка спектра дії, терапевтичної ефективності й переносимості карбімазолу (препарат Еспа-карб) порівняно з тіамазолом (препарат Мерказоліл-Здоров’я) у пацієнтів із гіпертиреозом.
Матеріали та методи. Під спостереженням перебувало 55 хворих на ДТЗ, розподілених на дві групи. Перша група (n = 30) отримувала карбімазол (препарат Еспа-карб), друга група (n = 25) — тіамазол (препарат Мерказоліл-Здоров’я). Групи хворих не відрізнялися за віком, статтю, розмірами щитоподібної залози, причинами і тривалістю тиреотоксикозу.
Результати. Аналіз отриманих даних свідчить про те, що в першій групі хворих відзначається більш суттєвий ефект від лікування порівняно з хворими другої групи. Середній об’єм щитоподібної залози вірогідно зменшився лише в першій групі. У середньому тиреоїдний об’єм зменшився з 37,2 ± 3,1 см3 до 29,3 ± 2,9 см3 (р < 0,05). У другій групі спостерігалася тенденція до зменшення, але без статистичної вірогідності (з 36,4 ± 3,9 см3 до 32,4 ± 2,8 см3; р > 0,05). У пацієнтів першої групи з ДТЗ спостерігалося вірогідне збільшення рівня ТТГ (з 0,027 ± 0,009 мМО/л до 0,37 ± 0,16 мМО/л; р < 0,05) і вірогідне зменшення рівнів вТ4 (з 29,3 ± 2,3 нмоль/л до 18,4 ± 1,8 нмоль/л; р < 0,05) і вТ3 (з 7,8 ± 1,6 нмоль/л до 3,2 ± ± 1,1 нмоль/л; р < 0,05). При цьому підвищення показника ТТГ у хворих другої групи не досягло рівня статистичної значущості (р > 0,05). У той же час у хворих другої групи відзначалося вірогідне зменшення рівнів вТ4 (з 31,4 ± 2,1 нмоль/л до 21,7 ± 1,8 нмоль/л; р < 0,05) і вТ3 (з 8,2 ± 1,4 нмоль/л до 3,7 ± 1,2 нмоль/л; р < 0,05). Зниження автоімунної агресії проявлялося зниженням концентрації антитіл до рТТГ, яке у хворих першої групи набуло рівня статистичної значущості. Якщо середня добова доза препаратів Еспа-карб і Мерказоліл-Здоров’я на початку лікування в обстежених групах хворих не відрізнялася, то через 6 місяців лікування середня доза карбімазолу в першій групі становила 15,8 ± 1,7 мг, а в другій групі доза тіамазолу — 19,2 ± 2,1 мг (р > 0,05). Побічних явищ при лікуванні хворих обох груп упродовж шести місяців не спостерігалося. Нормалізація вмісту периферичних гормонів (вТ4 і вТ3) через 90 днів спостереження досягнута в 96,2 % хворих першої групи і в 74,1 % — другої групи. Число хворих, які досягнули нормального рівня ТТГ, вірогідно вищим було в першій групі (93,3 проти 76 %).
Висновки. Встановлена більша ефективність карбімазолу порівняно з тіамазолом, що проявилося швидшим досягненням клінічного ефекту і компенсації тиреотоксикозу, вірогідним зменшенням тирео-їдного об’єму, рівня антитіл до рецептора ТТГ. Використання карбімазолу сприяє зменшенню добової дози тиреостатичних препаратів у хворих на ДТЗ, що зменшує ризик виникнення ускладнень терапії. При використанні карбімазолу протягом шести місяців у хворих на ДТЗ не було зареєстровано випадків непереносимості або будь-яких побічних ефектів.
В статье рассматриваются подходы к консервативному лечению больных с диффузным токсическим зобом (ДТЗ). Цель исследования — оценка спектра действия, терапевтической эффективности и переносимости карбимазола (препарат Эспа-карб) в сравнении с тиамазолом (препарат Мерказолил-Здоровье) у пациентов с гипертиреозом.
Материалы и методы. Под наблюдением находилось 55 больных с ДТЗ, распределенных на две группы. Первая группа (n = 30) получала карбимазол (препарат Эспа-карб), вторая группа (n = 25) — тиамазол (препарат Мерказолил-Здоровье). Группы больных не отличались по возрасту, полу, размерам щитовидной железы, причинам и длительности тиреотоксикоза.
Результаты. Анализ полученных данных свидетельствует о том, что в первой группе больных отмечается более существенный эффект от лечения по сравнению с больными второй группы. Средний объем щитовидной железы достоверно уменьшился лишь в первой группе. В среднем тиреоидный объем уменьшился с 37,2 ± 3,1 см3 до 29,3 ± 2,9 см3 (р < 0,05). Во второй группе наблюдалась тенденция к уменьшению, но без статистической достоверности (с 36,4 ± 3,9 см3 до 32,4 ± 2,8 см3; р > 0,05). У пациентов первой группы с ДТЗ наблюдалось достоверное увеличение уровня ТТГ (с 0,027 ± 0,009 мМЕ/л до 0,37 ± 0,16 мМЕ/л; р < 0,05) и достоверное уменьшение уровней свТ4 (с 29,3 ± 2,3 нмоль/л до 18,4 ± 1,8 нмоль/л; р < 0,05) и свТ3 (с 7,8 ± 1,6 нмоль/л до 3,2 ± 1,1 нмоль/л; р < 0,05). При этом повышение показателя ТТГ у больных второй группы не достигло уровня статистической значимости (р > 0,05). В то же время у больных второй группы отмечалось достоверное уменьшение уровней свТ4 (с 31,4 ± 2,1 нмоль/л до 21,7 ± 1,8 нмоль/л; р < 0,05) и свТ3 (с 8,2 ± 1,4 нмоль/л до 3,7 ±
± 1,2 нмоль/л; р < 0,05). Снижение аутоиммунной агрессии проявлялось снижением концентрации антител к рТТГ, которое у больных первой группы приобрело уровень статистической значимости. Если средняя суточная доза препаратов Эспа-карб и Мерказолил-Здоровье в начале лечения в обследованных группах больных не отличалась, то через 6 месяцев лечения средняя доза карбимазола в первой группе составляла 15,8 ± 1,7 мг, а во второй группе доза тиамазола — 19,2 ± 2,1 мг (р > 0,05). Побочных явлений при лечении больных обеих групп на протяжении шести месяцев не наблюдалось. Нормализация уровня периферических гормонов (свТ4 и свТ3) через 90 дней наблюдения достигнута у 96,2 % больных первой группы и у 74,1 % — второй группы. Число больных, которые достигли нормального уровня ТТГ, было достоверно выше в первой группе (93,3 против 76 %).
Выводы. Установлена большая эффективность карбимазола в сравнении с тиамазолом, что проявилось более быстрым достижением клинического эффекта и компенсации тиреотоксикоза, достоверным уменьшением тиреоидного объема, уровня антител к рецептору ТТГ. Использование карбимазола способствует уменьшению суточной дозы тиреостатических препаратов у больных с ДТЗ, что уменьшает риск возникновения осложнений терапии. При использовании карбимазола в течение шести месяцев у больных с ДТЗ не было зарегистрировано случаев непереносимости или других побочных эффектов.
The article discusses approaches to conservative treatment in patients with diffuse toxic goiter (DTG). The purpose of research — evaluation of coverage, therapeutic efficacy and tolerability of carbimazole (Espa-Carb) compared with thiamazolum (Mercazolil-Zdorovye) in patients with hyperthyroidism.
Materials and Methods. We observed 55 patients with DTG, divided into two groups. The first group (n = 30) received carbimazole (Espa-Carb), the second group (n = 25) — thiamazolum (Mercazolil-Zdorovye). The patient groups did not differ in age, sex, size of thyroid gland and duration of thyrotoxicosis.
Results. Analysis of the findings shows that the first group of patients has a more significant effect of treatment compared with patients of the second group. Average thyroid volume was significantly reduced only in the first group. At average, thyroid volume decreased from 37.2 ± 3.1 cm3 to 29.3 ± 2.9 cm3 (p < 0.05). In the second group we observed a tendency to decrease, but without statistical significance (from 36.4 ± 3.9 cm3 to 32.4 ± 2.8 cm3 (p > 0.05). In patients from the first group with DTG, a significant increase in TSH (from 0.027 ± 0.009 mIU/l to 0.37 ± 0.16 mIU/L; p < 0.05) and a significant decrease in the levels fT4 (from 29.3 ± 2.3 nmol/l to 18.4 ± 1.8 nmol/l; p < 0.05) and fT3 (from 7.8 ± 1.6 nmol/l to 3.2 ± 1.1 nmol/l; p < 0.05) were detected. At this, TSH increase in patients of the second group did not reach a statistical significance (p > 0.05). At the same time, the second group of patients reported a significant decrease in the levels fT4 (from 31.4 ± 2.1 nmol/l to 21.7 ± 1.8 nmol/l; p < 0.05) and fT3 (from 8.2 ± 1.4 nmol/l to 3.7 ± 1.2 nmol/l, p < 0.05). Reduced autoimmune aggression manifested by a decrease in concentration of antibodies to rTSH which in patients of the first group became statistically significant. If the average daily dose of Espa-Carb and Mercazolil-Zdorovye at the baseline did not differ in the examined groups of patients, then after 6 months of treatment, the mean dose of carbimazole in the first group was 15.8 ± 1.7 mg, and the second group — 19.2 ± 2.1 mg (p > 0.05). Side effects weren’t observed for six months during the treatment of patients in both groups. Normalization of peripheral hormones (fT4 and fT3) in 90 days of observation has been achieved in 96.2 % of patients in the first group and 74.1 % — in the second group. The number of patients who achieved normal TSH levels was significantly higher in the first group (93.3 % vs. 76 %).
Conclusions. We determined higher efficiency of carbimazole compared to thiamazolum that manifested by more rapid achievement of clinical effect and compensation thyrotoxicosis, significant decrease of thyroid volume, the level of antibodies to the TSH receptor. Using carbimazole reduces thyreostatics daily dose in patients with DTG, which reduces the risk of complications of therapy. When using carbimazole for six months in patients with DTG, cases of intolerance or other adverse effects weren’t reported.
тиреотоксикоз, карбімазол, тіамазол.
тиреотоксикоз, карбимазол, тиамазол.
thyrotoxicosis, carbimazole, thiamazole.
Статья опубликована на с. 43-48
Тиреотоксикоз — синдром, при якому спостерігаються клінічні та біохімічні прояви надмірного вмісту тиреоїдних гормонів у крові незалежно від причини підвищення їх рівня. У більшості випадків тиреотоксикоз розвивається внаслідок надмірної продукції гормонів щитоподібної залози (ЩЗ). Серед усіх форм тиреотоксикозу 90 % становлять дифузний токсичний зоб (ДТЗ) і тиреотоксична аденома [1]. ДТЗ — системне автоімунне захворювання, що розвивається внаслідок вироблення антитіл до рецептора тиреотропного гормону (ТТГ) і клінічно проявляється ураженням ЩЗ із розвитком синдрому тиреотоксикозу в поєднанні з екстратиреоїдною патологією: ендокринною офтальмопатією, претибіальною мікседемою, акропатією та ін. [2].
Поширеність синдрому тиреотоксикозу в Україні (станом на 01.01.2012 р.) становила 117,9 на 100 тис. населення, захворюваність населення України на тиреотоксикоз у 2011 р. становила 13,6 на 100 тис. Щорічний приріст числа зареєстрованих хворих досягає 4,7 % [5, 6]. Однак по окремих областях ці показники відрізняються. Найвища захворюваність відзначається в Донецькій, Дніпропетровській і Сумській областях. Це може бути обумовлено кращими діагностичними можливостями, активним виявленням, але більшою мірою — станом довкілля [3].
Тиреотоксикоз у структурі ендокринної патології займає одне з провідних місць. Але проблема тиреотоксикозу визначається не стільки його поширеністю, скільки тяжкістю наслідків: впливаючи на обмінні процеси, він може призводити до розвитку тяжких змін у багатьох системах організму (серцево–судинній, нервовій, репродуктивній тощо).
На сьогодні існують три підходи до лікування ДТЗ: консервативний, оперативний та радіологічний (при цьому жодний не є етіотропним). Мета лікування — досягнення стійкого еутиреозу або гіпотиреозу. Вибір методу лікування залежить від причини та тяжкості захворювання, розміру і розміщення зоба, наявності ендокринної офтальмопатії та супутньої патології, практики, що склалася в різних країнах, а також геофізичних особливостей місцевості (вміст йоду в їжі та воді), віку хворого і його побажань [4, 12].
У США основним методом лікування хворих віком понад 25 років залишається застосування радіоактивного йоду з подальшою замісною терапією препаратами тиреоїдних гормонів. В Європі при вперше виявленому неускладненому ДТЗ зазвичай призначають тиреостатики. В Україні дотримуються європейського підходу до лікування ДТЗ, альтернативною тиреостатикам зазвичай вважають операцію, радіоактивний йод використовується ще рідше, ніж у Європі.
Метою першого етапу лікування завжди залишається досягнення еутиреозу — нормалізації функціонального стану ЩЗ за допомогою тиреостатиків. Надалі (через 6–8 тижнів) медикаментозну терапію використовують як самостійний метод лікування, скерований на тривале підтримання еутиреоїдного стану й досягнення імунологічної ремісії. Консервативна терапія використовується також для підготовки до хірургічного лікування чи терапії радіоактивним йодом. Тиреостатична терапія, тобто базове тривале призначення препаратів, що блокують функцію ЩЗ (тиреостатиків), необхідна лише у тих випадках, коли захворювання розвинулося внаслідок ДТЗ, багатовузлового токсичного зоба, токсичної аденоми або йодіндукованого тиреотоксикозу.
Засобами патогенетичної терапії тиреотоксикозу, що пригнічують внутрішньотиреоїдний гормоногенез і блокують синтез тиреоїдстимулюючих антитіл, є похідні тіосечовини — карбімазол/тіамазол і пропілтіоурацил. У США традиційно віддають перевагу пропілтіоурацилу, в Європі — карбімазолу/тіамазолу. Клінічний ефект препаратів подібний, однак недоліком пропілтіоурацилу є необхідність частішого вживання (через кожні 6 годин), і, що найважливіше, стійкої ремісії на тлі лікування пропілтіоурацилом вдається досягти приблизно у 10 разів рідше, ніж при терапії тіамазолом. На другому етапі після досягнення клінічного еутиреозу дозу препаратів поступово (впродовж 3–4 тижнів) знижують по 1 табл. на тиждень до підтримуючої — 10 мг/добу (2 табл.) карбімазолу/тіамазолу. Підтримуючу терапію продовжують до 12–18 місяців без перерви [7].
Більшість пацієнтів добре переносять тиреостатичні препарати. В 1–5 % випадків розвиваються алергічні реакції у вигляді шкірного висипання, сверблячки, болю в суглобах, нудоти. У багатьох випадках вони зникають самостійно. При ДТЗ і без лікування відзначається лейкопенія. Побічним ефектом тиреостатиків є пригнічення кістковомозкової функції (в 0,2–0,5 % випадків), що може призвести до агранулоцитозу [11].
На сьогодні в Україні в практиці лікування тиреотоксикозу використовується новий антитиреоїдний препарат ЕСПА–КАРБ (карбімазол). Цей антитиреоїдний засіб належить до сірковмісних похідних імідазолу. Препарати групи тіонамідів, до яких належать карбімазол, тіамазол, пропілтіоурацил, вже понад 50 років широко використовуються у всьому світі для лікування гіпертиреозу. У той же час у Великобританії, Німеччині, Австрії, Франції, Австралії і Новій Зеландії перевагу віддають саме карбімазолу [9]. У США, Канаді, Японії використовують тіамазол, хоча в переважній більшості випадків для лікування ДТЗ застосовують радіоактивний йод.
Що стосується клінічних аспектів застосування карбімазолу, слід згадати дані Кокранівського огляду [7], які свідчать, що саме карбімазол показав сприятливіший профіль безпеки, тобто меншу частоту побічних ефектів. Карбімазол після абсорбції в шлунково-кишковому тракті конвертується в активну форму тіамазолу, після чого справляє відповідний терапевтичний ефект. Більшість хворих добре переносять карбімазол. В 1–7 % випадків можуть розвинутися алергічні реакції у вигляді шкірного висипання тощо. Для порівняння: частота виникнення висипання при застосуванні тіамазолу становила, за даними Кокранівського огляду, 11 %.
У прогностичному плані велике значення має визначення титру антитіл до рецептора ТТГ, підвищений рівень нерідко свідчить про необхідність хірургічного лікування [8, 10].
Отже, основними препаратами для лікування гіпертиреозу залишаються тіонаміди. В Україні лікарі-ендокринологи відтепер мають можливість використовувати і карбімазол для корекції гіпертиреозу.
Мета дослідження — оцінка спектра дії, терапевтичної ефективності й переносимості карбімазолу (препарат ЕСПА-КАРБ) порівняно з тіамазолом (препарат Мерказоліл-Здоров’я) у пацієнтів із гіпертиреозом.
Матеріали й методи дослідження
У дослідження, проведене в Українському науково-практичному центрі ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, було включено 55 пацієнтів віком від 23 до 68 років з уперше виявленим тиреотоксикозом, час спостереження становив 6 місяців. Критеріями включення були тиреотоксикоз унаслідок ДТЗ або вузлового токсичного зоба. Критеріями виключення були рак ЩЗ, інфаркт міокарда та інші серцево-судинні захворювання в анамнезі (ревматична хвороба серця, кардіоміопатія, вади серця), стани, що супроводжуються тиреотоксикозом без гіпертиреоїдизму або з низьким поглинанням радіоактивного йоду (підгострий тиреоїдит, ятрогенний тиреотоксикоз у результаті надмірного прийому препаратів тиреоїдних гормонів).
Діагноз ДТЗ встановлювали на підставі клінічних даних, ультразвукового дослідження (УЗД) ЩЗ, дослідження рівнів ТТГ, вільного тироксину (вТ4) і вільного трийодтироніну (вТ3). Референсні значення вТ4 становили 10–22 нмоль/л і вТ3 — 1,9–5,7 нмоль/л. Визначали рівні антитіл до рецептора ТТГ методом ІФА на автоматичному аналізаторі Personal Lab фірми Adaltis із використанням реагентів Medizym T.R.A. MEDIPAN GmbH. Значення < 1,5 МО/л розцінювалися як негативний результат, показники від 1,5 до 1,75 МО/л розглядалися як проміжні, > 1,75 МО/л — як позитивний результат.
55 хворих було розподілено на дві групи. Перша група (n = 30) отримувала карбімазол (препарат ЕСПА-КАРБ), друга група (n = 25) — тіамазол (препарат Мерказоліл-Здоров’я). Групи хворих не відрізнялися за віком, статтю, розмірами ЩЗ, причинами (ДТЗ і вузловий токсичний зоб) і тривалістю тиреотоксикозу. Розподіл хворих за віком і статтю наведений у табл. 1.
Групи хворих також були порівнянними за показниками ТТГ і гормонів ЩЗ на момент виявлення тиреотоксикозу (табл. 2).
Хворим на ДТЗ було призначено лікування згідно з міжнародними рекомендаціями, а також відповідно до «Клінічних протоколів діагностики та лікування ендокринних захворювань Українського НПЦ ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України» (2011). Повторне дослідження здійснювали через 1, 3 і 6 місяців.
Моніторинг хворих у процесі лікування здійснювали так: контроль рівня вТ4 і вТ3 — щомісячно, контроль рівня ТТГ — 1 раз на 3 місяці, УЗД ЩЗ — 1 раз на 4–6 місяців. Крім того, проводили загальний аналіз крові (з визначенням лейкоцитів і тромбоцитів) щотижнево протягом першого місяця тиреостатичної терапії, далі — 1 раз на місяць при переході на підтримуючі дози. Критерієм ефективності лікування є рівень ТТГ (стратегічний маркер функціонального стану ЩЗ) у крові, який при адекватній терапії досягає нормальних величин у більшості випадків через 6–12 місяців.
Успішність терапії також оцінювали за швидкістю досягнення нормалізації вмісту гормонів ЩЗ (вТ4 і вТ3), ТТГ, а також зменшення титру антитіл до рецептора ТТГ. Вірогідність рецидиву тиреотоксикозу в майбутньому оцінювали саме за останнім показником. Якщо після консервативного лікування впродовж шести місяців титр антитіл до рецептора ТТГ залишається високим, це вказує на значний ризик рецидиву тиретоксикозу. Якщо протягом першого місяця спостерігається нормалізація гормонів ЩЗ, це свідчить про адекватність дози тиреостатичної терапії. Через один місяць лікування визначення ТТГ не проводять, оскільки його зміни відбуваються більш повільно.
Статистичний аналіз проведений методами параметричної статистики з використанням t-критерію Стьюдента з визначенням показника вірогідності (р).
Результати дослідження та їх обговорення
Загалом у всіх пацієнтів із ДТЗ відзначалося поліпшення структури тканини ЩЗ (за даними УЗД), що проявлялося зменшенням вогнищевих змін.
У той же час проведений аналіз отриманих даних свідчить про те, що в першій групі хворих на ДТЗ (із призначенням препарату ЕСПА-КАРБ) відзначається більш суттєвий ефект від лікування порівняно з хворими другої групи.
Так, середній об’єм ЩЗ вірогідно зменшився лише в першій групі. У середньому тиреоїдний об’єм зменшився з 37,2 ± 3,1 см3 до 29,3 ± 2,9 см3 (р < 0,05). У другій групі спостерігалася тенденція до зменшення, але без статистичної вірогідності (з 36,4 ± 3,9 см3 до 32,4 ± 2,8 см3 (р > 0,05) (рис. 1).
У пацієнтів першої групи з ДТЗ спостерігалося вірогідне збільшення рівня ТТГ (із 0,027 ± 0,009 мМО/л до 0,37 ± 0,16 мМО/л; р < 0,05) і вірогідне зменшення рівнів вТ4 (із 29,3 ± 2,3 до 18,4 ± 1,8 нмоль/л; р < 0,05) і вТ3 (із 7,8 ± 1,6 нмоль/л до 3,2 ± 1,1 нмоль/л; р < 0,05). При цьому підвищення показника ТТГ у хворих другої групи не досягло рівня статистичної значущості (р > 0,05). Рівень ТТГ збільшився з 0,034 ± 0,008 мМО/л до 0,11 ± 0,09 мМО/л (р > 0,05). У той же час у хворих другої групи відзначалося вірогідне зменшення рівнів вТ4 (із 31,4 ± 2,1 нмоль/л до 21,7 ± 1,8 нмоль/л; р < 0,05) і вТ3 (із 8,2 ± 1,4 до 3,7 ± 1,2 нмоль/л; р < 0,05) (рис. 2, 3).
Особливої уваги заслуговують отримані результати стосовно зниження автоімунної агресії, що проявлялося зниженням концентрації антитіл до рТТГ. У хворих групи карбімазолу зниження цього показника набуло рівня статистичної значущості (рис. 4). Загалом по групі вміст антитіл до рТТГ зменшився з 9,6 ± 1,2 МО/л до 3,8 ± 0,8 МО/л (р < 0,05). У другій групі спостерігалася тенденція до зменшення концентрації антитіл до рТТГ (з 10,1 ± 1,6 МО/л до 7,1 ± 1,6 МО/л; р > 0,05).
Якщо середня добова доза препаратів ЕСПА–КАРБ і Мерказоліл–Здоров’я на початку лікування в обстежених групах хворих не відрізнялася, то через 6 місяців лікування середня доза карбімазолу в першій групі становила 15,8 ± 1,7 мг, а в другій групі доза тіамазолу — 19,2 ± 2,1 мг (р > 0,05).
Побічних явищ при лікуванні хворих обох груп упродовж шести місяців не спостерігалося.
Нормалізація вмісту периферичних гормонів (вТ4 і вТ3) через 90 днів спостереження досягнута в 96,2 % хворих першої групи і в 74,1 % — другої групи (рис. 5).
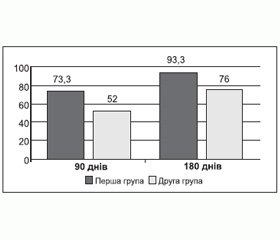
Число хворих, які досягнули нормального рівня ТТГ, вірогідно вищим було в першій групі — групі карбімазолу (93,3 проти 76 %) (рис. 6).
При оцінці ефективності терапії використання препарату ЕСПА-КАРБ в першій групі мало перевагу над призначенням Мерказолілу-Здоров’я в другій групі як за швидкістю досягнення компенсації тиреотоксикозу (через 90 днів лікування нормалізація вТ4 у пацієнтів першої групи — в 96 %, другої — в 74 %; через 180 днів спостереження нормалізація ТТГ — у 98 і 54 % відповідно), так і за рівнем зниження автоімунної агресії, про що свідчить вірогідне зниження рівня антитіл до рТТГ у групі карбімазолу з 9,6 ± 1,2 МО/л до 3,8 ± 0,8 МО/л (р < 0,05). Через 180 днів лікування пацієнти другої групи, які отримували Мерказоліл-Здоров’я без досягнення нормалізації ТТГ, були переведені на ЕСПА-КАРБ.
Висновки
1. Встановлена більша ефективність карбімазолу порівняно з тіамазолом, що проявилося швидшим досягненням клінічного ефекту та компенсації тиреотоксикозу, вірогідним зменшенням тиреоїдного об’єму, рівнем антитіл до рецептора ТТГ.
2. Використання карбімазолу сприяє зменшенню добової дози тиреостатичних препаратів у хворих на ДТЗ, що знижує ризик виникнення ускладнень терапії.
3. При використанні карбімазолу протягом шести місяців у хворих на ДТЗ не було зареєстровано випадків непереносимості або будь-яких побічних ефектів.
1. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Фундаментальная и клиническая тиреоидология: Руководство. — М.: Медицина, 2007. — 816 с.
2. Болезнь Грейвса и эндокринная офтальмопатия / Н.Ю. Сириденко, И.М. Беловалова, М.С. Шеремета [и др.]; под ред И.И. Дедова, Г.А. Мельниченко. — М.: МАИ-Принт, 2012. — 143 с.
3. Кравчун Н.А. Гипертиреоз: клиника, диагностика, терапия // Острые и неотложные состояния в пракатике врача. — 2013. — № 6. — С. 3–6.
4. Мкртумян А.М. Заболевания щитовидной железы. Рук-во для врачей / А.М. Мкртумян, С.В. Подачина, Н.А. Петунина. — М.: Медфорум, 2012. — 128 с.
5. Паньків В.І. Практична тиреоїдологія. — Донецьк: Видавець Заславський О.Ю., 2011. — 224 с.
6. Панькив В.И. Тиреостатические препараты в терапии диффузного токсического зоба / В.И. Панькив // Міжнародний ендокринологічний журнал. — 2013. — № 3(51). — С. 1–7.
7. Antithyroid drug regimen for treating Graves’ hyperthyroidism (Review) / P. Abraham, A. Avenell, S.C. McGeoch [et al.] // The Cochrane Library. — 2010. — Issue 1.
8. Bahn R.S., Burch H.B., Cooper D.S. et al.; American Thyroid Association; American Association of Clinical Endocrinologists. Hyperthyroidism and other causes of thyrotoxicosis: management guidelines of the American Thyroid Association and American Association of Clinical Endocrinologists. // Thyroid. — 2011. — Vol. 21(6). — P. 593–646. doi: 10.1089/thy.2010.0417.
9. Clinical Management of Thyroid Disease / Ed. by F.E. Wondisford, S. Radovick. — Baltimore, Maryland; John Hopkins University School of Medicine, 2009. — 860 p.
10. Mandel S.J., Larsen P.R., Davies T.F. Thyrotoxicosis // Melmed S., Polonsky K.S., Larsen P.R., Kronenberg H.M. Williams Textbook of Endocrinology. — 12th ed. — Philadelphia, Pa.: Elsevier Saunders, 2011. — Сhap. 12.
11. Pearce E.N. Risk for cardiovascular hospitalization is higher in patients with hyperthyroidism than in controls, and risk remains elevated long after thyroidectomy // Clinical Thyroidology. — 2014. — Vol. 26(6). — P. 155–156. doi:10.1089/ct.2014;26.155–156.
12. Reid J.R. Hyperthyroidism: diagnosis and treatment / J.R. Reid, S.F. Wheeler // Am. Fam. Physician. — 2005. — Vol. 72(4). — P. 623–630.

/45/45.jpg)
/46/46.jpg)
/47/47.jpg)