Журнал «Здоровье ребенка» 5 (56) 2014
Вернуться к номеру
Ефективність застосування Лаферобіону в дітей із рецидивуючим бронхообструктивним синдромом, які часто хворіють на гострі респіраторні захворювання
Авторы: Юрцева А.П., Фофанова О.В., Осадець Н.Б., Боднар О.П. - Івано-Франківський національний медичний університет
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
У статті викладені результати вивчення ефективності застосування Лаферобіону в дітей із бронхообструктивним синдромом, які часто хворіють на гострі респіраторні захворювання (ГРЗ). Установлено, що включення Лаферобіону в комплекс лікування і профілактики в цієї групи дітей сприяє зменшенню частоти ГРЗ у 2,6 раза, зниженню частоти нападів бронхообструкції на тлі ГРЗ у 2,8 раза, зменшенню тривалості бронхообструкції. Під впливом лікування Лаферобіоном спостерігається тенденція до нормалізації показників імунітету, підвищення вмісту інтерферону гамма та зниження концентрації інтерлейкіну-4, відбувається активація антиоксидантного захисту.
В статье изложены результаты изучения эффективности применения Лаферобиона у детей с бронхиальной астмой, часто болеющих острыми респираторными заболеваниями (ОРЗ). Установлено, что включение Лаферобиона в комплекс лечения и профилактики в этой группе детей способствует снижению частоты ОРЗ в 2,6 раза, снижению частоты приступов бронхообструкции на фоне ОРЗ в 2,8 раза, уменьшению продолжительности бронхообструкции. Под влиянием лечения Лаферобионом наблюдается тенденция к нормализации показателей иммунитета, повышению содержания интерферона гамма и снижению концентрации интерлейкина-4, происходит активация антиоксидантной защиты.
The paper presents the results of the study on the efficacy of Laferobionum application in children with bronchial asthma, who often suffer from acute respiratory diseases (ARD). It is found that the inclusion of Laferobionum in complex of treatment and prevention in this group of children helps to reduce the incidence of ARD by 2.6 times, to reduce the incidence of bronchial obstruction episodes on the background of ARD by 2.8 times, to decrease the duration of bronchial obstruction. Under the influence of treatment with Laferobionum we have noted a tendency towards normalization of immunity parameters, increase in the content of interferon gamma, and decrease in the concentration of interleukin-4, the activation of antioxidant protection.
діти, бронхообструктивний синдром, рекомбінантний α-2b-інтерферон, імунітет, лікування.
дети, бронхообструктивный синдром, рекомбинантный интерферон α-2b, иммунитет, эффективность лечения.
children, bronchoobstructive syndrome, recombinant interferon α-2b, immunity, efficacy of treatment.
Статья опубликована на с. 21-26
Вступ
Незважаючи на досягнення сучасної медицини, гострі респіраторні захворювання (ГРЗ) займають перше місце серед усіх захворювань у світі. Особливо сприйнятливі до ГРЗ діти в перші роки життя, що обумовлено відсутністю попереднього контакту з інфекційними агентами і відсутністю у зв’язку з цим банку імунологічної пам’яті [1, 4]. В той же час у дітей перших років життя відзначається не тільки найвища частота виникнення ГРЗ, але тяжчий їх перебіг. Так, у цій віковій групі ГРЗ нерідко супроводжуються розвитком бронхообструктивного синдрому (БОС). За даними різних авторів, частота розвитку БОС на тлі ГРЗ у дітей становить від 5 до 40 % [3, 12, 13].
Розвитку бронхіальної обструкції в дітей із частими ГРЗ значною мірою сприяють анатомо-фізіологічні особливості організму. Серед них важливе місце займають особливості дихального тракту: переважання бронхів дрібного калібру, схильність до набряку їх слизової оболонки, гіперсекреції і зміни в’язкоеластичних властивостей мокротиння, а також особливості реагування імунної системи: Th2-спрямованість імунної відповіді, зниження здатності до інтерфероногенезу, зменшення продукції імуноглобулінів класів A і G, а також незрілість Т- і В-лімфоцитів [3, 4, 6]. Як свідчать численні дослідження, найбільш етіологічно значимими вірусами, що беруть участь у розвитку БОС, є респіраторно-синцитіальний вірус, риновірус, аденовірус, вірус парагрипу 3-го типу, дещо рідше — віруси грипу, ентеровірус, коронавірус. Персистуючий перебіг цитомегаловірусної герпетичної інфекції в дітей перших трьох років життя також може обумовлювати розвиток бронхообструкції [5, 10, 14, 16]. Є переконливі докази ролі мікоплазмової і хламідійної інфекції в розвитку БОС [12, 14, 16]. Останнім часом з’явилися дані про нові респіраторні віруси, що сприяють розвитку БОС. Отримані докази участі в розвитку БОС у дітей перших років життя нових інфекційних чинників — метапневмовірусу й бокавірусу [1, 12].
Патогенна дія респіраторних вірусів зумовлена ушкодженням миготливого епітелію слизової оболонки респіраторного тракту, що призводить до розвитку запалення дихальних шляхів. Саме запалення є важливим чинником бронхіальної обструкції в дітей раннього віку. В результаті ушкоджуючої дії інфекційних агентів запускається каскад імунологічних реакцій, які індукують виділення в кровоток медіаторів запалення, посилюється проникність судин, з’являється набряк слизової оболонки бронхів, гіперсекреція в’язкого слизу. У результаті цього розвивається гіперреактивність бронхів і бронхоспазм. Багатьма дослідженнями доведено взаємозв’язок між сезонним підвищенням захворюваності на ГРЗ і частотою госпіталізацій з приводу нападу БОС [3, 8, 11, 14].
Інфекційний процес може стати тригером нападу бронхоспазму, а збудник — причинно-значимим алергеном [3, 14]. Рецидивуючі респіраторні інфекції в дітей сприяють гіперпродукції IgE, зниженню синтезу інтерферону (ІФН), посиленню реакцій гіперчутливості як сповільненого, так і негайного типу у відповідь на алергенну стимуляцію, розвитку гіперреактивності бронхів і сенсибілізації організму до неінфекційних алергенів. Пацієнти, які часто хворіють на ГРЗ, схильні до рецидивування БОС, у них відзначається зниження противірусного і протимікробного захисту, що певною мірою обумовлено наявністю дизрегуляторних порушень в системі інтерферону [4, 6, 10, 11, 16].
Інтерферони — найважливіші чинники вродженого імунітету; вважають, що це перша лінія протиінфекційного захисту [4, 7, 9, 10]. Особливе місце ІФН в антиінфекційній резистентності зумовлено тим, що індукція їх синтезу, передусім натуральними кілерами, клітинами моноцитарного ряду, а також дендритними клітинами передує формуванню специфічних імунних реакцій [4, 5, 9, 10]. Із позицій сьогоднішнього дня можна стверджувати, що основною функцією ІФН в організмі є активація специфічних клітинних реакцій імунітету та регуляція імунної відповіді [10–12]. Ці ефекти здійснюються через модуляцію активності NK-клітин, посилення експресії Fc-рецепторів до IgG на мембранах макрофагів під дією ІФН-а, зниження активності Т-лімфоцитів-супресорів під дією ІФН-а, підвищення активності Т-лімфоцитів під дією ІФН-а. Однією з важливих імунорегуляторних функцій ІФН є вплив на чутливість факторів імунної системи до цитокінів [9, 11].
Для лікування і профілактики ГРЗ/гострих респіраторних вірусних інфекцій (ГРВІ) в останні роки все частіше застосовуються інтерферони та індуктори ендогенного інтерферону. При цьому в педіатричній практиці найбільшої уваги заслуговує вітчизняний рекомбінантний а-2b-інтерферон (ІФН-а-2b) Лаферобіон («Біофарма», Україна), що має також і антиоксидантний ефект за рахунок вітамінів С і Е, які входять до його складу [5, 7, 9]. Найбільший терапевтичний ефект від препаратів інтерферону при лікуванні ГРЗ досягається в тих випадках, коли етіологія має вірусну або вірусно-бактеріальну природу, а лікування починається з перших годин захворювання [4, 6, 7, 9]. Рекомбінантний а-2b-інтерферон захищає клітини від ушкодження, активізує імунну систему, має антиоксидантну активність. Крім того, рекомбінантний ІФН-а-2b чинить не лише строго спрямований імунозамісний, а й досить широкий імуномодулюючий і протективний ефект. Цей метод лікування за сучасною класифікацією є неспецифічною активно-пасивною імуностимулюючою терапією, основною метою якої є активація імунної системи і посилення загального імунітету хворого [4, 6, 7]. Дані досліджень останніх років свідчать, що включення рекомбінантного ІФН-а-2b в комплексну терапію та профілактику ГРЗ дозволяє не тільки істотно зменшити вираженість запальних процесів і тривалість захворювання, а й знижує в цілому ризик розвитку ускладнень.
Мета нашого дослідження — визначити ефективність включення рекомбінантного а-2b-інтерферону Лаферобіону в комплексну терапію і профілактику бронхообструктивного синдрому в детей, які часто хворіють на ГРЗ/ГРВІ.
Матеріали і методи дослідження
Під спостереженням були 64 дитини віком 5–15 років із повторним БОС, які згідно з критеріями В.Ю. Альбицького та А.А. Баранова (1983) належали до групи часто хворіючих дітей, тобто хворіли 4–6 разів протягом року. Обстежені діти були розподілені на 2 групи, із них основну групу становили 34 дитини, яким до базисної терапії включали Лаферобіон у формі супозиторіїв, у групу порівняння ввійшли 30 дітей, які отримували лише базисну й симптоматичну терапію. Терапія призначалась дітям під час госпіталізації. Обидві групи були порівнянними за віком і статтю. Контрольну групу становили 20 дітей того ж віку. Усім хворим проведені загальне клініко-лабораторне обстеження, збір алергоанамнезу, інструментальні дослідження (функція зовнішнього дихання, ЕКГ), шкірне алерготестування (prick-тест) із стандартними наборами алергенів виробництва МП «Імунолог» (м. Вінниця, Україна). Алергодіагностику in vitro з широким спектром алергенів проводили за допомогою множинного алергосорбентного хемілюмінесцентного тесту (MAST CLA, Hitachi Chemical Diagnostics), що полягає у напівкількісному визначенні in vitro концентрації алерген-специфічних IgE. Визначення загального IgE проводили методом імуноферментного аналізу з набором реактивів ЗАТ «Вектор-Бест» (Росія). Стан перекисного окислення ліпідів (ПОЛ) у дітей, хворих на бронхіальну астму, оцінювали за вмістом первинних їх продуктів — дієнових кон’югат (ДК) та вторинних — тіобарбітурово-кислотних активних продуктів (ТБК-АП) за методикою Т.Н. Федорової і співавт. (1983). Антиоксидантний захист (АОЗ) визначали за активністю церулоплазміну (АЦП), глутатіонпероксидази (ГП) та глутатіонредуктази (ГР) за спектрофотометричною методикою. Статистичний аналіз отриманих результатів дослідження проведено за допомогою програмного забезпечення AtteStat Microsoft Excel 2007. Застосовували методи описової статистики з оцінкою середнього значення показників, величини середньої стандартної похибки, t-критерію Стьюдента. Вірогідність переваги однієї ознаки над іншою оцінювали за допомогою відношення шансів (ВШ) та їх довірчих інтервалів (ДІ).
Результати дослідження
Серед обстежених дітей переважали хлопчики (62,5 %), дівчатка становили 37,5 %. При вивченні перинатального анамнезу обстежених дітей звертає на себе увагу висока частота патологічного перебігу вагітності і пологів матерів в обстежених дітей. Так, у 57,8 % матерів дітей із БОС, які часто хворіють на ГРЗ, відмічено патологічний перебіг вагітності, у 37,5 % із них — патологічні пологи. У 20,3 % дітей установлена асфіксія в пологах. Ознаки перинатального ураження ЦНС в анамнезі встановлені у 28,1 % дітей із БОС, які часто хворіють на ГРЗ, що, на думку деяких авторів, є одним із факторів, що призводять до розвитку бронхообструкції та поліалергії [3, 6].
На винятково грудному вигодовуванні перебували 23,4 + 4,5 % обстежених дітей, на штучному та змішаному — 76,6+5,5 %. Зокрема, звертає на себе увагу значна частота раннього штучного вигодовування в дітей із БОС і частими ГРЗ, що у 2 рази вища, ніж серед здорових дітей. Так, 31,3 % обстежених дітей не одержували грудного молока після 2 місяців, а вигодовувалися сумішами з коров’ячого молока, антигенні властивості якого широко відомі. У 29 хворих (45,3 %) обтяжений сімейний анамнез щодо атопії, а в 36 (56,3 %) були прояви атопії в анамнезі переважно за рахунок атопічного дерматиту та харчової алергії.
При дослідженні показників системного імунітету в дітей, які часто хворіють на ГРЗ, ускладнені БОС, установлено, що в переважної більшості з них спостерігається дизімуноглобулінемія — значний уміст загального IgЕ, зниження — IgА та ІgМ при нормальному показнику IgG.
Уміст загального IgE в сироватці крові в дітей із частими ГРЗ і повторним БОС становив 212,81 ± 18,56 МО/мл (у здорових дітей — 34,21 ± 2,37 МО/мл, Р < 0,001). Відмічені значні коливання вмісту загального IgE в дітей із ГРЗ — від 28,89 до 450,56 МО/мл. Найвищі показники були в дітей з атопією в анамнезі. Звертає на себе увагу виражене порушення клітинної ланки імунітету в дітей, які часто хворіють на ГРЗ/ГРВІ. Щодо показників клітинного імунітету, то характерним є зниження числа Т-лімфоцитів (48,7 ± 2,1 %) порівняно із здоровими дітьми (63,4 ± 3,9 %, Р < 0,001) переважно за рахунок зменшення майже вдвічі субпопуляції CD4+ (22,4 ± 1,74 %; у дітей контрольної групи — 43,6 ± 1,9 %) та зниження у зв’язку з цим імунорегуляторного індексу (CD4+/CD8+) до 0,85 ± 0,04 (у дітей контрольної групи — 1,85 ± 0,09; Р < 0,001). Установлено також, що в обстежених дітей із частими ГРЗ у гострому періоді хвороби спостерігається зниження вмісту ІФН-a у 2,5 раза (135,0 ± 11,4 пг/мл) порівняно зі здоровими дітьми (337,4 ± 13,9 пг/мл) та вірогідне підвищення вмісту інтерлейкіну-4 (IL-4) до 15,6 ± 2,5 пг/мл проти 7,2 ± 1,28 пг/мл у здорових дітей (Р < 0,001). Слід звернути увагу на роль порушень вмісту ІФН-a та IL-4 у розвитку як частих ГРЗ, так і повторного БОС. Клітинами — продуцентами ІФН-a є Т-лімфоцити. Основна функція ІФН-a — це імунорегуляція (активація макрофагів, посилення Th1-відповіді, індукція експресії антигенів головного комплексу гістосумісності типу II на антигенпрезентуючих клітинах та ін.) [4, 5]. Як і інші інтерферони, він проявляє противірусну й антипроліферативну активність. В останні роки доведена його здатність пригнічувати продукцію IgE клітинами, що стимульовані IL-4 — одним з основних індукторів гіперпродукції IgE [4, 5].
Дослідження вмісту первинних та вторинних продуктів ПОЛ (ДК та ТБК-АП) у дітей із вірус-індукованим ГРЗ показало, що в нападному періоді у більшості з них відбувається інтенсифікація вільнорадикальних процесів. При цьому вміст ДК та ТБК-АП підвищувався більше ніж удвічі. Процесам гіперпероксидації ліпідів відводиться важлива роль у патогенезі запальних захворювань різної локалізації, бо саме ці процеси мають вирішальне значення у розвитку порушення стабільності біологічних мембран [2, 12, 13]. Відмічено, що тяжкість перебігу запального процесу і його перехід в хронічну форму збігається з наростанням концентрації в крові продуктів ПОЛ. Неконтрольована активація ПОЛ є особливо небезпечною для дітей, механізми антиоксидантного захисту у яких недосконалі. Уважають, що вільні радикали, які надлишково утворюються за рахунок оксидативного стресу в дихальних шляхах при ГРВІ, можуть брати участь у розвитку бронхоспазму при загостренні ГРЗ [7, 16].
Для оцінки АОЗ досліджували активність ферментів глутатіонового блоку (глутатіонпероксидази і глутатіонредуктази), які є найважливішими елементами антиоксидантної системи, а також мідьумісного антиоксидантного ферменту церулоплазміну. Захисна роль цих ферментів при оксидативному стресі полягає в тому, що глутатіонпероксидаза переносить водень на окислений глутатіон, а глутатіонредуктаза знімає цей водень і передає його на Н2О2, унаслідок чого утворюються дві молекули води.
Ознаками порушення механізмів АОЗ у дітей із частими ГРЗ є вірогідне зниження активності глутатіонпероксидази та глутатіонредуктази порівняно з показниками у здорових дітей. Щодо церулоплазміну відмічено, що його активність у 2,5 раза вища (58,12 ± 2,22 ум.од.), ніж у здорових дітей (23,76 ± 0,39, Р < 0,001). Трактування змін активності цього ферменту є неоднозначним. Можна розглядати підвищення активності ЦП у гострому періоді ГРЗ/ГРВІ як один із компенсаторних механізмів АОЗ. Церулоплазмін є головним позаклітинним антиоксидантом крові, що інгібує ПОЛ, діючи як антиоксидант-перехоплювач у вогнищах запалення, де фагоцитуючі клітини виділяють масу активних форм кисню [1, 2]. Однак, беручи до уваги, що ЦП відіграє важливу роль як інтерлейкін-6-залежний реактант гострофазових реакцій крові, то слід, очевидно, трактувати підвищення його активності і як ознаку інфекційного запального процесу. Так, відомо, що рівень ЦП у сироватці крові значно підвищується при різних інфекційних захворюваннях; гострому та хронічному запальних процесах, що супроводжуються деструктивними й некротичними змінами в тканинах [1, 2].
Лаферобіон призначали в дозі 500 000 МО дітям від 5 до 7 років, 1 000 000 МО дітям від 7 до 15 років (по 1 супозиторію) двічі на добу. В осінній період під час сезонного підвищення захворюваності на ГРЗ дітям, які часто хворіють і які мали в анамнезі епізоди БОС, із профілактичною метою призначали 1–2 курси Лаферобіону в тій же дозі. Перевагами призначення Лаферобіону в супозиторіях є зручність у використанні, добре всмоктування, висока концентрація і пролонгований ефект. До того ж слід відмітити, що діти добре переносять лікування саме такими лікарськими формами.
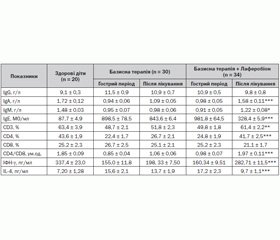
При порівняльній оцінці показників імунного статусу в динаміці хвороби в дітей із ГРЗ, ускладненими БОС, під впливом лікування Лаферобіоном установлено позитивну динаміку більшості досліджених параметрів імунітету (табл. 1).
І хоча повної нормалізації деяких із них не спостерігалося, простежувалися вірогідна тенденція до відновлення показників Т-клітинного імунітету, суттєвe підвищення концентрації ІФН-a, зниження загального вмісту IgE та IL-4. Отже, застосування Лаферобіону сприяє модуляції імунної відповіді за клітинним і гуморальним типами.
Завдяки вітамінам С і Е, що входять до складу Лаферобіону, та його протизапальній дії відбувається відновлення метаболічного забезпечення структурно-функціонального стану клітинних мембран [8, 11, 14]. Відзначаються позитивні зрушення в системі АОЗ — тенденція до нормалізації активності ферментів глутатіонового блоку (ГП, ГР), що призводить до зменшення інтенсивності процесів ПОЛ (табл. 2). В групі дітей, які не отримували рекомбінантний a-2b-інтерферон, вірогідної різниці показників у гострому періоді хвороби й після лікування не було. Зниження активності церулоплазміну після лікування в динаміці хвороби в дітей, які отримували Лаферобіон, може свідчити про зменшення ознак запального процесу. У дітей групи порівняння зниження його активності після лікування було невірогідним.
Клінічне спостереження за дітьми, які отримували Лаферобіон, проводилося впродовж 6 місяців і включало оцінку частоти й тяжкості загострень бронхообструкції, частоту ГРЗ/ГРВІ. Катамнестичне спостереження виявило протективний ефект рекомбінантного ІФН-a-2b Лаферобіону у дітей із частими ГРЗ та БОС, його застосування сприяє зниженню частоти ГРЗ у 2,6 раза, зменшенню частоти БОС — у 2,8 раза. Про ефективність і перевагу включення Лаферобіону в комплекс лікування у дітей із частими ГРЗ порівняно з традиційними методами базисної терапії свідчить і високий показник відношення шансів і довірчих інтервалів (ВШ 9,3333; ДІ 2,9157–29,8761) та висока вірогідність за критериєм x2 (Р < 0,00019).
Запропонований спосіб лікування Лаферобіоном часто хворіючих на ГРЗ/ГРВІ дітей у поєднанні з БОС слід вважати ефективним, оскільки препарат блокує реплікацію вірусів, каскад імунологічних і біохімічних реакцій, що лежать в основі інфекційного й алергічного запалення. Під впливом профілактичного застосування Лаферобіону знижується частота ГРЗ та рецидивів бронхообструкції. Він є безпечним, добре переноситься хворими і не призводить до розвитку побічних ефектів.
Висновки
1. Застосування Лаферобіону в дітей, які часто хворіють на ГРЗ, ускладнені БОС, сприяє модуляції імунної відповіді за клітинною і гуморальною ланками, під його впливом підвищується вміст ІФН-y та IL-4, знижується концентрація загального IgE.
2. Під впливом лікування Лаферобіоном відзначаються зменшення інтенсивності процесів ПОЛ та позитивна динаміка показників антиоксидантного захисту. Свідченням цього є зниження вмісту продуктів перекисного окислення ліпідів (ТБК-АП, ДК) та тенденція до нормалізації активності антиоксидантних ферментів глутатіонового блоку (глутатіонредуктази і глутатіонпероксидази) та церулоплазміну.
3. Профілактичне призначення Лаферобіону сприяє зниженню частоти ГРЗ та нападів бронхообструкції. Його використання є перспективним засобом як один із заходів профілактики бронхообструктивного синдрому у дітей, які часто хворіють на ГРЗ.
1. Абатуров А.Е. Роль интерферонов в противовирусной защите респираторного тракта / А.Е. Абатуров, Е.И. Юлиш // Здоровье ребенка. — 2007. — № 5(8). — С. 136-144.
2. Байкова В.Н. Особенности системы антиоксидантной защиты и ее коррекция у детей с хроническим тонзиллитом / Байкова В.Н., Карпова Е.П., Фейзуллаев Э.Ф. // Русский мед. журнал. — 2009. — Т. 17, № 4. — С. 303-308.
3. Балаболкин И.И. Современные проблемы терапии бронхиальной астмы у детей / Балаболкин И.И. // Педиатрия. — 2009. — Т. 87, № 2. — С. 6-11.
4. Зайцева О.В. Бронхиальная астма и респираторные инфекции у детей / Зайцева О.В., Зайцева С.В. // Вестник педиатрической фармакологии и нутрициологии. — 2008. — Т. 5, № 1. — С. 54-60.
5. Значение системы интерферонов в формировании иммунного ответа у детей с острыми респираторными вирусными инфекциями / Захарова И.Н., Чебуркин А.В., Малиновская В.В. [и др.] // Вопросы практической педиатрии. — 2009. — Т. 4, № 6. — С. 38-45.
6. Интерферонотерапия инфекционно-воспалительных заболеваний у детей — обзор современных исследований / Горелов А.В., Плоскирева А.А., Феклисова В.П. [и др.] // Лечащий врач. — 2012. — № 6. — С. 84-86.
7. Каганов С.Ю. Решенные и нерешенные проблемы аллергических болезней легких у детей // Российский вестник перинатологии. — 1995. — № 1. — С. 11-15.
8. Крамарьов С.О. Лікування інфекційного мононуклеозу Епштейна — Барр вірусної етіології у дітей із застосуванням рекомбінантного інтерферону a-2b ректальної форми / С.О. Крамарьов, О.В. Виговська // Современная педиатрия. — 2013. — № 2(50). — С. 30-35.
9. Модифицированная интерферонотерапия острых респираторных инфекций у детей раннего возраста: патогенетическое обоснование и эффективность / Захарова И.Н., Торшхоева Л.Б., Заплатников А.Л. [и др.] // Российский вестник перинатологии и педиатрии. — 2011. — Т. 56, № 3. — С. 49-54.
10. Мовчан О.С. Клінічні аспекти використання лаферобіону в педіатрії / О.С. Мовчан, Ю.В. Марушко // Современная педиатрия. — 2012. — № 7(47). — С. 79-83.
11. Нестерова И.В. Препараты интерферона альфа в клинической практике / И.В.Нестерова // Российский аллергологический журнал. — 2010. — № 2. — С. 43-52.
12. Осипова Л.С. Особенности клинического применения препаратов интерферона / Л.С. Осипова // Мистецтво лікування. — 2011. — № 2(78). — С. 70-73.
13. Симованьян Э.Н. Эффективность использования рекомбинантного Интерферона а2b (Виферона) при остром обструктивном бронхите у детей / Э.Н. Симованьян, Э.А. Харабаджахян, В.Б. Денисенко // Педиатрия. — 2008. — Т. 87, № 1. — С. 106-115.
14. Хаитов М.Р. Роль респираторных вирусов при бронхиальной астме / Хаитов М.Р., Царев С.В. // Русский медицинский журнал. — 2009. — Т. 17, № 2. — С. 136-140.
15. Юлиш Е.И. Противовирусная терапия в лечении острых респираторных заболеваний у детей / Юлиш Е.И. // Современная педиатрия. — 2013. — № 5(53). — С. 75-79.
16. Exacerbations of asthma and chronic obstructive pulmonary disease (COPD): focus on virus induced exacerbations / Mallia P., Contoli M., Caramori G. [et al.] // Curr. Pharm. Des. — 2007. — V. 13, № 1. — P. 73-97.
17. Mechanisms of virus-induced asthma exacerbations: state-of-the-art. A GA2 LEN and InterAirways document / Papadopoulos N.G., Xepapadaki P., Mallia P. [et al.] // Allergy. — 2007. — Vol. 62, № 5. — Р. 457-470.

/24/24.jpg)