Журнал «» 4 (36) 2014
Вернуться к номеру
Ефективність ниркової денервації в пацієнтів із резистентною гіпертензією з використанням сертифікованого обладнання (результати однорічного спостереження)
Авторы: Сіренко Ю.М., Рековець О.Л., Соколов Ю.М., Доброход А.С. - ДУ ННЦ «Інститут кардіології ім. акад. М.Д. Стражеска» НАМН України, м. Київ
Рубрики: Кардиология
Разделы: Клинические исследования
Версия для печати
Завершені контрольовані дослідження показали безпеку, але різну ефективність ниркової денервації (НДН) у хворих із резистентною артеріальною гіпертензією (АГ). Нами проведено НДН у 8 пацієнтів. Середній вік хворих становив 52,13 ± 3,88 року (40–66), середня тривалість АГ — 16,75 ± 2,17 (12–25) року. При надходженні в клініку інституту рівень артеріального тиску (АТ) становив 181,25/106,88 ± 4,3/4,0 мм рт.ст. (160–200/85–120 мм рт.ст.), ЧСС — 70,63 ± 3,03 уд/хв.
Оптимізація терапії в умовах стаціонару у цих хворих привела до достовірного зниження рівня АТ до 156,88/95,00 ± 2,98 мм рт.ст. (150–165/85–100 мм рт.ст.) та ЧСС — 68,88 ± 3,28 уд/хв. Число антигіпертензивних препаратів становило в середньому 5,5 на пацієнта. При добовому моніторуванні артеріального тиску (ДМАТ) на етапі оптимізації терапії середньодобовий систолічний АТ (САТ24) становив 149,16 ± 5,40 мм рт.ст., а діастолічний (ДАТ24) — 86,98 ± 5,08 мм рт.ст. Середньодобова частота серцевих скорочень (ЧСС24) була 70,12 ± 2,94 уд/хв. Усі пацієнти добре перенесли процедуру.
Середнє зниження середньодобового АТ (САТ/ДАТ) становило в динаміці на етапі 7 днів, 1, 6 та 12 місяців відповідно –15,73/–8,52 мм рт.ст., –11,45/–6,06 мм рт.ст., –10,70/–13,68 мм рт.ст. та
–17,91/–13,88 мм рт.ст. Величина ЧСС24 достовірно не змінилася. Зниження денних САТ/ДАТ становило в динаміці на етапах 7 днів, 1, 6 та 12 місяців –14,79/–5,64, –16,55/–5,60, –12,29/–12,79 та –20,45/–13,62 мм рт.ст. відповідно. Динаміка зниження нічних САТ/ДАТ становила на етапах 7 днів,
1 місяць, 6 місяців та 12 місяців –15,03/–8,42, –10,64/–4,57, –9,23/–12,38 та –19,39/–14,84 мм рт.ст. відповідно. При САТ24 ≥ 160 мм рт.ст. через 12 місяців після НДН спостерігалося найбільш значне зниження середньодобового АТ –30,5/–18,9 мм рт.ст. При САТ24 ≥ 140 мм рт.ст. та < 160 мм рт.ст. через 12 місяців після процедури зниження САТ24/ДАТ24 становило –20,1/–18,0 мм рт.ст. При
САТ24 < 140 мм рт.ст. достовірних змін у зниженні АТ не було. Середнє зниження офісного АТ становило в динаміці на етапах 7 днів, 1, 6 та 12 місяців відповідно –14,38/–5,63 мм рт.ст.,–9,02/–10,71 мм рт.ст., +3,12/–8 мм рт.ст. та –7,88/–5,0 мм рт.ст. Офісна ЧСС не змінилася.
Розрахунковий рівень кліренсу креатиніну, визначений за формулою Кокрофта — Гаулта, достовірно не змінився в жодного пацієнта. Таким чином, застосування процедури НДН у пацієнтів із резистентною АГ є безпечним та рекомендоване лише в пацієнтів, у яких САТ за даними ДМАТ 140 мм рт.ст. і вище. Рекомендоване обов’язкове використання ДМАТ для відбору та ефективного контролю після НДН.
Завершенные контролированные исследования показали безопасность, но разную эффективность почечной денервации (ПДН) у больных с резистентной артериальной гипертензией (АГ). Нами проведена ПДН у 8 пациентов. Средний возраст больных составил 52,13 ± 3,88 года (40–66), средняя продолжительность АГ — 16,75 ± 2,17 (12–25) года. При поступлении в клинику института уровень артериального давления (АД) составлял 181,25/106,88 ± 4,3/4,0 мм рт.ст. (160–200/85–120 мм рт.ст.), частота сердечных сокращений (ЧСС) — 70,63 ± 3,03 уд/мин. Оптимизация терапии в условиях стационара у этих больных привела к достоверному снижению уровня АД до 156,88/95,00 ± 2,98 мм рт.ст. (150–165/85–100 мм рт.ст.) и ЧСС — 68,88 ± 3,28 уд/мин. Число антигипертензивных препаратов составило в среднем 5,5 на пациента. При суточном мониторировании артериального давления (СМАД) на этапе оптимизации терапии среднесуточное систолическое АД (САД24) составило 149,16 ± 5,40 мм
рт.ст., а диастолическое (ДАД24) — 86,98 ± 5,08 мм рт.ст. Среднесуточная частота сердечных сокращений (ЧСС24) была 70,12 ± 2,94 уд/мин. Все пациенты хорошо переносили процедуру.
Среднее снижение среднесуточного АД (САД/ДАД) составило в динамике на этапе 7 дней, 1 месяц, 6 и 12 месяцев соответственно –15,73/–8,52 мм рт.ст., –11,45/–6,06 мм рт.ст., –10,70/–13,68 мм рт.ст. и –17,91/–13,88 мм рт.ст. Величина ЧСС24 достоверно не изменилась. Снижение дневных САД/ДАД составляло в динамике на этапах 7 дней, 1, 6 и 12 месяцев –14,79/–5,64, –16,55/–5,60, –12,29/–12,79 и –20,45/–13,62 мм рт.ст. соответственно. Динамика снижения ночных САД/ДАД составляла на этапах 7 дней, 1, 6 и 12 месяцев –15,03/–8,42, –10,64/–4,57, –9,23/–12,38 и –19,39/
–14,84 мм рт.ст. соответственно. При САД24 ≥ 160 мм рт.ст. через 12 месяцев после ПДН наблюдалось наиболее значимое снижение среднесуточного АД –30,5/–18,9 мм рт.ст. При САД24 ≥ 140 мм рт.ст. и < 160 мм рт.ст. через 12 месяцев после процедуры снижение САД24/ДАД24 составляло –20,1/–18,0 мм рт.ст. При САД24 < 140 мм рт.ст. достоверных изменений в снижении АД не было. Среднее снижение офисного АД составляло в динамике на этапах 7 дней, 1, 6 и 12 месяцев соответственно –14,38/–5,63 мм рт.ст., –9,02/–10,71 мм рт.ст., +3,12/–8 мм рт.ст. и –7,88/
–5,0 мм рт.ст. Офисная ЧСС не изменилась.
Расчетный уровень клиренса креатинина, определенный по формуле Кокрофта — Гаулта, достоверно не изменился ни у одного пациента. Таким образом, применение процедуры ПДН у пациентов с резистентной АГ является безопасным и рекомендовано лишь у пациентов, у которых САД по данным СМАД 140 мм рт.ст. и выше. Рекомендовано обязательное использование СМАД для отбора и эффективного контроля после ПДН.
Completed controlled trials have shown the safety but different effectiveness of renal denervation (RDN) in patients with resistant arterial hypertension (AH). We have carried out RDN in 8 patients. The average age of patients was 52.13 ±
± 3.88 years (40–66), mean duration of AH — 16.75 ± 2.17 (12–25) years. On admission to hospital institute, blood pressure (BP) level was 181.25/106.88 ± 4.3/4.0 mmHg (160–200/85–120 mmHg), heart rate (HR) — 70.63 ± 3.03 bpm. Optimization of treatment in a hospital in these patients led to a significant decrease in BP to 156.88/95.00 ± 2.98 mmHg (150–165/85–100 mmHg) and HR — 68.88 ± 3.28 bpm. The number of antihypertensive drugs was an average of 5.5 per patient. In ambulatory blood pressure monitoring (ABMP) on the stage of therapy optimization, the average systolic BP (SBP24) was 149.16 ± 5.40 mmHg, and diastolic (DBP24) — 86.98 ± 5.08 mmHg. Average daily heart rate (HR24) was 70.12 ± ± 2.94 bpm. All patients underwent the procedure well.
Mean reduction in the average daily BP (SBP/DBP) was in the dynamics at the stage of 7 days, 1, 6 and 12 months, respectively, –15.73/–8.52 mmHg, –11.45/–6.06 mmHg, –10.70/
–13.68 mmHg and –17.91/–13.88 mmHg. HR24 was not significantly changed. Reducing daytime SBP/DBP in the dynamics at the stages of 7 days, 1, 6 and 12 months was –14.79/–5.64,
–16.55/–5.60, –12.29/–12.79 and –20.45/–13.62 mmHg, respectively. Dynamics of decrease in nocturnal SBP/DBP at the stages of 7 days, 1, 6 and 12 months was –15.03/–8.42, –10.64/
–4.57, –9.23/–12.38 and –19.39/–14.84 mmHg, respectively. In SBP24 ≥ 160 mmHg 12 months after RDN we observed the most significant decrease in the average daily BP –30.5/–18.9 mmHg. In SBP24 ≥ 140 mmHg and < 160 mmHg 12 months after the procedure, reduction of SBP24/DBP24 was –20.1/–18.0 mmHg. When SBP24 < 140 mmHg, significant changes in BP reduction were not detected. Mean reduction in office BP was in the dynamics at the stages of 7 days, 1, 6 and 12 months, respectively, –14.38/–5.63 mmHg, –9.02/–10.71 mmHg, +3.12/–8 mmHg
and –7.88/–5.0 mmHg. Office heart rate did not change.
Estimated creatinine clearance level determined by Cockcrof- Gault equation was not significantly changed in any patient. Thus, the application of RDN in patients with resistant AH is safe and recommended only in patients with SBP140 mmHg and above, according to ABPM. Mandatory use of ABMP for selection and effective control after RDN is recommended.
резистентна гіпертензія, ниркова денервація, добове моніторування артеріального тиску.
резистентная гипертензия, почечная денервация, суточное мониторирование артериального давления.
resistant hypertension, renal denervation, ambulatory blood pressure monitoring.
Статья опубликована на с. 28-39
Вступ
З моменту першої публікації Schlaich et al. клінічного випадку пацієнта з артеріальним тиском (АТ) 161/107 мм рт.ст., у якого на фоні прийому 7 антигіпертензивних препаратів після процедури проведення ниркової денервації (НДН) відбулося зниження АТ до 127/81 мм рт.ст., розпочався етап проведення клінічних досліджень впливу ниркової денервації на АТ [19]. Завершені багатоцентрові дослідження Symplicity HTN-1 і Symplicity HTN-2, які показали ефективність і безпеку процедури катетерної радіочастотної денервації ниркових артерій у хворих із резистентною артеріальною гіпертензією (АГ). Однак після оприлюднення результатів дослідження Simplicity HNT-3, яке було закінчено достроково у зв’язку з недосягненням первинної кінцевої точки щодо зниження АТ після процедури НДН, виникли нові питання щодо ефективності власне самої процедури. Негативні результати дослідження Simplicity HNT-3 підняли питання як якості технічного виконання процедури НДН, так і відбору пацієнтів для її проведення [4]. Технічне удосконалення катетерів та зменшення залежності якості виконання процедури від досвіду лікаря, який її виконує, безумовно, може підвищити ефективність НДН, але, на нашу думку, ключовим моментом є саме ретельний відбір пацієнтів, яким буде проведена НДН. Світовий досвід кращих центрів показує, що процедуру НДН слід виконувати тільки в 1–2 % хворих, яких направляють із діагнозом резистентної гіпертензії [2]. Наш трирічний досвід відбору хворих для проведення НДН показує такий самий результат [1].
У той же час оцінка ефективності НДН, за даними реєстру Simplicity, більша, ніж у дослідженні Simplicity HNT-3, що пояснюють більш ретельним відбором пацієнтів. Як будь-який реєстр, реєстр Simplicity так само має недоліки, пов’язані з гетерогенністю включених пацієнтів. Сучасна оцінка тривалого антигіпертензивного ефекту процедури НДН у ретельно відібраного контингенту хворих залишається маловивченою. Саме ретельний відбір хворих за певними ознаками може допомогти визначити когорту пацієнтів, у яких ефективність процедури НДН буде найбільшою.
Метою нашого дослідження було визначення ефективності НДН за допомогою системи Symplicity (катетери та генератор) виробництва компанії Medtronic, Inc. (США) у пацієнтів з істинною резистентною АГ та визначення критеріїв найбільш ефективного зниження АТ після процедури НДН.
Матеріали і методи
Із 674 пацієнтів із підозрою на резистентну АГ, які були направлені та обстежені у відділенні симптоматичних артеріальних гіпертензій ДУ «ННЦ Інститут кардіології імені академіка М.Д. Стражеска» НАМН України з 2012 по 2014 рік, процедура НДН була проведена 8 (1,18 %) пацієнтам. Деталі відбору хворих на процедуру НДН нами були опубліковані раніше [1]. Якщо коротко, то це проводилося так: критеріями відбору пацієнтів з АГ для проведення НДН слугували: вік старше 18 років, рівень офісного САТ ≥ 160 мм рт.ст. (≥ 150 мм рт.ст. за наявності цукрового діабету 2-го типу), рівень АТ при добовому моніторуванні САТ 24 ДМАТ > 130 мм рт.ст. у пацієнтів на фоні прийому 4 і більше антигіпертензивних препаратів в адекватних дозах за умови, що один з них діуретик [10, 11, 16]. Пацієнти проходили повний курс клінічного обстеження для підтвердження резистентної АГ, виключаючи вторинну АГ, АГ «білого халата», псевдорезистентність та відсутність прихильності пацієнта до терапії. Обов’язково всім пацієнтам було проведене добове моніторування АТ (ДМАТ) (рівень добового систолічного АТ (САТ) — САТ24 — повинен був становити > 130 мм рт.ст.). Усім відібраним пацієнтам для НДН була виконана візуалізація ниркових артерій за допомогою комп’ютерної ангіографії для уточнення анатомії ниркових артерій перед проведенням процедури НДН. Критеріями виключення для проведення НДН були: діаметр основної ниркової артерії менше ніж 4 мм або довжина менше ніж 20 мм, відсутність попередніх втручань на ниркових артеріях (балонна ангіопластика або стентування) та ознак атеросклеротичного ураження ниркової артерії (стеноз ниркових артерій більше ніж 50 %), наявність декількох основних ниркових артерій, швидкість клубочкової фільтрації менше ніж 45 мл/хв. Пацієнти, які перенесли гостре порушення мозкового кровообігу (ГПМК), інфаркт міокарда або нестабільну стенокардію протягом останніх 3–6 місяців. Із 16 відібраних хворих для НДН половина відмовилася від проведення процедури через персональні причини. У результаті НДН була проведена 8 пацієнтам: 5 чоловікам (62,5 %) та 3 жінкам (37,5 %). Спочатку пацієнти, які були включені в дослідження, мали такі характеристики (табл. 1): середній вік становив 52,13 ± 3,88 року (40–66 років), середня тривалість АГ — 16,75 ± 2,17 (12–25) року. В одного пацієнта (12,5 %) був цукровий діабет 2-го типу.
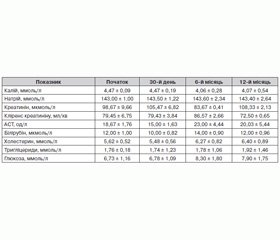
У середньому індекс маси тіла (ІМТ) становив 29,53 ± 0,85 кг/м2, 5 пацієнтів мали надлишкову масу тіла, у 3 пацієнтів було ожиріння I ступеня. Три пацієнти палили (37,5 %). Середній рівень загального холестерину (ХС) крові становив 5,62 ± 0,62 ммоль/л, тригліцеридів (ТГ) — 1,76 ± 0,18 ммоль/л, глюкози — 6,16 ± 1,05 ммоль/л, індекс маси міокарда лівого шлуночка (ІММЛШ) — 142,08 ± 7,82 кг/м2. Середня кількість антигіпертензивних препаратів становила 5,5. Призначення антигіпертензивних препаратів розподілилося так: інгібітори ангіотензинперетворюючого ферменту було призначено 5 пацієнтам (62,5 %), блокатори рецепторів до ангіотензину II — 3 (37,5 %), антагоністи кальцію — 8 (100 %), бета-адреноблокатори — 6 (75 %), діуретики тіазидоподібні — 6 пацієнтам (75 %), діуретики петльові — 3 (37,5 %), антагоністи альдостерону — 5 (62,5 %), препарати центральної дії — 7 (87,5 %), альфа-адреноблокатори — одному пацієнту (12,5 %).
У 2 пацієнтів в анамнезі було ГПМК (в одного — за ішемічним типом, в одного — за геморагічним типом), у жодного хворого не було в анамнезі інфаркту міокарда, серцевої недостатності вище від II функціонального класу (ФК). В одного пацієнта було хронічне захворювання нирок із рівнем клубочкової фільтрації до процедури 46 мл/хв. Один пацієнт страждав від стабільної ішемічної хвороби серця II ФК. У всіх хворих мали місце ЕКГ- і ехокардіографічні ознаки гіпертрофії лівого шлуночка. В однієї пацієнтки був цукровий діабет 2-го типу, контрольований пероральними цукрознижуючими препаратами та інсуліном.
При надходженні у відділення рівень офісного АТ у 8 відібраних пацієнтів становив 181,25/106,88 ± 4,3/4,0 мм рт.ст. (160–200/85–120 мм рт.ст.), ЧСС — 70,63 ± 3,03 уд/хв. Оптимізація терапії в умовах стаціонару в цих хворих привела до достовірного зниження рівня офісного АТ до 156,88/95,00 ± 2,98 мм рт.ст. (150–165/85–100 мм рт.ст.) (р < 0,05 для обох значень) та ЧСС — 68,88 ± 3,28 уд/хв. При ДМАТ на етапі оптимізації терапії середньодобовий систолічний АТ (САТ24) становив 149,16 ± 5,40 мм рт.ст., а діастолічний (ДАТ24) — 86,98 ± 5,08 мм рт.ст. Середньодобова частота серцевих скорочень (ЧСС24) була 70,12 ± 2,94 уд/хв.
Усім хворим на початку, через 7 днів, через 1, 6 та 12 місяців після НДН проводили: офісне вимірювання систолічного (САТ) та діастолічного (ДАТ) АТ із визначенням частоти серцевих скорочень (ЧСС); добове моніторування АТ (ДМАТ); визначення швидкості поширення пульсової хвилі (ШППХ) по артеріях еластичного (ШППХе) та м’язового (ШППХм) типів. Проводили ехокардіографічне (ЕхоКГ) обстеження. Вимірювали масу тіла та зріст пацієнта, розраховували індекс маси тіла (ІМТ = вага (кг)/зріст (м2)).
АТ вимірювали ртутним сфігмоманометром уранці (між восьмою та десятою годинами) відповідно до рекомендацій ESH/ESC 2013. Реєстрацію САТ та ДАТ у положенні сидячи проводили на одній і тій самій руці двічі з інтервалом 2 хв, якщо величини АТ не відрізнялися більше як на 5 мм рт.ст. У разі більшої різниці проводили третє вимірювання та обчислювали середнє значення двох або трьох послідовних вимірювань. ЧСС визначали після другого вимірювання.
ДМАТ проводили на портативному апараті АВРМ-04 (Medithech, Угорщина). Моніторування проводили в такому режимі: удень — кожні 15 хв, уночі (із 22.00 до 06.00) — кожні 30 хв. Хворі вели звичайний спосіб життя, виконуючи побутові навантаження. При цьому вивчали такі показники: середньодобові (24), денні (Д), нічні (Н) САТ, ДАТ, пульсовий АТ (ПАТ), ЧСС. Під час комп’ютерного аналізу ДМАТ для САТ і ДАТ розраховували часовий індекс (ЧІ), що характеризує перевантаження тиском протягом доби і визначається як відсоток вимірів АТ, що перевищує 15,82/10,17 кПа (140/90 мм рт.ст.) удень і 13,56/9,04 кПа (120/80 мм рт.ст.) уночі. Також визначали індекс навантаження тиском, тобто площу між кривою підвищеного АТ й лінією межі норми, індекс варіабельності АТ, що обчислювали як стандартне відхилення величини САТ та ДАТ. Крім того, за допомогою програмного забезпечення вираховували добовий індекс (ДІ) — відсоток зниження нічних САТ та ДАТ порівняно з денним.
Біохімічні показники крові визначали на автоматичному біохімічному аналізаторі Livia (Cormay, А-25, Польща) та на автоматичному аналізаторі (Ciba Corning, Англія). Величину кліренсу креатиніну (КК) розраховували за допомогою формули Cocroft — Gault [20]:
/30/30_2.jpg)
Визначення вмісту загального холестерину, тригліцеридів, холестерину ліпопротеїнів високої щільності (ХС ЛПВЩ), холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ), холестерину ліпопротеїнів дуже низької щільності (ХС ЛПДНЩ), індекс атерогенності (ІА). Рівні загального ХС, ТГ, ЛПВЩ визначали на апараті Еxpress pluss 550, Bayer (Німеччина) з використанням реактивів PLIVA-Lachema (Хорватія) за стандартною методикою. Уміст загального ХС, ТГ, ХС ЛПНЩ, ХС ЛПДНЩ визначали в ммоль/л, ІА — в умовних одиницях.
Фракції ХС ЛПНЩ, ХС ЛПДНЩ та ІА розраховували за формулою W. Friedwald [14]:
ХС ЛПНЩ (ммоль/л) = ЗХ – (ХС ЛПВЩ + ТГ/2,2),
ХС ЛПДНЩ (ммоль/л) = ТГ/2,2,
ІА (ум.од.) = (ЗХ – ХС ЛПВЩ)/ХС ЛПВЩ.
Визначали рівень глюкози крові, білірубіну, аланінамінотрансферази, аспартатамінотрансферази (АСТ), калію, натрію крові; проводили загальний аналіз сечі.
Показники внутрішньосерцевої гемодинаміки та скорочувальної здатності міокарда лівого шлуночка серця оцінювали за допомогою ехокардіографії на ультразвуковому діагностичному апараті Sonoline SL-1 (Siemens, Франція). Ультразвукове дослідження серця виконували в М- та В-режимі за стандартним способом. Визначали розмір лівого передсердя, кінцево-діастолічний (КДР) та кінцево-систолічний (КСР) розміри ЛШ, фракцію викиду ЛШ (ФВ). Масу міокарда ЛШ (ММЛШ) вираховували згідно з методикою Penn — Convention [8]:
ММЛШ (г) = 1,04 • ((КДР + ТЗС + ТМЖП)3 – – КДР3) – 13,6,
де ММЛШ — маса міокарда лівого шлуночка, КДР — кінцево-діастолічний розмір, см; ТЗС — товщина задньої стінки лівого шлуночка, см; ТМШП — товщина міжшлуночкової перегородки лівого шлуночка, см; 1,04 — коефіцієнт розрахунковий; 13,6 — коефіцієнт розрахунковий.
Площу поверхні тіла вираховували за стандартними таблицями за формулою Du Bois [8].
ІММЛШ вираховували за формулою:
/31/31_2.jpg)
ШППХ визначали за допомогою апарата SphygmoCor (AtCor, Medical Pty Ltd., Австралія), з’єднаного з персональним комп’ютером, за рекомендованою методикою [23]. Для усунення похибок під час вимірювання проводили визначення параметрів як мінімум два рази. Якщо різниця між даними була більше ніж 10 %, то проводили третє вимірювання. Повторні вимірювання пацієнту проводив один і той же лікар.
При проведенні процедури НДН у нашій групі пацієнтів використовувався радіочастотний генератор та однополюсний катетер системи Symplicity (виробництва компанії Medtronic, Inc., США) за стандартною методикою [6, 21]. Процедуру НДН виконували у відділенні інтервенційних втручань при ДУ «ННЦ Інститут кардіології імені академіка М.Д. Стражеска» НАМН України.
Первинною кінцевою точкою в нашому дослідженні було зниження систолічного та діастолічного АТ за даними ДМАТ. Вторинними точками дослідження були зниження систолічного та діастолічного АТ після НДН за даними офісного вимірювання, оцінка динаміки пружно-еластичних властивостей артерій, оцінка динаміки центрального АТ, оцінка безпечності процедури під час її проведення та за даними лабораторного обстеження в динаміці (оцінка біохімічних показників сироватки крові, умісту креатиніну, кліренсу креатиніну).
На основі отриманих даних була створена база даних у системі Microsoft Exсel. Статистичну обробку результатів проводили за допомогою пакета аналізу в системі Microsoft Exсel та пакета комп’ютерних програм Statistіca for Windows 5.0 (Stat Soft, США) та програми SPSS 11.0 з обчисленням таких показників: середньої арифметичної величини — М; стандартного відхилення від середньої арифметичної величини — m; коефіцієнта достовірності — р. Відмінність вважали достовірною при р < 0,05.
Достовірність отриманих даних вираховували методом парного двовибіркового тесту з використанням t-критерію Стьюдента для середніх величин або використовували двовибірковий незалежний t-тест для середніх величин у групах із непараметричним розподілом (метод Mann — Whitney) після визначення характеру розподілу. Також проводили багатофакторний регресійний аналіз, кореляційний аналіз для незалежних варіант та парний факторний кореляційний аналіз з обчисленням коефіцієнта кореляції Pearson та Spearmen – r. Кореляцію між двома варіантами вважали достовірною при рівні достовірності р < 0,05.
Результати
Усі хворі добре перенесли процедуру. Пацієнтам рекомендували продовжувати приймати підібрану до проведення НДН антигіпертензивну терапію без зміни дози і числа препаратів. З 2-го дня після проведення процедури НДН пацієнти суб’єктивно відзначили поліпшення стану: зменшення головного болю, болю в ділянці серця, поліпшення зору, підвищення працездатності.
Оцінюючи первинну кінцеву точку за даними добового моніторування АТ, слід зазначити, що спостерігалося значне та достовірне зниження АТ. Індивідуальна динаміка АТ при добовому моніторуванні наведена на рис. 1а, б. З рис. 1 видно, що рівень САТ і ДАТ знизився у всіх пацієнтів: САТ24 на 3–31 мм рт.ст., а ДАТ24 — на 0–21 мм рт.ст. Середнє зниження середньодобового АТ становило в динаміці на етапі 7 днів, 1, 6 та 12 місяців відповідно –15,73/–8,52 мм рт.ст., –11,45/–6,06 мм рт.ст., –10,70/–13,68 мм рт.ст. та –17,91/–13,88 ммрт.ст. Величина ЧСС24 достовірно не змінилася, її динаміка була такою: 0 уд/хв, –1 уд/хв, –6,49 уд/хв, –2,32 уд/хв на етапі 7 днів, 1, 6 та 12 місяців відповідно.
На фоні оптимізованої терапії середні цифри АТ при ДМАТ до процедури становили: САТ24 — 149,16 ± 6,04 мм рт.ст. та ДАТ24 — 86,98 ± 5,68 мм рт.ст. Після проведення процедури НДН рівень середнього добового АТ знижувався протягом усього періоду спостереження (табл. 2). Через 6 місяців средньодобовий АТ становив 138,46 ± 4,84 мм рт.ст. та 73,30 ± 2,44 мм рт.ст., а через 12 місяців — 131,25 ± 3,04 мм рт.ст. та 73,10 ± 3,65 мм рт.ст. Через 12 місяців зниження АТ за даними ДМАТ становило 17,91/13,88 мм рт.ст. (р < 0,05), ЧСС достовірно не змінилася. Також достовірно зменшився добовий індекс площі для САТ із 468,65 ± 116,25 мм рт.ст. • год до 130,44 ± 46,40 мм рт.ст. • год (р < 0,05).
Оцінюючи динаміку денних та нічних показників АТ при ДМАТ ми також відмітили достовірну динаміку в зниженні середньоденних та середньонічних показників САТ та ДАТ. Дані також наведені в табл. 2.
Так, зниження денних САТ/ДАТ становило в динаміці на етапах 7 днів, 1, 6 та 12 місяців –14,79/–5,64, –16,55/–5,60, –12,29/–12,79 та –20,45/–13,62 мм рт.ст. відповідно. Достовірна динаміка спостерігалась тільки на етапі 12 місяців, але, скоріше за все, така ситуація пов’язана з невеликою кількістю пацієнтів. Динаміка зниження нічних САТ/ДАТ становила на етапах 7 днів, 1, 6 та 12 місяців –15,03/–8,42, –10,64/–4,57, –9,23/–12,38 та –19,39/–14,84 мм рт.ст. відповідно. Так само достовірні зміни спостерігалися на етапі 12 місяців після НДН. Виявлена пряма кореляційна залежність між тривалістю АГ та нічним ПАТ на етапі оптимізації терапії: чим довша була тривалість АГ, тим вищим був пульсовий тиск до початку процедури, а також чим більшою була тривалість АГ, тим вищим був ПАТ24 через 12 місяців після НДН.
Ми проаналізували, як змінювався рівень середнього добового АТ залежно від його початкових значень. Ми розподілили пацієнтів за початковим рівнем САТ при ДМАТ на три підгрупи: перша — із рівнем САТ24 ≥ 160 мм рт.ст., друга — із рівнем САТ24 ≥ 140 мм рт.ст. та < 160 мм рт.ст. і третя — із рівнем САТ24 < 140 мм рт.ст. Дані наведені на рис. 2.
/33/33_2.jpg)
Як видно з рис. 2, найбільш ефективним та значним було зниження АТ у підгрупі пацієнтів із початково найбільш високими рівнями АТ, що не контролювалися за допомогою медикаментозної терапії. Так, у підгрупі пацієнтів із САТ24 ≥ 160 мм рт.ст. (n = 3) через 12 місяців після проведення ниркової денервації спостерігалося найбільш значне зниження середньодобового АТ, як систолічного — на 30,5 мм рт.ст., так і діастолічного — на 18,9 мм рт.ст. (р < 0,05 для обох значень). ЧСС у цих хворих достовірно не змінилася (рис. 2а). У підгрупі пацієнтів із САТ24 ≥ 140 мм рт.ст. та < 160 мм рт.ст. (n = 3) через 12 місяців після процедури спостерігалося також значне та достовірне зниження як систолічного на 20,1 мм рт.ст., так і діастолічного на 18,0 мм рт.ст. середньодобового АТ (р < 0,05 для обох значень). У цих пацієнтів середньодобова ЧСС також достовірно не змінилася, хоча спостерігалася тенденція до її зменшення — на 3,6 уд/хв (зміни недостовірні, імовірно, у зв’язку з невеликою кількістю пацієнтів у підгрупі) (рис. 2б). І зовсім протилежні зміни ми отримали в підгрупі з найменшим початковим рівнем АТ перед проведенням процедури НДН, де на фоні медикаментозної терапії САТ24 був меншим ніж 140 мм рт.ст. (n = 2): через 6 місяців (даних за 12 місяців у цих пацієнтів ще немає) відбулося недостовірне підвищення САТ24 на 12 мм рт.ст., ДАТ24 — на 2,2 мм рт.ст. (р > 0,05 для обох значень). При цьому ЧСС достовірно не мінялася, хоча також спостерігалася тенденція до її зменшення на 2,1 уд/хв (рис. 2в).
Таким чином, на основі отриманих даних можна зробити висновок, що проведення процедури НДН забезпечувала найбільший антигіпертензивний ефект у пацієнтів із резистентною АГ та цифрами середнього добового рівня САТ ≥ 140 мм рт.ст., навпаки, процедура НДН не ефективна при рівні середнього добового САТ < 140 мм рт.ст.
При оцінці вторинної кінцевої точки — офісного АТ ми виявили зниження АТ, але не таке значне, як при добовому моніторуванні. Так, через 7 днів після процедури рівень офісного АТ знизився у всіх пацієнтів і в середньому становив: САТ — 142,50 ± 3,90 мм рт.ст. та ДАТ — 89,38 ± 3,05 мм рт.ст. Рівень офісного АТ через 1 місяць продовжував утримуватися в межах 7–денного зниження і становив для САТ 147,86 ± 7,49 мм рт.ст., для ДАТ — 84,29 ± 4,14 мм рт.ст. Через 6 місяців офісний АТ становив 160,0/87,0 ± 10,37/3,67 мм рт.ст. Через 12 місяців офісний АТ знизився до 149,0/90,0 ± 5,37/4,37 мм рт.ст., що становило 7,88 мм рт.ст. для САТ та 5,0 мм рт.ст. для ДАТ. Середнє зниження офісного АТ становило в динаміці на етапах 7 днів, 1, 6 та 12 місяців відповідно –14,38/–5,63 мм рт.ст., –9,02/–10,71 мм рт.ст., +3,12/–8 мм рт.ст. та –7,88/–5,0 мм рт.ст. Офісна ЧСС також достовірно не змінилася, її динаміка становила +3 уд/хв, –3,17 уд/хв, –7,88 уд/хв, –2,13 уд/хв на етапах 7 днів, 1, 6 та 12 місяців відповідно. Достовірними зміни офісного АТ були на етапі 7 днів як для САТ, так і для ДАТ та на етапі 1 місяця для ДАТ. Недостовірність даних за 12 місяців пов’язана з невеликою кількістю пацієнтів. Дані наведені в табл. 3.
Звичайно, досягнення цільових рівнів АТ у пацієнтів із резистентною АГ — завдання надзвичайно складне. Так, на початку до процедури НДН у жодного пацієнта не вдалося досягнути цільового рівня АТ, незважаючи на прийом 5 препаратів у максимальних або максимально переносимих дозах. Однак після процедури НДН у нашому дослідженні ми виявили, що через 6 та 12 місяців спостерігалося досягнення цільового АТ як за даними офісного вимірювання, так і за даними добового моніторування у 20–25 % пацієнтів, у яких початково АТ був неконтрольованим (рис. 3), що свідчить про антигіпертензивний ефект НДН у пацієнтів із резистентною АГ.
Ми не відмітили достовірних змін центрального аортального тиску та швидкості поширення пульсової хвилі по артеріям м’язового та еластичного типу в наших пацієнтів через 12 місяців після процедури (рис. 4, 5). Можливо, такі зміни пов’язані з невеликою кількістю пацієнтів у нашому дослідженні.
Нами також були проаналізовані дані біохімічних показників крові в динаміці (табл. 4). Ми не відмітили достовірної різниці за жодним із досліджуваних показників. Розрахунковий рівень кліренсу креатиніну достовірно не змінився в жодного пацієнта і в середньому становив 79,45 ± 6,75 мл/хв до процедури, 86,57 ± 2,66 мл/хв — через 6 місяців після процедури і 72,50 ± 0,65 мл/хв — через 12 місяців, що відповідає тяжкості цієї категорії пацієнтів. Ми виявили обернену кореляційну залежність між тривалістю АГ та рівнем кліренсу креатиніну: чим більшою була тривалість АГ, тим меншим був кліренс креатиніну до початку процедури в наших пацієнтів.
Щодо ускладнень під час та після проведення процедури ниркової денервації, то ми спостерігали 3 випадки (37,5 %) гіпотонії під час проведення НДН, 1 випадок (12,5 %) брадикардії під час НДН, у 2 пацієнтів (25 %) — транзиторне підвищення рівня креатиніну в сироватці крові, у 2 пацієнтів (25 %) — відміну спіронолактону (підвищення вмісту калію в плазмі та гінекомастія), в 1 випадку (12,5 %) — зубний біль. Серйозних побічних ефектів, обумовлених процедурою, в нашому дослідженні не спостерігалося.
Таким чином, можна зробити висновок, що процедура НДН призвела до зниження як офісного АТ, так і АТ при добовому моніторуванні через 1, 6 та 12 місяців після проведення процедури. При цьому пацієнти не змінювали свій спосіб життя. Через 6 місяців після процедури ми відмітили, що пацієнти самостійно намагалися зменшити кількість та дози антигіпертензивних препаратів, що, можливо, й обумовило незначне підвищення офісного АТ на наступних візитах. Таким пацієнтам було рекомендовано повернутися до попередньої терапії, що була призначена перед процедурою, та не змінювати її.
Таким чином, можна зробити висновок, що процедура НДН має перспективне значення в лікуванні пацієнтів із резистентною АГ, безпечна та добре переноситься пацієнтами, однак необхідно ретельно підходити до відбору пацієнтів для НДН, використовуючи добове моніторування АТ як для включення пацієнтів у дослідження, так і для контролю ефективності процедури НДН.
Обмеженням нашого дослідженні були такі чинники: проведення дослідження в одному центрі, мала кількість пацієнтів та відсутність контрольної групи, відсутність контролю з візуалізацією ниркових артерій через 12 місяців.
Обговорення
Дані нашого дослідження стосовно відбору пацієнтів узгоджуються з результатами інших досліджень світової літератури. Так, за даними Salim S. Hayek зі співавт., із 1756 пацієнтів з АГ тільки 14 хворих (0,8 %) було відібрано для ниркової денервації [12]. Аналогічні дані наводить група M. Azizi [2]. У нашому ж дослідженні із 674 пацієнтів відібрані 8 (1,18 %), що свідчить про ретельний, довготривалий та кропіткий етап відбору таких пацієнтів. Стосовно характеристики пацієнтів, які були включені в дослідження, то також наші дані збігаються з даними інших досліджень. Так, у дослідження Symplicity HTN–1 [21] було включено 50 пацієнтів із резистентною гіпертензією, середній вік яких становив 58 ± 9 років. У середньому початкові цифри офісного САТ/ДАТ становили 177/101 мм рт.ст. на фоні прийому 5,1 антигіпертензивного препарату. У дослідженні Symplicity HTN2 [22], проведеному за участі 106 пацієнтів (середній вік 58 років), базовий рівень офісного АТ у пацієнтів із резистентною АГ становив 178/96 мм рт.ст. на фоні прийому 5,2 антигіпертензивного препарату. У дослідження Symplicity HTN3 були включені 364 пацієнти, яким була проведена НДН [4, 5]. Середній вік пацієнтів — 57,9 ± 10,4 року. Середня кількість антигіпертензивних препаратів — 5,1 ± 1,4. Symplicity HTN3 — це єдине дослідження, де була група контролю — 171 пацієнт, середній вік 56,2 ± 11,2 року. Середня кількість антигіпертензивних препаратів у групі контролю — 5,2 ± 1,4. Особливістю цього дослідження було те, що одну третину пацієнтів у дослі–дженні Symplicity HTN3 становили темношкірі хворі. У наше дослідження включені 8 пацієнтів європейської раси, середній вік яких був дещо меншим і становив 52,13 ± 3,88 року, початковий рівень офісного АТ був також дещо нижчим і становив 156,88/95,00 мм рт.ст. на фоні 5,5 антигіпертензивного препарату в максимальних або максимально переносимих дозах. Меншу кількість пацієнтів у нашому дослідженні можна пояснити більш ретельним відбором пацієнтів для НДН та відмовою половини з відібраних хворих від проведення процедури.
У дослідженні Symplicity HTN–1 офісний САТ/ДАТ після двосторонньої НДН знизився на –14/–10, –21/–10, –22/–11, –24/–11, –27/–17 мм рт.ст. на етапі 1, 3, 6, 9, 12 місяців після проведення процедури відповідно [21]. При більш довгостроковому спостереженні за 153 пацієнтами, у тому числі 45 пацієнтами з НДН, офісний САТ /ДАТ знизився на 20/10, 24/11, 25/11, 23/11, 26/14 та 32/14 мм рт.ст. на етапах 1, 3, 6, 12, 18 і 24 місяці після проведення НДН відповідно. У дослідженні Symplicity HTN–2 зниження офісного АТ на етапах 1, 3 та 6 місяців становило –20/–7, –24/–8 та –32/–12 мм рт.ст. відповідно [22].
У дослідженні EnligHTN I (де використовувалася багатоелектродна система для НДН на відміну від одноелектродної системи Symplicity, яка була використана у нашому дослідженні) зменшення офісного АТ на етапах 1, 3 та 6 місяців становило –28/10, –27/10 та –26/10 мм рт.ст. відповідно (р < 0,01) [25]. Через 6 місяців терапії в дослідженні Symplicity HTN-3 зниження офісного САТ становило 14,13 ± 23,93 мм рт.ст., що практично не відрізнялося від контрольної групи, де зниження було 11,74 ± 25,94 мм рт.ст., різниця між групами становила –2,39 мм рт.ст. [4, 5]. У нашому дослідженні на етапі 7 днів, 1, 6 та 12 місяців зниження офісного САТ/ДАТ становило –14,38/–5,63 мм рт.ст., –9,02/–10,71 мм рт.ст., +3,12/–8 мм рт.ст. та –7,88/–5,0 мм рт.ст. відповідно.
У Symplicity HTN-2 ДМАТ протягом 24 годин, яке було виконане в обмеженої кількості пацієнтів (n = 20), показало менш виражений характер змін АТ через 6 місяців після НДН порівняно з офісним АТ (–11/–7 мм рт.ст., p = 0,006 для рівня САТ, р = 0,014 для рівня ДАТ) [3, 22]. У Symplicity HTN-3 ДМАТ показало зниження САТ –6,75 ± 15,11 мм рт.ст. у групі пацієнтів, яким була проведена НДН, та –4,79 ± 17,25 мм рт.ст. у контрольній групі, різниця між групами становила –1,96 мм рт.ст. [4, 5]. У нашому дослідженні середнє зниження було більш значним — середньодобовий АТ у динаміці зменшився на етапах 7 днів, 1, 6 та 12 місяців після процедури НДН відповідно на 15,73/–8,52 мм рт.ст., –11,45/–6,06 мм рт.ст., –10,70/–13,68 мм рт.ст. та –17,91/–13,88 мм рт.ст. (р < 0,05 для обох значень на всіх етапах спостереження), що може свідчити про більш ретельний та правильний відбір пацієнтів для НДН.
Отримані нами дані щодо залежності ефективності процедури НДН від початкового рівня АТ перекликаються з даними світової літератури. Так, M. Bohm зі співавт. (2013) показали, що через 12 місяців після НДН у пацієнтів із офісним САТ ≥ 140 мм рт.ст. зменшення САТ відбувалося на 21 мм рт.ст., а ДАТ — на 11 мм рт.ст. При рівні офісного САТ ≥ 160 мм рт.ст. САТ знижувався на 22 мм рт.ст., ДАТ — на 11 мм рт.ст., а при показниках офісного САТ ≥ 180 мм рт.ст. зниження АТ відбувалося найбільше: САТ — на 37 мм рт.ст., ДАТ — на 23 мм рт.ст. [6, 7, 24]. За нашими даними, які ми оцінювали за даними добового моніторування АТ (як більш точного показника якості контролю АТ), спостерігалась аналогічна картина. Так, у пацієнтів із САТ24 ≥ 160 мм рт.ст. через 12 місяців після проведення НДН спостерігалося найбільш значне зниження середньодобового АТ, як систолічного (на 30,5 мм рт.ст.), так і діастолічного (на 18,9 мм рт.ст.) (р < 0,05 для обох значень). У пацієнтів із САТ24 ≥ 140 мм рт.ст. через 12 місяців після процедури спостерігалося зниження як систолічного (на 20,1 мм рт.ст.), так і діастолічного (на 18,0 мм рт.ст.) середньодобового АТ (р < 0,05 для обох значень). У пацієнтів із САТ24 менше ніж 140 мм рт.ст. через 6 місяців відбулося підвищення САТ24 на 12 мм рт.ст., ДАТ24 — на 2,2 мм рт.ст. Отримані дані доводять необхідність обов’язкового проведення амбулаторного моніторування АТ для більш якісного відбору пацієнтів для НДН: імовірно, що від цього буде залежати ефективність процедури.
Визначальними критеріями будь-якого методу лікування є безпека і тривалість досягнутого ефекту. Ускладнення, які виникали під час та після проведення процедури НДН описані вище. Як видно з цих даних, серйозних побічних ефектів, обумовлених процедурою НДН, у нашому дослідженні не спостерігалося. Ми не спостерігали протягом року після процедури достовірних змін функції нирок в жодного пацієнта. Це відповідає даним світової літератури. Так, у дослідженні Symplicity-2 у 7 (13 %) із 52 пацієнтів, які перенесли НДН, спостерігалась інтраопераційна брадикардія, що потребувало введення атропіну. Функція нирок не змінювалася через 6 місяців після процедури, хоча у 2 пацієнтів спостерігалося зменшення ШКФ більше ніж на 25 % [15, 17, 22]. У дослідженні Symplicity HTN-1 у 97 % пацієнтів (149 з 153) не було ускладнень. Чотири гострих процедурні ускладнення включали три псевдоаневризми стегнової артерії та одне розшарування ниркової артерії. В одного пацієнта через 6 місяців після процедури за даними комп’ютерної томографічної (КТ) ангіографії виявлено прогресування існуючого стенозу в усті однієї ниркової артерії, який було успішно усунуто за допомогою стентування. Оцінка функції нирок показала, що протягом першого року спостереження рівень швидкості клубочкової фільтрації залишається стабільним, а після 2 років не було випадків подвоєння рівня креатиніну сироватки або випадків розвитку та прогресування хронічного захворювання нирок до стадії 4 або 5 (хронічна ниркова недостатність) [15, 21]. У дослідженні EnligHTN I клубочкова фільтрація змінилася за 6 місяців від початкового рівня з 87 ± 19 мл/хв до 82 ± 20 мл/хв через 6 місяців (р > 0,05) [25].
Слід підкреслити, що при тривалому спостереженні в дослідженні Symplicity HTN-1 не спостерігалося ослаблення антигіпертензивного ефекту протягом 24 місяців, це дозволяє припустити, що протягом цього періоду часу функціональної реіннервації нирок не відбулося [13, 17]. Такі ж результати ми спостерігали й у нашому дослідженні.
У Symplicity HTN-2 у десяти із 49 пацієнтів (20 %), яким було проведено НДН, протягом наступних 6 місяців було зменшено прийом антигіпертензивних засобів, тоді як у групі контролю — тільки у трьох із 51 (6 %, p = 0,04). За даними спостереження за пацієнтами, які перенесли процедуру, протягом 3 років зберігався стабільний ефект зниження офісного АТ [22]. У нашому дослідженні ми жодному пацієнту не зменшували кількість та дозування препаратів, хоча деякі пацієнти на етапі 1–6 місяців самостійно намагалися зменшити дози та кількість антигіпертензивних препаратів, що, можливо, й обумовило зменшення антигіпертензивного ефекту на етапі 6 місяців спостереження. Але після повернення пацієнтів до попередньо підібраної терапії та наполяганні на незмінності рекомендованої терапії ми отримали позитивний результат у плані динаміки АТ.
Необхідність досліджувати довгострокову тривалість антигіпертензивного ефекту після НДН обумовлена тим, що нервові волокна можуть регенерувати [9, 13]. Тривають подальші дослідження щодо удосконалення техніки проведення процедури, пошуку та визначення ефективності нових методик та удосконалення катетерів для НДН [18, 25].
Таким чином, наш досвід річного спостереження за пацієнтами після застосування процедури НДН із використанням радіочастотного генератора Symplicity (виробництва компанії Medtronic, Inc., США) показує, що даний метод є перспективним для лікування пацієнтів із резистентною гіпертензією, але необхідно більш чітко визначити критерії відбору для проведення НДН.
Висновки
1. Застосування процедури ниркової денервації в пацієнтів із резистентною артеріальною гіпертензією рекомендоване лише тим, у кого систолічний артеріальний тиск за даними добового моніторування артеріального тиску 140 мм рт.ст. і вище.
2. Для відбору й контролю ефективності процедури ниркової денервації рекомендоване обов’язкове використання добового моніторингу артеріального тиску.
3. При описаному ретельному відборі пацієнтів для проведення процедури НДН зниження артеріального тиску за даними добового моніторування через 12 місяців після процедури склало для систолічного 17,91 мм рт.ст. та 13,88 мм рт.ст. для діастолічного.
4. При правильному відборі пацієнтів метод радіочастотної денервації ниркових артерій у хворих із резистентною артеріальною гіпертензією є безпечним.
1. Доброход Г.С. Власний досвід відбору хворих для проведення ниркової денервації // Артеріальна гіпертензія. — 2014. — № 3. — С. 45–48.
2. Azizi M., Steichen O., Frank M., Bobrie G., Plouin P., Sapoval M. Catheter–based radiofrequency renal-nerve ablation in patients with resistant hypertension // Eur. J. Vasc. Endovasc. Surg. — 2012. — Vol. 43(3). — P. 293–299.
3. Banegas J.R., Messerli F.H., Waeber B., Rodriguez-Artalejo F., de la Sierra A., Segura J. et al. Discrepancies between office and ambulatory blood pressure: clinical implications // Am. J. Med. — 2009. — Vol. 122. — P. 1136–1141.
4. Bhatt D.L., Kandzari D.E., O’Neill W.W., D’Agostino R., Flack J.M., Katzen B.T., Leon M.B., Liu M., Mauri L., Negoita M., Cohen S.A., Oparil S., Rocha-Singh K., Townsend R.R., Bakris G.L.; SYMPLICITY HTN–3 Investigators. A controlled trial of renal denervation for resistant hypertension // N. Engl. J. Med. — 2014. — Vol. 370(15). — P. 1393–401.
5. Bakris G.L., Townsend R.R., Liu M., Cohen S.A., D’Agostino R., Flack J.M., Kandzari D.E., Katzen B.T., Leon M.B., Mauri L., Negoita M., O’Neill W.W., Oparil S., Rocha-Singh K., Bhatt D.L.; SYMPLICITY HTN-3 Investigators. Impact of Renal Denervation on 24-hour Ambulatory Blood Pressure: Results from SYMPLICITY HTN-3 // J. Am. Coll. Cardiol. — 2014 May 17.
6. Böhm M., Linz D., Urban D., Mahfoud F., Ukena C. Renal sympathetic denervation: applications in hypertension and beyond // Nat. Rev. Cardiol. — 2013. — Vol. 10(8). — P. 465–476.
7. Böhm M., Linz D., Ukena C., Esler M., Mahfoud F. Renal Denervation for the Treatment of Cardiovascular High Risk-Hypertension or Beyond? // Circ. Res. — 2014 — Vol. 115(3). — P. 400–409.
8. Burton R.F. Estimating body surface area from mass and height: theory and the formula of Du Bois and Du Bois // Ann. Hum. Biol. — 2008. — Vol. 35(2). — P. 170–184.
9. Calhoun D.A., Jones D., Textor S., Goff D.C., Murphy T.P., Toto R.D. et al. Resistant hypertension: diagnosis, evaluation, and treatment. A scientific statement from the American Heart Association Professional Education Committee of the Council for High Blood Pressure Research // Hypertension. — 2008. — Vol. 51. — P. 1403–1419.
10. Di Bona G.F., Esler M. Translational medicine: the antihypertensive effect of renal denervation //Am. J. Physiol. Regul. Integr. Comp. Physiol. — 2010. — Vol. 298. — P. R245–R253.
11. Egan B.M., Zhao Y., Axon R.N., Brzezinski W.A., Ferdinand K.C. Uncontrolled and apparent treatment resistant hypertension in the United States, 1988 to 2008 // Circulation. — 2011. — Vol. 124. — P. 1046–1058.
12. Hayek S.S., Abdou M.H., Demoss B.D., Legaspi J.M., Veledar E., Deka A., Krishnan S.K., Wilmot K.A., Patel A.D., Kumar V.R., Devireddy C.M. Prevalence of resistant hypertension and eligibility for catheter–based renal denervation in hypertensive outpatients // Am. J. Hypertens. — 2013. — Vol. 26(12). — P. 1452–1458.
13. Hansen J.M., Abildgaard U., Fogh-Andersen N., Kanstrup I.L., Bratholm P., Plum I. et al. The transplanted human kidney does not achieve functional reinnervation // Clin. Sci. (Lond). — 1994. — Vol. 87. — P. 13–20.
14. Kannan S., Mahadevan S., Ramji B., Jayapaul M., Kumaravel V. LDL-cholesterol: Friedewald calculated versus direct measurement–study from a large Indian laboratory database // Indian J. Endocrinol. Metab. — 2014. — Vol. 18(4). — P. 502–504.
15. Krum H., Schlaich M., Whitbourn R., Sobotka P.A., Sadowski J., Bartus K. et al. Catheter-based renal sympathetic denervation for resistant hypertension: a multicentre safety and proof-of-principle cohort study // Lancet. — 2009. — Vol. 373. — P. 1275–281.
16. Mancia G., Schmieder R.E., Redon J., Grassi G., Kjeldsen S.E., Narkiewicz K., Parati G., Ruilope L., van de Borne P., Tsioufis C; European Society of Hypertension. Updated ESH position paper on interventional therapy of resistant hypertension // EuroIntervention. — 2013. — Vol. 9, Suppl. — R: R58–66.
17. Mahfoud F., Cremers B., Janker J., Link B., Vonend O., Ukena C., Linz D., Schmieder R., Rump L.C., Kindermann I., Sobotka P.A., Krum H., Scheller B., Schlaich M., Laufs U., Böhm M. Renal hemodynamics and renal function after catheter-based renal sympathetic denervation in patients with resistant hypertension // Hypertension. — 2012. — Vol. 60(2). — P. 419.
18. Papademetriou V., Tsioufis C.P., Sinhal A., Chew D.P. Meredith I.T., Malaiapan Y., Worthley M.I., Worthley S.G. Catheter-Based Renal Denervation for Resistant Hypertension: 12–Month Results of the EnligHTN I First-in-Human Study Using a Multielectrode Ablation System // Hypertension. — 2014. — Vol. 64(3). — P. 565–572.
19. Schlaich M.P., Sobotka P.A., Krum H., Whitbourn R., Walton A., Esler M.D. Renal denervation as a therapeutic approach for hypertension: novel implications for an old concept // Hypertension. — 2009. — Vol. 54. — P. 1195–1201.
20. Schuck O., Marusova L., Lanska V. Use of the Cocroft and Gault formula for evaluation of 24-hour urinary excretion of electrolytes // Bratisl. Lek. Listy. — 1999. — Vol. 100(8). — P. 422–425.
21. Simplicity HTN-1 Investigators 2011. Catheter-based renal sympathetic denervation for resistant hypertension: durability of blood pressure reduction out to 24 months // Hypertension. — 2011. — Vol. 57. — P. 911–17.
22. Simplicity HTN-2 Investigators, Esler M.D., Krum H., Sobotka P.A., Schlaich M.P., Schmieder R.E., Böhm M. Renal sympathetic denervation in patients with treatment-resistant hypertension (The Symplicity HTN-2 Trial): a randomised controlled trial // Lancet. — 2010. — Vol. 376. — P. 1903–1909.
23. Stea F., Bozec E., Millasseau S., Khettab H., Boutouyrie P., Laurent S. Comparison of the Complior Analyse device with Sphygmocor and Complior SP for pulse wave velocity and central pressure assessment // J. Hypertens. — 2014. — Vol. 32(4). — P. 873–880.
24. Zhang Y., Zhang X., Liu L., Zanchetti A. Is a systolic blood pressure target < 140 mmHg indicated in all hypertensives? Subgroup analyses of findings from the randomized FEVER trial // Eur. Heart J. — 2011. — Vol. 32. — P. 1500–1508.
25. Worthley S.G., Tsioufis C.P., Worthley M.I., Sinhal A., Chew D.P., Meredith I.T., Malaiapan Y., Papademetriou V. Safety and efficacy of a multi-electrode renal sympathetic denervation system in resistant hypertension: the EnligHTN I trial // Eur. Heart J. — 2013. — Vol. 34(28). — P. 2132–2140.

/30/30.jpg)
/32/32.jpg)
/32/32_2.jpg)
/33/33.jpg)
/34/34.jpg)
/34/34_2.jpg)
/35/35_2.jpg)
/35/35.jpg)