Журнал «» 4 (36) 2014
Вернуться к номеру
Оптимизация лечения пациентов с ишемической болезнью сердца и сопутствующей патологией. Реалии сегодняшнего дня
Авторы: Селюк М.Н., Козачок Н.Н. - Украинская военно-медицинская академия, г. Киев; Селюк О.В. - Ирпенский военный госпиталь
Рубрики: Кардиология
Разделы: Справочник специалиста
Версия для печати
В обзоре представлена современная тактика ведения пациентов с ишемической болезнью сердца в различных клинических ситуациях. Рассмотрены стандарты лечения данной нозологии, представлены некоторые положения новых Европейских рекомендаций по реваскуляризации миокарда (2014). Внимание авторов акцентировано на медикаментозной терапии, направленной на предупреждение развития как фатальных, так и нефатальных осложнений. Рассматриваются вопросы эффективности и безопасности основных лекарственных средств для лечения ишемической болезни сердца. Особое внимание уделено пациентам с коморбидными состояниями. Сделан акцент на анализе приверженности к лечению как одного из основных факторов залога успешной терапии.
В огляді подана сучасна тактика ведення пацієнтів із ішемічною хворобою серця в різних клінічних ситуаціях. Розглянуто стандарти лікування цієї нозології, наведені деякі положення нових Європейських рекомендацій із реваскуляризації міокарда (2014). Увагу авторів акцентовано на медикаментозній терапії, спрямованій на запобігання розвитку як фатальних, так і нефатальних ускладнень. Розглядаються питання ефективності та безпеки основних лікарських засобів для лікування ішемічної хвороби серця. Особливу увагу приділено пацієнтам із коморбідними станами. Зроблений акцент на аналізі прихильності до лікування як одного з основних чинників успішної терапії.
The review presented modern management of patients with coronary heart disease in different clinical situations. The authors considered standards of treatment for this nosology, presented some of the provisions of new European guidelines on myocardial revascularization (2014). Attention of the authors is focused on a drug therapy aimed at preventing the development of both fatal and non-fatal complications. The questions of the efficacy and safety of essential medicines for the treatment of coronary heart disease are considered. Particular attention is given to patients with comorbid conditions. Emphasis was made on the analysis of adherence to treatment as one of the main factors of successful therapy.
ишемическая болезнь сердца, стандарты лечения, группы риска, медикаментозное лечение, реваскуляризация, рациональная фармакотерапия.
ішемічна хвороба серця, стандарти лікування, групи ризику, медикаментозне лікування, реваскуляризація, раціональна фармакотерапія.
coronary heart disease, treatment standards, risk groups, medication, revascularization, rational pharmacotherapy.
Статья опубликована на с. 67-74
Ишемическая болезнь сердца (ИБС) является одним из самых частых заболеваний в клинической практике. Широкая распространенность данной нозологии во всем мире в различных возрастных группах дает основания ВОЗ характеризовать ИБС как эпидемию ХХ–ХХI веков. Считается, что именно ИБС является одной из ведущих причин потери трудоспособности и летальности населения в большинстве стран мира. В Украине, согласно материалам ежегодного отчета о состоянии здоровья и санитарно–эпидемиологической ситуации в стране, в структуре смертности также лидируют сердечно-сосудистые заболевания. На их долю приходится 65,8 % всех случаев смерти. Несмотря на то что уровень заболеваемости несколько снизился и на первом месте по данному показателю стоят заболевания органов дыхания (42,2 %), по распространенности сердечно-сосудистые заболевания остаются по-прежнему на первом месте. Наивысшие показатели в г. Киеве и Киевской области, Винницкой и Днепропетровской областях.
Распространенность ИБС зависит от возраста и пола. Так, в возрастной группе 45–54 лет заболевание доминирует у мужчин, а в группе 65–74 лет — у женщин. До инфаркта миокарда стенокардию напряжения отмечают у 20 % пациентов, после перенесенного инфаркта миокарда — у 50 % больных. Необходимо помнить, что в большинстве случаев встречается сочетание ишемической болезни сердца и артериальной гипертензии (АГ). Так, в 2010 г. распространенность комбинации АГ и ИБС среди взрослого населения Украины составляла 63,3 % случаев, а заболеваемость — 58,8 %. По сравнению с 1999 г. данные показатели выросли соответственно на 25,1 (с 50,3 до 63,3 %) и 29,8 % (с 45,3 до 58,8 %) [1].
Исходя из этого, ИБС и АГ следует рассматривать как ведущий фактор риска развития кардиальной и цереброваскулярной патологии, который существенно влияет на продолжительность жизни населения Украины.
Сегодня клиницисты в своей работе по ведению пациентов с ИБС и АГ руководствуются новыми европейскими рекомендациями (ИБС, АГ — 2013), национальными рекомендациями и приказами, в которых отображены все новейшие взгляды на диагностику и лечение данных нозологий.
Ведущими причинами ишемической болезни сердца являются атеросклероз коронарных сосудов, гиперкатехолемия, нарушения в свертывающей, антисвертывающей системах крови и недостаточное развитие коллатерального кровообращения. Все это приводит к развитию дисбаланса между доставкой кислорода к кардиомиоцитам и потребностью в нем. Потребность миокарда в кислороде определяется напряжением миокардиальной стенки, частотой сердечных сокращений и сократимостью миокарда.
Клинически стенокардия проявляется болью в грудной клетке сжимающего, давящего характера или чувством дискомфорта. Боль чаще всего локализуется за грудиной и иррадиирует в левую руку, шею, нижнюю челюсть, эпигастральную область.
К основным факторам, провоцирующим боль в груди, относят:
— физическую нагрузку (ФН): быструю ходьбу, подъем в гору или по лестнице, перенос тяжестей;
— повышение артериального давления (АД);
— холод;
— обильный прием пищи;
— эмоциональный стресс.
Обычно боль проходит в покое через 3–5 мин или в течение нескольких секунд или минут после сублингвального приема нитроглицерина в виде таблеток или спрея.
Боль, которая сохраняется более 20 минут (при этом исключен острый коронарный синдром — ОКС), следует дифференцировать с другими кардиалгиями (табл. 1).
Для верификации диагноза и принятия решения о тактике лечения пациентов проводят ряд исследований. В современных рекомендациях по обследованию пациентов с подозрением на ИБС предлагается алгоритм поэтапного подхода к ведению больного, состоящий из трех шагов (табл. 2). Начинают с определения индивидуальной претестовой вероятности заболевания (шаг 1) [2].
Белые клетки в табл. 2 соответствуют низкой претестовой вероятности ИБС — < 15 %. Больные с такими показателями не требуют дальнейшего тестирования на ИБС.
Светло-серые клетки — средне-низкая претестовая вероятность ИБС (15–65 %). В таких случаях для первичной диагностики может быть использован тест с дозированной физической нагрузкой (ДФН). Но более информативными будут неинвазивные тесты для выявления ишемии с визуализацией миокарда. Молодым пациентам рекомендованы радиологические методы диагностики.
Темно-серые клетки соответствуют средне-высокой претестовой вероятности ИБС (66–85 %). Для подтверждения диагноза ИБС у данной категории пациентов рекомендованы неинвазивные функциональные тесты с визуализацией.
Черные клетки — высокая претестовая вероятность ИБС — > 85 %. В таких случаях предполагается, что у пациентов имеется стабильная ИБС. Они нуждаются только в стратификации риска.
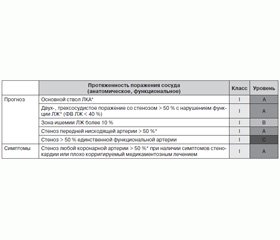
При наличии тяжелой симптоматики возможна ранняя инвазивная коронарография с соответствующим подтверждением гемодинамической значимости стеноза (измерения фракционного резерва кровотока — fractional flow reserve — ФРК) и последующей реваскуляризацией без предварительного проведения неинвазивного тестирования (шаги 2 и 3).
Осенью 2014 года вышли новые европейские рекомендации по реваскуляризации миокарда, в которых суммированы все последние положення по инвазивному лечению разных групп пациентов. В данных рекомендациях четко регламентированы показания для тех или иных методов исследования пациентов с подозрением/наличием ИБС в зависимости от уровня риска заболевания. Так, при низком уровне (< 15 %) не требуется проведения коронарографии, магнитно-резонансной томографии (МРТ), компьютерной томографии (КТ), позитронно-эмиссионной томографии (ПЭТ), стресс-ЭхоКГ, стресс-МРТ. Для пациентов со средним уровнем риска (до 85 %) для верификации диагноза проводят ядерную томографию, стресс-ЭхоКГ, стресс-МРТ. И для пациентов высокого риска (более 85 %) оптимальной считается коронарография [3]. Среди лабораторных тестов для всех больных сегодня рекомендуются следующие:
/69/69.jpg)
1. Определение уровней липидов натощак, включая общий холестерин, липопротеиды низкой и высокой плотности, триглицериды.
2. Гликемия натощак.
3. Общий анализ крови, включая определение гемоглобина и лейкоцитарной формулы.
4. Печеночные пробы.
5. Определение уровня креатинина с вычислением скорости клубочковой фильтрации (СКФ).
При наличии клинических показаний:
1. Выявление маркеров повреждения миокарда (тропонин T, I) при наличии признаков нестабильности или острого коронарного синдрома.
2. Определение показателей функции щитовидной железы.
3. Пероральная проба с нагрузкой глюкозой.
Далее рекомендуется проводить инструментальные исследования:
— электрокардиографию (ЭКГ);
— эхокардиографию (ЭхоКГ);
— нагрузочные тесты;
— стресс-визуализирующие исследования;
— коронароангиографию (КАГ);
— сцинтиграфию миокарда;
— однофотонную позитронно-эмиссионную компьютерную томографию миокарда (ОПЭКТ);
— компьютерную томографию.
Как уже говорилось ранее, в ряде клинических случаев требуется проведение проб с физической нагрузкой. Основными показаниями к проведению нагрузочных проб являются:
— дифференциальная диагностика ИБС и отдельных ее форм;
— определение индивидуальной толерантности к ФН (ТФН) у больных с установленным диагнозом ИБС и уточнение ФК стенокардии;
— оценка эффективности лечебных мероприятий;
— экспертиза трудоспособности;
— оценка прогноза;
— оценка эффективности антиангинальных препаратов.
В то же время необходимо учитывать противопоказания к проведению пробы с ДФН. Абсолютными противопоказаниями к проведению данного теста являются:
— острая стадия ИМ в течение 7 дней от его начала;
— нестабильная стенокардия;
— острое нарушение мозгового кровообращения;
— острый тромбофлебит;
— тромбоэмболия легочной артерии;
— СН III–IV ФК согласно классификации Нью-Йоркской ассоциации сердца (NYHA);
— выраженная легочная недостаточность, лихорадка.
При наличии тяжелой симптоматики возможна ранняя инвазивная коронарография с соответствующим подтверждением гемодинамической значимости стеноза (измерение фракционного резерва кровотока) и последующей реваскуляризацией без предварительного проведения неинвазивного тестирования.
Стратегия лечения заключается в восстановлении баланса между потребностью в кислороде и объемом его доставки к миокарду. Сначала ставятся симптоматические задачи, а затем решаются задачи предотвращения клинических осложнений и обострений болезни, уменьшения числа и сроков госпитализации. Целью медикаментозной терапии является улучшение прогноза — за счет снижения риска сердечно-сосудистых осложнений и улучшение качества жизни больных — за счет снижения частоты или устранения ангинозных приступов.
Согласно новым рекомендациям по реваскуляризации миокарда, данный метод лечения при стабильной ИБС рекомендован в основном для ослабления симптомов, и только при выраженных изменениях коронарных артерий и низком показателе фракционного резерва кровотока данный метод лечения улучшает прогноз [3].
Таким образом, в большинстве случаев пациентам со стабильной ИБС проводится медикаментозное лечение. Одним из препаратов, существенно влияющих на прогноз заболевания, является ацетилсалициловая кислота (АСК). Известная человечеству как лечебное средство еще со времен Гиппократа, вошедшая в кардиологию более 110 лет назад, АСК и сегодня лидирует в предупреждении самых грозных осложнений, продлевая жизнь пациентам.
Ацетилсалициловая кислота быстро всасывается в желудке и тонком кишечнике, период ее полувыведения составляет не более 15–20 мин. Концентрация АСК в плазме крови достигает пика через 30–40 мин, а подавление функции тромбоцитов наблюдается через 1 час после приема. При этом антитромботическое действие АСК сохраняется в интервале от 24 до 48 часов после приема, благодаря чему препарат можно назначать 1 раз в сутки.
Механизм действия АСК связан с ингибированием циклооксигеназы-1 (ЦОГ-1) и угнетением синтеза простагландинов (ПГ) [4–6]. В результате угнетения ЦОГ-1 происходит блокада синтеза ТХА2, которая сохраняется на протяжении 7–10 дней, т.е. всего периода жизни тромбоцита. При использовании низких доз АСК происходит значимое угнетение синтеза ТХА2 и в небольшой степени ингибируется образование ПГЕ2, который является цитопротектором слизистой оболочки желудочно-кишечного тракта (ЖКТ), и таким образом уменьшается локальный ульцерогенный эффект [6].
Среди дополнительных свойств АСК важную роль играют механизмы усиления фибринолиза и снижения свертывания крови. Также АСК нарушает процесс превращения фибриногена в фибрин, что препятствует образованию тромба. Под действием АСК разрыхляются нити фибрина, что облегчает доступ к ним активаторов плазминогена, вызывающих их лизис. Еще одно очень важное свойство АСК — это стабилизация атероматозной бляшки путем угнетения провоспалительных цитокинов (фактора некроза опухоли b и интерлейкина (ИЛ) 1b, ИЛ–8) [6, 7].
Многочисленные исследования влияния низких доз АСК на развитие осложнений показали высокую эффективность и хорошую переносимость этого препарата.
На сегодня можно смело утверждать, что АСК — идеальный антитромботический препарат для широкого круга пациентов. Так, в результате крупных исследований было показано, что АСК среди всех антитромбоцитарных препаратов имеет наибольшую доказательную базу. Проведенный в 2006 году группой ученых, возглавляемой J. Berger, метаанализ шести рандомизированных исследований по изучению эффективности АСК у 9853 больных со стабильными сердечно-сосудистыми заболеваниями, в том числе перенесенным инфарктом миокарда, стабильной стенокардией или инсультом/транзиторной ишемической атакой в анамнезе, показал, что при применении АСК риск сосудистых событий снизился на 21 %, в том числе нефатального инфаркта миокарда — на 26 %, инсульта — на 25 % и смерти от любых причин — на 13 % [8]. Очень важным свойством АСК является то, что применение данного препарата после коронарной ангиопластики снижает риск сердечно-сосудистых осложнений (ССО) на 53 % [6].
Также отмечено и снижение риска серьезных ССО на 23 % при лечении больных с облитерирующими заболеваниями периферических сосудов на фонe дoбавления АСК [9, 10].
Важная роль АСК в профилактике осложнений у пациентов с артериальной гипертензией (АГ) на сегодняшний день не вызывает сомнения. Подтверждением этого являются рекомендации по лечению АГ, УОК, ESH/ESC 2013 г., согласно которым АСК следует назначать больным с контролируемой АГ и нарушением функции почек или высоким сердечно-сосудистым риском.
Первичная профилактика ССЗ одно время подвергалась сомнениям. Но в 2009 г. U.S. Preventive Services Task Force (USPSTF) после дополнительного анализа включила АСК в перечень рекомендаций по первичной профилактике [11]. Согласно этим документам, АСК в качестве первичной профилактики сердечно-сосудистых заболеваний следует назначать (USPSTF):
— мужчинам в возрасте от 45 до 79 лет для снижения риска развития ИМ;
— женщинам в возрасте от 55 до 79 лет для снижения риска ишемического инсульта.
В качестве первичной профилактики ишемического инсульта АНА (2006) рекомендует прием АСК пациентам группы высокого риска (10–летний риск сердечно-сосудистых событий — 6–10 %). U.S. Preventive Services Task Force рекомендует АСК в качестве первичной профилактики мужчинам в возрасте 45–79 лет и женщинам в возрасте 55–79 лет при 10-летнем риске развития ИБС 3–12 % [12].
Американская диабетическая ассоциация (American Diabetes Association) рекомендует АСК для первичной профилактики больным СД старше 40 лет при наличии одного фактора риска (ФР) [13].
Таким образом, в соответствии с современными рекомендациями, базирующимися на данных крупных рандомизированных исследований, АСК рекомендована:
— для лечения и вторичной профилактики тромботических осложнений у больных с клиническими проявлениями атеросклероза (ИМ, нестабильная и стабильная стенокардия, чрескожная реваскуляризация миокарда, шунтирование коронарных артерий, ишемический инсульт и преходящие нарушения мозгового кровообращения, атеросклероз периферических артерий и др.);
— для первичной профилактики ИМ у больных высокого риска;
— при фибрилляции предсердий у больных с умеренным риском развития тромбоэмболических осложнений или при противопоказаниях к назначению антикоагулянтов непрямого действия (АКНД);
— при ревматическом митральном стенозе (если не используются АКНД);
— дополнительно к АКНД у отдельных больных с механическими искусственными клапанами сердца.
Однако успех АСК несколько омрачает активно обсуждаемая в последние годы проблема резистентности.
К причинам резистентности относят:
— фармакодинамические взаимодействия АСК с нестероидными противовоспалительными препаратами;
— наличие нетромбоцитарных источников синтеза тромбоксанов А2;
— экспрессию ЦОГ-2 во вновь образующихся тромбоцитах;
— гидролиз аспирина эстеразами слизистой оболочки ЖКТ;
— повышенный синтез тромбоксана А2;
— гиперлипидемию;
— анемию;
— мальабсорбцию;
— стресс, физические нагрузки, курение;
— генетические особенности.
Выделяют клиническую и биохимическую аспиринорезистентность. Биохимическая резистентность — это неспособность АСК уменьшать агрегацию тромбоцитов. Клиническая резистентность — это развитие острых сердечно–сосудистых катастроф на фоне приема препарата. Считается, что биохимическая резистентность не корригируется увеличением дозы АСК. Также в ряде работ подчеркивается, что не всегда биохимическая резистентность коррелирует с клинической [14].
В настоящее время предложено несколько тестов, позволяющих оценить антиагрегационный эффект АСК in vivo, с использованием индукции аденозиндифосфатом (АДФ) либо с помощью анализатора функции тромбоцитов PFA-100 [15].
Как показали более тщательные исследования, у большинства пациентов с так называемой резистентностью к АСК причиной данного феномена была плохая приверженность к лечению. В случаях, когда прием аспирина осуществляется под наблюдением медицинского персонала или родственников, распространенность аспиринорезистентности значительно уменьшается [16].
В качестве индуктора агрегации в данных тестах применяется АДФ. Необходимо помнить, что специфическими блокаторами рецепторов к АДФ являются тиенопиридины, тогда как аспирин первично воздействует на метаболизм арахидоновой кислоты.
Таким образом, использование АДФ в качестве индуктора является более специфичным для контроля эффектов тиенопиридинов и, соответственно, недостаточно объективно будет отображать дезагрегационные возможности АСК. С учетом данных особенностей на сегодняшний день считается, что тестирование функции тромбоцитов при использовании АСК не является обязательным [17].
Вторым вопросом является безопасность применения препарата. Уже давно доказано, что риск развития побочных эффектов зависит от дозы АСК.
Поражения ЖКТ, развивающиеся на фоне приема АСК, обусловлены ингибированием ЦОГ-1, снижением синтеза простагландинов слизистой желудка, нарушением защитных и репаративных процессов в эпителии (системное действие), а также местным воздействием лекарства. Частота возникновения данных осложнений прямо пропорционально зависит от принимаемой дозы препарата.
Выполненный V.L. Serebruany и соавторами (2005) метаанализ 31 клинического исследования с участием > 192 000 пациентов показал, что терапия АСК в дозе < 100 мг/сут связана с более низким риском кровотечений. Согласно рекомендациям Консенсуса по использованию антитромбоцитарных препаратов, польза терапии АСК значительно превышает риск развития желудочно-кишечных кровотечений, что дает основание для применения АСК в ходе первичной и вторичной профилактики ССЗ (Weisman S.M., Graham D.Y., 2002; Михайлова И.Е., Перепеч Н.Б., 2007; Терещенко С.Н., Джаиани Н.А., 2008).
Вторым препаратом, который обязательно назначается практически всем больным с кардиоваскулярными заболеваниями, является бисопролол. Благодаря своей уникальной фармакокинетике и фармакодинамике бисопролол является лидером среди бета-адреноблокаторов. По сравнению с другими бета-адреноблокаторами бисопролол обладает очень высокой степенью селективности к b1-адренорецепторам [18]. Индекс b1-селективности у бисопролола составляет 1 : 75, в то время как у метопролола — только 1 : 20. Кроме того, препарат не обладает симпатомиметической активностью.
Высокая биодоступность бисопролола, которая не зависит от приема пищи, также гарантирует успех лечения данным препаратом. Период полувыведения бисопролола составляет примерно 10–12 часов, пик действия наступает через 2–4 часа после приема, а продолжительность эффекта сохраняется в течение 24 часов, благодаря чему бисопролол можно назначать 1 раз в сутки [19].
Бисопролол на 50 % метаболизируется в печени, еще 50 % выводится почками в неизмененном виде [20, 21].
Лишь при выраженной почечной недостаточности требуется коррекция его дозы.
Очень важно, что бисопролол не вступает в клинически значимые лекарственные взаимодействия с такими препаратами, как сердечные гликозиды, метилдопа, резерпин и гуанфацин, блокаторы медленных кальциевых каналов (верапамил и дилтиазем), и не изменяет активность варфарина [21].
Благодаря своей высокой эффективности и хорошей переносимости бисопролол широко применяется в кардиологической практике для лечения практически всех нозологий: артериальной гипертензии, всех форм ишемической болезни сердца — острого инфаркта миокарда, стабильной и нестабильной стенокардии, тахиаритмий, фибрилляции предсердий, хронической сердечной недостаточности (ХСН) даже на фоне хронических обструктивных заболеваний легких (ХОЗЛ).
Необходимо подчеркнуть, что именно сердечная недостаточность — одно из наиболее тяжелых кардиоваскулярных осложнений, требующее тщательного подбора не только препарата, но и дозы. И только 4 препарата из группы бета-адреноблокаторов можно применять в данной ситуации. Но намного сложнее, когда имеется сопутствующая патология. На сегодня такое заболевание, как ХОЗЛ, занимает 4-е место в структуре смертности как в Украине, так и в большинстве стран мира. При наличии СН и сопутствующего ХОЗЛ, согласно европейским рекомендациям 2012 года, можно применять только три b-блокатора (бисопролол, небиволол и метопролола сукцинат). Об этом необходимо помнить, назначая лечение таким пациентам.
Бисопролол имеет самую большую доказательную базу переносимости и эффективности при большом спектре нозологий.
Его эффективность при АГ была продемонстрирована в ряде клинических исследований [22, 23].
У больных с мягкой и умеренной АГ при приеме 1 раз/сут бисопролол снижает АД на 15–20 %. В исследованиях с проведением повторных мониторирований АД в стационаре в условиях стандартного двигательного режима, избранного для каждого больного, бисопролол в дозе 10 мг 1 раз/сут оказывал наиболее плавный антигипертензивный эффект в течение суток по сравнению с метопрололом или пропранололом, которые назначали 2 раза/сут. Что касается динамики диастолического АД (ДАД), то отношение конечного эффекта к пиковому составило для бисопролола 91,2 %. Считается, что минимальное значение этого показателя для обеспечения плавного антигипертензивного эффекта в течение суток составляет 50 %.
В лечении ИБС бисопролол стоит в разделе «Влияние на симптомы», однако необходимо помнить, что в 63 % случаев ИБС сочетается с АГ и очень часто мы имеем дело с больными, у которых есть признаки СН. И уже когда мы видим перед собой реального больного, мы понимаем, что бисопролол влияет на прогноз, т.е., назначив этот препарат, мы продлеваем жизнь нашему больному [3].
Антиангинальное действие бисопролола при лечении ИБС получило подтверждение прежде всего в многоцентровом клиническом исследовании TIBBS, в котором было доказано, что данный препарат эффективно устраняет эпизоды ишемии миокарда у больных стабильной стенокардией [24].
Бисопролол способствует повышению толерантности к физической нагрузке намного эффективнее атенолола и метопролола. Также при сравнении этих препаратов было выявлено, что бисопролол в значительно большей степени улучшает качество жизни больных, снижает тревожность и утомляемость. Бисопролол уменьшает сердечно-сосудистую летальность и риск развития фатального ИМ у больных высокого риска, подвергаемых кардиохирургическим вмешательствам.
Более 40 лет БАБ относятся к отдельному классу антиаритмических препаратов и активно применяются при различных нарушениях сердечного ритма. Бисопролол используется для лечения синусовой тахикардии, суправентрикулярных нарушений ритма сердца, в частности при мерцательной аритмии для контроля ЧСС и для уменьшения количества желудочковых экстрасистол. При фибрилляции предсердий бисопролол способствует удержанию синусового ритма после электрической кардиоверсии [25, 26], а также оказывает профилактическое воздействие на частоту возникновения пароксизмов [27].
Как уже говорилось ранее, бисопролол — один из немногих бета-адреноблокаторов, рекомендованных для лечения ХСН. Крупные исследования, такие как CIBIS, CIBIS-II и CIBIS-III, доказали высокую эффективность бисопролола в терапии ХСН [28]. В последнее время у больных сердечно-сосудистыми заболеваниями нередко выявляется сахарный диабет. Было показано, что бисопролол не влияет на уровень глюкозы крови, при его приеме не требуется коррекции дозы пероральных антидиабетических препаратов. Бисопролол не влияет на уровень тиреоидных гормонов при гипертиреоидных состояниях, не вызывает гипокалиемию. Литературные данные свидетельствуют об отсутствии отрицательного влияния на липидный спектр у пациентов, принимающих бисопролол в течение длительного времени [29, 30].
При сравнительном изучении различных БАБ было доказано, что атенолол и метопролол снижают чувствительность к инсулину примерно на 25 %, пропранолол — на 30 %, а бисопролол увеличивает на 10 % [31]. Также были развеяны опасения насчет отрицательного влияния бисопролола на липидный обмен. Было доказано, что бисопролол не оказывал негативного влияния на общий холестерин и триглицериды, а уровень липопротеидов высокой плотности при его применении достоверно возрастал на 9 % [32].
Таким образом, бисопролол — препарат с доказанной эффективностью и безопасностью для пациентов с ИБС и сопутствующими сердечно–сосудистыми состояниями.
Благодаря бисопрололу нам удается продлить жизнь пациента, предотвратить осложнения и улучшить качество жизни нашему больному.
Остается вопрос комплайентности. Всегда проще добиться приверженности к лечению, если количество принимаемых лекарственных средств минимально, а прием однократный в сутки. На сегодня отечественным врачам представилась уникальная возможность реализовать оптимальную схему лечения. На рынке Украины появился единственный комбинированый препарат, в состав которого входит АСК и бисопролол — Кординорм® Плюс. Кординорм® Плюс имеет две различные дозировки: бисопролол 5 мг/АСК 75 мг и бисопролол 10 мг/АСК 75 мг.
Кординорм® Плюс был создан в Великобритании после тщательного изучения вопроса о наиболее назначаемых препаратах для лечения пациентов с кардиоваскулярной патологией. Так как и бисопролол, и АСК имеют наибольшую доказательную базу, являются препаратами первого выбора при различных клинических ситуациях, то и назначались эти два лекарственных средства в максимальном количестве случаев. Чтобы упростить схему лечения и увеличить приверженность к проводимой терапии, ученые Великобритании разработали комбинированный препарат, в состав которого входят бисопролол и АСК. Число назначений комбинации неуклонно растет каждый год. Именно поэтому препарат Кординорм® Плюс находит широкое применение в клинической практике. Данная комбинация в странах Европы применяется при стабильной и нестабильной ИБС, ФП, АГ, у пациентов с сопутствующим СД 2-го типа, при КМП, при СН даже на фоне ХОЗЛ, для профилактики ишемических инсультов [33]. Кординорм® Плюс позволяет добиться большей приверженности пациентов к лечению и, соответственно, сократить число как фатальных, так и нефатальных кардиоваскулярных осложнений.
Бытующее мнение, что активные вещества, входящие в состав препарата, должны назначаться в разное время суток, не нашло широкого подтверждения в клинической практике. Работы, на которых основывались данные взгляды, не легли в основу рекомендаций, именно поэтому ни в одном из случаев (будь то рекомендации или циркуляр по приему препарата) врачи не найдут регламентированного времени приема. Аргументы в пользу лучшего всасывания в определенное время суток не подтверждаются, так как всасывание сугубо индивидуально и зависит от ряда дополнительных факторов. Что касается времени максимальной агрегации тромбоцитов, то при постоянной терапии, когда больной не пропускает прием лекарственного средства, концентрация активного вещества в плазме сохраняется на терапевтическом уровне без каких-либо колебаний, воздействуя на патогенетическое звено тромбообразования в течение суток.
Таким образом, удобство приема, эффективность и безопасность препарата Кординорм® Плюс дают возможность назначать его очень широкому кругу пациентов. Прием лекарственного средства один раз в сутки и максимальное воздействие на многие звенья патогенеза ИБС, АГ, СН, ФП выведет Кординорм® Плюс в лидеры среди кардиологических препаратов.
1. Щорічна доповідь про стан здоров’я населення, санітарно-епідемічну ситуацію та результати діяльності системи охорони здоров’я України 2012 р. / За ред. Р.В. Богатирьової. — К., 2013. — 464 с.
2. 2013 ESC guidelines on the management of stable coronary artery disease // European Heart Journal. — 2013. — 34. — 2949–3003.
3. 2014 ESC/EACTS Guidelines on myocardial revascularization // Eur. Heart J. — 2014. doi: 10.1093
4. Vane J.R. Inhibition of prostaglandin synthesis as a mechanism of action of aspirin-like drug // Nature (New Biol.). — 1971. — Vol. 231. — P. 232–235.
5. Smith J.H., Willis A.L. Aspirin selectively inhibits prostaglandin production in human platelets // Nature (New Biol.). — 1971. — Vol. 231. — P. 235–237.
6. Бубнова М.Г. Аспирин в профилактике атеротромбоза и коронарной болезни сердца // Российский кардиологический журнал. — 2010. — № 4 (84). — С. 115–121.
7. Воскобой В.И., Ребров А.П. Влияние антиагрегантов на концентрацию цитокинов плазмы крови у больных с острым коронарным синдромом // Клиническая медицина. — 2003. — Т. 81, № 6. — С. 23–28.
8. Berger J. Low-dose aspirin in patients with stable cardiovascular disease: a meta-analysis / J. Berger, D. Brown, R. Becker // Am. J. Med. — 2006. — — Vol. 121, № 1. — Р. 43–49.
9. Antithrombotic Trials Collaboration. Prevantion of death, myocardial infarction and stroke by antiplatelet therapy in high-risk patients // BMJ. — 2002. — Vol. 324. — P. 71–86.
10. Baigent C., Blackwell L., Collins R. et al. Antithrombotic Trialists (ATT) Collaboration. Aspirin in the primary and secondary prevention of vascular disease: collaborative meta-analysis of individual participant data from randomised trials // Lancet. — 2009. — Vol. 373 (9678). — P. 1849–1860.
11. Aspirin fоr the Prevention of Cardiovascular Disease. http://www.uspreventiveservicestaskforce.org/uspstf/uspsasmi.htm.
12. U.S. Preventive Services Task Force. Aspirin for the prevention of cardiovascular disease: U.S. Preventive Services Task Force. Recommendation statement // Ann. Intern. Med. — 2009. — Vol. 150 (6). — P. 396–404.
13. Бокарев И.Н. К 125-летию ацетилсалициловой кислоты // Рациональная фармакотерапия в кардиологии. — 2011. — № 7 (4). — С. 492–500.
14. Волков В.И., Рябуха В.В., Запровальная О.Е., Ладный А.И. Диагностика резистентности к аспирину у больных с ишемической болезнью сердца // Укр. кардіол. журн. — 2006. — № 3. — С. 36–39.
15. Patrono C., Rocca B. Феномен резистентности к антитромбоцитарным препаратам // Практична ангіологія. — 2008. — № 1. — С. 58–67.
16. Dalen J.E. Aspirin Resistance: Is it Real? Is it Clinically Significant? // Am. J. Med. — 2007. — 120, 1. — 1–4.
17. Gorog D.A., Fuster V. Platelet Function Tests in Clinical Cardiology. Unfulfilled Expectations // Am. Coll. Cardiol. — 2013. — 61. — 2115.
18. Baker J.G. The selectivity of beta-adrenoceptor antagonists at the human beta1, beta2 and beta3 adrenoceptors // Br. J. Pharmacol. — 2005. — Vol. 144 (3). — Р. 317–322.
19. Leopold G., Pabst J., Ungethum W. et al. Basic pharmacokinetics of bisoprolol, a new highly beta 1-selective adrenoceptor antagonist // J. Clin. Pharmacol. — 1986. — Vol. 26 (8). — Р. 616–621.
20. Horikiri Y., Suzuki T., Mizobe M. Pharmacokinetics and metabolism of bisoprolol enantiomers in humans // J. Pharm. Sci. — 1998. — Vol. 87 (3). — Р. 289–294.
21. Warrington S.J., Johnston A., Lewis Y. et al. Bisoprolol: studies of potential interactions with theophylline and warfarin in healthy volunteers // J. Cardiovasc. Pharmacol. — 1990. — Vol. 16, Suppl. 5. — Р. 164–168.
22. Лукина Ю.В., Марцевич С.Ю. Бисопролол — высокоселективный бета-адреноблокатор с позиции доказательной медицины // Рациональная фармакотерапия в кардиологии. — 2010. — № 6 (1). — С. 103–107.
23. Осадчий К.К. β-адреноблокаторы при артериальной гипертензии: фокус на бисопролол // Кардиология. — 2010. — № 1. — С. 84–89.
24. Von Arnim T. Medical treatment to reduce total ischemic burden: total ischemic burden bisoprolol study (TIBBS), a multicenter trial comparing bisoprolol and nifedipine. The TIBBS Investigators // J. Am. Coll. Cardiol. — 1995. — Vol. 25 (1). — Р. 231–23822.
25. Katritsis D.G., Panagiotakos D.B., Karvouni E. et al. Comparison of effectiveness of carvedilol versus bisoprolol for maintenance of sinus rhythm after cardioversion of persistent atrial fibrillation // Am. J. Cardiol. — 2003. — Vol. 92 (9). — Р. 1116–1119.
26. Plewan A., Lehmann G., Ndrepepa G. et al. Maintenance of sinus rhythm after electrical cardioversion of persistent atrial fibrillation; sotalol vs bisoprolol // Eur. Heart. J. — 2001. — Vol. 22 (16). — Р. 1504–1510.
27. Ishiguro H., Ikeda T., Abe A. et al. Antiarrhythmic effect of bisoprolol, a highly selective beta1-blocker, in patients with paroxysmal atrial fibrillation // Int. Heart J. — 2008. — Vol. 49 (3). — Р. 281–293.
28. A randomized trial of beta-blockade in heart failure. The Cardiac Insufficiency Bisoprolol Study (CIBIS). CIBIS Investigators and Committees // Circulation. — 1994 Oct. — Vol. 90 (4). — Р. 1765–1773.
29. Кукес В.Г., Остроумова О.Д., Батурина А.М., Зыкова А.А. β-блокаторы в лечении артериальной гипертонии у больных с сахарным диабетом: противопоказание или препараты выбора? // Русский медицинский журнал. — 2002. — № 10. — С. 446–449.
30. Остроумова О.Д. Возможности применения высокоселективных β-блокаторов у больных с сопутствующими заболеваниями // Русский медицинский журнал. — 2004. — Т. 12, № 12. — С. 721–725.
31. Lithell H.L. Effect of antihypertensive drugs on insulin, glucose and lipid metabolism // Diabetes Care. — 1991. — Vol. 14. — Р. 203–209.
32. Linen P. Biochemical mechanisms involved in the beta-blocker induced changes in serum lipoproteins // Am. Heurt J. — 1992. — Vol. 124. — Р. 549–556.
33. Bisoprolol and Aspirin fixed dose combination capsules clinical jverview prepared by Dr. J.S. McLay. — November 2010.

/68/68.jpg)
/70/70.jpg)