Журнал «Травма» Том 15, №5, 2014
Вернуться к номеру
Мультимодальна анестезія/аналгезія в комплексі анестезіологічного забезпечення протезування кульшового суглоба
Авторы: Гомон М.Л. - Вінницький національний медичний університет ім. М.І. Пирогова
Рубрики: Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
Проведено анестезіологічне забезпечення 45 хворих при тотальному та субтотальному протезуванні кульшового суглоба (3–4-й ступень операційного ризику за АSA), із яких у 23 випадках використовувалась спінальна анестезія (3,9 ± 0,1 мл 0,5% бупівакаїну), у 22 випадках — редукована (3,4 ± 0,1 мл 0,5% бупівакаїну) спіноперидуральна анестезія/аналгезія (0,25% бупівакаїном). Для зменшення резорбції неполімеризованого цементу використовували керовану гіпертензію титрованим мезатоном. Встановлено, що використання спіноперидуральної анестезії з редукцією дози спінального компонента та підвищення артеріального тиску в момент використання неполімеризованого цементу забезпечує менші коливання гемодинамічних показників протягом оперативного втручання порівняно зі спінальною анестезією. Наведена методика забезпечує достатню антиноцицептивну протекцію, характеризується малим токсичним впливом на пацієнта, вимагає меншого використання седативної, симпатоміметичної та інфузійної терапії. Рекомендовано широко використовувати методику редукованої спіноперидуральної анестезії/аналгезії та керованої гіпертензії при протезуванні кульшового суглоба.
Проведено анестезиологическое обеспечение 45 больных при тотальном и субтотальном протезировании тазобедренного сустава (3–4-я ст. операционного риска по АSA), из которых в 23 случаях использовалась спинальная анестезия (3,9 ± 0,1 мл 0,5% бупивакаина), в 22 случаях — редуцированная (3,4 ± 0,1 мл 0,5% бупивакаина) спиноперидуральная анестезия/аналгезия (0,25% бупивакаином). Для уменьшения резорбции неполимеризованного цемента использовали управляемую гипертензию титрованным мезатоном. Установлено, что использование спиноперидуральной анестезии с редукцией дозы спинального компонента и повышение артериального давления в момент использования неполимеризованного цемента обеспечивает меньшие колебания гемодинамических показателей в течение оперативного вмешательства по сравнению со спинальной анестезией. Данная методика обеспечивает достаточную антиноцицептивную протекцию, характеризуется малым токсическим воздействием на пациента, требует меньшего использования седативной, симпатомиметической и инфузионной терапии. Рекомендуется широко использовать методику редуцированной спиноперидуральной анестезии/аналгезии и управляемой гипертензии при протезировании тазобедренного сустава.
There was provided an anesthetic management of total and subtotal hip prosthetics in 45 patients with 3–4 degree of operation risk on ASA. There was used spinal anesthesia (3.9 ± 0.1 ml 0.5% bupivacaine) in 23 cases, reduced (3.4 ± 0.1 ml 0.5% bupivacaine) spinal peridural anesthesia (0.25% bupivacaine) in 22 cases. There was used controlled hypertension with 0,1% mesatonum for reduction of non-polymerized cement resorption. It was found that the use of spinal-epidural anesthesia whith reduced anesthetic spinal component dose and increasing blood pressure during the non-polymerized cement use provides less fluctuation of the hemodynamic parameters during surgery compared with spinal anesthesia. This technique provides better protection of antinociceptive effect, has low toxic action on the patient, results to the less use of sedative, sympathomimetic and infusion therapy. The technique of reduced spinal-epidural anesthesia/analgesia and controlled hypertension in hip prosthetics is widely recommended.
редукована спіноперидуральна анестезія/аналгезія, протезування кульшового суглоба.
редуцированная спиноперидуральная анестезия/аналгезия, протезирование тазобедренного сустава.
reduced spinal peridural anesthesia/analgesia, hip prosthetics.
Статья опубликована на с. 65-59
Вступ
Стратегія вибору анестезіологічного забезпечення протезування кульшового суглоба залежить від провідних факторів ризику, що можуть бути причиною несприятливого перебігу оперативного втручання. Найбільш малопрогнозованим є токсична реакція на цемент при використанні його для фіксації компонентів протеза. Важливим фактором ризику є малорухомий спосіб життя при недостатній функціі кульшового суглоба, часто — похилий вік пацієнта з наявністю супутніх захворювань, що є причиною нестабільної гемодинаміки та тромбоемболічних ускладнень [2, 3, 14]. Указані особливості — причини вибору різних варіантів анестезіологічного забезпечення. Наявність складної наркозно-дихальної апаратури в країнах Європи і США є причиною використання переважно загальної анестезії. Суттєвим обмеженням до використання наркозу є наявність супутніх захворювань серцево-судинної та дихальної систем, що загострюються після використання загальної анестезії. Перевагою загальної анестезії при протезуванні кульшового суглоба є превентивна протекція функції дихання та частково гемодинаміки на випадок виникнення токсичних реакцій на цемент. У нашій країні при анестезіологічному забезпеченні протезування кульшового суглоба віддають перевагу регіонарній анестезії — спінальній або подовженій перидуральній анестезії [6, 9, 12]. Слід відмітити відсутність єдиної позиції в перевазі якогось одного з методів анестезіологічного забезпечення. Спінальна анестезія технічно проста та забезпечує гарантовану антиноцицептивну протекцію шокової зони кульшового суглоба, однак створює умови прихованої гіповолемії, яка суттєво посилюється і є малокерованою при реакції на цемент чи розвитку серцевої недостатності. Подовжена перидуральна анестезія часто складновиконувана на деформованому хребті та не завжди забезпечує центральне положення катетера і рівномірний розподіл анестетика в деформованому перидуральному просторі, що є причиною складнодіагностованої в похилому віці мозаїчності та нестабільності анестезії. Однак суттєвою перевагою методики є її висока керованість, включаючи керований вплив на вираженість симпатичного блока, відповідно на гемодинаміку. Суттєвою перевагою подовженої перидуральної анестезії є можливість проведення післяопераційного знеболювання, що особливо важливо для ранньої активації хворих і профілактики тромбоемболічних ускладнень [5, 7, 11].
Відсутній єдиний підхід до профілактики та інтенсивної терапії токсичних реакцій на цемент. Найчастіше анестезіологи використовують розширення об’єму і якості інфузійної терапії, часто доводячи її до абсурдних цифр — 6–8 літрів. Незважаючи на активну стабілізацію гемодинаміки таким шляхом у хворих розвивається інтерстеційний набряк на відрізках мікроциркуляції, який приводить до низької ефективності відповіді а1-адренорецепторів на фармакологічні препарати при виникненні гіпотонії, особливо при токсичних гіпотоніях, що характеризуються збільшенням капілярної проникності. Несприятливим та досить малодослідженим є вплив волемічного інтерстиційного набряку на процеси заживлення в рані, що є важливим фактором для вираженості післяопераційного больового синдрому, ранньої активації та кінцевого результату лікування — протезування кульшового суглоба. Шлях збільшення об’єму інфузійної терапії часто відрізаний при субкомпенсованій супутній патології серця. Частина анестезіологів, які стояли біля початків анестезіологічного забезпечення протезування кульшового суглоба, вірять в адсорбуючі та профілактичні властивості колоїдних розчинів, плазми, альбуміну. Однак використання цих груп препаратів (особливо препаратів крові) як профілактичних не регламентовано фармакопеєю [1, 4, 12].
Наступним за частотою використання напрямком профілактики та лікування токсичних реакцій на цемент є застосування глюкокортикоїдів. У кожного анестезіолога існує свій погляд та схеми використання цієї групи препаратів. Більшість анестезіологів вірять в ефективність високих доз комбінації дексаметазону, преднізолону та гідрокортизону або продовжених глюкокортикоїдів. Однак світова доказова література не підтримує таку позицію. Звичайно, теоретично ніхто не заперечує стабілізуючу роль глюкокортикоїдів при токсичних і анафілактичних реакціях, очевидна їх профілактична роль при ризику реакції на цемент, проте використання великих доз малообґрунтовано. Достатньо часто при розвитку гіпотонії, після використання цементу, анестезіологи застосовують препарати симпатоміметичної дії. Частіше — мезатон, рідко — норадреналін, адреналін, дофамін. Слід відмітити, що ця група препаратів справляє суто симптоматичний ефект.
Таким чином, існує проблема вибору методики анестезії, яка мінімально впливає на гемодинаміку, забезпечує достатній антиноцицептивний захист під час протезування кульшового суглоба та в післяопераційному періоді, знижує ризики, а бажано і виникнення токсичної реакції на цемент при його використанні під час протезування кульшового суглоба [8, 10, 13].
Мета роботи: сформувати гемодинамічно стабільну, безпечну концепцію анестезіологічного забезпечення з урахуванням токсичної реакції на цемент при протезуванні кульшового суглоба.
Матеріали і методи
Проведений порівняльний аналіз перебігу мультимодальної анестезії/аналгезії в комплексі анестезіологічного забезпечення протезування кульшового суглоба у 45 хворих із 3–4-м ступенем операційного ризику за ASA. Хворі рандомізовані за віком, характером, обсягом, тривалістю оперативних втручань та розділені на 2 групи залежно від методики анестезіологічного забезпечення. У 1-й (контрольній) групі з 23 чоловік використана стандартна спінальна анестезія 3,9 ± 0,1 мл 0,5% бупівакаїну, у 2-й (дослідній) групі з 22 чоловік — редукована спіноперидуральна анестезія/аналгезія. Редукція дози спінального компонента становила 3,4 ± 0,1 мл 0,5% бупівакаїну, традиційну післяопераційну анестезію замінили на аналгезію 0,25% бупівакаїном.
Для статистичного аналізу вибрані показники динаміки середнього артеріального тиску (САТ), частоти серцевих скорочень (ЧСС). Як критерії адекватності перебігу анестезії порівнювали кількість використаних препаратів для симпатоміметичної підтримки, інфузійної та симптоматичної терапії, седації. Премедикацію проводили з обов’язковим включенням анксіолітиків.
Статистичну обробку результатів проводили з використанням методів параметричного аналізу. Для судження про вірогідність відмінностей між групами за аналізованим показником використовували t-критерій Стьюдента. Рівень вірогідності коефіцієнта оцінювали стандартним способом і вважали прийнятним при р < 0,05.
Результати та їх обговорення
Основною причиною використання редукованої спіноперидуральної анестезії/аналгезії замість традиційної спінальної анестезії було завдання зменшення негативного впливу останньої на вираженість симпатичного блоку і відповідно на ступінь депресії та керованість гемодинаміки. Зменшення симпатичного блока створило можливість зниження об’єму інфузійної терапії, підвищення ефективності симпатоміметиків та керованості гемодинаміки. Разом із тим паралельне використання редукованого спінального компонента та катетеризації перидурального простору дало можливість застосовувати для збільшення керованості анестезіологічним забезпеченням знижені концентрації бупівакаїну, що знову ж таки зменшило негативний вплив на гемодинаміку та підвищило керованість анестезії. Наступним результатом зниження симпатичного блока та підвищення ефективності та керованості симпатоміметиків є можливість створювати керовану нормотонію під час використання цементу. Вираженість гіпотонії хворого прямо пропорційна дозі неполімеризованого цементу, який за перші 1–3 хвилини потрапляє в судинне русло. В подальшому полімеризований цемент є інтактним і не має фізичної здатності до всмоктування. Кількість неполімеризованого цементу, що потрапляє в кровотік, пропорційна різниці тиску між компресією травматолога на тканини при утримуванні компонента протезу і САТ в судинному руслі. Якість постановки компонента протеза залежить від його прикріплення до кісткових структур, тому поверхня не повинна містити крові. Це досягається також за рахунок зниження САТ, як наслідок симпатичного блока спінальної анестезії, а при його недостатності за рахунок використання керованої гіпотонії, що зустрічається рідше лише при надлишковій інфузійній терапії. Таким чином, на момент постановки цементу створені оптимальні умови до його надходження в кровотік, а саме — знижений САТ та компресія тканин місця постановки компонента протеза. Для зменшення градієнта надходження неполімеризованого цементи в кровотік, використовуючи збільшення чутливості адренорецепторів до симпатоміметиків за рахунок запропонованої редукованої спіноперидуральної анестезії/аналгезії, відразу після компресії компонента протезу ми підвищували САТ на 20 % порівняно з вихідним за рахунок титрованих доз мезатону (0,1%), а при наявності брадикардії — комбінацією з атропіном або адреналіном. Використана методика мультимодальної анестезії/аналгезії в комбінації з керованою гіпертензією після фіксації компонентів протеза на цемент характеризувалась кращою ноцицептивною протекцією перебігу анестезіологічного забезпечення протезування кульшового суглоба порівняно із спінальною анестезією (табл. 1).
Так, після виконання спінальної анестезії через 30 хвилин відбулось зниження САТ у першій і другій групах до 84,3 ± 2,6 мм рт.ст. та 87,9 ± 2,3 мм рт.ст. відповідно. При цьому використання зниженої дози бупівакаїну в другій групі викликало невірогідне зниження САТ (87,9 ± 2,3 мм рт.ст.), тоді ж як у першій групі зниження було вірогідне. Аналіз коливання САТ протягом анестезії виявив в першій групі вірогідну тенденцію до гіпотонії (81,2 ± 1,5 мм рт.ст.), оскільки мінімальний САТ вірогідно знижувався порівняно з вихідним. Зниження САТ у першій групі також вірогідно було меншим порівняно з другою групою. У другій групі вірогідного зниження САТ порівняно з вихідним не виявлено. Аналіз стабільності гемодинаміки протягом анестезії показав вірогідні коливання між максимальним і мінімальним САТ лише в першій групі, чого не виявлено в другій групі. На кінець оперативного втручання вірогідних коливань САТ між групами не виявлено. Таким чином, використання редукованої спіноперидуральної анестезії/аналгезії та методики керованої гіпертензії під час застосування цементу забезпечило невірогідне від фізіологічних показників коливання САТ та більш стабільні показники порівняно із спінальною анестезією.
Порівняльна характеристика динаміки ЧСС є більш складна, оскільки перебіг основної частини анестезіологічного забезпечення відбувався на фоні часткового або повного збереження свідомості. Для зменшення впливу психоемоційного стресу використовували розширену премедикацію з залученням анксіолітиків та в емоційно лабільних пацієнтів застосовували седацію і медикаментозний сон протягом анестезії з вибірковим використанням сибазону, тіопенталу. Однак в обох групах досягнута рандомізація за вихідною ЧСС, оскільки даний стартовий показник ЧСС вірогідно не відрізнявся в 1-й та 2-й порівнюваних групах і становив 84,6 ± 4,2 уд/хв та 85,7 ± 4,7 уд/хв відповідно (табл. 1). Через 30 хвилин після виконання анестезії у першій групі встановлена вірогідна тенденція до зниження ЧСС відповідно до 63,7 ± 1,9 уд/хв, чого не виявлено в другій групі. Таким чином, адаптаційні механізми брадикардії, які характерні для швидкої симпатичної блокади при спінальній анестезії, були значно слабше виражені при використанні редукованої спіноперидуральної анестезії. Встановлено вірогідне зниження мінімальної ЧСС порівняно з вихідним показником протягом анестезії в обох групах, що свідчить про існування основного механізму дистрибуції між ємкістю судинного русла і об’ємом циркулюючої крові як при повному, так і частковому симпатичному блоці. Однак у другій групі він вірогідно менший за мінімальним показником ЧСС порівняно з першою групою. Крім того, у першій групі виявлено вірогідне коливання ЧСС між максимальним та мінімальним показником, чого не спостерігалось у другій групі. Таким чином, редукована спіноперидуральна анестезія/аналгезія та методика керованої гіпертензії під час використання цементу викликали менші компенсаторні коливання ЧСС порівняно із спінальною анестезією.
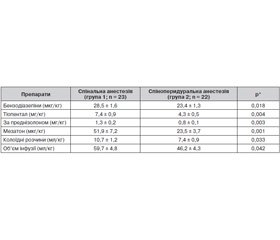
Частота використання медикаментозних засобів під час оперативного втручання наведена в табл. 2. Аналіз перебігу анестезії у пацієнтів 1-ї та 2-ї груп показав, що частота використання медикаментозних засобів для седації була більшою при спінальній анестезії. Так, у цій групі використано 28,5 ± 1,6 мкг/кг сибазону, 7,4 ± 0,9 мг/кг тіопенталу, що вірогідно більше, ніж у другій групі. Препаратів, що забезпечують гемодинамічну стабільність, також було використано більше при застосуванні спінальної анестезії. Так, у першій групі глюкокортикоїдів у перерахунку на преднізолон використано 1,3 ± 0,2 мг/кг, мезатону 51,9 ± 7,2 мкг/кг, що вірогідно більше порівняно з другою групою. У першій групі використано також вірогідно більші об’єми якісних розчинів інфузійної терапії. Таким чином, редукована спіноперидуральна анестезія/аналгезія та методика керованої гіпертензії під час використання цементу забезпечили більш гладкий перебіг анестезії, про що свідчить застосування вірогідно меншої кількості протективних засобів, об’єму та якості інфузійної терапії.
Висновки
1. Оптимальною методикою анестезіологічного забезпечення протезування кульшового суглоба є спіноперидуральна анестезія/аналгезія з редукцією дози спінального компонента.
2. Дана методика забезпечує адекватну антиноцицептивну протекцію, збалансовану гемодинаміку, вищу чутливість судинного русла до медикаментозної корекції гіпотонії.
3. Основним фактором зниження вираженості токсичної реакції на цемент при цементному протезуванні кульшового суглоба є керована гіпертензія під час компресії неполімеризованого цементу.
1. Глумчер Ф.С., Дубров С.А., Мамонова М.Ю. Эффективность применения селективного ингибитора ЦОГ-2 династата для лечения острого послеоперационного и посттравматического болевого синдрома // Біль, знеболювання і інтенсивна терапія. — 2006. — № 1(д). — С. 114-116.
2. Гужевский И.В., Герасименко С.И., Панченко Л.М. Тактика и особенности техники эндопротезирования тазобедренного сустава у больных с коксартрозом, возникшим на почве спондило-эпифизарной дисплазии // Вісник ортопедії, травматології та протезування. — 2012. — № 1(72). — С. 34-38.
3. Лоскутов А.Е., Васильченко Е.В. Ранние результаты эндопротезирования тазобедренного сустава с использованием цементной фиксации // Вісник ортопедії, травматології та протезування. — 2013. — № 4(79). — С. 26-29.
4. Овечкин А.М., Ефременко И.В. Фармакотерапия острой послеоперационной боли, основанная на применении препаратов, воздействующих на NMDA-рецепторный комплекс // Анестезиология и реаниматология. — 2013. — № 3. — С. 63-67.
5. Потапов А.Л., Кобеляцкий Ю.Ю. Обезболивание после объемных оперативних абдоминальных операций — опиаты или эпидуральная анальгезия? // Боль, обезболивание и интенсивная терапия. — 2011. — № 4. — С. 39-42.
6. Смирнова Л.М. Органопротективность регионарной анестезии и антиноцицептивного внутривенного наркоза // Біль, знеболювання і інтенсивна терапія. — 2012. — № 1. — С. 53-58.
7. Солярик С.О., Глумчер Ф.С., Кучин Ю.Л. Влияние контролируемой пациентом эпидуральной анальгезии на воспалительную реакцию в послеоперационном периоде // Біль, знеболювання і інтенсивна терапія. — 2012. — № 2. — С. 76-79.
8. Строкань А.М., Шлапак И.П. Периферическая регионарная анестезия. — К., 2014. — С. 114-142.
9. Таркила П. Эпидуральная анальгезия: нуждаемся ли мы в ней до сих пор после обширных вмешательств на колене и тазобедренном суставе // Регионарная анестезия и лечение острой боли. — 2011. — Т. V, № 2. — С. 42-45.
10. Торчинський В.П., Ніршберг О.Є. Тотальне ендопротезування кульшового суглоба у хворих на асептичний некроз головки стегнової кістки // Вісник ортопедії, травматології та протезування. — 2013. — № 2(77). — С. 38-41.
11. Фомин И.В., Грачев С.С. Применение малых доз местных анестетиков при анестезиологическом обеспечении плановых ортопедических вмешательств // Медицинский журнал: научно-практический рецензируемый журнал / Учредитель — Белорусский государственный медицинский университет. — 2013. — № 2. — С. 118-120.
12. Adnan F., Wrigbt P. Total Hip Repleicement in the Displastic Hip The Use of Cementless Acetabular Components // Malaysian Orthopaedic J. — 2011. — Vol. 5, 2. — P. 20-23.
13. Arbona L. Ultrasound-Guided Regional Anesthesia: A Practical Approach to Peripheral Nerve Blocks and Perineural Catheters / Fernando L. Arbona, Babak Khabiri, John A. Norton. — Cambridge University Press, 2011. — 194 р.
14. Wan Z., Boutary M., Dorr D.L. The Influence of Acetabular Component Position on Wear in Total Hip Arthroplasty // J. Arthroplasty. — 2008. — Vol. 23 (Iss. 1). — P. 51-56.

/67/67.jpg)
/68/68.jpg)