Журнал «Травма» Том 15, №6, 2014
Вернуться к номеру
Системний аналіз оперативного методу лікування діафізарних переломів і фактори впливу на репаративну регенерацію
Авторы: Андрейчин В.А., Білінський П.І. — Івано-Франківський національний медичний університет, Клінічна лікарня № 1, м. Івано-Франківськ; Національна медична академія післядипломної освіти ім. П.Л. Шупика, м. Київ
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
Проаналізовано сучасний стан оперативного методу лікування діафізарних переломів і визначені фактори впливу на репаративну регенерацію. Виділено доопераційні, операційні і післяопераційні фактори впливу на репаративну регенерацію та проведено концептуальний аналіз її розладів.
Проанализировано современное состояние оперативного метода лечения диафизарных переломов и определены факторы влияния на репаративную регенерацию. Выделены дооперационные, операционные и послеоперационные факторы влияния на репаративную регенерацию и проведен концептуальный анализ ее расстройств.
The current state of surgical treatment for shaft fractures was analysed and the factors influencing the reparative regeneration were determined. Preoperative, operative and postoperative factors influencing the reparative regeneration were marked and conceptual analysis of its disorders was carried out.
діафізарні переломи, розлади репаративної регенерації.
диафизарные переломы, расстройства репаративной регенерации.
shaft fractures, disorders of reparative regeneration.
Статья опубликована на с. 59-64
Вступ
Використання нових, сучасних фіксаторів не завжди забезпечує зрощення кісткових відламків. Відсутність системного аналізу, імплікативного мислення при плануванні операції остеосинтезу відламків не дозволяє розібратися у гносеології проблеми, не дає можливості з’ясувати вплив засобів фіксації на регенарацію кісткових фрагментів у просторовому і часовому вимірі, пов’язати наслідок фіксації із багатьма чинниками, що її визначають.
Часто увага приділяється взаємодії окремих елементів, не простежується динаміка процесу, вплив нових важливих чинників, зв’язок структури і функції, коректність методологічного підходу, раціональність тактичних рішень. Цих проблем можна уникнути при використанні системного підходу як найбільш прогресивної методології наукового дослідження, що розглядає елементи і підсистеми у взаємозв’язку, орієнтованого на досягнення кінцевої мети [5, 26]. Саме на основі системного підходу можна розробити профілактичні заходи і прогнозувати наслідок загоювання перелому.
Мета дослідження: проаналізувати сучасний стан оперативного методу лікування діафізарних переломів і визначити фактори впливу на репаративну регенерацію.
Матеріали і методи
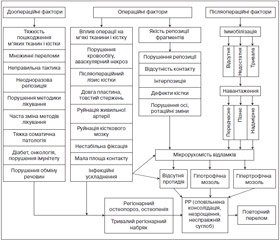
На підставі власних уявлень [1, 4] та даних використаної літератури нами проведено концептуальний аналіз виникнення розладів репаративної регенерації (РРР) при діафізарних переломах (рис. 1). При концептуальному аналізі використано найбільш прогресивний системний гносеологічний метод наукового дослідження з цілісним уявленням РРР при переломі та врахуванням доопераційних, операційних і післяопераційних факторів впливу на неї.
Ефективне оперативне лікування діафізарних переломів можливе на підставі глибокого знання біології кістки, процесу зрощення фрагментів, біомеханіки взаємодії «фіксатор — кістка», елементів, що її становлять, формуванні кісткової мозолі у просторовому і часовому розташуванні з позицій системного підходу [2, 5, 11, 26].
Оперативний метод лікування хворих із діафізарними переломами є складним і тривалим процесом. Він вимагає правильного ведення доопераційного періоду, ґрунтовного доопераційного планування, наявності власного клінічного досвіду, доброго матеріального забезпечення, знання багатьох, на перший погляд простих факторів, наприклад, дотримання правильної техніки виконання операції та правильного ведення пацієнта у післяопераційному періоді, від яких залежить кінцевий результат лікування (рис. 1). Вирішення існуючих проблем також значною мірою залежить від рівня розвитку технічного прогресу [1, 6], а проблема РРР діафізарних переломів вимагає правильного розуміння шляхів їх оптимізації [3, 4].
Результати і обговорення
Згідно з застосованим системним підходом нами виділені і детально проаналізовані доопераційні, операційні і післяопераційні фактори впливу на репаративний остеогенез при переломі (рис. 1). Причин, що призвели до РРР, у кожного окремо взятого пацієнта, як правило, буває декілька, і вони взаємопов’язані. Успіх лікування діафізарних переломів кісток може забезпечити правильне розуміння суті процесу РРР, механізму дії на них факторів різних рівнів, а також застосування адекватної комплексної лікувальної тактики із спостереженням у часі стану кістки в зоні пошкодження [8–10].
Нами виділено доопераційні суб’єктивні та об’єктивні фактори: неправильна тактика, порушення методики, неодноразова репозиція, часта зміна методів лікування, тяжкість пошкоджень м’яких тканин і кістки, множинні переломи, тяжка соматична патологія (діабет, судинні захворювання, онкохвороби, порушення імунітету та обміну речовин). Дані фактори, безсумнівно, негативно впливають на репаративний остеогенез. Вони приводять до тривалого регіонарного набряку і дисрегенерації. Перебіг репаративної регенерації залежить від успішної репозиції фрагментів, збереження їх кровопостачання. Важливу роль у запуску регенеративного процесу кістки відіграє посттравматичне запалення у зоні перелому [16, 20]. Традиційно вважається, що ургентне оперативне втручання при переломі кісток гомілки дозволяє покращити наслідки лікування [11].
У попередженні незрощень відламків при діафізарних переломах велике значення в доопераційному періоді мають діагностика і лікування закритих пошкоджень м’яких тканин. Більшість пацієнтів надходять у стаціонар з ізольованими закритими переломами. Оптимально їх треба оперувати протягом однієї доби, щоб знизити небезпеку розвитку багатьох ускладнень [10]. Але тяжкі травми м’яких тканин ведуть до мікросудинних і клітинних пошкоджень у зоні перелому, тому у таких випадках остеосинтез погружними металоконструкціями треба відстрочити на 2–3 тижні. У зв’язку з цим розробники АО за біологічністю і травматичністю засоби остеосинтезу розташували у наступному порядку: апарати для позавогнищевої фіксації, блокуючі інтрамедулярні стержні, накісткові пластини [6, 15, 18, 21, 24].
Аналіз причин помилок і ускладнень, що виникають після остеосинтезу заглибними металоконструкціями, свідчить, що далеко не завжди хірург-травматолог, здійснюючи остеосинтез, усвідомлює, чим обумовлений вибір фіксатора в конкретному випадку і на який результат можна очікувати [2, 22, 25]. Механістичне ставлення до остеосинтезу, нехтування факторами, що впливають на репаративну регенерацію, не сприяють зрощенню фрагментів [18, 23, 24]. Конструкція фіксатора розрахована на певну кількість циклів навантаження, після чого відбувається його злам. Ціль лікування полягає в досягненні зрощення кістки до того, як це відбудеться [6, 30].
У сучасних умовах повинен застосовуватись сформульований АО minimally invasive plate osteosynthesis (МІРО). Важливим постулатом МІРО є малоінвазивність, виконання з невеликих хірургічних доступів з мінімальною травматизацією м’яких тканин і збереженням кровопостачання кісткових відламків [9, 17]. Застосування довгих контактних пластин не завжди забезпечує дотримання цих принципів [21]. Відкрите введення товстих стержнів приводить до руйнації внутрішньої живильної артерії та кісткового мозку (КМ) [24]. Відомо, що ендостальне живлення забезпечує 2/3 кортикалу діафізарної частини кістки.
Можливості всіх засобів для остеосинтезу реалізуються на стику відламків. У цьому місці проходять складні біологічні процеси репаративної регенерації. Кожен вид перелому має свій теоретично можливий мінімальний строк зрощення фрагментів. Суть хірургічної технології, направленої на вдосконалення лікування переломів кісток, полягає в скороченні різниці між можливим і реальним строком зрощення відламків. Головна задача травматолога — це створення умов, які б гарантували максимально швидку консолідацію фрагментів [6, 13, 17, 29].
Експериментально Г.А. Ілізаров (1993) довів, що в певних умовах кістковий мозок діафіза проявляє виключно високу остеогенну активність. Він продукує повноцінну кісткову тканину в короткі терміни і у великому обсязі з надлишком [8].
Наш власний досвід застосування аутологічного кісткового мозку в комплексному оперативному лікуванні 28 хворих із незрощеннями і несправжніми суглобами діафіза довгих кісток свідчить про його виражену оптимізуючу роль у репаративній регенерації. Так, у всіх 28 хворих відбулося зрощення кісткових фрагментів і відновлення працездатності. Пересадку КМ у пацієнтів здійснювали 1–3 рази в міжфрагментарну зону під рентгенологічним контролем або під контролем електронно-оптичного перетворювача. Середній строк введення аутологічного кісткового мозку з дня перелому становив при незрощеннях 189,7 дня, при несправжніх суглобах — 247,3 дня [1].
Застосування блокуючого інтрамедулярного остеосинтезу пов’язано з багатьма проблемами. При несвіжих переломах та інтерпозиції у ряді випадків хірург змушений здійснювати відкриту репозицію, порушуючи концепію МІРО. Ротаційні помилки при остеосинтезі гомілки становлять до 25 % [27, 33]. Для виправлення цих помилок доводиться робити повторні травматичні оперативні втручання. Головною причиною сповільненої консолідації є також допущений діастаз між фрагментами і пізнє осьове навантаження. Для попередження цього приходиться виконувати через 6–8 неділь динамізацію стержня [10, 24]. Використання тонких стержнів пов’язане із вторинним зміщенням відламків, зламом стержня та РРР [27, 32].
Погрішності заглибного металоостеосинтезу у вигляді нестабільної фіксації, малої площі контакту кінців відламків, а також інфекційні ускладнення теж призводять до РРР [7, 25]. Для зменшення травматичності оперативного втручання виконання остеосинтезу накістковими пластинами АО рекомендує дотримуватись техніки MIPO. Важливими постулатами нової концепції АО є відновлення довжини зламаної кістки, осьових співвідношень, усунення ротації, а анатомічна репозиція фрагментів не є обов’язковою [6, 14, 21, 32]. При недотриманні наведених принципів навіть тривала іммобілізація та повна відсутність навантаження на кінцівку не приводять до бажаних результатів. Рання функція можлива тільки після анатомічної репозиції та стабільної фіксації кісткових відламків [5, 6]. При відсутності доброго контакту між фрагментами, стабілізації їх LCP-пластиною, що блокує мікрорухомість відламків, розвивається псевдоартроз.
Класично шинування пошкодженого сегмента повноконтактною накістковою пластиною передбачає тривале стабільне знерухомлення відламків, первинне їх зрощення, при анатомічній репозиції, без утворення періостальної мозолі, що, власне, і вважали розробники системи АО основною перевагою остеосинтезу повноконтактними накістковими пластинами. Але внаслідок резорбції кістки навколо гвинтів порушуються біомеханічні умови стабільності остеосинтезу, пластина обростає кістковою мозолю, відбувається вторинне зрощення фрагментів. Часто фіксатори для контактного остеосинтезу не забезпечують створення стабільної конструкції «фіксатор — кістка» та оптимальних умов для перебігу репаративної регенерації [2, 4]. У таких умовах профілактикою розвитку несправжнього суглоба може служити введення в зону перелому стовбурових мезенхімальних клітин або аутологічного кісткового мозку, створення додаткової лікувальної іммобілізації та оптимальні величина і строк навантаження [1, 11, 12, 28].
У нормі кістка виконує функцію опори, має внутрішні напруження, що переводять зовнішні навантаження в енергію біомеханічних реакцій, гідродинамічні та п’єзоелектричні ефекти, які запускають і регулюють репаративну регенерацію [7, 13, 17]. Вони орієнтують колагенові молекули вздовж силових ліній, сприяють відкладенню гідроксилапатиту, посилюють гемопоетичну активність кісткового мозку, сприяють появі пула недиференційованих остеогенних клітин [7]. Виходячи з цього, ціль остеосинтезу — не механічне з’єднання фрагментів, а створення умов для виникнення внутрішніх напружень, що міняються [22].
Фіксатор повинен стабілізувати відламки еластично, сила впливу фіксатора на кістку повинна викликати в ній адекватне напруження. Функція фіксатора полягає лише у протидії боковим переміщенням дистального відламка відносно проксимального, при збереженні контактної передачі напруження через зону регенеруючих тканин [13, 19, 20]. Більшість внутрішніх фіксаторів блокують передачу напруження в зоні контакту відламків, тому не сприяють повноцінній репаративній регенерації [6, 30].
Стан внутрішнього напруження навколо перелому залежить від жорсткості і деформативності системи «фіксатор — кістка», а також навантаження, що діє на неї. Напруження колагену, у свою чергу, пов’язане із розтягненням або стисненням, а вони — із переміщенням відламків та їх мікрорухомістю [7, 31]. Жорсткість фіксації можна оцінити за величиною лінійного переміщення відламків відносно один одного. Жоден фіксатор не здатний повністю знерухомити кінці відламків [5, 22].
Мікрорухомість фрагментів, що виникає при навантаженні, сприяє репаративному остеогенезу, якщо деформація є нижчою від критичного рівня для регенерату в зоні перелому [31, 32]. Абсолютна жорсткість фіксації не бажана, мікрорухомість фрагментів у зоні перелому сприятливо діє на розвиток періостальної мозолі [4]. Жорстка фіксація фрагментів пластиною сповільнює процес зрощення, ослаблює кортикальну кістку [4, 6]. Мікрорухомість веде до розвитку періостальної мозолі, обсяг останньої залежить від величини мікрорухомості, це відбувається за рахунок збільшення кількості остеогенних капілярів. А остеогенні капіляри, у свою чергу, перетворюються в остеобласти [17, 20].
Oсновна проблема накісткового остеосинтезу полягає у недосконалості принципів фіксації — у притисканні пластини до кістки, проведенні гвинтів в одній площині, відсутності взаємодії «пластина — гвинт» і, як результат, відсутності стабільної конструкції «фіксатор — кістка». Виникають сили, що при косопоперечному переломі з боку пластини сприяють компресії фрагментів, з протилежного боку від пластини діють сили, спрямовані на дистракцію. Репаративний процес проходить із затримкою через посилення лізису кістки під пластиною і навколо гвинтів. При одноплощинному проведенні гвинтів це призводить до зниження стабільності остеосинтезу, посилення періостальної реакції [5]. Результатом остеосинтезу може бути зрощення фрагментів, дисрегенерація веде до псевдоартрозу через можливі переломи гвинтів, пластини, відхід пластини від кістки. При первинному зрощенні ймовірна рефрактура після зняття пластини.
Значною мірою стабільної фіксації можна досягнути при використанні LCP-пластин [2, 6, 30]. Проте їх застосування вимагає анатомічної репозиції фрагментів. Наявність щілини між ними при блокуванні мікрорухомості призводить до РРР. Загалом еластичність фіксатора повинна наближатися до еластичності кістки [4]. На стадії ремоделювання регенерату, при формуванні пластинчастої кістки фіксатор має сприяти структуризації кісткової мозолі через навантаження на кінцівку. Таким чином, до певної міри можна впливати на характер розміщення кісткових балок, тип зрощення. Задача травматолога — індивідуальний вибір оптимального фіксатора для кожного пацієнта залежно від типу пошкодження м’яких тканин, виду перелому, що забезпечують оптимальні умови для перебігу репаративної регенерації [15, 17].
Негативний вплив на репаративний остеогенез поряд з оперативними факторами мають також і післяопераційні фактори впливу (рис. 1), через допущені травматологом помилки: відсутня, недостатня або більш тривала, ніж потрібно, лікувальна іммобілізація; передчасне, надмірне або пізнє навантаження. При стабільній фіксації, особливо із застосуванням інтрамедулярних блокуючих фіксаторів та LCP-пластин, додаткова фіксація, як правило, не потрібна. При прийнятті рішення щодо функціонального навантаження на хвору кінцівку повинна бути врахована стабільність фіксації фрагментів. Відсутність протидії вторинному зміщенню фрагментів при недостатній жорсткості остеосинтезу також веде до розладів репаративного остеогенезу. Таку протидію достатньою мірою забезпечують фіксатори для малоконтактного багатоплощинного остеосинтезу [5].
При ранньому значному навантаженні після остеосинтезу накістковою пластиною посилюється лізис кістки навколо фіксуючих гвинтів, що веде до дестабілізації фрагментів. Продовження дії зовнішньої сили сприяє переходу мікрорухомості у макропереміщення фрагментів, їх дестабілізації [4, 14, 16]. Одноплощинна фіксація, відсутність елемента взаємодії «пластина — гвинт» не протидіє такому переходу. Таким чином, накісткові пластини вимагають досить уважного ставлення в післяопераційному періоді, добрий результат можливий за відсутності значного тривалого навантаження на прооперовану кінцівку. Дозоване навантаження, післяопераційна мікрорухомість призводять до розвитку періостальної мозолі, стабільність сегмента зростає. У доступній нам літературі ми знайшли мало інформації про величину мікрорухомості фрагментів залежно від способу фіксації, дії зовнішньої сили [5, 20, 31].
Фізіотерапію з метою м’язової реабілітації та реабілітації м’яких тканин необхідно розпочинати якомога швидше після операції і продовжувати до відновлення нормальної функції кінцівки.
Таким чином, використана за показаннями, методично правильно виконана конкретна оперативна методика лікування перелому забезпечує добрий клінічний результат. Вона повинна базуватись на знанні багатьох факторів, що визначають перебіг репаративного остеогенезу. Існує залежність методів лікування і стану остеосинтезу від рівня розвитку технічного прогресу і прикладних наук. При відсутності системного підходу до лікування переломів, під впливом існуючих стереотипів, традицій зміна принципів лікування без побудови структурних концептуальних функціональних моделей створює більше проблем, ніж вирішує завдань. Сучасні знання постійно доповнюються новими уявленнями про роль репозиції, оперативної фіксації та функції в лікуванні діафізарних переломів, цієї складної механічної та біологічної проблеми.
Висновки
1. Оперативне лікування діафізарних переломів може супроводжуватись розладами репаративної регенерації, на розвиток яких впливають множинні фактори.
2. Перед виконанням остеосинтезу відповідно до характеру перелому повинно проводитися його доопераційне планування із системним аналізом факторів, що визначають репаративний остеогенез в просторовому і часовому вимірі.
3. Пацієнти з діафізарними переломами повинні лікуватись з дотриманням особливостей існуючих методик сучасного остеосинтезу та створених необхідних умов оптимального ведення післяопераційного періоду. Тільки усвідомлений, концептуальний аналіз всіх факторів, що впливають на процес зрощення кістки, може бути гарантією успіху.
1. Андрейчин В.А. Лікування хворих з незрощеннями кісткових відламків, несправжніми суглобами та повторними переломами довгих кісток / Андрейчин В.А., Шибель І.В., Непорадний І.Д. [та ін.] // Збірник наукових праць XVІ з’їзду ортопедів-травматологів України. — Харків, 2013. — С. 225-226.
2. Андрейчин В.А. Фактори, які визначають перебіг загоєння діафізарних переломів / В.А. Андрейчин, В.С. Пелих // Галицький лікарський вісник. — 2012. — Т. 19, № 1. — С. 146-148.
3. Малоінвазивний заглибний остеосинтез у постраждалих із діафізарними переломами кісток гомілки / Анкін М.Л., Анкін Л.М., Сатишев М.М. [та ін.] // Травма. — 2011. — Т. 12, № 3. — С. 80-84.
4. Білінський П.I. Малоконтактний багатоплощинний остеосинтез переломів кісток та їх наслідків (теоретичне, експериментальне обґрунтування, клінічна реалізація: Автореф. дис… на здобуття наук. ступеня доктора мед. наук: спец. 14.01.21 «Травматологія та ортопедія» / П.І. Білінський. — Х., 2004. — 36 с.
5. Білінський П.І. Теорія і практика малоконтактного багатоплощинного остеосинтезу / П.І. Білінський. — К.: Макрос, 2008. — 375 с.
6. Блокируемые пластины для переломов конечностей / Anglen J., Kyle R.F. [et al.] // Остеосинтез. — 2011. — № 1(14). — С. 13-14; JAAOS. — 2009. — Vol. 17, № 7. — P. 647-657.
7. Гончарова Л.Д. Концепция внутренних напряжений опорных структур и ее место в вопросах остеосинтеза / Л.Д. Гончарова, А.А. Тяжелов, Г.В. Лобанов // Травма. — 2008. — Т. 9, № 2. — С. 227-231.
8. Илизаров Г.А. Новые данные об остеогенных возможностях костного мозга диафиза / Г.А. Илизаров, А.А. Шрейнер, И.А. Имерлишвили // Ортопедия, травматология и протезирование. — 1993. — № 5. — С. 5-8.
9. Ирьянов Ю.М. Современные представления о гистологических аспектах репаративной регенерации костной ткани / Ю.М. Ирьянов, Т.А. Силантьева // Гений ортопедии. — 2007. — № 2. — С. 111-116.
10. Калашников А.В. Интрамедуллярный блокирующий остеосинтез в лечении больных с расстройствами репаративного остеогенеза / А.В. Калашников, Ю.А. Ставинский, П.В. Никитин // Збірник наукових праць XV з’їзду ортопедів-травматологів України. — Дніпропетровськ, 2010. — С. 190.
11. Влияние этиологического фактора травмы на течение репаративного остеогенеза. Часть 1. Сращение диафизарных переломов голени при непрямом механизме травмы / Климовицкий В.Г., Пастернак В.Н., Оксимец В.М. [и др.] // Травма. — 2007. — Т. 8, № 1. — С. 7-12.
12. Механизмы влияния мезенхимальных стволовых клеток на репаративный остеогенез / Климовицкий В.Г., Гринь В.К., Оксимец В.М. [и др.] // Травма. — 2009. — № 2. — С. 123-132.
13. Концепция внутренних напряжений опорных структур и репаративный остеогенез: (обзор литературы) / Kuliev A.M., Verdiev V.G., Abdullaev N.T., Aliev G.A. // Ортопедия и травматология Азербайджана. — 2010. — № 2. — С. 76-79.
14. Корж Н.А. Новые технологии в регенерации кости / Н.А. Корж, Н.В. Дедух // Збірник наукових праць XV з’їзду ортопедів-травматологів України. — Дніпропетровськ, 2010. — С. 79.
15. Формирование национальной концепции лечения диафизарных переломов конечностей (100-летний опыт института им. проф. М.И. Ситенко) / Корж А.А., Попсуйшапка А.К., Тяжелов А.А. [и др.] // Тези доповідей XІV з’їзду ортопедів-травматологів України. — Одеса, 2006. — С. 31-32.
16. Корж Н.А. Репаративная регенерация кости: современный взгляд на проблему. Локальные факторы, влияющие на заживление перелома / Н.А. Корж, Л.Д. Горидова, К.К. Романенко // Ортопедия, травматология и протезирование. — 2006. — № 3. — С. 99-105.
17. Мартель И.И. Cовременные представления об условиях консолидации переломов и возможность их обеспечения различными типами фиксаторов (обзор литературы) / Мартель И.И., Мацукатов Ф.А., Шигарев В.М., Бойчук С.П. // Гений ортопедии. — 2012. — № 4. — С. 131-136.
18. Помилки та ускладнення в ортопедо-травматологічній практиці / Корж М.О., Яременко Д.О., Горидова Л.Д., Романенко К.К. // Ортопедия, травматология и протезирование. — 2010. — № 2. — С. 5-10.
19. Попсуйшапка А.К. Лечение несросшихся диафизарных переломов конечностей путем стимуляции фибриногенеза и создания напряжений регенерирующих тканей / А.К. Попсуйшапка, В.А. Литвишко // Травма. — 2010. — Т. 11, № 4. — С. 437-440.
20. Попсуйшапка А.К. Сращение отломков после перелома кости / А.К. Попсуйшапка, В.А. Литвишко, О.А. Подгайская // Междунар. мед. журн. — 2009. — Т. 15, № 2(58). — С. 73-80.
21. Ріхтер О.А. Металофіксатори для накісткового остеосинтезу: розуміння вибору — розумний вибір / О.А. Ріхтер // Ортопедия, травматология и протезирование. — 2009. — № 4. — С. 81-83.
22. Романенко К.К. Абсолютная и относительная стабильность при остеосинтезе длинных костей / К.К. Романенко, А.И. Белостоцкий, Д.В. Прозоровский // Ортопедия, травматология и протезирование. — 2009. — № 1. — С. 97-100.
23. Романенко К.К. Діафізарні переломи довгих кісток, що не зрослися (чинники ризику, діагностика, лікування): Автореф. дис… канд. мед. наук: спец 14.01.21 «Травматологія та ортопедія» / К.К. Романенко. — Харків, 2002. — 18 с.
24. Рубленик І.М. Блокуючий інтрамедулярний металополімерний остеосинтез у лікуванні наслідків переломів кісток гомілки / І.М. Рубленик, В.Л. Васюк, П.Є. Ковальчук, І.М. Циркот // Травма. — 2008. — Т. 9, № 1. — С. 71-73.
25. Рушай А.К. Особенности лечения травматического остеомиелита длинных костей у больных после применения различных видов остеосинтеза / А.К. Рушай // Травма. — 2010. — Т. 11, № 3. — С. 303-307.
26. Сименач Б.И. Фрактурология — некоторые аспекты теоретизации учения о переломах костей. Часть 2. Управление процессами репарации / Б.И. Сименач // Ортопедия, травматология и протезирование. — 2000. — № 4. — С. 105-117.
27. Ситник А.А. Интрамедуллярный блокируемый остеосинтез длинных трубчатых костей. Современный уровень развития / А.А. Ситник // Медицинский журнал. — 2007. — № 4. — С. 22-25.
28. Остеогенные потенции нативного аутологического костного мозга, индуцированного кристаллическим химотрипсином, при лечении посттравматических нарушений костной регенерации / Склянчук Е.Д., Зоря В.И., Гурьев В.В. [и др.] // Травматология и ортопедия России. — 2009. — № 1. — С. 42-49.
29. Шимон В.М. Перспективні напрями лікування діафізарних переломів кісток гомілки / В.М. Шимон, А.А. Шерегій // Травма. — 2010. — Т. 11, № 4. — С. 363-366.
30. Gardner M.J. Failure of fracture plate fixation / M.J. Gardner, J.M. Evans, R.P. Dunbar // J. Am. Acad. Orthop. Surg. — 2009. — Vol. 17, № 10. — P. 647-657.
31. Perren S. Evolution of the internal fixation of long bone fractures / S. Perren // J. Bone Jt. Surg. [Br.]. — 2002. — Vol. 84-B. — P. 1093-1110.
32. Ruedi Th.R. AO Principles of fracture management / Th.R. Ruedi, R.E. Buckley, Ch.G. Moran. — Stuttgart, New York: Thieme, 2007. — 947 р.
33. Strecker W. Torsional Deformities Following Intramedullary Nailing of Femur and Tibia / W. Strecker, D. Popp, P. Keppler // Osteo Trauma Care. — 2004. — № 12. — P. 215-218.

/60/60.jpg)