Газета «Новости медицины и фармации» 1 (525) 2015
Вернуться к номеру
Эффекты Мексиприма у больных с артериальной гипертензией
Авторы: Долженко М.Н., Нудченко А.О., Лурье С.З., Сорока И.Н. - Национальная медицинская академия последипломного образования имени П.Л. Шупика, г. Киев; Филимонова И.А., Шершнева О.В. - Запорожская медицинская академия последипломного образования, Запорожский государственный медицинский университет
Рубрики: Кардиология
Разделы: Клинические исследования
Версия для печати
Статья опубликована на с. 3-5 (Укр.)
Профилактика сердечно-сосудистых заболеваний (ССЗ) является основной задачей современной кардиологии, что приводит к снижению заболеваемости и смертности, а также увеличению средней продолжительности жизни. Однако основная польза профилактических мероприятий, по данным неинтервенционных рандомизированных клинических исследований, заключается в доказательствах эффективности модификации образа жизни (отказ от курения, диета, физические упражнения), лечении артериальной гипертензии (АГ), гиперлипидемии и сахарного диабета, а также использования профилактической медикаментозной терапии (антиагреганты, бета-блокаторы, блокаторы ренин-ангиотензин-альдостероновой системы, гиполипидемические средства). Данные мероприятия доказанно снижают риск сердечно-сосудистой заболеваемости и смертности, кроме того, могут снизить риск вторичных осложнений [1–4].
Четвертое европейское исследование профилактики ССЗ и сахарного диабета (EUROASPIRE IV) проходило под эгидой Европейского общества кардиологии (ESC), Еврообсервационной исследовательской программы (EORP) и проводилось Европейской ассоциацией сердечно-сосудистой профилактики и реабилитации и Ассоциации кардиологов Украины. По разрешению исполнительного комитета EUROASPIRE IV параллельно с основным исследованием для украинской популяции проводили основные и дополнительные исследования.
Известно, что Американская ассоциация сердца (АНА) внесла депрессию в список факторов риска развития ССЗ. По данным EUROASPIRE III, среди 8580 пациентов из 22 европейских стран, которых наблюдали в течение 6 мес. после госпитализации по поводу ишемической болезни сердца, распространенность депрессии варьировала от 8,2 до 35,7 % среди мужчин и от 10,3 до 62,5 % — среди женщин. Распространенность тревожных расстройств варьировала от 12,0 до 41,8 % среди мужчин и от 21,5 до 63,7 % — у женщин [5].
В исследование по программе EUROASPIRE IV (линия общей практики) также вошли опросники по выявлению депрессивных эпизодов как фактора риска развития ССЗ. Согласно последним данным, депрессии являются основным диагнозом в 5–10 % всех случаев обращения за первичной медицинской помощью, а при наличии соматической патологии сопутствующую клиническую картину депрессии фиксируют у 12–25 % больных [6].
В мае 2012 года в журнале Hypertension был опубликован обзор, основанный на обследовании 22 367 пациентов в течение 9,6 года, и было доказано, что депрессия увеличивает риск развития АГ (ОР 1,46; 95% ДИ 1,09–1,86; Р = 0,009) [7].
Однако диагностируемая энцефалопатия у пациентов с АГ проявлялась когнитивными нарушениями, что требовало назначения антиоксидантных и антигипоксантных препаратов для торможения перекисного окисления липидов и улучшения когнитивных функций пациентов.
Одним из наиболее перспективных препаратов группы антиоксидантов являются производные 3-оксипиридина, в частности этилметилгидроксипиридина сукцинат, способный проникать через гематоэнцефалический барьер [8]. Проявляя антиоксидантные свойства, данный препарат угнетает процессы свободнорадикального окисления, перекисного окисления липидов, а с другой стороны, активируя супероксиддисмутазу, повышает активность физиологической антиоксидантной системы в целом, оказывает влияние на физико–химические свойства мембраны, при этом вязкость мембраны уменьшается и увеличивается ее текучесть, в результате происходят изменения ее функциональной активности. Это приводит к конформационным изменениям синаптических мембран, вследствие чего проявляется модулирующий эффект на активность мембраносвязанных ферментов, ионных каналов и рецепторных комплексов, в том числе бензодиазепинового, ГАМК, ацетилхолинового, усиливается их способность связывания с лигандами, повышается активность нейромедиаторов и активация синаптических процессов.
Цель исследования: оценить эффективность, безопасность и переносимость препарата этилметилгидроксипиридина сукцината (препарат Мексиприм, фирма «Штада») у больных с АГ на поликлиническом этапе оказания медицинской помощи.
Материалы и методы
Данное клиническое исследование проводили как открытое сравнительное, по сокращенной программе. Его выполняли в соответствии с требованиями, предъявляемыми Хельсинкской декларацией Всемирной медицинской ассоциации (2004) и Государственным фармакологическим центром МЗ Украины, о клинических испытаниях лекарств (2006) [9].
Для проведения исследования был задействован центр клинических исследований кафедры кардиологии НМАПО имени П.Л. Шупика на базе ГУ «Институт кардиологии имени академика Н.Д. Стражеско НАМН Украины» в г. Киеве и 4-я клиническая городская больница г. Запорожья. В исследование были включены 152 больных с умеренной АГ (ІІ стадией, 2-й степенью повышения уровня артериального давления (АД)). В соответствии с рекомендациями ESH/ESC все больные получали базовое лечение: блокатор ренин-ангиотензиновой системы, при недостижении целевого уровня АД 140/90 мм рт.ст. дополнительно назначали диуретик. Ста двум больным дополнительно к базовой терапии был назначен Мексиприм в дозе 0,125 мг 3 раза в сутки, 50 больных АГ составили контрольную группу.
Учитывая рекомендации ESC/ESH (2013) по ведению пациентов с АГ о важности домашнего измерения АД, больным было рекомендовано измерять уровень АД утром и вечером ежедневно в течение 60 дней и записывать в дневник.
Исследование включало следующие этапы: 1-й период — скрининг и клиническая верификация АГ, а также коморбидных соматических состояний (подготовительный период); 2-й период — активная терапия 60 дней.
Дизайн исследования: офисное и домашнее измерение уровня АД, обследование по шкале Бека, шкале Гамильтона для оценки тревоги (HARS) и депрессии (HDRS), шкале самооценки («Самочувствие. Активность. Настроение» — САН), когнитивные нарушения оценивали по шкале MMSE, проведение общих анализов крови и мочи, биохимическое исследование крови, оценка терапевтической переносимости препарата. Состояние больных оценивали до начала терапии и на 60-й день лечения, нежелательные явления — во время каждого визита; были зафиксированы все нежелательные явления, происходившие с пациентами после приема первой дозы исследуемого препарата и до окончания лечения.
Полученные результаты обработаны статистически с применением разностного метода и критерия Стьюдента. Результаты представлены как M ± q.
Результаты исследования и их обсуждение
При оценке ориентации по шкале MMSE (табл. 1) количество баллов в группе Мексиприма и контрольной группе составило в среднем 8,2 ± 1,8 и 8,1 ± 2,0 соответственно. После приема Мексиприма количество баллов по оценке ориентации достоверно повысилось до 8,9 ± 1,7 (P = 0,0047). В контрольной группе показатель составил 8,3 ± 1,5 (Р = 0,5729). При оценке памяти исходное количество баллов в группе Мексиприма и контрольной группе составило в среднем 5,2 ± 1,4 и 5,3 ± 1,4 соответственно. После лечения данный показатель в группе Мексиприма составил 5,9 ± 1,3 (Р = 0,003), а в контрольной группе — 5,4 ± 1,3 (Р = 0,7121). Среднее количество баллов при оценке счетных операций до начала исследования составило 4,1 ± 1,1 в группе Мексиприма и 4,2 ± 1,4 — в контрольной группе. После лечения показатель достоверно повысился в группе Мексиприма до 4,7 ± 1,4 (Р = 0,0008), в то время как в контрольной группе данный показатель повысился статистически несущественно — до 4,25 ± 1,00 (Р = 0,8376). Прием Мексиприма привел к достоверному повышению среднего показателя оценки перцептивно–гностической функции с 8,1 ± 2,1 до 8,8 ± 2,0 (Р = 0,0156). В контрольной группе изменения показателя оказались статистически незначимыми — повышение с 8,09 ± 2,80 до 8,1 ± 2,0 (Р = 0,983). Исходный общий показатель когнитивной продуктивности составил в среднем 28,5 ± 3,4 в группе Мексиприма и 28,4 ± 4,6 — в контрольной группе. В группе Мексиприма после лечения отмечали достоверное повышение указанного показателя до 29,8 ± 4,3 (Р = 0,0175). В свою очередь, в контрольной группе аналогичный показатель составил 28,1 ± 5,6, а изменения исходных значений оказались статистически недостоверными (Р = 0,1161).
После лечения между группой Мексиприма и контрольной группой были отмечены достоверные отличия во всех показателях оценки когнитивной эффективности по шкале MMSE: ориентации (Р = 0,0354), количества баллов оценки памяти (Р = 0,0274), счетных операций (Р = 0,0440), перцептивно-гностической функции (Р = 0,0440) и общего показателя когнитивной продуктивности (Р = 0,0404) (табл. 1).
При оценке суммарного количества баллов по шкале MMSE (табл. 2) оказалось, что до начала приема Мексиприма у 10 пациентов отмечались умеренные когнитивные нарушения (10,2 %), у 40 человек — легкие когнитивные нарушения (40,8 %). У 50 участников (53,4 %) когнитивная продуктивность нарушена не была. После приема Мексиприма количество пациентов с умеренными когнитивными нарушениями уменьшилось на 60 %, количество пациентов с легкими когнитивными нарушениями уменьшилось на 57,5 %. В итоге количество пациентов без нарушения когнитивной продуктивности увеличилось на 55,1 % и составило 81 (82,62 %).
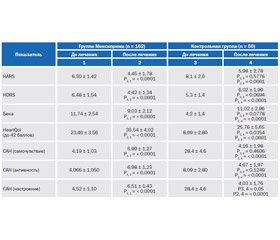
При оценке уровня тревожности по шкале HARS у пациентов группы Мексиприма оказалось, что прием препарата приводил к достоверному снижению среднего количества баллов с 6,30 ± 1,42 до 4,45 ± 1,78 (P < 0,0001). В то же время в контрольной группе показатели до и после лечения достоверно не отличались и составили 6,24 ± 1,76 и 5,98 ± 2,78 соответственно (Р = 0,5776). Применение Мексиприма привело к статистически значимому снижению количества баллов по шкале оценки депрессии HDRS с 6,48 ± 1,54 до 4,42 ± 1,34 (P < 0,0001). В контрольной группе исходное среднее количество баллов составляло 6,76 ± 2,04, после лечения — 6,02 ± 1,99, а разница между показателями оказалась недостоверной (Р = 0,0694).
Кроме того, наличие у пациентов депрессивных расстройств до и после лечения оценивали и по шкале Бека.
В группе Мексиприма отмечали достоверное снижение среднего количества баллов с 11,74 ± 2,54 до 9,03 ± 2,12 (Р < 0,0001). В контрольной группе также было выявлено снижение среднего количества баллов с 12,04 ± 2,76 до 11,02 ± 2,96, однако оно оказалось статистически незначимым (Р = 0,0778).
При оценке качества жизни по шкале HeartQol оказалось, что прием Мексиприма ассоциировался с достоверным повышением среднего количества баллов с исходных 23,40 ± 3,56 до 35,54 ± 4,02 после лечения (P < 0,0001). В контрольной группе было выявлено повышение среднего количества баллов с 23,67 ± 4,01 в начале исследования до 25,76 ± 5,65 — после лечения, которое также оказалось статистически значимым (Р = 0,0354). Следует, однако, отметить, что в опроснике HeartQol, содержащем 14 вопросов, лишь 4 касаются психоэмоциональной сферы — ощущений подавленности, разочарованности, беспокойства и невозможности расслабиться и освободиться от напряжения. Остальные 10 вопросов связаны с физическим состоянием и толерантностью к физическим нагрузкам. Принимая во внимание тот факт, что все пациенты данного исследования дополнительно принимали препараты, влияющие на сердечно-сосудистую систему, можно заключить, что достоверное повышение показателей по шкале HeartQol у пациентов контрольной группы было достигнуто за счет улучшения физического состояния на фоне приема рекомендованной сопутствующей терапии.
При оценке самочувствия по шкале САН оказалось, что применение Мексиприма ассоциировалось с достоверным увеличением среднего количества баллов с 4,19 ± 1,03 до 5,99 ± 1,27 (P < 0,0001). В контрольной группе отмечали снижение среднего количества баллов с 4,43 ± 1,65 до 4,16 ± 1,98, которое, однако, оказалось статистически недостоверным (Р = 0,4606).
В группе Мексиприма отмечали достоверное повышение среднего количества баллов при оценке активности по шкале САН с 4,066 ± 1,050 до 6,98 ± 1,23 (P < 0,0001). В контрольной группе аналогичные показатели составили 4,12 ± 1,56 до лечения и 4,67 ± 1,97 — после лечения, а разница между ними оказалась недостоверной (Р = 0,1249).
Наконец, при анализе настроения по шкале САН оказалось, что в группе Мексиприма среднее количество баллов статистически существенно возросло с 4,52 ± 1,10 до 6,51 ± 1,43 (P < 0,0001). В контрольной группе исходный аналогичный показатель составил 4,67 ± 1,45, который после лечения снизился до 4,03 ± 1,76, хотя снижение не достигло критериев достоверности (Р = 0,05).
Следует отметить, что если показатели всех приведенных шкал в двух группах были сравнимы до лечения, то после лечения по всем шкалам различия между группой Мексиприма и контрольной группой стали статистически значимыми (P < 0, 0001) (табл. 3).
В отношении оценки уровня АД следует отметить, что офисное измерение АД показало достижение целевого уровня 140/90 мм рт.ст. у 72 % пациентов в группе Мексиприма и 68 % — у пациентов контрольной группы.
Однако при подсчете количества пациентов, достигших целевого уровня при домашнем измерении АД в течение 60 дней, в среднем было выявлено достоверное увеличение количества пациентов, достигших целевого уровня АД в группе Мексиприма по сравнению с контрольной группой (84 % по сравнению с 69 %; Р = 0,0343), что подчеркивает как важность эмоционального, депрессивного фактора в развитии АГ, так и эффективность самой методики домашнего измерения АД для оценки среднего уровня АД в течение 60 дней.
Как видно из табл. 4, применение Мексиприма в течение двух месяцев не влияло на липидограмму, печеночные пробы, креатинин, мочевину, глюкозу крови, гликозилированный гемоглобин, С-реактивный протеин, общий белок, что говорит о нейтральном действии Мексиприма на основные биохимические жизненные показатели.
Переносимость Мексиприма представлена в табл. 5, ее оценивали как хорошую у 95,09 % пациентов, удовлетворительную — у 4,9 %.
Выводы
1. У 49 % больных с артериальной гипертензией ІІ стадии и 2-й степени отмечено умеренное и легкой степени нарушение когнитивных функций. Применение препарата Мексиприм у больных с АГ достоверно повышает когнитивную продуктивность, так как у большинства пациентов отмечали отчетливое и равно выраженное улучшение всех оцениваемых параметров при тестировании по шкале ММSЕ.
2. У 46,9 % больных с АГ ІІ стадии и 2-й степени были диагностированы проявления тревожного и легкого депрессивного состояния по шкалам HARS, HDRS и Бека. Применение Мексиприма снижает и нормализует показатели этих шкал.
3. Применение Мексиприма повышало показатели физической и психической активности, настроения, улучшало самочувствие, что наблюдалось у больных с АГ и было диагностировано с помощью шкал САН и HeartQol.
4. Выявлено достоверное повышение количества пациентов, достигших целевого уровня при домашнем мониторировании АД в течение 60 дней. Так, в группе Мексиприма 84 % пациентов достигли целевого уровня АД по сравнению с 69 % пациентов контрольной группы (Р = 0,0343), что подтверждает как важность эмоционального, депрессивного фактора в развитии АГ, так и эффективность самой методики домашнего измерения АД для оценки среднего уровня АД в течение 60 дней.
5. Переносимость Мексиприма в течение 60 дней оценивали как хорошую 95,09 % пациентов на фоне нейтрального влияния Мексиприма на основные биохимические жизненные показатели.
1. Cooney M.T., Kotseva K., Dudina A. et al. Determinants of risk factor control in subjects with coronary heart disease: a report from the EUROASPIRE III investigators // European Journal of Preventive Cardiology. — 2013. — Vol. 20. — P. 686–691.
2. Kotseva K., Wood D., De Backer G. et al. EUROASPIRE III. Management of cardiovascular risk factors in asymptomatic high-risk patients in general practice: cross-sectional survey in 12 European countries // European Journal of Preventive Cardiology. — 2010. — Vol. 17. — P. 530–540.
3. Kotseva K., Wood D., De Backer G. et al. Use and effects of cardiac rehabilitation in patients with coronary heart disease: results from the EUROASPIRE III survey // European Journal of Preventive Cardiology. — 2013. — Vol. 20. — P. 817–826.
4. Gyberg V., Kotseva K., Dallongeville J. et al. Does pharmacologic treatment in patients with established coronary artery disease and diabetes fulfil guideline recommended targets? A report from the EUROASPIRE III cross-sectional study // European Journal of Preventive Cardiology. — April 1, 2014. — 2047487314529353.
5. Pajkа A., Jankowski P., Kotseva K. Depression, anxiety, and risk factor control in patients after hospitalization for coronary heart disease: the EUROASPIRE III Study // European Journal of Preventive Cardiology April. — 2013. — Vol. 20. — Р. 331–340.
6. Смулевич А.Б. Депрессии в общей медицине: Руководство для врачей. — М.: Мед. информ. агентство, 2001. — 256 с.
7. Meg L., Chen D., Yang Y. et al. Depression increases risk of hypertension incidence: a meta-analyses of prospective cohort study // Journal of Hypertension. — 2012. — Vol. 30. — P. 842–851.
8. Мексидол: применение препарата при остром нарушении мозгового кровообращения. — М.: Фармсофт, 2000. — 13 с.
9. World Medical Association Declaration of Helsinki. Ethical Principles for Medical Research Involving Human Subjects. — WMA, 2004 (Хельсинкская декларация Всемирной медицинской ассоциации. Этические принципы для медицинских исследований с привлечением человека в качестве субъекта испытания. — WMA, 2004).

/4_u/4_u.jpg)
/4_u/4_u2.jpg)
/5_u/5_u.jpg)