Журнал «» 2 (40) 2015
Вернуться к номеру
Суточное мониторирование артериального давления с использованием интеллектуального анализа данных: новые диагностические возможности
Авторы: Хурса Р.В. — Белорусский государственный медицинский университет, г. Минск; Войтикова М.В. - Институт физики им. Б.И. Степанова НАН Республики Беларусь, г. Минск
Рубрики: Кардиология
Разделы: Клинические исследования
Версия для печати
С помощью интеллектуального анализа данных разработана классификация гемодинамических состояний по коэффициентам линейной регрессии параметров артериального давления при суточном мониторировании и представлена в виде номограмм для функциональной диагностики за дневной, ночной и суточный периоды наблюдения. Номограмма позволяет по регрессионным коэффициентам дифференцировать 10 различных гемодинамических состояний (классов) у пациентов с клинической артериальной гипертензией, гипотензией и нормотензией: гемодинамику гармонического типа, дисфункциональных типов (диастолического или систолического), а также квазигипертензию у нормотензивных лиц с гармоническим типом (впервые открытый класс). Предложенный подход открывает новые возможности диагностики клинически латентных патологических состояний гемодинамики у нормотензивных лиц, определяя контингент нуждающихся в дообследовании и динамическом наблюдении, а также индивидуальных гемодинамических особенностей у пациентов с артериальной гипертензией и гипотензией, что требует дифференцированных подходов к лечению.
За допомогою інтелектуального аналізу даних розроблена класифікація гемодинамічних станів за коефіцієнтами лінійної регресії параметрів артеріального тиску при добовому моніторуванні і наведена у вигляді номограм для функціональної діагностики за денний, нічний і добовий періоди спостереження. Номограма дозволяє за регресійними коефіцієнтами диференціювати 10 різних гемодинамічних станів (класів) у пацієнтів із клінічною артеріальною гіпертензією, гіпотензією та нормотензією: гемодинаміку гармонійного типу, дисфункціональних типів (діастолічного або систолічного), а також квазігіпертензію у нормотензівних осіб із гармонійним типом (уперше відкритий клас). Запропонований підхід відкриває нові можливості діагностики клінічно латентних патологічних станів гемодинаміки у нормотензівних осіб, визначаючи контингент, який потребує дообстеження і динамічного спостереження, а також індивідуальних гемодинамічних особливостей у пацієнтів з артеріальною гіпертензією та гіпотензією, що потребує диференційованих підходів до лікування.
Classification of hemodynamic states is developed using data mining by coefficients of linear regression of blood pressure parameters within 24-hour ambulatory blood pressure monitoring and is presented as diagnostic nomograms for functional diagnostics for the day, night and daily periods of observation. The nomograms enable to diagnose 10 various hemodynamic states (classes) by regression coefficients in patients with arterial hypertension, hypotension and normotension: hemodynamics of harmonious type, of dysfunctional types (either diastolic or systolic), as well as the quasi-hypertension in normotensive persons with harmonious type (it is a newly open class). The offered approach opens new possibilities of diagnostics for clinically latent pathological hemodynamic states in normotensive persons, determining those who need further observation and case follow-up, as well as individual hemodynamic features in hypertensive and hypotensive patients that require differentiated approaches to the treatment.
артериальное давление, линейная регрессия, гемодинамика, классификация, диагностическая номограмма.
артеріальний тиск, лінійна регресія, гемодинаміка, класифікація, діагностична номограма.
blood pressure, linear regression, hemodynamics, classification, diagnostic nomogram.
Статья опубликована на с. 34-40
Перспективным стратегическим направлением борьбы с артериальной гипертензией (АГ) и предупреждения ее последствий является раннее выявление заболевания и проведение адекватных профилактических и лечебных мероприятий. Однако при кажущейся простоте диагностики, базирующейся на выявлении повышенных цифр артериального давления (АД) при обычных измерениях с последующим уточнением сердечно-сосудистого риска, у значительного числа пациентов заболевание распознается поздно, уже при наличии поражения органов-мишеней или тяжелых сердечно-сосудистых осложнений. Такая запоздалая диагностика препятствует успешной вторичной профилактике при этом заболевании и указывает на необходимость своевременного выявления контингента лиц, нуждающихся в целенаправленной первичной профилактике. В связи с этим актуален поиск наиболее информативных предвестников развития АГ, поскольку клинически явному заболеванию, несомненно, предшествует период латентных нарушений функционирования сердечно-сосудистой системы. К таким «доклиническим» предикторам у лиц с еще нормальным АД и отсутствием явных сердечно-сосудистых заболеваний можно отнести (помимо известных факторов риска — анамнестических, антропометрических и др.) отклонения функциональных показателей, всегда в той или иной степени сопровождающие АГ: повышенную вариабельность АД в течение суток, увеличение сосудистой жесткости, изменение параметров центральной гемодинамики и др. Однако выявление таких нарушений требует использования специальных инструментальных методик, что в реальной медицинской практике проводится только по обоснованным показаниям.
Суточное мониторирование артериального давления (СМАД) стандартизованными аппаратными средствами позволило лучше выявлять АГ и выделять различные ее варианты, отличающиеся в прогностическом аспекте: истинную гипертензию (true hypertension); гипертензию белого халата (white coat hypertension); скрытую (маскированную) гипертензию (masked hypertension) по T. Pickering et al. В проспективных исследованиях показано, что относительный риск сердечно-сосудистой смерти или инсульта у лиц с истинной и скрытой гипертензией (нормальное АД при традиционных измерениях, но повышенное при СМАД) достоверно выше, чем у истинно нормотензивных людей (нормальное АД как при традиционных измерениях, так и при СМАД) [1, 2].
Несмотря на длительный период (несколько десятилетий) клинического использования СМАД, применение этого метода по-прежнему имеет определенные ограничения и не до конца решенные вопросы. Это касается требований к качеству аппаратуры и ее унификации, продолжительности мониторирования (обсуждается, в частности, целесообразность 48-часовой длительности исследования), учета влияния на результаты СМАД образа жизни пациента и его комплайентность (не все пациенты согласны на такую процедуру и выдерживают ее необходимое время) и т.п.
Имеются также вопросы по оценке результатов исследования. На основе получаемого при СМАД ряда величин АД предложено большое количество различных расчетных индексов, но по многим из них отсутствует международная унификация нормативов, нечетко определены диагностическая и прогностическая значимость многих индексов, нет единых стандартов формулировки заключений по результатам СМАД и др. Известно, что традиционные (наиболее употребляемые) показатели СМАД при изолированном применении имеют низкую информативность (особенно для ранних стадий АГ), а интерпретация результатов исследования у конкретного пациента нередко вызывает трудности из-за часто выявляемых отклонений от нормы отдельных параметров, хотя при групповом анализе большинство используемых показателей достоверно различаются у пациентов с АГ и у нормотензивных людей.
Поэтому в настоящее время идет поиск эффективных методов анализа, в том числе многомерное статистическое моделирование. Большинство предлагаемых моделей пока мало используются в широкой клинической практике (сложны для клинической интерпретации, ограничены трудно выполнимыми на живом организме условиями и др.), однако возможности статистического моделирования далеко не исчерпаны.
В частности, нами предложен и обоснован методологический подход, предполагающий построение статистической модели индивидуального кровообращения по временнóму ряду величин АД пациента, которая представляет собой зависимости (линейные регрессии) систолического (S) и диастолического (D) давления от пульсового давления W (где W = S – D). Регрессионная модель кровообращения в общем аналитическом виде выглядит сопряженными уравнениями: S = Q + aW, D = Q + (a – 1)W, где коэффициенты a и Q имеют индивидуальные числовые значения и характеризуют кровообращение в интервале времени наблюдения. По существу получаемой регрессии постоянная Q имеет смысл величины давления крови в области исчезающей пульсовой волны (такой кровоток имеет место в конечной части артериол), а соотношение прессорного (a) и депрессорного (a – 1) коэффициентов, отражающее соответственное участие сердца и сосудов в продвижении крови, определяет гемодинамический тип. Обоснованы граничные значения коэффициента a, разделяющие функциональные гемодинамические типы, и клиническое содержание последних. Применение индивидуальной линейной регрессии параметров S и D по W в качестве способа функциональной диагностики гемодинамики дает характеристику кровообращения как взаимодействия сердца и сосудов в процессе продвижения крови и названо способом КАСПАД — количественный анализ связей параметров АД [3, 4].
Определенный диагностический потенциал имеет и регрессия между такими параметрами, как S и D: S = B + A · D, где B и A — индивидуальные коэффициенты регрессии. В частности, в качестве одного из параметров СМАД предложен так называемый амбулаторный индекс жесткости артерий (AASI), определяемый по линейной регрессии D на S, поскольку была показана корреляция коэффициентов этой регрессии со скоростью распространения пульсовой волны [5, 6].
Различные гемодинамические типы по КАСПАД — гармонический (нормальный) или дисфункциональные (патологические) — наблюдаются у лиц как с нормальным измеряемым АД, так и с патологическим (гипертензия, гипотензия) и при этом сопровождаются разной величиной давления Q — как нормальной, так и измененной в обе стороны. По нашим данным, полученным при КАСПАД, у 556 практически здоровых людей молодого возраста (до 30 лет) среднее значение Q составило 86,4 мм рт.ст. (95% доверительный интервал (ДИ) 85,1–87,7), в том числе по типам: при диастолическом дисфункциональном (102 чел.) — 61,9 мм рт.ст. (95% ДИ 59,3–64,5), при гармоническом (354 чел.) — 90,2 мм рт.ст. (95% ДИ 88,8–91,6), при систолическом дисфункциональном (34 чел.) — 123,9 мм рт.ст. (95% ДИ 115,9–131,9) [7]. При АГ в начальных стадиях в большинстве случаев отмечается гармонический КАСПАД-тип с высоким Q (более 100 мм рт.ст.). На фоне лечения обычно формируется диастолический дисфункциональный тип (у 60–70 %), сопровождающийся разной степенью снижения его величины, причем порой чрезмерной (менее 50 мм рт.ст.) [3, 4, 8].
Поэтому рассмотренная выше идентификация гемодинамики пациента по КАСПАД (как определенный тип кровообращения с индивидуальной величиной давления Q) может быть дополнена путем совместного учета всех параметров регрессии (a, Q, A, B) или выбора их оптимальных комбинаций. В частности, современные информационные технологии и алгоритмы интеллектуального анализа данных (Data Mining) обладают большим потенциалом в данном направлении.
Цель исследования: дальнейшее развитие метода регрессионного моделирования параметров АД с помощью интеллектуального анализа данных при СМАД для дифференциации (классификации) гемодинамических состояний по показателям линейной регрессии и определение перспектив его применения в функциональной диагностике сердечно-сосудистой системы.
Материалы и методы исследования
Изучались ряды величин АД 214 пациентов, зарегистрированные при СМАД в течение стандартных периодов наблюдения (за день, ночь и суммарно за сутки). Собственная база данных получена при помощи мониторов серии BPLab (Россия), с интервалом измерений через 15 мин в дневное время, 30 мин — в ночное. Нормотензивные пациенты были представлены здоровыми и практически здоровыми лицами (группы диспансерного наблюдения ДI и ДII соответственно) в количестве 121 человека (57 мужчин и 64 женщины) в возрасте 18–48 (23,8 ± 5,1) лет. Группу лиц с впервые выявленной (согласно действующим рекомендациям) АГ 1–2-й степени, риск 1–3 до начала лечения, составили 50 пациентов (24 женщины и 26 мужчин) в возрасте 19–59 (32,7 ± 9,8) лет.
Была также использована электронная база данных СМАД [9], представленная временными рядами АД 43 пациентов отделения интенсивной терапии с вторичной гипотонией, обусловленной разными тяжелыми основными заболеваниями (посттравматическая легочная недостаточность, инфаркт миокарда, сердечная недостаточность и др.), которые пережили хотя бы один эпизод острой гипотензии. Эту группу составили 21 мужчина в возрасте 22–90 (64,3 ± 20,4) лет и 22 женщины в возрасте 60–90 (74,8 ± 12,5) лет (группы H1, H2, C2 с высоким риском вторичной гипотонии из [9]). В обработку взяты АД-сигналы с интервалом 15 мин в дневной и 30 мин в ночной периоды. Предварительный анализ рядов АД позволил установить, что удаление отдельных величин или изменение частоты дискретизации ряда АД практически не влияет на вычисляемые регрессионные коэффициенты.
Для каждого пациента проводилось регрессионное моделирование параметров АД с нахождением индивидуальных коэффициентов a, Q, A, B, которые служили координатами векторов для использования Data Mining, в частности, алгоритма Support Vector Machine (SVM — машина опорных векторов) [10].
SVM-алгоритм применялся неоднократно, что каждый раз обеспечивало разный состав обучающей выборки, и к различным сочетаниям параметров регрессии {Q, a, A, B}. С помощью ROC-критерия выбран классификатор, оптимальный по качеству, наглядности и простоте. Уравнения разделяющих прямых получены методом наименьших квадратов и использованы для построения диагностических номограмм (карт) раздельно за дневной, ночной и суточный периоды СМАД.
Полученные номограммы были тестированы в двух параллельных исследованиях. Во-первых, на ретроспективных данных СМАД 385 пациентов с разными заболеваниями, обследованных в отделении функциональной диагностики 9-й клинической больницы г. Минска с помощью отечественного монитора «Кардиан-МД», определена распространенность гемодинамических классов согласно предложенной классификации. Во-вторых, на собственных данных СМАД, полученных на мониторах BPLab (Россия), у 126 практически здоровых молодых людей в возрасте 22 (21; 24) лет (группа 1) и у 49 пациентов того же возрастного периода — 30 (26; 38) лет с впервые установленной АГ 1–2-й степени до начала лечения (группа 2) проведен сравнительный анализ традиционных параметров СМАД при разных гемодинамических классах. Анализировались средние показатели суточного, дневного и ночного систолического (САД), диастолического (ДАД), среднего гемодинамического (СрАД) и пульсового (ПАД) давления; показатели «нагрузки давлением» и «нагрузки гипотензией» (индексы времени, площади, измерений САД и ДАД), вариабельность САД и ДАД; суточный индекс (СИ) — степень ночного снижения давления; величина и скорость утреннего подъема (ВУП и СУП) САД и ДАД, а также показатели ригидности артерий: время распространения пульсовой волны (РТТ2), которое определяется по идентификации волны отражения от бифуркации аорты, максимальная скорость нарастания АД (dP/dtmax), индекс ригидности артерий (ASI), индекс аугментации (AIx%), амбулаторный индекс жесткости (AASI), систолический индекс площади (Ssys) [11].
Установление соответствия вида распределения признаков закону нормального распределения проводилось по критериям Шапиро — Уилка и Лиллиефорса, анализ достоверности различий — по критериям Манна — Уитни (U-критерий) и x2 (для относительных величин). Различия считались достоверными при Р < 0,05.
Результаты и обсуждение
Технологии интеллектуального анализа данных (Data Mining) основаны на поиске в базе данных каких-то скрытых закономерностей (шаблонов информации), действующих на основе правил, формализующих экспертные знания, тогда как традиционные статистические методы анализа ориентированы в основном на проверку заранее сформулированных гипотез. SVM — один из эффективных алгоритмов с простой математической постановкой задачи, не страдающий от «переобучения» (влияния частных закономерностей в обучающей выборке) в отличие от нейронных сетей. Этот машинный алгоритм основан на обучении на примерах (библиотека образцов) и предполагает разделение объектов (их классификацию) в пространстве признаков с помощью гиперплоскости, максимально разделяющей векторы характерных признаков объектов из разных классов. Координаты вектора описывают отдельные атрибуты объекта. Алгоритм предусматривает автоматическое разбиение случайным образом общей базы данных на обучающую (библиотека образцов) и контрольную выборки в соотношении 75 и 25 % (в настоящем исследовании — 160 и 54 пациента соответственно). SVM строит классифицирующую функцию при непрерывном уменьшении эмпирической ошибки классификации объектов; обучение SVM-классификатора завершается при достижении максимального качества разделения образцов.
Применение SVM к любым сочетаниям параметров {Q, a, A, B} позволило получить несколько классификаторов: на основе 2, 3 и 4 параметров регрессии. В итоге оптимальным оказался классификатор на основе только 2 параметров: {Q, a}. Критериями такого выбора были качество классификации по ROC-критерию (число верно/неверно классифицированных образцов), наглядность на номограмме (максимальное разделение образцов в пространстве) и простота (уменьшение входных признаков до двух). Применение алгоритма SVM к другой естественной паре параметров {A, B} дало сходное качество разделения образцов, но при худшей наглядности номограммы.
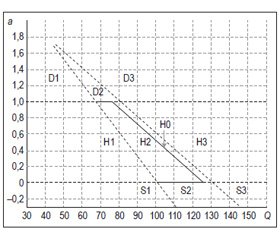
Были установлены границы раздела гемодинамических состояний пациентов трех клинических групп (областей гипотензия/нормотензия/гипертензия), учитывающие параметры регрессии a и Q. Уравнения границ раздела (разделяющих функций) гемодинамических областей для дневного, ночного и суточного АД пациентов по результатам SVM-классификации различались (табл. 1, рис. 1–3).
Рис. 1–3 демонстрируют основную идею SVM-классификатора в плоскости вектора атрибутов x = {Q, a} для дневного, ночного и суточного периодов наблюдения в виде номограмм с нанесенными линейными разделяющими функциями (наклонные косые) и горизонтальными пунктирными линиями раздела КАСПАД-типов: между гармоническим и систолическим дисфункциональным типами на уровне а = 0, гармоническим и диастолическим дисфункциональным на уровне а = 1.
На номограммах (рис. 1–3) видно, что у одной части пациентов с АГ имеется гармоничное кровообращение, то есть 0 < a < 1 (это означает, что пропульсивная работа сердца в обеспечении циркуляции крови составляет большую часть, а участие сосудов, соответственно, меньшую, причем отрицательно направленную), а у другой — диастолическое дисфункциональное: 1 < a < 2. Значение 1 < a указывает на возникновение противоположно направленной составляющей в диастолическом давлении из-за чрезмерного возрастания роли систолической составляющей (то есть работы сердца) в процессе кровообращения при соответствующем снижении роли его диастолической (сосудистой) составляющей [12]. Такая гемодинамика наиболее характерна для длительно существующей АГ, особенно на фоне лечения [4], что позволяет заподозрить позднюю диагностику заболевания у некоторых пациентов в данном исследовании. На рис. 1–3 также видно, что АГ отличается от нормотензии более высокими значениями давления Q при любом гемодинамическом типе.
/38/38.jpg)
Для пациентов с вторичной гипотензией (область «Гипотензия») характерна диастолическая дисфункция кровообращения с низким давлением в области затухающей пульсовой волны (1 < а, Q < 70 мм рт.ст.), что подтверждает нашу трактовку данного КАСПАД-типа как типа, при котором кровоток обеспечивается за счет усилий сердца при недостаточном участии сосудов [3, 4].
Отсутствие в настоящем исследовании лиц с систолическим дисфункциональным типом в областях «Гипертензия» и «Гипотензия» не исключает его принципиальной возможности при такой патологии, поскольку этот гемодинамический КАСПАД-тип чрезвычайно редок в популяции [3, 4, 8].
Наиболее важные гемодинамические различия касаются области «Нормотензия», особенно в дневной период наблюдения: зона нормотензии с диастолическим дисфункциональным типом значительно сужается по мере увеличения коэффициента а, максимально приближаясь к двум противоположным патологическим гемодинамическим состояниям — к гипотензии и АГ (рис. 1). Эти гемодинамические состояния с принципиально разными измеряемыми величинами АД объединены общностью механизмов адаптации сердечно-сосудистой системы: гипертрофированной ролью работы сердца в процессе продвижения крови при недостаточном участии сосудистой составляющей этого процесса, о чем свидетельствует диастолический дисфункциональный КАСПАД-тип. Данный тип всегда сопровождается снижением Q, что, видимо, является признаком адаптационной гемодинамической реакции организма [3].
Ранее мы показали, что практически здоровые молодые лица с таким типом гемодинамики имеют функциональные сосудистые нарушения в виде ухудшения эндотелийзависимой вазодилатации и увеличения скорости распространения пульсовой волны [13]. Изложенные обстоятельства подтверждают патологический характер дисфункционального диастолического типа и дают основания предполагать, что нормотензивные пациенты с таким кровообращением имеют латентные гемодинамические нарушения с возможной (в долгосрочной перспективе) манифестацией сердечно-сосудистой патологии, в первую очередь АГ. В связи с этим нормотензивные пациенты с дисфункциональным кровообращением по данным КАСПАД нуждаются в дальнейшем мониторинге как группа повышенного риска АГ.
SVM-анализ АД за дневной период выявил еще одно важное обстоятельство: в зоне гармонического типа среди нормотензивных лиц классификатор выделил область, названную «Квази-АГ» (то есть подобный АГ), где множества гипер- и нормотензивных лиц перекрываются. То есть гемодинамика лиц, попавших в эту область, хоть и характеризуется гармоническим кровообращением (0 < а < 1), но по каким-то скрытым характеристикам сходна с гемодинамикой пациентов с АГ, также оказавшихся в этой области, где равновероятно представлены регрессионные параметры АД нормо- и гипертензивных пациентов. Можно предположить, что эта подгруппа представляет пациентов с переходным к АГ гемодинамическим состоянием.
С учетом выделения области «Квази-АГ», которая на номограмме находится в границах –0,02Q + 2,52 < a < < –0,02Q + 2,62, 0 < a < 1, область истинно гармонического нормотензивного кровообращения для дневного периода (рис. 1) заключена пределах: –0,03Q + 3,03 < < a < –0,02Q + 2,52 (табл. 1). Следует особо отметить, что квази-АГ отсутствует на номограммах ночного (рис. 2) и суточного (рис. 3) периодов наблюдения, а разделяющая функция между нормотензией и квази-АГ в эти периоды сливается с разделяющей функцией между нормотензией и гипертензией. Возможно, это связано со снижением влияния корковых структур центральной нервной системы на гемодинамику в ночное время, приводящим к нормализации последней в этот период, и согласуется с известными представлениями об АГ как психосоматическом заболевании. Вероятно, по той же причине на «ночной» номограмме в зоне нормотензии оказывается большее число наблюдений, чем на «дневной», а также увеличивается дистанция между гипотензией и гипертензией за счет расширения области нормотензии.
Таким образом, созданная диагностическая номограмма позволяет дифференцировать 10 гемодинамических классов (рис. 4): артериальная гипертензия гармонического (H3) или дисфункциональных типов (диастолического — D3, систолического — S3); артериальная гипотензия гармонического (H1) или дисфункциональных типов (диастолического — D1, систолического — S1); гемодинамика гармонического типа у нормотензивых лиц (H2), латентные гемодинамические нарушения у нормотензивных лиц в виде дисфункциональных (диастолического — D2 или систолического — S2) типов и квазигипертензия (квази-АГ) у нормотензивных лиц (H0). Следует подчеркнуть, что класс квази-АГ (впервые обнаруженный) определяется исключительно на номограмме дневного периода СМАД, который следует признать наиболее важным в диагностическом плане.
/39/39.jpg)
Для использования номограммы в функциональной диагностике необходимо нанести на нее координаты — значения индивидуальных коэффициентов линейной регрессии параметров АД a и Q, а точка пересечения этих координат попадает в область, определяющую принадлежность пациента к одному из указанных гемодинамических классов.
Применение номограммы к ретроспективным данным СМАД 385 пациентов, госпитализированных с различной патологией, выявило нормотензивное гармоническое кровообращение (класс H2) у 28 % пациентов группы, у остальных — различные патологические классы, в том числе квази-АГ (H0) у 13,5 % (табл. 2).
Результаты SVM-классификации по данным СМАД, выполненного нами в двух группах пациентов (группа 1 — здоровые молодые люди, группа 2 — пациенты с впервые диагностированной АГ), представлены в табл. 3. В группе 1 классификатор отнес к гармоническому нормотензивному классу (оптимум нормы — Н2) только 58,7 %, у остальных были различные варианты патологического кровообращения, в том числе квази-АГ (H0) — у 13,5 % (17 чел.) и даже АГ разных типов (у 11,9 %): гармонического типа (H3) — 13 чел., диастолического дисфункционального (D3) — 2 чел.
В группе 2 преобладающее большинство пациентов (67,3 %) закономерно относились к классу H3 (АГ гармонического типа), 16,3 % — к АГ диастолического дисфункционального типа (что более характерно для АГ на фоне лечения или длительного периода болезни); 6,1 % — к квази-АГ; по 1 пациенту — даже к гипотензии гармонического и диастолического дисфункционального типов (табл. 3), что, несомненно, указывает на использование этими пациентами гипотензивных средств, причем неадекватно. Такая разная организация кровообращения при АГ должна предусматривать дифференцированные подходы к медикаментозной терапии.
Поскольку выделение патологических гемодинамических классов базируется исключительно на результатах SVM-анализа коэффициентов линейной регрессии параметров АД, то встает вопрос об особенностях характеристик кровообращения этих пациентов по традиционным оценочным критериям СМАД, в частности у нормотензивных лиц. О патологическом характере диастолического дисфункционального типа у нормотензивных лиц упомянуто выше, поэтому вызвали интерес классы квази-АГ (Н0) и Н3 (гармонический гипертензивный тип), выявленные у практически здоровых молодых людей.
В группе 1 традиционные показатели СМАД (среднегрупповые) по подавляющему большинству параметров соответствовали принятым нормам и с высокой достоверностью отличались от таковых у пациентов с АГ. Не выявлено достоверных отличий групп по величине ЧСС, ВУП САД и ВУП ДАД, СИ по САД, а также по «сосудистым показателям» — индексу ригидности артерий, индексу аугментации, индексу жесткости, максимальной скорости нарастания АД. Это может быть связано с достаточно молодым возрастом и невысокой, в основном, степенью АГ у пациентов группы 2. Однако при индивидуальном анализе почти у каждого пациента из группы здоровых лиц хотя бы один из показателей СМАД выходил за пределы принятых норм. Так, имелось превышение нормы ПАД днем (> 46 мм рт.ст.) у 64 чел. (50,8 %), ВУП САД (> 56 мм рт.ст.) — у 8 чел. (6,4 %), ВУП ДАД (> 36 мм рт.ст.) — у 22 чел. (17,5 %), СУП САД и/или СУП ДАД — у 119 чел. (94,4 %), различные нарушения суточного индекса САД и/или ДАД имели 86 чел. (68,2 %) и т.д. У 8 здоровых молодых людей (6,3 %) были повышенные среднесуточные индексы нагрузки давлением (ИВСАД, ИВДАД), а среднесуточные параметры их АД соответствовали повышенным нормальным.
У нормотензивных лиц патологических SVM-классов средние значения параметров СМАД также не выходили за пределы принятых норм, но отдельные из них имели статистически значимые различия с классом H2 (оптимальная гемодинамика нормотензивных лиц) и отсутствие различий с группой 2 при наличии таковых в классе H2.
Так, класс H3 (гипертензия гармонического типа, диагностированная SVM-классификатором у практически здоровых людей) демонстрировал статистически значимые отличия (Р < 0,05) от класса Н2: более высокие показатели АД (САД, ДАД, СрАД), ЧСС и систолического индекса площади (Ssys) за все периоды наблюдения, индексов «нагрузки давлением» (площади, времени, измерений САД и ДАД) за дневной и суточный периоды, вариабельности САД днем, степени ночного снижения САД и ДАД (СИ), а также более низкие значения времени распространения пульсовой волны РТТ2. По ряду этих параметров класс Н3 не отличался значимо от пациентов с АГ, тогда как класс Н2 имел достоверные отличия (табл. 4).
Класс Н0 (квази-АГ) также имел статистически значимые отличия (Р < 0,05) от класса Н2: более высокие значения АД (САД, ДАД, СрАД, ПАД) и максимальной скорости прироста АД за все периоды наблюдения, индексов «нагрузки давлением» (площади, времени, измерений САД и ДАД) за дневной и суточный периоды, вариабельности САД и ДАД в дневной период, суточного индекса САД и ДАД. По ряду этих параметров класс Н0 не отличался значимо от пациентов с АГ, тогда как класс Н2 такие отличия имел.
В классах Н3 и Н0 были также достоверно ниже, чем в классе Н2, индексы «нагрузки гипотензией» (площади, времени, измерений по САД и по ДАД) за дневной и суточный периоды. Причем по большинству гипотензивных показателей они не отличалась от пациентов с АГ, а класс Н2 отличался. Таким образом, эпизоды значительного снижения АД (менее 100/60 мм рт.ст. днем и 85/48 мм рт.ст. ночью), наблюдавшиеся у некоторых здоровых лиц класса Н2, у лиц с АГ практически не встречались, а у пациентов из категории Н0 и Н3 они были крайне редки и кратковременны.
Сравнительные характеристики некоторых традиционных параметров СМАД у пациентов классов Н2 (нормотензивные лица с оптимальным гармоническим кровообращением), Н0 (квази-АГ), Н3 (гармоническая гемодинамика гипертензивных лиц) из группы 1 и у пациентов с АГ (группа 2 в целом) приведены в табл. 4.
Обращает на себя внимание достаточная большая распространенность различных нарушений СИ как у лиц с АГ, так и у нормотензивных, причем без значимых отличий, в том числе между классами группы 1 (Р > 0,05): в группе 2 — у 63,2 % (31 чел.), в группе 1 — у 66,7 % (50 чел.) в классе Н2; у 82,3 % (14 чел.) в классе Н0; 76,9 % (10 чел.) в классе Н3. То есть наибольшее число нарушений СИ было у классов квази-АГ и Н3, самым частым был тип overdipper: по ДАД — 52,9 % (9 чел.) и 69,2 % (9 чел.) соответственно, по САД и ДАД — 11,8 % (2 чел.) и 23,1 % (3 чел.) соответственно, что значимо больше, чем таких нарушений в классе H2 (1,3 %).
Таким образом, гемодинамика пациентов группы 1, отнесенная классификатором (исключительно на основе коэффициентов линейной регрессии параметров АД) к «патологическим» классам — Н3 (гипертензия) и Н0 (квази-АГ), по значениям традиционных показателей СМАД, принятых в качестве диагностических признаков АГ, занимает промежуточное положение между таковыми у нормотензивных лиц и у пациентов с АГ. При этом отмеченные выше показатели не выходят за пределы принятых для них норм, но уже достоверно отличаются от таковых показателей у нормотензивных лиц с оптимальным гармоническим кровообращением, и по ряду из них уже не отличаются от таковых при АГ.
Является ли данное обстоятельство достаточным основанием для диагностики у нормотензивных пациентов гемодинамических классов Н0 и Н3 клинического заболевания — АГ? Наверное, однозначно утвердительного ответа на этот вопрос дать нельзя, но совершенно очевидно, что таких пациентов нужно рассматривать как группу повышенного риска АГ, требующую дообследования и динамического наблюдения. Такого же отношения требуют и нормотензивные лица с дисфункциональными гемодинамическими типами (классы D и S), как показано нами в предыдущих исследованиях. Что касается клинически явной гипотензии или АГ, то их гемодинамическая неоднородность должна быть учтена при выборе медикаментозной терапии. Кроме того, остается открытым вопрос о прогностической значимости гемодинамических классов и КАСПАД-типов в плане развития не только АГ, но и связанных с ней сердечно-сосудистых осложнений и исходов.
Выводы
1. Дальнейшее развитие метода регрессионного моделирования параметров АД при СМАД путем использования SVM-алгоритма интеллектуального анализа данных (Data Mining) для индивидуальных регрессионных коэффициентов a и Q позволило создать диагностическую номограмму (карту гемодинамических классов) для дневного, ночного и суточного периодов наблюдения.
2. Номограмма позволяет только по регрессионным коэффициентам дифференцировать 10 различных гемодинамических состояний (классов) у пациентов с клинической артериальной гипертензией, гипотензией и нормальным АД: гемодинамику гармонического типа, дисфункциональных типов (диастолического или систолического), а также квази-АГ у нормотензивных лиц с гармоническим типом — впервые открытый класс.
3. Тестирование диагностической номограммы на разных базах данных СМАД подтвердило возможность выявления всех описанных гемодинамических состояний (классов) у пациентов различных клинических групп. Класс квази-АГ определяется только в дневной период СМАД.
4. У 10,3 % (13 чел.) практически здоровых нормотензивных молодых людей по номограмме выявлен класс АГ гармонического типа, у 13,5 % (17 чел.) — квази-АГ. У лиц с этими патологическими гемодинамическими классами ряд традиционных показателей СМАД, наиболее информативных для диагностики АГ, достоверно отличается от таковых у нормотензивных лиц с оптимальным гармоническим кровообращением, занимая по значениям промежуточное положение между нормотензивными лицами и пациентами с АГ. По некоторым из показателей эти классы не отличались значимо от пациентов с АГ, тогда как класс оптимального гармонического типа имел достоверные отличия.
5. Предложенный подход и разработанная номограмма гемодинамических состояний (классов) имеют перспективы применения в функциональной диагностике сердечно-сосудистой системы, так как открывают новые возможности выявления клинически латентных патологических состояний гемодинамики, определяя контингент лиц, нуждающихся в дообследовании и динамическом наблюдении, а также индивидуальных гемодинамических особенностей у пациентов с АГ и гипотензией, требующих дифференцированных подходов к лечению.
1. Pickering T.G., Davidson K., Gerin W., Schwartz J.E. Masked Hypertension // Hypertension. — 2002. — № 40. — Р. 795–796.
2. Sega R., Trocino G., Lanzarotti A. et al. Alterations of cardiac structure in patients with isolated office, ambulatory, or home hypertensions: data from general population (Pressione Arteriose Monitorate E Loro Associazioni [PAMELA] Study) // Circulation. — 2001. — № 104. — Р. 1385–1392.
3. Хурса Р.В., Чеботарев В.М. Гемодинамические детерминанты гомеостаза и адаптации // Клинич. физиология кровообращения. — 2007. — № 4. — С. 71–77.
4. Хурса Р.В. Пульсовое давление крови: роль в гемодинамике и прикладные возможности в функциональной диагностике // Мед. новости. — 2013. — № 4. — С. 13–19; Артериальная гипертензия. — 2014. — № 5(37). — С. 21–28.
5. Benetos A., Lacolley P. From 24-Hour Blood Pressure Measurements to Arterial Stiffness: A Valid Short Cut? // Hypertension. — 2006. — Vol. 47. — P. 327–328.
6. Dolan E., Thijs L., Li Y. et al. Ambulatory arterial stiffness index as a predictor of cardiovascular mortality in the Dublin Outcome Study // Hypertension. — 2006. — Vol. 47. — P. 365–370.
7. Хурса Р.В. Латентные нарушения кровообращения у молодых людей и их коррекция при модификации образа жизни с включением физических нагрузок // Оздоровительная физическая культура молодежи: актуальные проблемы и перспективы: Материалы II Международной научно-практической конференции, Минск, 2–3 апреля 2015 года. — Минск, БГМУ, 2015. — С. 131–136. — http://www.bsmu.by/page/8/2908/ [Электронный ресурс].
8. Хурса Р.В. Непульсирующий компонент АД при разных способах определения и новые гемодинамические характеристики // Артериальная гипертензия и профилактика сердечно-сосудистых заболеваний: Материалы VI Международной конф. — Витебск, ВГМУ, 2011. — С. 83–87.
9. The MIMIC II Project database. URL: http://physionet.org/physiobank/database/mimic2db
10. Войтикова М.В., Войтович А.П., Хурса Р.В. Применение интеллектуального анализа данных для классификации гемодинамических состояний // Врач и информационные технологии. — 2013. — № 1. — С. 32–41.
11. Рогоза А.Н. Суточное мониторирование артериального давления при гипертонии (методические вопросы) / А.Н. Рогоза, В.П. Никольский, Е.В. Ощепкова [и др.]. — М., 1997.
12. Способ диагностики диастолической дисфункции кровообращения: Патент BY № 6950 / В.М. Чеботарев, Р.В. Хурса. — Заявка № а20010017; Приор. 09.01.2001.
13. Хурса Р.В. Функциональное состояние сосудов у практически здоровых лиц с патологическими гемодинамическими типами (по данным линейной регрессии параметров артериального давления) // Медицинская панорама. — 2014. — № 7. — С. 5–9; Артериальная гипертензия. — 2014. — № 6(38). — С. 39–45.

/37/37.jpg)
/37/37_2.jpg)
/39/39_2.jpg)