Журнал «Травма» Том 16, №3, 2015
Вернуться к номеру
Сравнительный анализ напряжений в системе «кость — имплантат» при эндопротезировании головки лучевой кости разными конструкциями
Авторы: Страфун С.С. - Отдел микрохирургии и реконструктивно-восстановительной хирургии верхней конечности НИИ травматологии и ортопедии НАМН Украины, г. Киев; Бойко И.В. - Государственное управление делами Президента Украины, ГНУ «НПЦ ПКМ», центр малоинвазивной хирургии, г. Киев; Макаров В.Б. - ГУ «Специализированная медико-санитарная часть № 6», г. Днепропетровск; Щербаков Д.Е. - Отделенческая больница на ст. Кривой Рог Главный; Раджабов О.С. - Частное конструкторское бюро, г. Харьков; Страфун А.С. - Отдел микрохирургии и реконструктивно-восстановительной хирургии верхней конечности НИИ травматологии и ортопедии НАМН Украины, г. Киев
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
С целью определения особенностей распределения напряжений в системе «кость — имплантат», а также особенностей контакта суставных поверхностей в локтевом суставе после эндопротезирования головки лучевой кости имплантатом с «плавающей» головкой построена геометрическая модель локтевого сустава и различные модели эндопротезов головки лучевой кости. На основе конечно-элементной модели выполнен количественный эксперимент. Установлено, что характер перемещений головки разработанного авторами эндопротеза во всех расчетных случаях демонстрирует тенденцию к уменьшению расстояния между контактными суставными поверхностями. Установлено отсутствие моментов сил, которые выводят систему из равновесия. Максимальное напряжение в контактных участках не превышает 3 МПа, что свидетельствует об уменьшении нагрузки при использовании разработанного эндопротеза.
З метою визначення особливостей розподілу напружень у системі «кістка — імплантат», а також особливостей контакту суглобових поверхонь у ліктьовому суглобі після ендопротезування головки променевої кістки імплантатом із «плаваючою» головкою побудовані геометрична модель ліктьового суглоба та різні моделі ендопротезів головки променевої кістки. На основі кінцево-елементної моделі виконаний чисельний експеримент. Установлено, що характер переміщень головки розробленого авторами ендопротеза в усіх розрахункових випадках демонструє тенденцію до зменшення відстані між контактними суглобовими поверхнями. Установлена відсутність моментів сил, що виводять систему з рівноваги. Максимальне напруження в контактних ділянках не перевищує 3 МПа, що свідчить про зменшення навантаження під час використання розробленого ендопротеза.
In order to determine the characteristics of the stress distribution in the «bone — implant» system, as well as the of the contact of the articular surfaces in the elbow joint after radial head replacement using implant with «floating» head, there was created a geometric model of the elbow joint and various models of radial head prosthesis. Based on the finite element model, a quantitative experiment has been carried out. It was found that the nature of the movements of head endoprosthesis developed by authors in all cases shows a tendency to decrease in the distance between the contact joint surfaces. The absence of torques that put the system out of balance has been detected. The maximum stress in the contact areas doesn’t exceed 3 MPa, indicating a decrease of load when using the developed endoprosthesis.
головка лучевой кости, эндопротез головки лучевой кости, «плавающая» головка, напряженно-деформированное состояние, конечно-элементная сетка.
головка променевої кістки, ендопротез головки променевої кістки, «плаваюча» головка, напружено-деформований стан, кінцево-елементна сітка.
radial head, radial head prosthesis, «floating» head, stress-strain state, finite-element mesh.
Статья опубликована на с. 5-12
Введение
Переломы головки (ГЛК) и шейки лучевой кости составляют 1,7–5,4 % от всех повреждений костей скелета человека и около 30 % повреждений в области локтевого сустава [1, 2]. Более 80 % повреждений ГЛК и шейки лучевой кости наблюдается у пациентов в возрасте от 20 до 60 лет [1, 2]. Замещение ГЛК имплантатом показано в случаях технически невыполнимого остеосинтеза при переломах и переломовывихах ГЛК III–IV типа по Broberg — Morrey [1] для достижения стабильности локтевого сустава и восстановления длины лучевой кости [1–5].
В настоящее время в клинической практике используются как моноблочные эндопротезы ГЛК, так и униполярные с «плавающей» головкой [5]. В англоязычной литературе их принято называть биполярными эндопротезами ГЛК благодаря наличию пары трения между головкой и ножкой имплантата [3–6]. Так, «плавающий» биполярный эндопротез Жюде (Judet), впервые примененный в клинической практике в 1988 г., успешно используется до сих пор [6]. Тем не менее за последние десятилетия появились новые биполярные эндопротезы ГЛК, отличающиеся друг от друга как дизайном ножки и/или головки, так и парой трения в сферическом шарнирном узле [7]. Остается дискутабельным вопрос о том, какой тип эндопротеза ГЛК отвечает требованиям восстановления кинематики локтевого сустава [8]. В работе [9] авторы показали, что головка лучевой кости не имеет строго фиксированного радиуса перемещения относительно головочки плечевой кости при различных углах пронации и супинации, что компенсируется высокой конгруэнтностью и сложной геометрической формой суставных поверхностей. Таким образом, сравнительное изучение особенностей распределения напряжений в головке и шейке лучевой кости, а также контактных напряжений в плечелучевом и лучелоктевом суставах, характера перемещений в нормальном локтевом суставе и в случае эндопротезирования ГЛК различными конструкциями имплантатов является актуальным вопросом, требующим дальнейшего исследования.
Цель исследования: сравнить распределение напряжений в системе «кость — имплантат» при эндопротезировании головки лучевой кости различными конструкциями.
Материалы и методы
На основе данных, предоставленных компанией Visual Human (U.S.), с помощью программного комплекса FEMAP построены необходимые, максимально точные геометрические модели (на основе Spline–поверхностей), отвечающие достаточным требованиям для проведения исследования [9] (рис. 1), а также модели в комплексе ANSYS 11.0 (ANSYS Inc., Canonsburg, PA) для уточнения параметров конечно–элементной модели, расчета и визуализации результатов. Количество элементов: 53 700. Тип элементов: линейный тетраэдр (SOLID45), контактные линейные элементы (CONTA173/TARGE170).
Использование одной исходной модели нормального локтевого сустава (рис. 1а) позволяет сохранить геометрические характеристики сравниваемых моделей и проводить качественный сравнительный анализ результатов в зависимости от имплантата. Для построения геометрической и конечно–элементной модели моноблочного имплантата ГЛК выбран эндопротез rHEAD™ Radial Implant System (Small Bone Innovations, Inc., U.S.) (рис. 2а) [10].
На рис. 1в представлена конечно–элементная модель локтевого сустава с эндопротезом UNI–Elbow Radio Capitellum System (Small Bone Innovations, Inc., U.S.) (рис. 2б) [11]. Конечно–элементная модель на рис. 1г включает в себя разработанный имплантат ГЛК (патент Украины на полезную модель № 83334) [12]. Отличительной особенностью разработанного металлического эндопротеза ГЛК является наличие сферического шарнира между головкой имплантата и его ножкой с формированием пары трения металл–металл. Конструктивно сферический шарнир был выполнен таким образом, чтобы угол поворота головки имплантата относительно оси ножки имплантата не превышал 15° (рис. 3).
Так как анализ данной задачи подразумевает расчет модели при различных углах поворота лучевой кости в локтевом суставе при пронации и супинации, то, чтобы учесть взаимное влияние разных тел, входящих в модель, каждая задача ставилась как контактная с учетом возможности возникновения контакта между отдельными участками контактирующих тел (рис. 4).
Свойства материалов, а также характер нагружения модели для всех расчетов были приняты постоянными и одинаковыми (табл. 1, 2) [13, 14]. Величина коэффициента Пуассона для всех материалов была принята равной 0,3. Металл, из которого сделан разработанный эндопротез, — нержавеющая сталь марки S31673, изготовленная по стандарту ASTM F138 (аналог в СНГ — 08Х17Н13М2), устойчивая к агрессивным средам и разрешенная для изготовления медицинских имплантатов во всем мире [15].
Учитывая, что предметом анализа является только лучевая кость, мы допустили, что положение локтевой и плечевой костей при пронации и супинации предплечья остается неизменным, т.е. угол сгибания в локтевом суставе для всех расчетных случаев принят 90°. Чтобы сохранить обратное влияние на лучевую кость со стороны контактирующих участков зафиксированных костей, фиксация была выполнена в узлах конечно–элементной сетки, наиболее удаленных от мест контакта с лучевой костью. Так как предполагается анализ результатов расчетов статических задач уравновешенных моделей при различных углах поворота лучевой кости вокруг своей оси в локтевом суставе, то каждый расчет подра–зумевает наличие уравновешивающей системы сил, действующих на модель. Нагружение лучевой кости предполагает получение уравновешенного состояния за счет осевого давления на диафизарную часть с одной стороны и реакции опоры со стороны головки плечевой кости.
Учитывая геометрические особенности суставных поверхностей со стороны головки лучевой и головочки плечевой костей, а именно их сложную сферичность, и относительно больший радиус головки лучевой кости, можно считать, что до определенного уровня нагружения результирующая сил реакции опоры на суставных поверхностях не позволит головке лучевой кости выйти из контакта с плечевой костью. Таким образом, задавая осевую нагрузку на лучевую кость в направлении локтевого сустава, зафиксировав при этом положение плечевой и локтевой костей, мы получим установившееся статическое положение системы.
Для оценки осевой нагрузки на лучевую кость учтем то, что эта нагрузка появляется вследствие отжимания на руках. Так как более удобным способом представления этой нагрузки в расчетной модели является не сила, а давление, то, приняв вес тела человека за 70 кг, получим величину 1,43 МПа. Следует заметить, что если величина осевой нагрузки на лучевую кость приведет к достаточно большим напряжениям в головке или шейке лучевой кости, то на практике это вызовет ее разрушение. Результаты расчета не смогут показать разрушение как таковое. Но причины, приводящие к дальнейшему разрушению, могут быть обнаружены. Если до наступления критических напряжений в головке или шейке лучевой кости в контактных поверхностях произойдут достаточно большие перемещения, то это автоматически приведет к неуравновешенности системы сил и реакций опоры и как следствие — выходу головки лучевой кости из стабильного соединения с плечевой костью. Расчет включал в себя анализ напряженно–деформированного состояния системы в 3 различных углах супинации и пронации в локтевом суставе — 0° (полная супинация), 75° и 150° (пронация), при фиксированном положении сгибания в локтевом суставе — 90°.
Результаты и их обсуждение
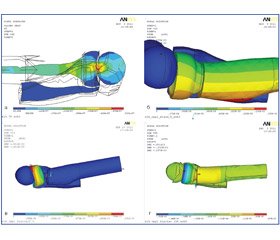
Выполнены четыре серии расчетов напряженно–деформированного состояния локтевого сустава под действием осевой нагрузки на лучевую кость при пронации и супинации. В качестве иллюстрации на рис. 3 представлены области контактных напряжений при полной супинации предплечья для всех четырех случаев.
Полученные данные в четырех сериях расчетов при различных углах пронации и супинации представлены в табл. 3–6.
Анализ табл. 3 и 4 показывает, что применение монополярного имплантата приводит к увеличению напряжений в плечевой кости на 47–114 %, а в шейке лучевой кости — на 162–207 % в сравнении с нормальным локтевом суставом. В случае применения биполярного эндопротеза UNI–elbow (при котором замещается суставная поверхность головочки плечевой кости) и разработанного биполярного эндопротеза уровень напряжений в плечевой кости снизился на 44–62 %, а в шейке и диафизарной части лучевой кости, удаленной от локтевого сустава, вырос на 135–150 % в сравнении со здоровым локтевым суставом (табл. 3, 5, 6).
Учитывая, что максимально допустимый уровень напряжений для костей предплечья составляет 117–132 МПа, а для сплавов, из которого изготовлены детали имплантата, — 520–1050 МПа, что во много раз выше полученных значений максимальных напряжений в соответствующих материалах, можно сказать, что при данном нагружении мы получили действительную картину напряженно–деформированного состояния.
Напряжения в контактной области «плавающей» головки эндопротеза и плечевой кости не превышали 3 МПа (для обоих биполярных эндопротезов), что демонстрирует значительную разгрузку локтевого сустава по отношению к напряжениям даже в нормальной головке лучевой кости. При сравнении максимальных напряжений, возникающих во всех расчетных значениях угла поворота лучевой кости при пронации и супинации в норме и при замещении головки лучевой кости разработанным эндопротезом ГЛК, установлен факт их уменьшения на 45–60 % (табл. 3, 6).
Во всех расчетных значениях угла поворота при пронации и супинации для разработанного биполярного эндопротеза максимальные значения напряжений были локализованы в первой борозде металлической ножки униполярного эндопротеза и варьировались от 28 до 107 МПа. Полученный уровень напряжений гарантирует запас прочности разработанного эндопротеза со значением: 520/107 = 4,85. Значения напряжений в лучевой кости (в области крепления ножки имплантата) находятся в диапазоне от 27 до 36 МПа, что значительно меньше уровня предельно допустимых значений прочностных характеристик для костных тканей. Запас прочности костных тканей составляет: 149/36 = 4,1. Другими словами, рассматриваемая система «кость — имплантат» будет работоспособной и не разрушится при 4–кратной перегрузке.
Сравнивая значения перемещений головки лучевой кости или головок эндопротезов ГЛК (рис. 5) относительно суставной поверхности головочки плечевой кости для рассмотренных четырех вариантов расчетов, можно отметить, что при монополярном эндопротезе ГЛК в отличие от трех остальных вариантов возникает большее смещение как области контакта относительно оси лучевой кости, так и самой головки эндопротеза относительно суставной поверхности головочки плечевой кости. В то же время в случае биполярных эндопротезов ГЛК (третий и четвертый варианты расчетов) головка сохраняла стабильное положение на суставной поверхности головочки плечевой кости, что возможно благодаря дополнительной степени свободы, добавленной сферическим шарниром между головкой и ножкой имплантата.
Таким образом, можно предположить, что в случае монополярного эндопротеза ГЛК при пронации и супинации одновременно с осевым нагружением лучевой кости следует ожидать относительно большого растяжения мягких тканей, вызванного смещением головки имплантата. Для случаев с биполярными имплантатами, охватывающими головку тканей, предпосылки для растяжения отсутствуют.
Место контакта имплантата головки лучевой кости с головочкой плечевой кости всегда совпадает с осью диафизарной части лучевой кости в третьем и четвертом случаях расчета. Такое положение системы тел возможно благодаря наличию сферического шарнира между ножкой имплантата и его головкой, в результате чего головка принимает устойчивое положение между ножкой эндопротеза и плечевой костью, при этом отсутствуют моменты сил, выводящие лучевую кость из положения равновесия.
Выводы
1. Головка лучевой кости не имеет строго фиксированного радиуса перемещения относительно головочки плечевой кости при различных углах пронации и супинации. Соответствие суставных поверхностей в здоровом локтевом суставе обеспечивается сложной конфигурацией головки лучевой кости и головочки плечевой кости.
2. Применение монополярного имплантата увеличивает как напряжения в костях локтевого сустава, так и контактные напряжения на хрящевых суставных поверхностях на 114–207 %.
3. Применение биполярного имплантата увеличивает напряжения в плечевой кости и контактные напряжения на головочке плечевой кости на 44 %.
4. Под действием осевой нагрузки на лучевую кость при пронации и супинации применение монополярного имплантата головки лучевой кости приводит к росту как контактных напряжений, так и напряжений в костях локтевого сустава в 2 раза, а также увеличивает перемещение головки кзади, что приводит к растяжению мягких тканей, охватывающих головку лучевой кости.
5. Применение биполярных имплантатов головки лучевой кости показывает стабильное положение головки эндопротезов на суставной поверхности головочки плечевой кости и отсутствие роста напряжений в костях и на хрящевых поверхностях локтевого сустава в сравнении со здоровым локтевым суставом.
6. Характер перемещения головки биполярных эндопротезов с «плавающей» головкой в устойчивое положение для всех расчетных значений угла поворота при пронации и супинации демонстрирует тенденции сокращения расстояния между контактными поверхностями лучевой кости по отношению как к плечевой, так и к локтевой кости. Исходя из этого, можно предположить, что при рассматриваемых нагружениях связки, охватывающие локтевой сустав, испытывать какие–либо дополнительные нагрузки не будут.
7. Напряжения в контактной области «плавающей» головки разработанного эндопротеза и плечевой кости не превышали 3 МПа, что демонстрирует значительную разгрузку локтевого сустава по отношению к напряжениям, возникающим при расчетных случаях в нормальном локтевом суставе.
8. При сравнении максимальных напряжений, возникающих во всех расчетных значениях угла поворота лучевой кости при пронации и супинации в норме и при замещении головки лучевой кости разработанным эндопротезом ГЛК с «плавающей» головкой, установлен факт их уменьшения на 45–60 %.
9. Сравнительный анализ напряжений, возникающих в системе «кость — имплантат» в норме и при замещении ГЛК разработанным униполярным эндопротезом с «плавающей» головкой, не выявил перегрузок, которые могут привести к разрушению системы, а также показал отсутствие моментов сил, выводящих систему из равновесия.
10. Исходя из вышеуказанных особенностей контакта лучевой кости с головочкой плечевой кости, при рассмотрении вопроса о выборе имплантата для замещения головки лучевой кости необходимо отдавать предпочтение модульным биполярным эндопротезам с «плавающей» головкой.
1. Broberg M. Results of treatment of fracture–dislocations of the elbow / M. Broberg, B. Morrey // Clin. Orthop. Relat. Res. — 1987. — Vol. 216. — P. 109–119.
2. Morrey B. The elbow and its disorders / B. Morrey. — 3ed. — Philadelphia, London, New York: W.B. Saunders company, 2000. — 934 p.
3. Hartzler R. Radial head reconstruction in elbow fracture–dislocation: monopolar or bipolar prosthesis? / R. Hartzler, B. Morrey, S. Steinmann [et al.] // Clin. Orthop. Relat. Res. — 2014. — Vol. 472(7). — P. 2144–2150.
4. Moon J. Radiocapitellar joint stability with bipolar versus monopolar radial head prostheses / J. Moon, L. Berglund, D. Zachary [et al.] // J. Shoulder Elbow Surg. — 2009. — Vol. 18. — P. 779–784.
5. Arbter D. Results after Judet radial head prosthesis for nonreconstructable radial head fractures / D. Arbter, S. Piatek, A. Probst [et al.] // Unfallchirurg. — 2012. — Vol. 115(11). — P. 1000–1008.
6. Judet T., Garreau de Loubresse C., Piriou P., Charnley G. A floating prosthesis for radial–head fractures // J. Bone Joint. Surg. — 1996. — 78–B. — 244–249.
7. Acevedo D.C., Paxton E.S., Kukelyansky I., Abboud J., Ramsey M. Radial Head Arthroplasty: State of the Art // J. Am. Acad. Orthop. Surg. — 2014 Oct. — 22(10). — 633–642.
8. Radiocapitellar joint contacts after bipolar radial head arthroplasty / F. Moungondo, W. El Kazzi, R. van Riet [et al.] // J. Shoulder Elbow Surg. — 2010. — Vol. 19(2). — P. 230–235.
9. Бойко И.В. Биомеханическое изучение особенностей распределения нагрузок в головке и шейке лучевой кости / И.В. Бойко, В.Б. Макаров, Д.Е. Щербаков и др. // Вісник ортопедії, травматології та протезування. — К., 2013. — № 1. — С. 22–27.
10. Morrey B. Radial Head Prosthetic Replacement with the Avanta Implant / B. Morrey // Treatment of Elbow Lesions. — 2008. — P. 167–174.
11. Matthew M. The Emerging Role for UNI–ElbowTM Arthroplasty / M. Matthew, M. Tomaino // Am. J. Orthop. — 2008. — Vol. 37(8 suppl). — P. 26–28.
12. Пат. 83334 Україна, МКИ6 А 61F 2/38 Ендопротез голівки променевої кістки / І.В. Бойко, В.Б. Макаров, Д.Є. Щербаков, О.В. Сабсай. — № 201214490; Заявл. 18.12.12; Опублік. 10.09.13, Бюл. № 17.
13. Карлов А.В. Системы внешней фиксации и регуляторные механизмы оптимальной биомеханики / А.В. Карлов, В.П. Шахов. — Томск: STT, 2001. — 480 с.
14. Трушко А.В. АСМ–анализ хрящевых тканей / А.В. Трушко, С.А. Чижик: Мат–лы VII междунар. семинара (1–3 ноября 2006 г., Минск). — Минск: ИТМО НАН Беларуси, 2006. — С. 162–168.
15. ISO 7153–1: 1991 Инструменты хирургические. Металлические материалы. Часть 1. Нержавеющая сталь. — 4 с.

/6/6.jpg)
/7/7.jpg)
/8/8.jpg)
/9/9.jpg)
/10/10.jpg)