Статья опубликована на с. 14-16 (Укр.)
/ukraina/15-5.jpg) Остеоартрит (ОА) є прогресуючим захворюванням, при якому в патологічний процес утягуються всі структури суглоба — хрящ, субхондральна кістка, синовіальна оболонка, прилеглі сухожилки та зв’язки, жирова тканина, м’язи [26]. Водночас ОА не є унікальним захворюванням, а являє собою гетерогенну групу з різними клініко-патогенетичними фенотипами, які постійно змінюються, гетерогенно прогресують, що в остаточному підсумку призводить до спільних клінічних проявів [7]. Отже, ОА — це група патогенетично близьких захворювань, але таких, що мають різну етіологію, однак призводять до однотипних біохімічних і клінічних наслідків, характеризуються прогресуючою втратою гіалінового хряща й патологічним ремоделюванням субхондральної кістки [3]. ОА має різнопланові фактори ризику, що охоплюють генетичну схильність, вік і стать; водночас важливим фактором ризику є підвищена маса тіла [5, 40, 45]. Підвищення маси тіла характеризується зростанням ризику ураження колінного суглоба (OR = 2,81), дрібних суглобів кисті (OR = 2,59), але не кульшового суглоба (OR = 1,1) [13].
Остеоартрит (ОА) є прогресуючим захворюванням, при якому в патологічний процес утягуються всі структури суглоба — хрящ, субхондральна кістка, синовіальна оболонка, прилеглі сухожилки та зв’язки, жирова тканина, м’язи [26]. Водночас ОА не є унікальним захворюванням, а являє собою гетерогенну групу з різними клініко-патогенетичними фенотипами, які постійно змінюються, гетерогенно прогресують, що в остаточному підсумку призводить до спільних клінічних проявів [7]. Отже, ОА — це група патогенетично близьких захворювань, але таких, що мають різну етіологію, однак призводять до однотипних біохімічних і клінічних наслідків, характеризуються прогресуючою втратою гіалінового хряща й патологічним ремоделюванням субхондральної кістки [3]. ОА має різнопланові фактори ризику, що охоплюють генетичну схильність, вік і стать; водночас важливим фактором ризику є підвищена маса тіла [5, 40, 45]. Підвищення маси тіла характеризується зростанням ризику ураження колінного суглоба (OR = 2,81), дрібних суглобів кисті (OR = 2,59), але не кульшового суглоба (OR = 1,1) [13].
Патогенетичний зв’язок ожиріння й ОА залишається повністю не з’ясованим. Історично склалося так, що висока частота ОА колінного суглоба реєструвалася саме в огрядних людей, у зв’язку з цим виникло припущення про суто механічний зв’язок: надмірна вага збільшує навантаження на суглоб, унаслідок чого він скоріше зношується [31]. Водночас було показано, що ожиріння асоціювалося з ОА суглобів, що не несуть значного навантаження, наприклад зап’ястка та кисті [11]. Крім того, втрата ваги може призупинити прогресування ОА, зменшити прояви запалення й больового синдрому [45]. Це означає, що тільки механічним перевантаженням суглобів не може бути пояснений зв’язок між ОА й ожирінням. Сьогодні жирова тканина розглядається не тільки як пасивний акумулятор жирних кислот, але і як потужний ендокринний орган, а також продуцент прозапальних сигнальних молекул, наявність яких знаменує хронічне імунне запалення [5, 32]. Отже, жирова тканин як ендокринний орган здатна продукувати субстанції з локальним (автокринним) і системним (ендокринним) ефектами [6]. Крім того, огрядність пов’язана з порушеннями ліпідного обміну, що призводить до системно низького рівня ліпопротеїдів високої щільності (ЛПВЩ) і високого рівня вільних жирних кислот (ВЖК), тригліцеридів (ТГ) і окислених ліпопротеїдів низької щільності.
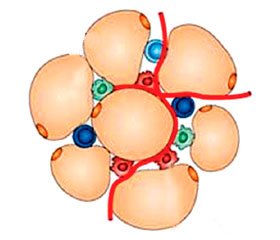
Важливою характеристикою ожиріння є запалення жирової тканини. Жирова тканина просякнута макрофагами, що утворюють короноподібну структуру навколо гіпертрофованих адипоцитів [44]. На відміну від «худої» жирової тканини, що містить в основному протизапальні М2-макрофаги, при ожирінні жирова тканина містить насамперед прозапальні макрофаги M1 (рис. 1). Крім того, «огрядна» жирова тканина багата на дендритні клітини, Т- і В-клітини, нейтрофіли й адипоцити. Саме вони секретують гормони, цитокіни й сигнальні молекули, що регулюють численні біологічні процеси та підтримують низькорівневе запалення. При ожирінні зростає продукція й вивільнення саме прозапальних цитокінів і адипокінів — лептину, резистину, ліпокаліну-2, RBP4, ІЛ-6, ІЛ-18, фактора некрозу пухлини альфа (ФНП-α), моноцитарного хемоатрактантного білка 1 (МСР-1), NAMPT, CXCL5 тощо. При огрядності виникає не тільке низькорівневе системне запалення, джерелом адипокінів виступає й власна жирова тканина суглобів, наприклад інфрапателярна жирова тканина (ІПЖТ) колінного суглоба. Завдяки своєму розташуванню ІПЖТ може відігравати важливу роль у місцевому запаленні колінних суглобів. Сьогодні відомі принаймні 3 цитокіни, що продукуються разом жировою тканиною й ІПЖТ: ІЛ-6, ФНП-a та VEGF (судинний ендотеліальний фактор росту) [9, 42].
/71-1.jpg)
Рівень фактора некрозу пухлини a при ОА суттєво зростає в синовіальній оболонці, субхондральній кістці та хрящі. Цей цитокін гальмує синтез компонентів екстрацелюлярного матриксу: протеогліканів, колагену ІІ типу й хрящ-зв’язуючого протеїну (HAPLN1 — hyaluronan and proteoglycan link protein 1). HAPLN1 зазвичай відповідає за стабілізацію комплексу гіалурон — агрекан, тим самим зберігаючи міцність та еластичність хряща. Крім того, ФНП-α активує експресію й вивільнення різних матриксних металопротеїназ (ММП), таких як ММП-1, ММП-3 і ММП-13, а також інших прозапальних хемокінів і цитокінів: ІЛ-6, ІЛ-8, хемо–атрактантних білків тощо [41]. Загалом підвищена концентрація ФНП-α корелює з інтенсивністю втрат суглобового хряща, що підтверджує роль низькорівневого запалення в патогенезі ОА [38].
При ОА також зростає рівень ІЛ-6 у сироватці крові й синовіальній оболонці. У літературі досконало описані впливи ІЛ-6 на суглобовий хрящ: у присутності свого розчинного рецептора (SIL-6R) ІЛ-6 пригнічує транскрипцію компонентів екстрацелюлярного матриксу — агрекану, колагену ІІ типу, низки зв’язуючих білків. Крім того, він підвищує індуковане ІЛ-1 руйнування суглобового хряща. Костимуляція ІЛ-1, ІЛ-6 та SIL-6R синер–гетично підвищує експресію ММП-1 і ММП-13 на хондроцитах людини й вивільнення колагену з бичачого хряща [33].
VEGF — ангіогенний ростовий фактор, що утворюється в синовіальній оболонці при ОА [17]. У культурі –хондроцитів VEGF стимулює підвищення вивільнення ММП-1, ММП-3, ММП-13. У синовіальній оболонці VEGF, швидше за все, бере участь в ангіогенезі й тим самим індукує та підтримує загострення запального процесу. Експресія VEGF є вищою саме в запалених ділянках синовіальної оболонки. Крім того, VEGF збільшує утворення оcтеофітів завдяки своїй ангіогенній активності, утім цей процес остаточно не з’ясований [27].
Подібно до цитокінів, адипокіни секретуються жировою тканиною і також ІПЖТ [18]. Лептин, так званий гормон голоду, був першим відкритим адипокіном (у 1994 році); саме з нього почалася ера вивчення ендокринної функції жирової тканини. За останні роки ідентифіковано більше ніж 100 різних адипокінів. Біла жирова тканина продукує низку пептидів — біологічно активних молекул, у тому числі адипокінів, що відповідальні за контроль над об’ємом їжі, яка вживається, енергетичний баланс і масу тіла (лептин), гомеостаз глюкози (адипонектин, резистин, адипонутрин), метаболізм ліпідів (ретинол-зв’язуючий протеїн, холестерол-естер-трансфер-протеїн), ангіо–генез (VEGF), фібриноліз (інгібітор активатора плазміногену-1), про- й протизапальні ефекти (ФНП-a, ІЛ-6), сексуальний розвиток і репродукцію (лептин) [6]. Секреторний профіль жирової тканини суттєво змінюється залежно від ожиріння чи ліпоатрофії (рис. 1). Разом із місцевою продукцію адипокінів ІПЖТ це може мати згубні наслідки для суглобових тканин [41, 43]. Встановлено, що лептин, вісфатин, резистин, ліпокалін-2, хемерин та низка нових адопокінів причетні до розвитку й прогресування ОА [4, 34]. Дані про ці адипокіни та їх патогенетичну роль при ОА подані в табл. 1.
/72-1.jpg)
/73-2.jpg)
Адипонектин, також відомий як AdipoQ i ACRP30, являє собою виділений з адипоцитів колагеноподібний білок, що був отриманий в результаті пошуку продуктів транскрипції генів жирової тканини в проекті «Геном людини» в 1995 році [22]. Незважаючи на те, що адипонектин був відкритий майже одночасно з лептином, його захисна роль проти ожиріння та його ускладнень була визначена й визнана багато років поспіль. Адипонектин є специфічним адипокіном, тобто він синтезується виключно адипоцитами, а експресія мРНК адипонектину в підшкірній жировій клітковині вища, ніж у вісцеральній жировій тканині. Він збільшує чутливість до інсуліну, має антиатерогенні й протизапальні властивості, регулює метаболізм ліпопротеїдів, багатих на тригліцериди. Встановлено, що низький рівень адипонектину передує розвитку інсулінорезистентності [2]. Показано, що чим вищий уміст цього гормона, тим менший ризик розвитку інфаркту міокарда. Припускається, що адипонектин протидіє нагромадженню жирів в стінках артерій, таким чином зменшуючи вірогідність утворення тромбів [2, 10].
Концентрація адипонектину в плазмі крові зменшується при ожирінні, водночас вона збільшується при ОА [24]. І хоча кінцева роль адипокіну в патогенезі ОА, індукованому ожирінням, остаточно не встановлена, його участь у розвитку ОА загалом є незаперечною (табл. 1). Наприклад, його рівні в синовіальній оболонці негативно корелюють з болем і тяжкістю гонартрозу, справляючи при цьому захисний вплив на суглобовий хрящ. В остеоартрозному суглобі джерелом адипонектину є суглобовий хрящ, остеофіти, синовіальна мембрана, меніски й інтрапателярна жирова тканина. Сироватковий рівень адипонектину вірогідно підвищується у жінок з ерозивним ОА суглобів кистей рук, що дозволяє говорити про участь саме цього адипокіну в патогенезі ерозивного ОА.
Лептин являє собою білок, що кодується в жирових клітинах геном, який зумовлює огрядність. Він належить до класу І цитокінової суперродини [29], тобто це цитокінподібний гормон, що запускає біологічні ефекти шляхом зв’язування зі специфічним рецептором. Рецептор лептину присутній у 6 різних варіантах, що відомі на сьогодні, і проявляє гомологічну подібність із рецептором онко–статину М. Головним позаклітинним сигнальним шляхом його ідентифікації є пато–фізіологічний шлях JAK-STAT [12]. Рівень лептину корелює з об’ємом білої жирової тканини й індексом маси тіла (ІМТ). Сьогодні широко обговорюється його роль в патогенезі не лише ОА й ревматоїдного артриту (РА), але й остео–порозу [8].
Роль лептину в патогенезі ОА постійно оновлюється [4, 8, 12, 34, 45]. In vitro лептин посилює синтез прозапальних медіаторів в остеоартрозному хрящі, таких як ІЛ-6, ІЛ-8 і простагландин Е2 у NO-залежному середовищі. Введення екзогенного лептину підвищує продукцію інсуліноподібного фактора росту 1 і трансформуючого фактора росту a хондроцитами колінного суглоба щурів, демонструючи, що високі рівні лептину можуть здійснювати протекцію хряща в огрядних осіб від остеоартритичної дегенерації. Ця можлива протекторна роль лептину широко дискутується в науковій літературі та піддається сумнівам, оскільки добре відомим є інший факт: стимуляція лептином продукції матриксних металопротеїназ (ММП-3,
ММП-9, ММП-13), що справляють агресивний деструктивний вплив на суглобовий хрящ [8]. Лептин викликає апоптоз хондроцитів, змінює їх фенотип та загалом стимулює деградацію суглобового матриксу.
Одним з перших досліджень, що встановили залежність між експресією лептину, функціонуванням його рецептора та ступенем пошкодження суглобового хряща, було дослідження T. Simopoulou et al. (2007) [35]. Вони досліджували експресію лептину хондроцитами й спостерігали збільшення матричної РНК лептину в хондроцитах в осіб, які страждали від ожиріння, при цьому це зростання не було пов’язано з пошкодженням хряща, але корелювало з розгорнутою стадією ОА. Лептин справляв на хондроцити прозапальний і катаболічний вплив, спо–стерігалася стимуляція секреції інтерлейкіну-1, ММП-9, -13. Підвищення експресії лептину асоціювалося зі значним пошкодженням суглобового хряща, демонструючи, що лептин виступає тригером суглобової деструкції. Лептин синергетично діє з ІЛ-1, зумовлюючи підвищення продукції оксиду азоту. NO, як відомо, впливає на функцію хондроцитів, викликаючи пошкодження суглобового матриксу, гальмування синтезу колагену ІІ типу, активацію ММП. За останніми даними, лептин дозозалежно підвищує рівень ММР-9 і ММР-13 — двох головних металопротеїназ, відомих своїм деструктивним впливом на хрящовий матрикс. Саме взаємозв’язок між лептином і ММР підтверджує катаболічну роль лептину в хрящовому метаболізмі [34].
Ще одне дослідження викликало широкий резонанс й обговорення. У лептин-дефіцитних мишей (лінія ob/ob) та у лептин-рецептор-дефіцитних мишей (лінія db/db) порівнювалися зміни в колінних суглобах. В обох лініях мишей частота ожиріння була збільшена в 10 разів порівняно з контролем [14]. Але виражене ожиріння не призводило до збільшення частоти ОА колінних суглобів, проте викликало суттєві морфологічні зміни субхондральної кістки й суглобового хряща. Так, у мишей з дефіцитом лептину спостерігалося зменшення товщини субхондральної кістки та збільшення відносного об’єму трабекулярної кістки епіфіза гомілки без формування ОА. При цьому рівень системних прозапальних цитокінів залишався високим в ob/ob (лептин-дефіцитні) і db/db (дефіцит рецептора лептину) мишей. Ці результати дозволили постулювати думку про участь лептину у розвитку ОА, а також висловити гіпотезу, що без лептину ожиріння є недостатнім фактором, щоб викликати системне запалення й прогресування ОА.
Резистин. У 2001 році група вчених Пенсильванського університету на чолі зі C.M. Steppan, досліджуючи гени, що задіяні в процесі диференціювання адипоцитів, виявила невідомий раніше адипокін, який пізніше був названий резистином — гормоном інсулінорезистентності. Резистин належить до класу багатих на цистеїн білків — резистиноподібних молекул (RELM). Участь резистину в запальних реакціях підтверджується тим, що його секретують клітини мононуклеарного ряду [44]. Крім того, рівень резистину пов’язаний з міжклітинними молекулами адгезії 1 (ІСАМ 1) у пацієнтів з синдромом сонних апное, а в пацієнтів з атеросклерозом позитивно пов’язаний із ліпопротеїн-асоційованою фосфоліпазою А2 і розчинним рецептором ФНП-a. Сироватковий рівень резистину перевищує його концентрацію в синовіальній рідині при ОА, при цьому циркулюючий рівень не відображає суглобового рівня цього гормона. Для з’ясування ролі резистину в суглобовій деградації проведені дослідження в пацієнтів після травматичного пошкодження суглобів. Так, після травми рівень резистину знижується з подовженням часу після травми й прямо впливає на обмінні процеси в матриксі суглобового хряща та продукцію цитокінів, підтверджуючи роль цього адипокіну в травма-індукованому ОА [25].
Вісфатин являє собою пептид, що першочергово був виявлений у печінці, скелетних м’язах, кістковому мозку як фактор росту попередників В-лімфоцитів, це сприяло появі декількох назв цього гормона. У недавніх публікаціях зазначено, що людські хондроцити здатні продукувати вісфатин. Цей синтез підвищується під впливом ІЛ-1a та індукує надмірне вивільнення простагландину Е2 та інших запальних медіаторів. Крім того, вісфатин має катаболічну функцію в суглобовому хрящі й може відігравати важливу роль у патогенезі ОА [4, 12].
Отже, якщо раніше ефекти адипокінів обмежувалися метаболічною активністю, то сьогодні цей клас біологічно активних речовин розглядається як нова потужна родина цитокінів, що можуть виступати новими яскравими гравцями в комплексній мережі медіаторів, утягнених у патофізіологію артритів та ОА [34]. Сьогодні ми є свідками тільки ранніх стадій глибоких досліджень, що не дозволяють намалювати повну картину ефектів і дій адипокінів, утім у подальшому призведуть до розуміння їх ролі як про- та проти–запальних медіаторів.
Ожиріння характеризується не тільки надмірним навантаженням на опорні суглоби, формуванням системного нізькорівневого запалення, але й аномальним ліпідним профілем — дисліпідемією. Дисліпідемія, асоційована з ожирінням, характеризується високим рівнем тригліцеридів у плазмі крові, низьким вмістом холестерину ліпопротеїдів високої щільності, часто підвищеним вмістом ліпопротеїдів низької щільності (ЛПНЩ) та підвищеним вмістом вільних жирних кислот. Крім того, при ожирінні функції ЛПВЩ порушуються [20]. Різні дослідження довели, що метаболізм ліпідів може відігравати певну роль у патогенезі ОА. Високий рівень холестерину в сироватці крові пов’язаний з генералізованим ОА, це доводить, що гіперхолестеринемія може бути системним фактором ризику для ОА. Крім того, загальний холестерин у сироватці крові, високі рівні тригліцеридів і дисбаланс ліпопротеїдів були пов’язані з виникненням вогнищ жирового пошкодження кісткового мозку. Ураження кісткової тканини й кісткового мозку є джерелом болю при ОА й зумовлює прогресуючі втрати хряща. Ще один важливий висновок підкреслює значущість ліпідів у патогенезі ОА: хондроцити здатні накопичувати ліпіди, що позитивно корелює з тяжкістю захворювання.
Високі рівні циркулюючих вільних жирних кислот при ожирінні викликані порушенням гальмування внутрішньоклітинного ліполізу, що призводить до зростання вивільнення ВЖК із жирової тканини. ВЖК здатні активувати макрофаги, стимулюючи Toll-подібний рецептор 2/4 та призводячи до передачі сигналу с-Jun N-термінальній кіназі й до подальшої активації макрофагів [28]. У свою чергу, макрофаги можуть секретувати прозапальні медіатори, зокрема такі як ФНП-α. Існування подібної паракринної «петлі» між адипоцитами й макрофагами може посилювати запалення жирової тканини. Оскільки макрофаги також присутні в синовіальній вистилці, цей процес водночас може також викликати й підтримувати локальне запалення суглобів.
Численні дослідження також вказують на вагому роль дисбалансу холестерину ЛПВЩ у патогенезі ОА, засновану на спостереженні, що їх рівень в сироватці крові зменшуються у хворих на ОА [37]. Іншою характеристикою пов’язаних з ожирінням дисліпідемій є високий системний рівень окислених ЛПНЩ. Вони визначаються в синовіальній оболонці при ОА та корелюють з індексом маси тіла [36]. Основним рецептором окислених ЛПНЩ є лектин-подібний рецептор (LOX-1), що експресує на хондроцитах та стимулює їх до вивільнення VEGF [19]. Судинний ендотеліальний фактор росту (VEGF) відомий своєю здатністю підвищувати секрецію ММП-1, ММП-3 і ММП-13 з культивованих хондроцитів; окрім того, як було показано, VEGF збільшує експресію ІЛ-1β, ІЛ-6 і ФНП-α [30]. Отже, окислені ЛПНЩ можуть індукувати деградацію суглобового хряща через продукцію VEGF, що, у свою чергу, викликає секрецію численних хрящ-руйнуючих факторів. Водночас продемонстровано, що в остеоартрозному хрящі суттєво зростає експресія LOX-1, що корелює з тяжкістю ОА.
Звичайно, ожиріння супроводжується надмірним навантаженням на опорні суглоби, насамперед на медіальні й латеральні ділянки колінних суглобів. У людей з ожирінням суттєво змінюється хода, що додатково збільшує сукупне навантаження на суглоби [16]. Суперечка про можливе тільки механічне пошкодження суглобового хряща була фактично припинена після відкриття внутрішньоклітинного механосигналінгу [15]. Виявилося, що будь-яке ненормальне механічне напруження — розтягнення, стиснення, компресія, напруження зсуву, гідростатичний тиск — може бути перетворене на внутрішньоклітинні сигнали за допомогою збудження механорецепторів, розташованих на поверхні клітин суглоба. Ці сигнали можуть призвести до надлишкової експресії прозапальних медіаторів, таких як простагландини, цитокіни, хемокіни в хондроцитах і остеобластах/остеоцитах субхондральної кістки [39]. Надмірне тривале навантаження індукує перш за все експресію катаболічних ферментів у хондроцитах, таких як ММП. Перетворення механічного сигналінгу на синтез медіаторів запалення опосередковується активацією внутрішньоклітинних сигнальних шляхів, насамперед через NF-bВ і МАРК.
Численні експериментальні моделі продемонстрували, що ненормальне навантаження на суглоб дійсно може змінити метаболізм клітин хряща й субхондральної кістки, що врешті-решт призведе до деградації суглобового хряща й прогресування ОА. Сьогодні особлива увага приділяється впливу надмірного навантаження на субхондральну кістку. Експериментальні досліди довели, що ненормальне навантаження на колінні суглоби мишей призводить до потовщення субхондральної кістки й до змін метаболічної активності остеобластів [21]. Тривале навантаження зумовлює фено–типові зміни остеобластів і формування так званого запального фенотипу клітин, що продукують значну кількість прозапальних цитокінів і факторів росту. Ці активні молекули проникають у хрящ (унаслідок утворення мікротріщин і судинної інвазії в зону кальцифікованого хряща) та втягуються в деградацію хрящової тканини [23]. Ці процеси є наслідком порушення ремоделювання субхондральної кістки під впливом надмірного навантаження, що зсувається в бік посилення кісткової резорбції на ранніх стадіях ОА і підвищеного кісткоутворення в подальшому [1]. Отже, надмірне навантаження на суглоби при ожирінні є важливим додатковим фактором ризику розвитку ОА в опорних суглобах.
/ukraina/16.jpg)
Отже, ожиріння є одним з основних факторів ризику розвитку й прогресування ОА. Зв’язок між цими захворюванням є складним і багатофакторним (рис. 2). Переконання в тому, що тільки надмірне навантаження, властиве огрядності, справляє негативний патогенетичний вплив на суглобовий хрящ, залишилося в далекому минулому. На сьогодні добре відомо, що ожиріння асоціюється із секрецією численних цитокінів і факторів росту, низькорівневим запаленням і дисліпідемією, що відіграють не менш важливу роль у розвитку ОА, що остаточно доведено для неопорних суглобів. Розуміння ролі ожиріння в розвитку ОА має декілька важливих клінічних наслідків. По-перше, втрата ваги у пацієнтів з ожирінням, що зменшує навантаження на суглоби, може значно знизити ризик розвитку ОА в несучих суглобах [45]. По-друге, дієта з низьким умістом жирів повинна бути рекомендована всім пацієнтам с ОА чи наявними іншими факторами ризику розвитку ОА. Суттєве зменшення фракції вільних жирних кислот може позитивно позначитися на перебігу ОА, водночас виключення цього тригерного механізму може зменшити ймовірність розвитку ОА [41]. По-третє, терапія, спрямована на блокаду адипокінів та цитокінів при ОА, може бути корисною стратегією, тож антицитокінові препарати та, можливо, інгібітори лептину з часом посядуть важливе місце в лікувальних схемах ОА.
/ukraina/15-5.jpg) Остеоартрит (ОА) є прогресуючим захворюванням, при якому в патологічний процес утягуються всі структури суглоба — хрящ, субхондральна кістка, синовіальна оболонка, прилеглі сухожилки та зв’язки, жирова тканина, м’язи [26]. Водночас ОА не є унікальним захворюванням, а являє собою гетерогенну групу з різними клініко-патогенетичними фенотипами, які постійно змінюються, гетерогенно прогресують, що в остаточному підсумку призводить до спільних клінічних проявів [7]. Отже, ОА — це група патогенетично близьких захворювань, але таких, що мають різну етіологію, однак призводять до однотипних біохімічних і клінічних наслідків, характеризуються прогресуючою втратою гіалінового хряща й патологічним ремоделюванням субхондральної кістки [3]. ОА має різнопланові фактори ризику, що охоплюють генетичну схильність, вік і стать; водночас важливим фактором ризику є підвищена маса тіла [5, 40, 45]. Підвищення маси тіла характеризується зростанням ризику ураження колінного суглоба (OR = 2,81), дрібних суглобів кисті (OR = 2,59), але не кульшового суглоба (OR = 1,1) [13].
Остеоартрит (ОА) є прогресуючим захворюванням, при якому в патологічний процес утягуються всі структури суглоба — хрящ, субхондральна кістка, синовіальна оболонка, прилеглі сухожилки та зв’язки, жирова тканина, м’язи [26]. Водночас ОА не є унікальним захворюванням, а являє собою гетерогенну групу з різними клініко-патогенетичними фенотипами, які постійно змінюються, гетерогенно прогресують, що в остаточному підсумку призводить до спільних клінічних проявів [7]. Отже, ОА — це група патогенетично близьких захворювань, але таких, що мають різну етіологію, однак призводять до однотипних біохімічних і клінічних наслідків, характеризуються прогресуючою втратою гіалінового хряща й патологічним ремоделюванням субхондральної кістки [3]. ОА має різнопланові фактори ризику, що охоплюють генетичну схильність, вік і стать; водночас важливим фактором ризику є підвищена маса тіла [5, 40, 45]. Підвищення маси тіла характеризується зростанням ризику ураження колінного суглоба (OR = 2,81), дрібних суглобів кисті (OR = 2,59), але не кульшового суглоба (OR = 1,1) [13]./ukraina/16.jpg)

/71-1.jpg)
/72-1.jpg)
/73-2.jpg)