Журнал «Травма» Том 16, №4, 2015
Вернуться к номеру
Эффективность препарата Пиаскледин в комплексной терапии у пациентов с остеоартрозом в условиях коморбидности.
Авторы: Курята А.В., Черкасова А.В., Гармиш И.П. — ГУ «ДМА МЗ Украины», кафедра госпитальной терапии № 1 и профпатологии.
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
Статья опубликована на с. 15-20
Остеоартроз (ОА) — группа гетерогенных заболеваний суставов различной этиологии, характеризующихся прогрессирующим течением, деградацией суставного хряща с последующими изменениями в субхондральной кости и развитием краевых остеофитов, приводящих к потере хряща и сопутствующему поражению других компонентов сустава (синовиальная оболочка, связки, капсула и периартикулярные мышцы) [1]. ОА является наиболее частой причиной поражения суставов, с преимущественной локализацией в коленном и тазобедренном суставах (24 и 11 % соответственно) [2]. По результатам Фрамингемского эпидемиологического исследования (Framingham Osteoarthritis Study) показано, что за последние 20 лет частота ОА коленных суставов в популяции значительно увеличилась [3]. Так, по данным эпидемиологических исследований, люди, страдающие ОА, составляют почти 15 % населения Земли. В Европе и странах с высоким экономическим уровнем ОА по распространенности среди населения в возрасте 45–59 лет занимает второе место после ишемической болезни сердца (ИБС) и цереброваскулярной патологии. Согласно отчету Всемирной организации здравоохранения о социальных последствиях заболеваний ОА коленных суставов находится на 4-м месте среди причин нетрудоспособности у женщин и на 8-м — у мужчин. Увеличение продолжительности жизни и нарастающая доля людей с повышенной массой тела — основные причины стремительного роста заболеваемости ОА [4]. Учитывая повышение продолжительности жизни, прогнозируется увеличение числа пациентов, длительно страдающих тяжелыми формами ОА [2].
ОА — многофакторная нозология, к вероятным предикторам которой можно отнести: возраст, пол, генетическую предрасположенность, избыточную массу тела.
Деполимеризация белково-полисахаридных комплексов с образованием более мелких соединений, а также нарушение функции хондритов, синтезирующих менее стабильные протеогликаны, являются патогенетическим плацдармом формирования протеогликановой недостаточности — основного звена в развитии ОА [3].
В настоящее время терапия ОА направлена на достижение двух целей: облегчение боли и ослабление функциональных нарушений. Одним из способов достижения данных целей является патогенетическая терапия — актуальный вопрос, обсуждаемый в ревматологии на протяжении последних лет. Препараты, используемые в терапии ОА, делятся на две основные группы: симптом-модифицирующие препараты (анальгетики и нестероидные противовоспалительные средства — НПВС), уменьшающие боль и воспаление в суставах, и структурно-модифицирующие препараты, способные модифицировать структуру хряща. Последняя группа препаратов не только замедляет прогрессирование заболевания, но и активно влияет на основные симптомы ОА — воспаление и боль, т.е. обладает и симптом-модифицирующим эффектом [6].
Европейская антиревматическая лига (EULAR — The European League Against Rheumatism) отдельно выделила группу лекарственных средств, определяемых как препараты замедленного действия для симптоматической терапии остеоартроза (SYSADOA — symptomatic slow acting drugs for osteoarthritis) [7, 8]. В рекомендациях по лечению ОА колена (2003) и бедра (2004), принятых EULAR, среди медленнодействующих симптоматических средств представлены неомыляемые компоненты авокадо и соевых бобов. К данной группе относится препарат Пиаскледин, обладающий доказанной клинической эффективностью и потенциальными хондропротективными свойствами. Пиаскледин представляет собой неомыляемые соединения авокадо и соевых бобов, получаемые в результате гидролиза, в пропорции 1 : 2 (Пиаскледин, A1S2, Laboratoires Expanscience, Courbevoie, France). Было показано, что сочетанное применение экстрактов авокадо и сои вызывает более выраженную ингибицию цитокинов по сравнению с их изолированным применением, а степень ингибиции зависит от соотношения этих ингредиентов [6].
Цель: оценить клиническую эффективность препарата неомыляемых соединений масел авокадо и сои (Пиаскледин, Laboratoires Expanscience, Courbevoie, France) в комплексном лечении пациентов с остеоартрозом в условиях коморбидности.
Материалы и методы
Для оценки эффективности и переносимости препарата Пиаскледин было проведено открытое когортное клиническое исследование в двух группах. В исследование были включены 25 пациентов (21 женщина и 4 мужчин) с установленным диагнозом остеоартроза. Диагноз «остеоартроз» был установлен в соответствии с критериями ACR 1987 г. согласно приказу Министерства здравоохранения Украины от 12.10.2006 № 676. Исследование проводилось на базе отделения ревматологии ОКБ им. И.И. Мечникова.
Критериями включения были:
— ОА I–III ст. (согласно Kellgren-Lawrence);
— возраст 40–75 лет;
— наличие одного из коморбидных состояний: дислипидемия, ожирение I–II ст., сахарный диабет, кардио–васкулярная патология (артериальная гипертензия, стабильная ИБС, хроническая сердечная недостаточность);
— информированное согласие пациента.
Критерии исключения:
— ОА ІV ст.;
— остеопороз I типа;
— использование симптоматических препаратов замедленного действия в течение последних трех месяцев (глюкозамина сульфат, хондроитина сульфат, гиалуроновая кислота);
— СД І типа;
— другие заболевания, сопровождающиеся костно-хрящевой резорбцией;
— онкологические заболевания;
— гемодинамические значимые аритмии и пороки сердца;
— острая кардиоваскулярная патология;
— заболевания кишечника (колит, энтерит);
— скорость клубочковой фильтрации ниже
60 мл/мин/1,73 м2;
— нарушение функции щитовидной железы (гипо-, гипертиреоз);
— заболевания крови.
Все пациенты случайным образом были разделены на 2 сопоставимые по возрасту и длительности заболевания группы (табл. 1) в соответствии с получаемой терапией. Пациенты 1-й группы (n = 15) в составе комплексной терапии получали Пиаскледин в дозе 300 мг 1 раз в день. Пациенты 2-й группы (n = 10) — только симптом-модифицирующие препараты (анальгетики и НПВС). Срок наблюдения составил 3 месяца.
Как видно из табл. 1, преобладали пациенты с ОА коленных суставов в обеих группах наблюдения: 9 человек (60 %) в основной группе и 7 (70 %) — в конт–рольной.
В ходе исследования у всех пациентов использовали:
1) общеклиническое исследование, включая общий анализ крови, почечно-печеночный комплекс, ревмокомплекс;
2) четырехбалльную шкалу оценки эффективности лечения пациентом/врачом;
3) рентгенографию суставов с определением рентгенологической стадии заболевания;
4) оценку боли в покое и при физической нагрузке (визуальная аналоговая шкала (ВАШ));
5) определение степени нарушения функции суставов (HAQ-ID);
6) оценку функционального состояния больных (WOMAC)
7) определение психоэмоционального состояния (шкала тревоги и депрессии HADS);
8) оценку степени приверженности пациентов к терапии (шкала Мориски — Грина).
В ходе исследования была проанализирована взаимосвязь интенсивности боли и активности процесса, получаемой терапии, степени –функциональных нарушений суставов и рентгенологической стадии. Длительность наблюдения составила 3 месяца. Динамику клинических изменений определяли по результатам повторного анкетирования (HAQ-ID, WOMAC, шкала тревоги и депрессии HADS), оценки боли согласно ВАШ через 1, 2 и 3 месяца после начала исследования.
Статистический анализ проводился с помощью Microsoft Excel 2010 (Microsoft), STATISTICA for Windows 7.0 (StatSoft Inc., США). Количественные показатели представлены в виде n, M ± m, где n — количество наблюдений, М — среднее, m — стандартное отклонение. Достоверность различий определяли с помощью t-критерия Стьюдента для непараметрических данных. Критическое значение уровня значимости (p) ≤ 0,05.
Результаты
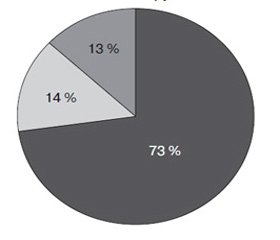
В начале исследования всем пациентам определяли индекс комплайентности к терапии согласно шкале Мориски — Грина. Уровень приверженности к терапии был достаточно высоким — 73 % пациентов в основной группе и 70 % — в контрольной относились к приверженным (комплайентным) (рис. 1).
Все пациенты основной группы отмечали субъективное улучшение самочувствия на фоне приема Пиаскледина. Согласно четырехбалльной шкале оценки эффективности лечения пациентом большинство оценили ее как «хорошую» — 66,7 % (10 человек) (табл. 3).
Все пациенты с ОА I рентгенологической стадии субъективно оценили эффективность лечения на «отлично», большая часть пациентов со II рентгенологической стадией ОА (90,1 %) — «хорошо» (табл. 4).
Интенсивность боли в коленных суставах согласно ВАШ достоверно снизилась как при нагрузке, так и в покое после третьего месяца приема препарата — на 59,7 и 56,7 % соответственно (p < 0,01) (рис. 2).
Выраженность боли в суставах кистей также имела тенденцию к снижению. В основной группе боль при физической нагрузке к концу наблюдения уменьшилась на 60,8 %, в покое — на 55 %. Тогда как в контрольной группе интенсивность боли при нагрузке снизилась лишь на 16,7 % при отсутствии динамики выраженности боли в покое (рис. 3).
Исходя из полученных результатов, ОА тазобедренного сустава характеризуется менее выраженным клиническим ответом по сравнению с ОА суставов кисти и коленных суставов. Так, в основной группе боль в покое снизилась на 33,3 %, при физической нагрузке — на 50 %, в контрольной группе не было зарегистрировано достоверной динамики этих показателей.
Через 3 месяца после начала лечения отмечено достоверное (р < 0,01) уменьшение болевого синдрома и улучшение функционального состояния пациентов (улучшение повседневной активности, меньшее –ограничение подвижности) в обеих группах наблюдения, что подтверждено результатами анкетирования WOMAC (рис. 4). В контрольной же группе не было зарегистрировано достоверного снижения ни одного из показателей WOMAC (рис. 5).
Через 3 месяца после начала исследования отмечен хороший клинический эффект Пиаскледина у пациентов с ОА, что проявлялось улучшением таких клинических показателей, как индекс HAQ. Через 3 месяца лечения было достигнуто достоверное снижение функционального индекса HAQ у пациентов основной группы (–0,67) — с 1,41 ± 0,23 до 0,74 ± 0,19 (p < 0,05) (рис. 6).
В начале исследования у пациентов обеих групп зарегистрирована субклинически и клинически выраженная депрессия. К концу исследования была отмечена положительная динамика психоэмоционального статуса. Так, в основной группе проявления субклинически выраженной тревожности и депреcсии снизились на 19,99 (p < 0,01) и 33,33 % (p < 0,01) соответственно. Сходная динамика отмечалась и в группе пациентов с клинически выраженной тревожностью. У пациентов основной группы зарегистрировано улучшение психоэмоционального статуса согласно госпитальным шкалам тревоги и депрессии (HADS-А, HADS-D).
В ходе исследования была проанализирована необходимость в дополнительном обезболивании (прием НПВС) (табл. 5).
У пациентов, принимавших Пиаскледин, была отмечена тенденция к снижению потребности в приеме НПВС (рис. 7). В группе контроля динамики снижения потребности в дополнительном приеме НПВС не наблюдалось.
За 12 недель применения препарата Пиаскледин у больных с ОА значимых побочных реакций, требующих отмены препарата, не зарегистрировано. Таким образом, хороший клинический эффект и переносимость препарата Пиаскледин позволяют использовать его как препарат выбора у пациентов с остеоартрозом.
Выводы
1. При использовании Пиаскледина у пациентов с ОА отмечалось снижение выраженности болевого синдрома как при физической нагрузке, так и в покое более чем в два раза, что привело к улучшению функционального состояния суставов.
2. Хороший ответ на терапию был получен у пациентов с ОА коленных суставов, аналогичная динамика наблюдалась у пациентов с ОА кистей. Наименее чувствительной к терапии была группа пациентов с ОА тазобедренных суставов.
3. Уменьшение болевого синдрома и расширение двигательной активности привело к улучшению качества жизни и психосоматического статуса пациентов.
4. Пиаскледин оказал хороший эффект у пациентов с начальными стадиями ОА (I–II по Kellgren-Lawrence), с максимальной эффективностью на первой. Таким образом, целесообразно начинать терапию как можно раньше для получения более выраженного клинического ответа.
5. Использование Пиаскледина у пациентов с ОА в условиях коморбидности не привело к декомпенсации и изменению течения сопутствующей патологии, требующей коррекции терапии (набор веса, повышение артериального давления или функционального класса ИБС, развитие гипо- и гипергликемических состояний).
Список литературы
1. Поворознюк В. Здоров’я України: современные принципы лечения / В.В. Поворознюк // Здоров’я України. — 2015. — № 2 (39). — С. 65-69.
2. Зоткин Е.Г. Особенности ведения пациентов с остео–артрозом в первичном звене здравоохранения / Е.Г. Зоткин, С.Ю. Шкиреева // РМЖ. — 2012. — № 27. — С. 32-36.
3. Борткевич О.П. Ефективність препарату Піаскледин 300 у лікуванні пацієнтів з остеоартрозом: доведено в дослідженнях, підтверджено європейською практикою // Український ревматологічний журнал. — 2015. — № 1 (59). — С. 61-65.
4. Очертяная Н.С. Хондропротекторы при заболеваниях суставов: здоровье, которое дарит природа / Н.С. Очертяная // Здоров’я України. — 2012, сентябрь. — С. 78.
5. Шостак Н.А. Остеоартроз: актуальные вопросы диагностики и лечения / Н.А Шостак // РМЖ. — 2014. — № 4. — С. 278.
6. Fernandes L., Hagen K.B., Bijisma J.W. EULAR recommendations for the non-pharmacological core management of hip and knee osteoarthritis // Ann. Rheum. Dis. — 2013. — P. 1-11.
7. Zhang W., Donerty M., Peat G. et al. EULAR evidence-based recommendations for the diagnosis of knee osteoarthritis // Ann. Rheum. Dis. — 2010. — Vol. 69 (3). — P. 483-489.
8. Наказ Міністерства охорони здоров’я України від 12.10.2006 № 676 Клінічний протокол надання медичної допомоги хворим із остеоартрозом (ОА), Код МКХ-10: М15

/16-1.jpg)
/16-2.jpg)
/17.jpg)
/18.jpg)
/19-1.jpg)
/19-3.jpg)
/19-2.jpg)