Газета «Новости медицины и фармации» Гастроэнтерология (551) 2015 (тематический номер)
Вернуться к номеру
К вопросу о безопасности ингибиторов протонной помпы
Авторы: Т. Тлустова
Рубрики: Гастроэнтерология
Разделы: Справочник специалиста
Версия для печати
Статья опубликована на с. 21-25
Одними из наиболее частых гастроэнтерологических патологий являются кислотозависимые заболевания, к которым относят язвенную болезнь желудка и двенадцатиперстной кишки, гастроэзофагеальную рефлюкс–ную болезнь и редкие гиперсекреторные состояния (в частности, синдром Золлингера — Эллисона) (Степанов Ю.М., Будзак И.Я., 2013). В лечении этих заболеваний традиционно применяют антисекреторные препараты, в первую очередь ингибиторы протонной помпы (ИПП). ИПП могут применяться как в комбинации с антибиотиками (при наличии Helicobacter pylori), так и в виде монотерапии в течение длительного времени.
ИПП, действуя на париетальную клетку, контролируют дневную, стимулированную пищей, и ночную секрецию, ингибируют продукцию соляной кислоты независимо от стимула, воздействующего на рецепторы париетальных клеток, не вызывают развития синдрома рикошета и толерантности, быстро подавляют секрецию кислоты. Именно поэтому ИПП позволяют осуществлять 24-часовой контроль за желудочной секрецией и являются основным средством для лечения кислотозависимых заболеваний.
С начала применения ИПП существует опасение, что глубокое ингибирование секреции соляной кислоты может привести к гипергастринемии, которая, в свою очередь, приводит к гиперплазии эндокринных клеток и возможному развитию предраковых изменений.
Первые исследования безопасности ИПП были экспериментальными и проводились на животных: у крыс, которые длительно постоянно получали высокие дозы омепразола, развивалась гипергастринемия, которая приводила к карциноидным опухолям из энтерохромаффиноподобных (ЭХП) клеток, клеток в кислотопродуцирующей слизистой и развитию карциноидной опухоли желудка почти у 30 % самок крыс.
В 1996 г. были опубликованы результаты исследования E.J. Kuipers с соавт., проведенного в Нидерландах и Швеции. Авторами исследования был сделан вывод о том, что пациенты с рефлюксэзофагитом и хеликобактерной инфекцией при лечении омепразолом имеют повышенный риск развития атрофического гастрита (Kuipers E.J., Lundell L., KlinkenbergKnol E.C. et al., 1996).
Однако дальнейшие исследования показали, что в развитии атрофического гастрита более «виновны» хеликобактерии, чем длительное применение ИПП. Так, уже в 1999 г. в исследовании Nordic Gerd Study Group был сделан вывод: «Кислотосупрессивная терапия в виде поддерживающей терапии омепразолом в течение 3 лет не приводит ни к развитию железистой атрофии слизистой тела желудка, ни к развитию кишечной метаплазии у H.pylori-инфицированных больных с гастроэзофагеальной рефлюксной болезнью» (Lundell L., Miettinen P., Myrvold H.E. et al., 1999).
В 2001 году опубликованы результаты исследования R. Lamberts с соавт., в котором была проведена оценка влияния 10-летнего применения ИПП на экзокринную и эндокринную функцию желудка у больных с кислотозависимыми заболеваниями. Был сделан вывод о безопасности длительного лечения ИПП в плане неопластических изменений экзокринной и эндокринной функции желудка.
Однако ни одно из этих исследований не было долгосрочным. В 2012 году опубликованы результаты долгосрочного открытого исследования, касающегося безопасности и эффективности непрерывной поддерживающей терапии пептической язвенной болезни тяжелой степени пантопразолом продолжительностью до 15 лет (G. Brunner, C. Athmann, A. Schneider). Одно из основных преимуществ данного исследования заключается в непрерывном сборе данных о безопасности, и в частности гистологических данных желудка, получаемых на протяжении 15-летней ежедневной терапии пантопразолом. Это самое продолжительное из исследований, в которых проводился анализ каких-либо ИПП.
Дизайн исследования
После заживления острых желудочно-кишечных поражений в результате терапии пантопразолом в течение 4–12 недель пациенты получали открытую поддерживающую терапию пантопразолом сроком до 15 лет в том же центре в Германии, где проводилось комбинированное исследование (первоначальное исследование в течение 10 лет с последующим расширенным исследованием в течение 5 лет) с 20 сентября 1990 года по 27 сентября 2007 года. Исследование проводилось в соответствии с Хельсинкской декларацией, правилами проведения качественных клинических исследований и этическими нормами, утвержденными соответствующими локальными этическими комитетами.
В первоначальное исследование, проводимое в течение 10 лет, были включены пациенты в возрасте 18–80 лет с наличием эндоскопически подтвержденной язвы или рефлюкс-эзофагита, если они имели поражение, устойчивое к терапии антагонистами гистаминовых рецепторов 2-го типа (АГР2Т), непереносимость терапии АГР2Т; если у них было по меньшей мере три рецидива язвенной болезни или рефлюкс-эзофагита в течение предыдущих 5 лет; продолжительный рецидив заболевания, развившийся после оперативного вмешательства на желудочно-кишечном тракте по причине осложнений, или непереносимость омепразола.
Пациенты, которые соответствовали критериям включения, зачислялись в остром периоде исследования и получали пантопразол в дозе 40 мг один раз в день в течение 4 недель. По достижении эндоскопической ремиссии им назначалась поддерживающая терапия в течение 4 недель. Если после 4-недельного курса терапии заживление было неполным, острую терапию продолжали еще в течение 4–8 недель, в зависимости от эндоскопических результатов; доза пантопразола могла корректироваться (до 80 мг/день) на усмотрение исследователя. Если заживление язвы происходило по истечении 12 недель, пациенты начинали долгосрочную фазу поддерживающей терапии. Пациенты, у которых не произошло заживления язв на 12-й неделе, исключались из исследования.
Пациенты, завершившие первоначальную 10-летнюю терапию пантопразолом, включались в дополнительную фазу расширенного исследования продолжительностью 5 лет, если у них отсутствовали осложнения пептической язвенной болезни (как было определено ранее), изменения пищевода, вызванные системными заболеваниями (как было определено ранее), а также синдром Золлингера — Эллисона.
В 5-летнем расширенном исследовании пантопразол назначали в стандартной суточной дозе 40 мг, дозы корректировались индивидуально по усмотрению исследователя на основании терапевтической дозы, указанной в первоначальном 10-летнем исследовании.
Общая цель комбинированного исследования заключалась в изучении переносимости, безопасности и эффективности терапии пантопразолом длительностью до 15 лет у пациентов с пептической язвенной болезнью тяжелой степени. В остром периоде (в период заживления) первичной конечной точкой являлось полное заживление язвенных поражений желудочно-кишечного тракта, которое определялось как полная эпителизация пептической язвы и полное отсутствие (0-я стадия) рефлюкс-эзофагита в соответствии с модифицированной классификацией Савари — Миллера.
Первичной конечной точкой первоначального 10-летнего периода поддерживающей терапии был промежуток времени между заживлением очага поражения желудочно-кишечного тракта и рецидивом, который определялся как наличие эндоскопически диагностированной пептической язвы или рефлюкс-эзофагита, возникшего после наступления заживления. Вторичными конечными точками являлись желудочно-кишечные симптомы (боль, изжога, отрыжка кислым, дисфагия и ощущение полноты), классифицируемые по 4-балльной шкале (от 0 — отсутствие жалоб до 3 — наличие сильных жалоб) каждые 4 недели в течение периода заживления и каждые 3 или 6 месяцев в течение фазы 10-летней поддерживающей терапии.
В случае возникновения дополнительных желудочно-кишечных симптомов их оценивали по 3-балльной шкале (от 1 — слабые жалобы до 3 — выраженные жалобы). В течение периода исследования эффективность пантопразола была установлена в крупных пилотных исследованиях. Таким образом, основное внимание исследования переместилось на рассмотрение конечных точек, касающихся безопасности и переносимости терапии. Это нашло свое отражение в первичной конечной точке 5-летнего расширенного исследования поддерживающей терапии, которая заключалась в переносимости терапии пантопразолом в дозе 40 мг один раз в день.
Лабораторная диагностика проводились перед началом терапии, через каждые 4 недели в острой фазе исследования (фазе заживления), а затем каждые 3 месяца в течение первых 5 лет и каждые 6 месяцев в течение оставшегося 15-летнего периода поддерживающей терапии. Диагностика включала как гематологические (гемоглобин, гематокрит, СОЭ, Квик-тест, эритроциты, тромбоциты и лейкоциты), так и биохимические исследования (натрий, калий, кальций, мочевая кислота, креатинин, общий билирубин, сывороточная глутаматоксалоацетаттрансаминаза, сывороточная глутаматпируваттрансаминаза, щелочная фосфатаза, гамма-глутамилтрансфераза, общий холестерин и триглицериды).
Концентрацию гастрина в сыворотке натощак определяли при каждом посещении во время острой фазы (фазы заживления), а затем каждые 6 месяцев в течение первых 5 лет поддерживающей терапии и каждые 12 месяцев для оставшегося ее периода, используя радио–иммунный анализ.
Эндоскопия (проводимая натощак в течение 12 ч) пищевода, желудка и двенадцатиперстной кишки, а также взятие биопсии выполнялись с 4-недельными интервалами во время острой фазы (фазы заживления), а затем каждые 6 месяцев в течение первых 5 лет поддерживающей терапии и каждые 12 месяцев для оставшегося 15-летнего периода исследования. Дополнительные эндоскопические исследования проводились в случае, если пациент испытывал типичную для язвенной болезни или рефлюкс-эзофагита боль, предполагающую развитие ее рецидива. Во время каждого эндоскопического исследования для гистологической оценки, включающей оценку гастрита, хеликобактерного статуса и изменений в эндокринных клетках, брали по меньшей мере по три образца ткани на биопсию из тела и антрального отдела желудка.
Наличие H.pylori определяли гистологически с помощью модифицированной окраски по Гимзе. Плотность ЭХП-клеток определяли количественно с помощью морфометрической программы CUE-2 после окрашивания срезов ткани по Гримелиусу. Для обеспечения качества подмножество гистологических образцов подвергали повторной оценке опытными патологоанатомами в независимых патологоанатомических центрах в различные периоды времени на протяжении всего исследования.
Побочные эффекты (ПЭ) регистрировали как легкие, средней степени или серьезные на каждом визите. Классификация серьезных ПЭ подвергалась корректировке в ходе первоначального исследования 10-летней поддерживающей терапии в соответствии с требованиями Международной конференции по гармонизации. При этих условиях ПЭ классифицировался как серьезный, если он приводил к смерти, был опасным для жизни, приводил к стойкой или выраженной инвалидности/нетрудоспособности или необходимости длительной госпитализации.
Результаты исследования
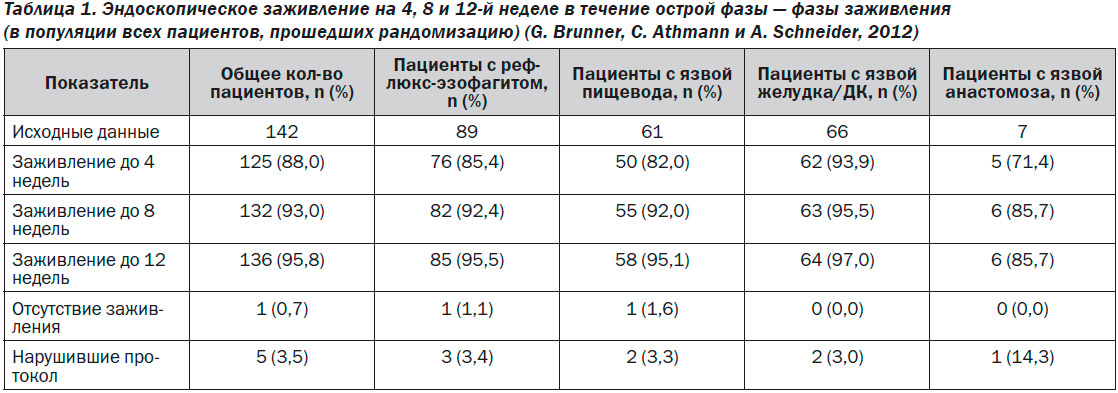
В общей сложности в популяцию для комплексной оценки безопасности вошли 142 пациента. Исходные демографические данные представлены в табл. 1. 10-летнее исследование завершили 99 пациентов, и 79 были зачислены в дополнительную фазу 5-летнего периода последующего наблюдения, из них 36 пациентов завершили 15-летнюю терапию.
Во время острой фазы (фазы заживления) 88,0 % из 142 пациентов достигли эндоскопического заживления в течение 4 недель; 93,0 % пациентов достигли заживления к 8-й неделе, и 95,8 % — к 12-й неделе. Частота заживления для каждого отдельного желудочно-кишечного заболевания представлена в табл. 1. Примерно у 50 % всех излеченных пациентов (n = 136) до завершения пятилетнего комбинированного периода исследования развился рецидив заболевания, средний период до развития рецидива составил 6,90 ± 0,53 года.
Безопасность
Побочные эффекты. Средняя продолжительность терапии составила 9,2 ± 5,8 года. В течение 15-летнего исследования у 101 пациента (71,1 %) были получены данные о развитии 410 ПЭ, большинство из которых (92,9 %) были оценены исследователями как не имеющие никакого отношения к исследуемому препарату.
В общей сложности 16 эпизодов ПЭ (3,9 %) были признаны имеющими возможную связь с исследуемым препаратом, и только 3 ПЭ были оценены исследователями как «скорее связанные» или «определенно связанные с терапией данным препаратом». Считалось, что они имели среднюю степень выраженности; к ним относились периферические отеки, которые прекращались при снижении дозы препарата, депрессия, которая почти полностью проходила с уменьшением дозы, и глоссалгия, которая проходила после прекращения терапии; два последних эффекта имели место у одного и того же пациента. Три пациента были исключены из исследования по причине побочных эффектов, включая периферические отеки (определенно связанные с исследуемым препаратом), почечной анемии и астении.
В течение 15-летнего периода терапии у 64 пациентов (45,1 %) было зарегистрировано 137 серьезных ПЭ (128 эпизодов), из которых 50,8 % были классифицированы как легкие или средней степени выраженности (в 2 случаях интенсивность симптомов оценена не была). Ни один их серьезных ПЭ не был оценен как «скорее связанный» или «определенно связанный с терапией данным препаратом». Девять пациентов умерли в ходе исследования; ни один из случаев смерти, как считалось, не был связан с приемом исследуемого препарата.
Колонизация H.pylori. На этапе включения 77 пациентов (57,0 %) были H.pylori-позитивными и 58 пациентов (43,0 %) были H.pylori-негативными. В ходе исследования после терапии, направленной на эрадикацию H.pylori, количество H.pylori-позитивных пациентов уменьшилось. Среднее значение колонизации у изначально H.рylori-позитивных пациентов составляло 3,37 ± 2,99 балла на этапе включения и за период исследования снизилось до 0,59 ± 1,80 балла к 15-му году терапии, с тенденцией к приближению к нулю (где 0 баллов — отсутствие колонизации, а 6 баллов — колонизация).
Как и следовало ожидать, у H.рylori-отрицательных пациентов на всех посещениях средние оценки в баллах были равны нулю или чуть больше нуля.
Эрадикационная терапия была проведена 33 пациентам, у 27 из которых H.рylori были успешно ликвидированы. У пациентов, прошедших успешную эрадикацию, средняя оценка стабильно снижалась и спустя примерно 10 лет терапии достигла значений, приближавшихся к нулю, что отражало различные временные точки успешной эрадикационной терапии у отдельных больных. Средние оценки в баллах также показали существенное уменьшение количества бактерий в течение периода исследования и у H.pylori-позитивных пациентов, не прошедших успешной эрадикации.
Концентрация гастрина в сыворотке. На протяжении всего исследования средние уровни гастрина натощак возрастали по сравнению с исходными (110,2 ± 128,8 нг/л) и достигли уровня, который был выше верхней границы нормы (25–111 нг/л). В конце периода исследования (15-го года) средние уровни гастрина натощак составляли 320,0 ± 448,0 нг/л. Между пациентами наблюдалась высокая степень колебаний. Заметное увеличение средней концентрации гастрина натощак по сравнению с исходным уровнем наблюдалось между 14-м и 15-м годами (200,2 ± 226,4 нг/л). В предыдущий же 12-месячный период (с 13-го по 14-й год) отмечалось уменьшение его величины. H.рylori-позитивные пациенты, прошедшие успешную эрадикационную хеликобактерную терапию, в ходе исследования продемонстрировали значительно более низкие средние значения гастрина в сыворотке по сравнению с пациентами, которые остались H.рylori-позитивными в последующие визиты клинического исследования.
Плотность ЭХП-клеток. Средняя плотность ЭХП-клеток в кислотопродуцирующей слизистой оболочке показала умеренное первоначальное увеличение в течение первых 3 лет терапии (от 0,34 ± 0,24 % на этапе включения до 0,59 ± 0,40 % на 3-м году). После этого плотность ЭХП-клеток оставалась стабильной в течение всего периода 15-летнего исследования, не увеличиваясь выше 0,62 ± 0,36 % (на 5-м году). Подобные изменения в плотности ЭХП-клеток наблюдались как у H.pylori-позитивных, так и у H.pylori-негативных пациентов.
Плотность лимфоплазмацеллюлярной инфильтрации. На протяжении исследования средние значения плотности лимфоплазмацеллюлярной инфильтрации в поверхностном слое тела или антрального отдела желудка снизилась с приблизительно низкой степени (4 балла) до отсутствия инфильтрации (0 баллов).
На этапе включения среднее значение плотности лимфоплазмацеллюлярной инфильтрации в поверх–ностном слое тела желудка составляло 4,21 ± 1,38 балла. С 1-го до 15-го года средние значения снизились с 4,95 ± 3,29 балла до 2,24 ± 2,69 балла. Кроме того, среднее значение плотности лимфоплазмацеллюлярной инфильтрации в поверхностном слое антрального отдела снизилось с 5,40 ± 3,03 балла на этапе включения до 2,30 ± 2,70 балла на 15-м году; минимальное значение наблюдалось на 12-м году и составляло 2,16 ± 2,67 балла.
Как в теле, так и в антральном отделе желудка средние значения на этапе включения были выше у H.pylori-позитивных, чем у H.рylori-негативных пациентов. Они уменьшались на протяжении всего периода исследования в обеих группах пациентов до аналогичных низких уровней на 15-м году.
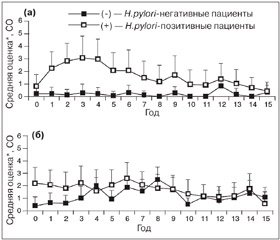
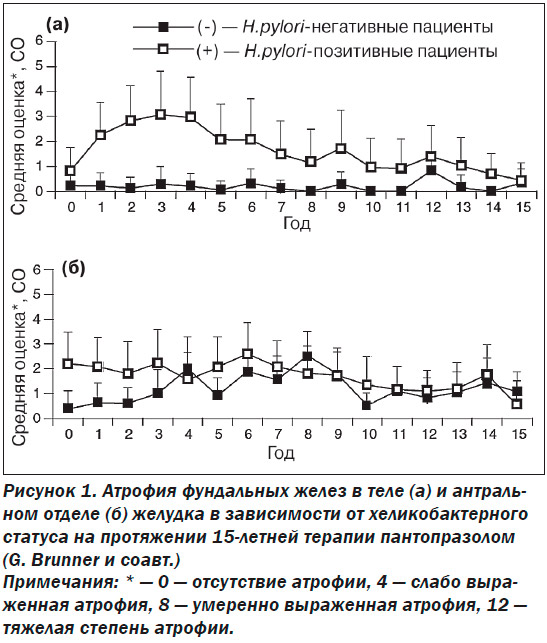
Атрофия фундальных желез. На протяжении всего периода 15-летнего исследования имело место небольшое изменение в значениях средней степени атрофии фундальных желез как в корпусе, так и в антральном отделе желудка, при этом данные показывали значения в районе «отсутствия атрофии».
Исходное среднее значение степени атрофии фундальных желез тела желудка составляло 0,61 ± 0,82 балла. В ходе исследования эта величина достигла максимального значения в 2,05 ± 1,46 балла на 4-м году и снизилась до 0,49 ± 1,33 балла к концу исследования (на 15-м году) (рис. 1). Увеличение степени атрофии желез в первые годы исследования было очевидным у H.pylori-позитивных пациентов, демонстрируя максимальное среднее значение в 3,09 ± 1,70 балла на 3-м году, после чего оно снизилось до 0,53 ± 0,69 балла на 15-м году. В отличие от этого средняя степень атрофии фундальных желез тела желудка у H.рylori-негативных пациентов оставалась неизменно низкой на протяжении всего периода 15-летней поддерживающей терапии пантопразолом.
Средняя степень атрофии фундальных желез антрального отдела желудка снизилась с 1,44 ± 1,22 балла на этапе включения до 0,92 ± 0,86 балла на 15-м году, демонстрируя максимальное значение в 2,25 ± 1,23 балла на 6-м году. У H.pylori-позитивных пациентов наблюдалось устойчивое снижение средней степени атрофии фундальных желез антрального отдела желудка (с 2,09 ± 1,33 балла на этапе включения до 0,53 ± 0,87 балла на 15-м году; при этом у H.pylori-негативных пациентов степень атрофии увеличивалась по сравнению с исходным значением (0,32 ± 0,72 балла) до 2,43 ± 1,00 балла на 8-м году, а затем снижалась до 0,97 ± 0,85 балла на 15-м году.
Дилатация фундальных желез тела желудка. Во время терапии как у H.pylori-позитивных, так и у H.pylori-негативных пациентов в одинаковой степени развивалась дилатация фундальных желез тела желудка легкой и средней степени. На этапе включения средняя оценка дилатации фундальных желез тела желудка составляла 1,37 ± 1,15 балла. Впоследствии, в ходе исследования, ее значение повышалось в среднем до легкой и средней степени дилатации, достигая плато через 9 лет терапии. Максимальная средняя оценка наблюдалась на уровне 6,54 ± 1,78 балла на 9-м году, а по 12-балльной шкале ее значение составляло 4 балла (где 0 баллов — отсутствие дилатации, а 12 баллов — тяжелая степень дилатации).
Метаплазия. На протяжении исследования средние значения кишечной метаплазии в теле желудка, выраженные в баллах, были близки к нулю (0,11 ± 0,40 балла на этапе включения и 0,14 ± 0,47 балла на 15-м году); в целом результаты были аналогичными как для H.pylori-позитивных, так и для H.рylori-негативных пациентов. В антральном отделе желудка среднее значение кишечной метаплазии было немного выше нуля на этапе включения (1,02 ± 1,28 балла) и снижалось до 0,60 ± 0,91 балла на 15-м году. Данные значения были несколько выше у H.pylori-позитивных (1,27 ± 1,45 балла), чем у H.рylori-негативных (0,60 ± 0,91 балла) пациентов в начале исследования. Однако с 6-го года и до конца исследования наблюдались некоторые различия в значениях метаплазии в зависимости от хеликобактерного статуса.
Обсуждение
Данный многофакторный анализ основывался на двух клинических исследованиях, проведенных пре–имущественно по идентичному дизайну и включавших тех же пациентов; при этом основное внимание уделялось оценке переносимости, безопасности и эффективности ИПП у пациентов с хроническими жалобами на язвенную болезнь на протяжении 15-летней терапии исследуемым препаратом. Данные подтверждают, что поддерживающая терапия пептической язвенной болезни тяжелой степени длительностью до 15 лет, включающая ежедневный прием пантопразола, является эффективной и хорошо переносимой. В частности, на протяжении исследования не наблюдалось увеличения симптоматики, связанной с риском развития рака желудка.
Долгосрочная эффективность
На протяжении 15-летней поддерживающей терапии у всех пациентов, за исключением двух, которые были исключены из исследования, симптоматическая и эндоскопическая ремиссия, а также заживление рецидивирующего язвенного или рефлюкс-эзофагита было достигнуто путем ежедневного применения пантопразола в суточных дозах 40–160 мг. У большинства пациентов заживление острых поражений происходило в течение 4 недель.
Эндоскопически подтвержденные рецидивы имели место преимущественно в течение первых 5 лет после заживления, что предполагает тот факт, что пациенты, пребывающие в стадии ремиссии, в течение по меньшей мере 5 лет имеют малую вероятность того, что рецидив заболевания разовьется позже этого периода. Кроме того, в тактике ведения рецидива было эффективным использование более высокой дозы пантопразола, без необходимости переключения на другой кислотоподавляющий препарат. Большое количество цензурированных наблюдений в данном исследовании, вероятно, привело к недооценке среднего интервала времени до развития рецидива, рассчитанного в 6,9 года.
Купирование отдельных желудочно-кишечных симптомов заметно усилилось по сравнению с исходными данными: более 90 % пациентов сообщили об отсутствии каких-либо жалоб на протяжении 15-летнего периода исследования. Эти результаты были подкреплены данными средней оценки желудочно-кишечных симптомов, выраженными в баллах, количество которых существенно снизилось за период исследования.
Долгосрочная безопасность
Данные, полученные из текущего исследования, показывают, что ежедневная поддерживающая терапия пантопразолом в течение 15 лет является хорошо переносимой. Проблем с безопасностью препарата выявлено не было. Не было никаких клинически значимых изменений в лабораторных показателях и ПЭ, по мнению исследователей, связанных с приемом пантопразола, которые бы могли в редких случаях привести к отмене терапии.
Умеренная пантопразол-индуцированная гипергастринемия и ее воздействие на гомеостаз эпителия не были связаны с какими-либо клинически значимыми трансформациями слизистой оболочки желудка. Кроме того, пациенты, подвергшиеся в ходе исследования успешной эрадикации H.pylori, в течение непрерывной терапии пантопразолом продемонстрировали продолжительную регрессию гастрита антрального отдела и тела желудка.
Выводы
Одно из основных преимуществ данного исследования заключается в непрерывном сборе данных о безопасности, и в частности гистологических данных желудка, полученных на протяжении 15-летней еже–дневной терапии пантопразолом. В свете описанных ранее проблем с безопасностью препаратов из группы ИПП, охватывающих последствия гипергастринемии, эти результаты дают убедительные доказательства долгосрочной безопасности пантопразола.
Данное исследование показывает, что ежедневная поддерживающая терапия пантопразолом пептической язвенной болезни тяжелой степени длительностью до 15 лет является эффективной и хорошо переносимой и не имеет проблем, связанных с безопасностью.