Газета «Новости медицины и фармации» 10 (543) 2015
Вернуться к номеру
Мікст-інфекція в акушерстві й гінекології та сучасні підходи до її лікування
Авторы: Бойчук А.В.
Кафедра акушерства та гінекології ННІ післядипломної освіти Тернопільського державного медичного університету ім. І.Я. Горбачевського
Рубрики: Акушерство и гинекология
Разделы: Справочник специалиста
Версия для печати
Статья опубликована на с. 16-17 (Укр.)
Запальні процеси в жіночих статевих органах залишаються актуальною проблемою сучасного акушерства та гінекології. Незважаючи на значну кількість наукових досліджень та впроваджень новітніх антибактеріальних засобів, частота запальних захворювань не має тенденції до зниження. Останніми десятиріччями в усьому світі констатується збільшення частоти інфекцій, які передаються статевим шляхом [5].
Основний спектр мікроорганізмів, що можуть викликати запальні захворювання геніталій, становлять переважно мікробно-протозойно-вірусні асоціати, що передаються статевим шляхом [1, 4]. Вони характеризуються якісно новими властивостями, особливостями клінічного перебігу і не є сумою патологічних складових окремих інфекційних компонентів. Неправильно підібрані препарат, доза, режим і тривалість застосування, недбалість самої пацієнтки призводять до хронізації запалень, періодичних їх загострень, що зумовлює пошук засобів підвищення ефективності терапії запальних процесів. У таких випадках необхідне застосування максимально ефективних засобів.
Це потребує від лікаря вироблення нової стратегії й тактики для діагностики та лікування запальних генітальних захворювань [3].
Гонорейна, трихомонадна, кандидозна, хламідійна, мікоуреаплазмова та вірусна інфекції можуть персистувати в організмі людини довічно, бути причиною періодичного загострення аднекситів, цервіцитів, кольпітів, бартолінітів, циститів тощо [2].
Недіагностовані трихомонади часто приводять до відсутності успіхів у лікуванні інших інфекцій і трактуються як реінфекція.
Морфологічні дослідження довели, що через 3–4 тижні після зараження трихомоніазом запальний процес переходить у хронічну форму.
Приховану трихомонадну інфекцію при хронічних рецидивуючих формах перебігу запальних захворювань внутрішніх статевих жіночих органів за допомогою спеціальних методів діагностували у 80 % випадків.
Особливістю персистування трихомонадної інфекції є здатність трихомонад фагоцитувати й зберігати в живому вигляді мікроорганізми. Загальновідомим є біологічний феномен — здатність вагінальних трихомонад захоплювати й резервувати різні патогенні й умовно-патогенні мікроорганізми. Цим феноменом пояснюється поява рецидивів захворювання навіть після масивних антибактеріальних курсів лікування в разі відсутності протитрихомонадного лікування.
Тому першим кроком у лікуванні мікст-інфекції є санація від трихо–монадної інфекції. Для цього використовують такі широко відомі в практиці лікарів препарати, як тинідазол, метронізадол, трихопол та ін. Але за кілька десятків років їх використання відбулося генетичне моделювання нових пулів трихомонад, які виробили захисні механізми щодо антипротозойної дії цих засобів. Це спонукало до пошуку та розробки нових надійних препаратів.
Особливістю препаратів нового покоління орнідазолів є наявність в їх структурі активного радикала, завдяки якому препарат проникає в клітину шляхом активного та пасивного транспорту, вибірково накопичуючись.
Орнідазол містить активний радикал з атомом хлору. Під впливом нітроредуктаз анаеробних мікроорганізмів (які в аеробів відсутні) відбувається відновлення нітрогрупи у складі молекули орнідазолу з одночасним утворенням вільних радикалів. Продукти відновлення орнідазолу взаємодіють з ДНК мікробної клітини, спричиняючи її деградацію, і таким чином порушують процес реплікації й транскрипції ДНК, що призводить до загибелі мікробної клітини. Крім того, відновлені продукти орнідазолу та вільні радикали справляють прямий цитотоксичний вплив, порушують процеси клітинного дихання анаеробів [2].
Отже, механізм дії орнідазолу полягає в порушенні синтезу й структури ДНК за рахунок складних метаболічних процесів за участю ферментативних систем, що призводить до загибелі мікроорганізму. Курсова доза препарату має враховувати тривалість життєвого циклу розвитку трихомонади, що визначається 7–10 днями. Обов’язковим є одночасне лікування статевого партнера. Цікавим є той факт, що якісний та кількісний склад спермограми після такого курсу лікування покращується на 10–15 %.
На другому місці щодо поширеності та присутності в мікробних асоціаціях знаходяться хламідії, мікоплазми та уреа–плазми. Тому до протизапального лікування має ввійти препарат із широким спектром антибактеріальної дії, активний щодо хламідійної, уреаплазмової та мікоплазмової інфекції, а також до стафілококів, пневмококів, кишкової палички, протея й інших грампозитивних і грамнегативних мікроорганізмів.
Завершують лікування санація кандидомікозної інфекції та противірусна терапія. Але починають цей етап лікування тільки після переконливого негативного контролю трихомоніазу, гонореї, хламідійної інфекції, після загострюючої терапії пірогеналом, гоновакциною чи продигіозаном.
Метою даного дослідження була оцінка ефективності використання Грандазолу в лікуванні комбінованих мікст-інфекцій у хворих із безплідністю для передопераційної санації, оцінка переносимості препарату, а також вивчення впливу проведеного лікування на післяопераційні ускладнення та віддалені результати відновлення репродуктивного здоров’я.
Нами було обстежено й проліковано 50 хворих, які знаходились у гінекологічному відділенні Тернопільської міської комунальної лікарні № 2 на підготовці до оперативного лікування з приводу тривалої трубно-перитонеальної безплідності. Вік хворих коливався від 21 до 37 років. З анамнезу було з’ясовано, що в минулому в кожної третьої жінки був запальний процес жіночих статевих органів, причому тільки в кожної десятої у минулому діагностовано трихомонадний кольпіт. Протягом останніх 6 місяців жодна жінка не отримувала ніякого антибактеріального чи протитрихомонадного лікування. Серед супутніх захворювань в обстежуваних жінок були виявлені хронічний пієлонефрит та тонзиліт у 2 хворих. Зміни в серцево-судинній системі визначались ще у 2 осіб.
Діагностика хламідійного, мікоплазмового та уреаплазмового чи трихомонадного інфікування проводилась імуноферментним методом. Діагноз кандидозу встановлювали за загальноприйнятою методикою ідентифікації. Обстеження проводили до початку лікування та після нього. Статистично вірогідною вважали відмінність при значеннях p < 0,05.
Усі обстежені пацієнтки були розділені на 2 групи. У першу групу ввійшли 25 пацієнток, яким в післяопераційному періоді внутрішньовенно вводили щоденно по 1 г цефтріаксону та 100 мл метронідазолу протягом 5 днів. До другої групи ввійшли хворі, які для передопераційної санації протягом 2 днів отримували внутрішньовенно Грандазол (левофлоксацин у дозі 2,5 мг та 5 мг орнідазолу) внутрішньо–венно один раз на добу та в подальшому, в післяопераційний період, у тій же дозі впродовж 3 днів (25 жінок). Висока активність левофлоксацину зумовлена пошкоджуючою дією на цитоплазматичну мембрану мікробних клітин, дезорганізацію потоків метаболітів усередині з їх швидкою наступною загибеллю.
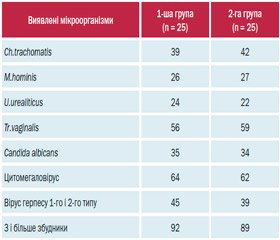
Як для хламідійно-бактеріального, так і для змішаного інфікування характерною була значна частота ураження органів сечовидільної та статевої системи. На тлі вираженого дисбактеріозу піхви в усіх обстежених хворих мали місце ті чи інші титри різних мікробних збудників (табл. 1).
Аналізуючи дані табл. 2, можна відмітити, що за клінічною симптоматикою інфекційних ускладнень у групі, де був використаний Грандазол, спостерігалось вірогідне зменшення кількості омфалітів, вторинних загоювань ран через розходження швів, порушень сечовипускання та віддалених наслідків оперативного втручання з приводу двобічної непрохідності маткових труб. Зокрема, вагітність протягом року після втручання у групі з використанням Грандазолу наставала в жінок в 1,8 раза частіше, ніж у групі з традиційною антибактеріальною терапією. Динаміка об’єктивної зміни симптоматики порівняно з контрольною групою подана в табл. 2. Як видно з наведених даних, запропонований курс передопераційної підготовки веде до значного й вірогідного зниження проявів захворювання і, що особливо важливо, досягнуте покращання переважає результати в першій групі.
Оцінка переносимості препарату проводилась як лікарем, так і пацієнткою. Проведений аналіз дозволяє сказати, що хворі оцінили цей показник суб’єктивно як «дуже добре» в 33 % випадків, «добре» — у 47 %, «задовільно» — у 20 % випадків. Незадовільної оцінки не було.
Клінічні дані були підтверджені не лише клінічними дослідженнями, але й лабораторними показниками (табл. 3). Отримані дані свідчать, що за активністю Грандазол переважає традиційні препарати, що дозволяє активно й ефективно проводити передопераційну підготовку та післяопераційне лікування гнійно-септичних ускладнень.
Коротко підсумовуючи викладене, можна сказати, що топічний діагноз в гінекології обов’язково мусить бути доповненим етіологічним. Антибіотикотерапія має бути призначена вчасно й тільки після визначення збудника. Трихомонадна інфекція значно поширена в популяції, але її збудники змінили свої властивості, виділяються в асоціаціях, рідко визначаються рутинними методами й потребують особливих підходів до лікування. Лікування за наявності збудників в асоціаціях має обов’язково включати протитрихомонадну терапію за ії наявності. Грандазол завдяки своїй різнонаправленій дії є ідеальним засобом для профілактики й лікування післяопераційних ускладнень при трубно-перитонеальній безплідності, що лікується шляхом лапароскопічного доступу.
Список литературы
1. Адаскевич В.П. Инфекции, передава–емые половым путем. — Нижний Новгород; Москва: Изд-во НГМА; Медицинская книга, 1999. — 416 с.
2. Жилка Н., Іркіна Т., Стешенко В. Стан репродуктивного здоров’я в Україні: Медико-демографічний огляд. — К.: МОЗ України, НАН: Інститут економіки, 2001. — 68 с.
3. Кисина В.И. Урогенитальный трихомониаз: проблемы и пути их решения // ИППП. — 2001. — № 6. — С. 14-17.
4. Ромащенко О.В., Руденко А.В., Білоголовська В.В. Діагностика та лікування запальних захворювань сечовидільних шляхів та геніталій у жінок репродуктивного віку // ПАГ. — 2003. — № 4. — C. 95-99.
5. Bowden F., Garnet G. Trichomonas vaginalis epidemiology: parametrerising and analysing a model of treatment inventions // Sex. transm. Infect. — 2000. —Vol. 76. — P. 248-256.

/16-1.jpg)
/16-2.jpg)
/16-3.jpg)