Журнал "Гастроэнтерология" 3 (57) 2015
Вернуться к номеру
Современные достижения в оценке стеатоза печени
Авторы: Диденко В.И. - ГУ «Институт гастроэнтерологии НАМН Украины», г. Днепропетровск
Рубрики: Гастроэнтерология
Разделы: Справочник специалиста
Версия для печати
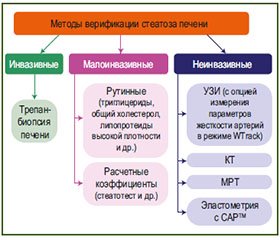
Статья посвящена обзору научных публикаций, посвященных проблеме верификации стеатоза печени. Сегодня все большее значение приобретает проблема своевременного выявления и лечения хронических диффузных заболеваний печени, в патогенезе которых ключевую роль играют фиброз и стеатоз печени. Считается, что стеатоз печени характеризуется накоплением липидов в гепатоцитах, превышающим 5 % массы печени. В последнее время особое внимание уделяется методам верификации стеатоза печени, которые можно разделить на инвазивные, малоинвазивные и неинвазивные. Не утратили актуальности инвазивные методы, к которым относится трепанбиопсия печени — золотой стандарт. Малоинвазивные методы верификации стеатоза печени основаны на биохимическом исследовании венозной крови. Малоинвазивные методы условно можно разделить на рутинные — триглицериды, общий холестерол, липопротеиды высокой плотности и др. — и расчетных коэффициентов: стеатотест и др., результат которых рассчитывается на основании нескольких показателей. К неинвазивным методам верификации относятся: УЗИ, КТ, МРТ, эластометрия с САРТМ-функцией (Фиброскан, модель 502). На наш взгляд, перспективным для верификации стеатоза печени является использование УЗИ с опцией измерения параметров жесткости артерий в режиме WТrack. Из неинвазивных методов верификации стеатоза печени в определенном смысле революцию произвела эластометрия печени при помощи аппарата FibroScan-502-touch с CAP™-функцией. Открывающиеся возможности ранней верификации стеатоза печени позволяют своевременно назначать комплекс лечебно-профилактических мероприятий и создавать предпосылки для остановки прогрессирования, а возможно, и для регресса стеатоза печени.
Стаття присвячена огляду наукових публікацій, присвячених проблемі верифікації стеатозу печінки. Сьогодні все більшого значення набуває проблема своєчасного виявлення та лікування хронічних дифузних захворювань печінки, в патогенезі яких ключову роль виконують фіброз і стеатоз печінки. Вважається, що стеатоз печінки характеризується накопиченням ліпідів у гепатоцитах, що перевищує 5 % маси печінки. Останнім часом особлива увага приділяється методам верифікації стеатозу печінки, які можна розділити на інвазивні, малоінвазивні і неінвазивні. Не втратили актуальності інвазивні методи, до яких відноситься трепан-біопсія печінки — золотий стандарт. Малоінвазивні методи верифікації стеатозу печінки засновані на біохімічному дослідженні венозної крові. Малоінвазивні методи умовно можна розділити на рутинні — тригліцериди, загальний холестерол, ліпопротеїди високої щільності та ін. — та розрахункових коефіцієнтів — стеатотест та ін., результат яких розраховується на підставі декількох показників. К неінвазивним методам верифікації відносяться: УЗД, КТ, МРТ, еластометрія з САРТМ-функцією (Фіброскан, модель 502). На наш погляд, перспективним для верифікації стеатозу печінки є використання УЗД з опцією вимірювання параметрів жорсткості артерій у режимі WТrack. Із неінвазивних методів верифікації стеатозу печінки в певному сенсі революцію справила еластометрія печінки за допомогою апарату FibroScan-502-touch з CAP™-функцією. Відкриваються можливості ранньої верифікації стеатозу печінки, які дозволяють своєчасно призначати комплекс лікувально-профілактичних заходів і створювати передумови для зупинки прогресування, а можливо, і для регресу стеатозу печінки.
The article deals with a review of scientific works on the issue of hepatic steatosis verification. Nowadays, the problem of timely detection and treatment of chronic diffuse liver diseases, in the pathogenesis of which fibrosis and hepatic steatosis play key role, becomes more and more important. It is recognized that hepatic steatosis is characterized by the accumulation of lipids in hepatocytes exceeding 5 % of the liver mass. In recent years, special attention is paid to the methods for verification of hepatic steatosis, which can be divided into invasive, minimally invasive and non-invasive. Invasive methods are still relevant, they include liver core needle biopsy — the gold standard. Minimally invasive methods for hepatic steatosis verification are based on the biochemical study of venous blood. Minimally invasive methods can be conditionally divided into routine — triglycerides, total cholesterol, high density lipoproteins etc., and calculated coefficients: SteatoTest and others. Their results are calculated on the basis of several indicators. Non-invasive methods of verification include: ultrasound, computed tomography, magnetic resonance imaging, elastometry with CAP™function (Fibroscan, model 502). In our opinion, for verification of hepatic steatosis, it is promising to use the ultrasound with the option of measuring the parameters of arterial stiffness in the WТrack mode. Among the non-invasive methods of hepatic steatosis verification, liver elastometry using FibroScan-502-touch device with CAP™ function made a breakthrough in some specific sense. Opening possibilities for early detection of hepatic steatosis enable to place on timely preventive and therapeutic measures and to create the conditions for stopping the progression, and possibly for the regression of hepatic steatosis.
стеатоз, трепан-биопсия, методы верификации стеатоза, УЗИ с функцией WТrack, эластометрия с САРТМ-функцией.
стеатоз, трепан-біопсія, методи верифікації стеатоза, УЗД з функцією WТrack, еластометрія з САРТМ-функ-цією.
steatosis, core needle biopsy, methods of hepatic steatosis verification, ultrasound with WTrack function, elastometry with CAP™ function.
Статья опубликована на с. 94-100
/94.jpg)
Хронические диффузные заболевания печени (ХДЗП) являются одной из сложнейших проблем клинической медицины как в Украине, так и во всем мире в связи с их высокой распространенностью, этапностью течения и развитием тяжелых осложнений. Приблизительно у четверти населения развитых стран выявляется стеатоз печени, а у 3,5–11,0 % — неалкогольный стеатогепатит и цирроз печени [1–3].
/95.jpg)
1. Степанов Ю.М. Стеатоз і стеатогепатит-тригери печінкового фіброгенезу / Ю.М. Степанов, О.Ю. Філіппова // Гастроентерологія + Gastrоenterology: збірник наукових статей. — Дніпропетровськ, 2013. — № 2. — С. 98-107.
2. Степанов Ю.М. Стеатоз печени и стеатогепатит — неизбежность смешанного генеза / Ю.М. Степанов // Гастроентерологія + Gastrоenterology: збірник наукових статей. — Дніпропетровськ, 2014. — № 4 (54). — С. 136-142.
3. Особенности выявления неалкогольной жировой болезни печени в клинической практике / Л.Н. Елисеева, Т.М. Будашова, Т.Ю. Допанова [и др.] // Российские медицинские вести. — 2009. — Т. 14, № 1. — С. 31-36.
4. Степанов Ю.М. Дислипидемия у пациентов с неалкогольным стеатозом печени и билиарной патологией и пути ее коррекции / Ю.М. Степанов, А.Ю. Филиппова // Сучасна гастроентерологія. — 2010. — № 4. — С. 46-51.
5. Степанов Ю.М. Современные подходы к верификации фиброза печени / Ю.М. Степанов, В.И. Диденко // Здоров’я України. — 2013. — № 18 (319). — С. 16-17.
6. Современный взгляд на патогенез, диагностику и лечение неалкогольной жировой болезни печени / С.Н. Мехтиев, Е.Н. Зиновьева, О.А. Мехтиева, С.В. Соколовский // Профилактическая и клиническая медицина. — 2010. — № 3–4. — С. 113-116.
7. Neuschwander-Tetri B.A. Non-alcoholic steatohepatitis: summery of an AASLD Single Topic Conference / В.А. Neuschwander-Tetri, S.H. Caldwell // Hepatology. — 2003. — Vol. 37. — P. 1202-1219.
8. Angulo P. Non-alcoholic fatty liver disease / Р. Angulo, K.D. Lindor // J. Gastroenterol. Hepatol. — 2002. — Vol. 17 (–Suppl. 1). — P. 186-190.
9. Kuntz E. Hepatology. Principles and Practice / E. Kuntz, H-D. Kuntz. — Heidelberg: Springer Medizin Verlag, 2006.
10. Пиманов С.И. Американские рекомендации по диагностике и лечению неалкогольной жировой болезни печени: кое-что проясняется / С.И. Пиманов // Гастроэнтерология. Приложение к журналу Consilium Medicum. — 2012. — № 2. — С. 92-96.
11. Павлов Ч.С. Место пункционной биопсии в диагностике хронических диффузных заболеваний печени / Ч.С. Павлов, Д.В. Глушенков, В.Т. Ивашкин // Фарматека. — 2012. — № S1. — С. 3.
12. Сравнительная характеристика данных ультра-звукового и гистологического исследования при определении степени стеатоза печени у больных хроническим вирусным гепатитом С / О.О. Голик, Д.Ю. Константинов, Л.Л. Попова [и др.] // Уральский медицинский журнал. — 2010. — № 7. — С. 69-72.
13. Evidence of NAFLD progression from steatosis to fibrosing-steatohepatitis using paired biopsies: implications for prognosis and clinical management / S. McPherson, T. Hardy, E. Henderson [et al.] // J. Hepatol. — 2015. — № 62 (5). — P. 1148-1155.
14. Hepatic steatosis estimated microscopically versus digital image analysis / A.R. Hall, A.P. Dhillon, A.C. Green [et al] // Liver Int. — 2013. — № 33 (6). — P. 926-935.
15. Fibrosis progression in nonalcoholic fatty liver vs nonalcoholic steatohepatitis: a systematic review and meta-analysis of paired-biopsy studies / S. Singh, A.M. Allen, Z. Wang [et al] // Clin. Gastroenterol. Hepatol. — 2015. — № 13 (4). — P. 643-654.
16. O’Shea R.S. Alcoholic Liver Disease / R.S. O’Shea, S. Dasarathy, A.J. McCullough // Am. J. Gastroenterol. — 2010. — № 105. — С. 14-32.
17. EASL Clinical Practical Guidelines: Management of Alcoholic Liver Disease / P. Mathurin, A. Hadengue, R. Bataller [et al.] // J. Hepatol. — 2012. — № 57. — С. 399-420.
18. A new index for non-invasive assessment of liver fibrosis / N. Ichino, K. Osakabe, T. Nishikawa [et al] // World J. Gastroenterol. — 2012. — № 16. — P. 4809-4816.
19. Пат. № 2403576 RUS. Способ диагностики стеатоза печени по биохимическим маркерам / Т. Пойнар; опубл. 03.02.2006.
20. Bellentani S. Prevalence of and risk factors for hepatic steatosis in Northern Italy / S. Bellentani et. al. // Ann. Intern. Med. — 2000. — № 132 (2). — Р. 112-117. http://www.springerlink.com / content / h32g2016tlwl8412 / fulltext.pdf.
21. Пиманов С.И. Алкогольная болезнь печени: новое в американском и европейском подходах / С.И. Пиманов, Е.В. Макаренко, Л.В. Тихонова // Гастроэнтерология. Приложение к журналу Consilium Medicum. — 2013. — № 1. — С. 56-60.
22. Maccalau A.J. New information for non-alcoholic fatty liver disease / A.J. Maccalau // J. Clin. Gastroenterology. — 2002. — № 34. — P. 255-262.
23. Степанов Ю.М. Клинические особенности течения неалкогольного стеатогепатита в зависимости от сопутствующих заболеваний / Ю.М. Степанов, А.Ю. Филиппова // Сучасна гастроентерологія. — 2006. — Т. 29, № 3. — С. 4-7.
24. Минушкин О.Н. Приводит ли удлинение сроков лечения Эссенциале Н к увеличению эффективности терапии больных алкогольным поражением печени? / О.Н. Минушкин, Л.В. Масловский // Трудный пациент. — 2004. — № 3. — С. 18-22.
25. Hashimono E. Diagnostic criteria for non-alcoholic steatohepatitis / E. Hashimono // Nippon Rinsho. — 2006. — Vol. 64 (6). — P. 1025-1032.
26. Терновой С.К. Диагностическое значение протонной магнитно-резонансной спектроскопии печени по водороду в оценке терапии стеатоза и стеатогепатита / С.К. Терновой, Д.Т. Абдурахманов, Г.А. Ширяев // Кардиологический вестник. — 2014. — Т. 9, № 3. — С. 105-110.
27. Буеверова Е.Л. Атерогенная дислипидемия и печень / Е.Л. Буеверова, О.М. Драпкина, В.Т. Ивашкин // Рос. мед. вести. — 2008. — № 1. — С. 17-23.
28. Морфофункциональные изменения органов гепатопанкреатобилиарной системы при экспериментальной дислипипротеидемии / А.Д. Дибиров, В.А. Петухов, Д.А. Сон [и др.] // Бюлл. экспер. биол. и мед. — 2000. — № 130 (7). — 45-50.
29. Клинико-морфологические изменения печени при атерогенной дислипидемии и при лечении статинами / Л.Б. Лазебник, Л.А. Зеленогородская, И.А. Морозов [и др.] // Тер. архив. — 2003. — № 5. — С. 8-12.

/95_2.jpg)
/96.jpg)
/97.jpg)
/98.jpg)