Статья опубликована на с. 29-32
Введение
Дегенеративно-дистрофические заболевания суставов широко распространены среди населения и занимают ведущее место среди причин болевого синдрома, функциональных нарушений и инвалидности [1, 2, 5, 12]. В Украине в структуре заболеваний костно-мышечной системы и соединительной ткани артрозы занимают первое место и составляют 26,5 % [1]. Ежегодно количество пациентов с артрозами суставов продолжает увеличиваться. В 2011 году в Украине заболеваемость артрозом составила 605,6 на 100 тыс. населения, что превысило показатель 2010 года (594,6 на 100 тыс. населения) [1]. В Великобритании болями в суставах страдает 8,5 миллиона жителей, в США признаки остеоартроза отмечаются у 27 миллионов взрослого населения старше 25 лет [8, 11]. По данным других авторов, артрозом страдает от 5 до 28 % населения старше 45 лет, а у лиц старше 65 лет признаки артроза выявляются в 33,6–40 % наблюдений [3, 10, 14, 17]. Периартикулярные или внутрисуставные инъекции кортикостероидов входят в различные рекомендации и протоколы по лечению артроза и ревматических поражений суставов [6, 9, 14–16]. Способность кортикостероидов ингибировать воспалительные реакции на клеточном уровне, подавлять синтез простагландинов обеспечивает стойкое противовоспалительное и обезболивающее действие в месте введения [3, 7, 14]. В литературе отражены примеры использования локальной терапии кортикостероидами в комбинации с внутрисуставным введением гиалуроновой кислоты, а также применение локальной периартикулярной терапии при лечении послеоперационных болей у больных после эндопротезирования коленного сустава [4, 5, 13].
Целью нашего исследования было изучение влияния локальной терапии глюкокортикостероидом пролонгированного действия Депос® на функциональную активность суставов у больных с артрозом коленного сустава, оценка переносимости препарата и на основании сравнения результатов лечения пациентов определение терапевтической эквивалентности по показателю эффективности в сравнении с препаратом дипроспан.
Материалы и методы
В исследовании приняли участие пациенты с артрозом коленного сустава І–ІІ стадии, которые проходили курс консервативного лечения на базе отделения ортопедии № 2 КУ «Днепропетровская областная клиническая больница им. И.И. Мечникова». Пациенты были разделены на 2 группы (основную — 35 человек и контрольную — 35 человек) методом простой рандомизации. Основная группа получала однократную периартикулярную инъекцию суспензии Депос® производства ПАО «Фармак» (Украина). Контрольной группе выполнялось периартикулярное введение препарата дипроспан производства фирмы Schering-Plough (США).
Пациентам проводили клиническое обследование до и после периартикулярного введения исследуемых препаратов. Оценка клинической эффективности проводилась по динамике уровня болевых ощущений до и после лечения по визуальной аналоговой шкале (ВАШ) и изменению функциональной активности по индексу Лекена [18]. Также проводили изучение переносимости препарата на основании жалоб пациентов, параметров общего анализа крови, биохимического анализа крови и по частоте возникновения побочных реакций.
Возраст пациентов из основной группы варьировал от 30 до 75 лет, средний возраст составил 51,3 ± 11,9 года. Мужчин было 13, женщин — 22 (табл. 1).
У семи пациентов основной группы выявлен гон–артроз І стадии по классификации Косинской, у 28 больных диагностирован гонартроз ІІ стадии (табл. 2).
В контрольную группу были включены 24 женщины и 11 мужчин, возраст больных варьировал от 30 до 75 лет, средний возраст составил 53,4 ± 10,8 года (табл. 3).
В указанной группе у 8 пациентов выявлен гонартроз І стадии по классификации Косинской, у 27 больных диагностирован гонартроз ІІ стадии (табл. 4).
Результаты и их обсуждение
Как известно, водно-кристаллическая суспензия препаратов Депос® и дипроспан содержит два активных вещества: 2 мг бетаметазона динатрия фосфата, который легко растворим в воде, быстро всасывается и оказывает немедленный терапевтический эффект (пиковая концентрация достигается через несколько минут после введения препарата), а также 5 мг бетаметазона дипропионата, обеспечивающего длительное лечебное воздействие благодаря очень медленному всасыванию, постепенной метаболизации и длительному периоду выведения.
К преимуществам бетаметазона динатрия фосфата можно отнести безболезненность введения и возможность его применения без анестетика, что уменьшает риск развития аллергических реакций, а также высокую клиническую эффективность при минимальной введенной дозе, что позволяет удлинять интервал между инъекциями и снижает опасность развития побочных эффектов.
В обеих группах наблюдаемых нами пациентов была использована техника периартикулярной инъекции гормонального препарата в точку наибольшей болезненности, которая чаще всего локализовалась по медиальному краю суставной щели. В случае двустороннего поражения коленных суставов доза препарата делилась пополам и вводилась периартикулярно с двух сторон.
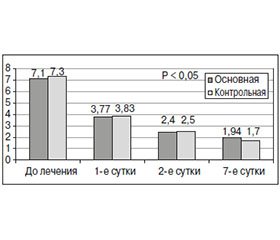
Следует отметить, что первые признаки клинического улучшения (уменьшение суставных болей) после периартикулярного введения глюкокортикоидов наблюдались уже через 3–4 часа, достигая максимального эффекта на 2-е сутки.
При этом выраженный клинический эффект у больных основной группы сохранялся на протяжении недели, так же как и у подавляющего большинства пациентов контрольной группы (рис. 1).
После периартикулярной инъекции кортикостероидных препаратов в обеих группах пациентов отмечено улучшение функциональной активности, о чем свидетельствовали изменения индекса Лекена (рис. 2).
Таким образом, проведенное клиническое исследование показало, что после терапии исследуемым препаратом Депос® производства ПАО «Фармак» (Украина) у пациентов на фоне существенного улучшения состояния отмечалась положительная динамика болевого синдрома, на что указывали значения ВАШ и функциональной активности суставов и что подтвердили показатели индекса Лекена.
В контрольной группе пациентов, которым назначали референтный препарат дипроспан производства фирмы Sсhering-Plough (США), отмечался аналогичный терапевтический эффект.
Анализ динамики клинических симптомов выявил изменения субъективной картины гонартроза в обеих исследуемых группах, при этом существенное уменьшение выраженности болевого синдрома отмечали 91,7 % больных основной группы, которым вводился препарат Депос®, и 93,4 % пациентов контрольной группы, которым вводился дипроспан. Уменьшение локального отека мягких тканей в области пораженного сустава отмечалось у 83,3 % больных основной группы и у 87,3 % — контрольной группы. При этом 100 % больных в обеих группах отметили улучшение функционального состояния пораженного сустава и увеличение физической активности и переносимости физических нагрузок.
Анализ переносимости исследуемых препаратов показал, что объективные данные общего состояния больных, полученные в ходе проведения исследования, данные лабораторного обследования, проводимого до начала и по завершении курса лечения, не выявили патологических изменений в ходе лечения.
В ходе исследования у пациентов обеих групп не было выявлено клинически значимых отклонений в клинико-лабораторных показателях, что свидетельствует о хорошей переносимости исследуемых препаратов (табл. 5).
В процессе лечения переносимость препарата оценивалась также на основании субъективных ощущений пациентов и объективных данных. Каких-либо жалоб, указывающих на побочные эффекты, отмечено не было. Также не было выявлено изменений состояния кожи в месте инъекции и отсутствовали аллергические реакции.
Ухудшения состояния больных по основному заболеванию на фоне применения исследуемого препарата не происходило.
В целом переносимость препарата Депос® суспензия для инъекций производства ПАО «Фармак» (Украина) была оценена у всех пациентов как хорошая.
В ходе исследования при лечении препаратом Депос® суспензия для инъекций производства ПАО «Фармак» (Украина) серьезных побочных явлений не наблюдалось ни у одного пациента.
В результате проведенного исследования доказано, что исследуемый препарат Депос® по терапевтической эффективности не уступает препарату сравнения дипроспан.
Таким образом, проведенное исследование подтвердило эффективность и безопасность применения препарата Депос® суспензия для инъекций производства ПАО «Фармак» (Украина) в лечении артроза І–ІІ клинико-рентгенологической стадии.
Выводы
Результаты проведенного исследования позволяют заключить, что препарат Депос® производства ПАО «Фармак» (Украина) является эффективным и безопасным средством терапии остеоартроза, характеризуется быстрым и длительным терапевтическим действием и хорошей переносимостью и не уступает по терапевтической эффективности и переносимости препарату сравнения дипроспан производства фирмы Sсhering-Plough (США).
Список литературы
1. Коваленко В.М. Ревматичні захворювання в Україні: стан проблеми та шляхи вирішення / В.М. Коваленко // Український ревматологічний журнал. — 2012. — № 3 (49). — С. 84-86.
2. Корж Н.А. Форум экспертов по ступенчатой терапии остеоартроза / Н.А. Корж // Ортопедия, травматология и протезирование. — 2014. — № 3. — С. 144-145.
3. Остеоартроз: консервативная терапия / Под ред. Н.А. Коржа, Н.В. Дедух, И.А. Зупанца. — Харьков: Золотые страницы, 2007. — 424 с.
4. Ayhan E. Intraarticular injections (corticosteroid, hyaluro–nic acid, platelet rich plasma) for the knee osteoarthritis / E. Ayhan, H. Kesmezacar, I. Akgun // World J. Orthop. — 2014. — Vol. 18, № 5 (3). — P. 351-361.
5. Comparison of intra-articular injections of Hyaluronic Acid and Corticosteroid in the treatment of Osteoarthritis of the hip in comparison with intra-articular injections of Bupivacaine. Design of a prospective, randomized, controlled study with blinding of the patients and outcome assessors / Colen S. et al. // BMC Musculoskeletal Disorders. — 2010. — Vol. 11. — P. 264-272.
6. Current concepts on the use of corticosteroid injections for knee osteoarthritis / Law T.Y. et al. // Phys. Sportsmed. — 2015, Feb 23. — P. 1-5. [Epub ahead of print]
7. Efficacy comparisons of the intraarticular steroidal agents in the patients with knee osteoarthritis / Yavuz U. et al. // Rheumatol. Int. — 2012. — Vol. 32, № 11. — P. 3391-3396.
8. Estimates of the Prevalence of Arthritis and Other Rheuma–tic Conditions in the United States, Part II / R.C. Lawrence et al. // Arthritis Rheum. — 2008. — Vol. 58, № 1. — P. 6-35.
9. Habib G.S. Local effects of intra-articular corticosteroids / G.S. Habib, W. Saliba, M. Nashashibi // Clin. Rheumatol. — 2010. — Vol. 29, № 4. — P. 347-356.
10. Hylan G.-F. 20 — Ontario Health Technology Assessment Series. — 2005. — Vol. 5, № 10. — 66 p.
11. Neogi T. Osteoarthritis Prevention / T. Neogi, Y. Zhang // Curr. Opin. Rheumatol. — 2011. — Vol. 23, № 2. — P. 185-191.
12. Non-invasive imaging of cartilage in early osteoarthritis / Glyn-Jones S. et al. // Bone Joint J. — 2013. — Vol. 95-B, № 6. — P. 738-746.
13. Peri-articular steroid injection in total knee arthroplasty: a prospective, double blinded, randomized controlled trial / Chia S.K. et al. // J. Arthroplasty. — 2013. — Vol. 28, № 4. — P. 620-623.
14. Ringdahl E. Treatment of Knee Osteoarthritis / E. Ring–dahl, S. Pandit // American Family Physician. — 2011. — Vol. 83, № 11. — P. 1287-1292.
15. Snibbe J.C. Treatment options for osteoarthritis / J.C. Snibbe, R.A. Gambardella // Orthopedics. — 2005. — Vol. 28, –Suppl. 2. — S. 215-220.
16. The efficacy and duration of intra-articular corticosteroid injection for knee osteoarthritis: a systematic review of level I stu–dies / Hepper C.T. et al. // J. Am. Acad. Orthop. Surg. — 2009. — Vol. 17, № 10. — P. 638-646.
17. Woolf A.D. Burden of major musculoskeletal conditions / A.D. Woolf, B. Pfleger / Bull. World Health Organ. — 2003. — Vol. 81. — P. 646-656.
18. Lequesne M.G. The algofunctional indices for hip and knee osteoarthritis / M.G. Lequesne // J. Rheumatol. — 1997. — Vol. 24, № 4. — P. 779-781.

/30.jpg)
/31.jpg)
/31_3.jpg)