Статтю опубліковано на с. 33-38
Вступ
За даними Всесвітньої організації охорони здоров’я (ВООЗ), при аналізі структури причин звернення до педіатра чи лікаря загальної практики — сімейної медицини близько 70 % випадків припадає на гострі респіраторні інфекції (ГРІ) [1]. В Україні щорічно на ГРІ хворіють 10–14 млн осіб, серед них 5 млн дітей, що становить 25–30 % від загальної та близько 75–90 % — від інфекційної захворюваності [7, 9]. У середньому частота ГРІ у дітей становить 4–6 випадків на рік, а в дітей, які часто хворіють, — 6–10 випадків на рік, що робить ГРІ одним з найбільш частих інфекційних захворювань у дітей усього світу [1, 5]. Експерти ВООЗ відзначають, що дана група захворювань останніми роками має постійну тенденцію до збільшення. Окрім епідеміологічних особливостей, це пов’язано з глобальним процесом зростання урбанізації та посиленням міжконтинентальних міграційних процесів.
Гостра респіраторна інфекція визначається як будь-яке гостре інфекційне захворювання із залученням верхніх і/або нижніх дихальних шляхів, що супроводжується розвитком респіраторного синдрому та інтоксикаційними проявами різного ступеня вираженості [8]. Збудниками ГРІ можуть бути як віруси, так і бактерії. Респіраторний синдром проявляється топічним ураженням дихальних шляхів (фарингіт, ларингіт, трахеїт тощо). Серед інтоксикаційних проявів особливе місце посідає лихоманка, що є однією з найбільш поширених причин звернення до педіатра. Понад 25 мільйонів звернень на рік батьків дітей у Сполучених Штатах Америки реєструються з приводу гіпертермії. При цьому, згідно зі статистичними дослідженнями, 60–80 % випадків підвищення температури тіла в дитини батьки купірують жарознижуючими препаратами самостійно, без залучення медичної допомоги [12]. У Великобританії від 10 до 20 % звернень до відділення дитячої невідкладної допомоги зумовлені лихоманкою із гіпертермічним синдромом [15].
Перше питання, з яким стикається практикуючий лікар-педіатр при обстеженні дитини зі скаргами батьків на підвищення температури тіла, — це інтерпретація термометрії. Цікаво, що чутливість та специфічність батьківської скарги «на дотик дитина горить» становить до 75–85 % щодо об’єктивного підтвердження лихоманки. Що стосується інструментального вимірювання температури тіла, то, згідно з рекомендаціями Американської академії педіатрії (American Academy of Pediatrics, AAP), термометрія в дітей віком до 3 міс. повинна проводитися ректально, від 3 міс. до 3 років — ректально або аксилярно, від 4 до 5 років — ректально, орально або аксилярно, старше від 5 років — орально або аксилярно [7]. При цьому лихоманкою прийнято вважати таку ректальну температуру: у віці до 3 міс. — понад 38,0 °C; від 3 місяців до 2 років — понад 38,3 °C; старше від 2 років — понад 38,0 °C. Аксилярно підвищення температури тіла констатується при цифрах, що перевищують 37,2 °C (Totapally B.R., 2005).
В Україні традиційно дотримуються таких клінічних показань для призначення антипіретичної терапії: температура в дитини понад 38,5 °С, а для групи дітей із обтяжуючими факторами (фебрильні судоми в анамнезі, супутні захворювання центральної нервової та серцево-судинної систем) — понад 38,0 °С.
Лихоманка (febris) — захисно-пристосувальна реакція організму, яка виникає у відповідь на дію пірогенних подразників і характеризується перебудовою процесів терморегуляції (підвищення температури тіла), внаслідок чого зростає імунологічна реактивність організму за рахунок активації фагоцитозу, підвищення синтезу інтерферону, стимуляції гострофазової відповіді на запалення, що в цілому сприяє процесу антитілоутворення [3, 4].
Найбільш поширеною є класифікація лихоманки за ступенем підвищення температури тіла, згідно з якою прийнято розрізняти: субфебрилітет — температура тіла у межах 37,0–37,9 °С; помірну лихоманку — 38,0–39,9 °С; високу лихоманку — 40,0–40,9 °С; надмірну лихоманку, або гіперпірексію, — понад 41,0 °С.
Найчастішими патогенними подразниками, що призводять до зміщення установочної точки термостату довгастого мозку в бік підвищення температури, є дія на центр терморегуляції прозапальних цитокінів (інтерлейкінів-1, -6, фактора некрозу пухлини α), які синтезуються при ГРІ. Останні викликають локальне збільшення концентрації простагландинів у терморегуляторному центрі, що й призводить до зсуву встановленої температурної межі та порушення терморегуляторного балансу в бік посилення теплопродукції та зменшення тепловіддачі. Зниження місцевого синтезу простагландинів у гіпоталамусі та терморегуляторному центрі є механізмом антипіретичної дії більшості жарознижувальних препаратів. Окремо виділяють гіпертермічний синдром — патологічний процес, що розвивається на фоні довгострокової лихоманки, яка призводить до зриву компенсаторних можливостей терморегуляції й характеризується поліорганними мікроциркуляторними й дисметаболічними розладами [3, 4].
Педіатр повинен звернути увагу батьків на такі ознаки переносимості лихоманки дитиною, як рівень активності, апетит, адекватне споживання рідини. Проте, незважаючи на захисно-пристосувальний характер, якщо лихоманка сама по собі порушує загальний стан та самопочуття дитини, знижуючи комплайєнс до надання медичної допомоги, необхідним є її ефективне симптоматичне лікування. Це підтверджується роботами Chiappini et al. [11], Rainsford [18] та рекомендаціями ААР: використання жарознижувальних засобів є доцільним лише тоді, коли дитина відчуває дискомфорт, при проведенні антипіретичної терапії дозування препарату повинно проводитися тільки з урахуванням маси тіла, а не віку дитини.
Згідно з чинним Уніфікованим клінічним протоколом первинної медичної допомоги дорослим та дітям «Гострі респіраторні інфекції», затвердженим наказом МОЗ України № 49 від 16.07.20149 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при грипі та гострих респіраторних інфекціях», медикаментозну корекцію лихоманки проводять ібупрофеном або парацетамолом (ацетамінофеном). Ацетилсаліцилова кислота не повинна призначатися для зниження температури тіла при ГРІ дітям (до 18 років) [8].
Для лікаря-практика постає питання вибору поміж цими двома засобами. Звернемося до даних доказової медицини для відповіді на це питання. Perrott et al. (2004) провели метааналіз сімнадцяти досліджень порівняння ефективності ібупрофену та парацетамолу в дітей із лихоманкою та болем. При цьому в стандартному дозуванні (5–10 мг/кг на дозу для ібупрофену та 10–15 мг/кг для парацетамолу) ібупрофен виявився більш ефективним антипіретиком на 2, 4 та 6-й годинах після прийому разової дози обох препаратів [17]. Hay et al. (2009) провели рандомізоване плацебо-контрольоване дослідження PITCH щодо використання ібупрофену та парацетамолу для лікування 3746 дітей з лихоманкою. При цьому час, протягом якого температура залишалася нормальною через 4 години після призначення обох препаратів, у середньому становив 116,2 хв для парацетамолу та 157,2 хв для ібупрофену. Час до нормалізації температури після прийому ліків становив у середньому 71 хв для парацетамолу та 42,2 хв для ібупрофену. Нормальна активність та сон спостерігалися в 58 та 50 % дітей, які прийняли ібупрофен, проти 40 та 37 % дітей відповідно, яким був призначений парацетамол. Автори підсумували, що для лікування дітей з лихоманкою як препарат першого вибору рекомендовано призначати ібупрофен (і радити батькам у першу чергу вживати саме цей засіб) [13].
Отже, швидкість та тривалість дії ібупрофену, згідно з даними Hay et al. (2009), виявилися більшими, ніж у парацетамолу. Раніше швидкість жарознижувального ефекту ібупрофену вже була продемонстрована в дослідженні F. Pelen, F. Verriere et al. (1998), за результатами якого зниження температури у хворих спостерігалося вже через 15 хвилин після прийому препарату. Тривалість жарознижуючого ефекту після прийому ібупрофену в дозі 10 мг/кг становила 12 годин незалежно від початкового рівня лихоманки [16]. Більш тривалий антипіретичний ефект ібупрофену порівняно з парацетамолом відображений також у рекомендаціях щодо частоти використання препаратів за добу. Так, стандартне дозування парацетамолу становить 10–15 мг/кг кожні 4–6 годин (до 4 разів на добу), тоді як ібупрофен використовується в дозі 5–10 мг/кг кожні 6–8 годин (до 3 разів на добу) [13].
Важливою характеристикою ібупрофену є наявність протизапальної та знеболюючої дії поруч із жарознижуючою. При такій патології, як гострий середній отит, гострий тонзиліт, гострий фарингіт, афтозний стоматит, важливе значення має усунення місцевого больового синдрому, що додатково завдає страждань дитині та порушує такі фізіологічні процеси, як прийом їжі та рідини. Завдяки системному блокуванню циклоксигенази-2 (як у центральній нервовій системі, так і у вогнищі запалення — центральний та периферичні механізми дії) ібупрофен пригнічує пов’язаний із місцевим запальним процесом больовий синдром. Так, Шотландська міжколегіальна мережа клінічних рекомендацій (Scottish Intercollegiate Guidelines Network, 2010) зазначає, що ібупрофен може використовуватися в дітей та дорослих із болем у горлі із метою знеболювання [2]. Отже, ібупрофен можна вважати препаратом першої лінії для купірування лихоманки та супутнього больового синдрому в дітей.
Використання будь-яких препаратів у педіатричній практиці вимагає як ефективності, так і належного профілю їх безпеки. Метааналіз 24 рандомізованих плацебо-контрольованих досліджень показав відсутність вірогідної різниці в переносимості та профілі безпеки використання ібупрофену, парацетамолу та плацебо (Southey Е., 2009). Раніше S.M. Lesko, A.A. Mitchell (1995) було проведене рандомізоване мультицентрове подвійне сліпе дослідження щодо порівняння ймовірності госпіталізації із приводу шлунково-кишкових кровотеч, ниркової недостатності або анафілаксії, синдрому Рейє у дітей на фоні короткострокового прийому ібупрофену та парацетамолу, що включало 84 192 дитини. Результати показали, що ризик наведених ускладнень був порівнянним і не був підвищеним при короткотривалому використанні ібупрофену. Аналіз 12 електронних баз даних (MEDLINE, EMBASE, Cochrane Database та ін.) показав, що застосування ібупрофену в дитячій популяції не пов’язане з ризиком виникнення бронхіальної астми в дітей, а при використанні ібупрофену як антипіретика в дітей з діагнозом бронхіальної астми відзначається більш низький ризик госпіталізації (0,63) та амбулаторних відвідувань (0,56) порівняно з використанням парацетамолу [14]. Потрібно пам’ятати, що в процесі метаболізму парацетамолу в печінці під впливом цитохрому Р450 можливе утворення реактивних метаболітів, які токсично діють на тканини. Ліки, що посилюють синтез цитохрому Р450, збільшують ймовірність токсичної дії парацетамолу (фенобарбітал, дифенін та інші протиепілептичні засоби, зиксорин, рифампіцин, глюкокортикоїди). При наявності в дитини недостатності глюкозо-6-фосфатдегідрогенази та редуктази глутатіону призначення парацетамолу може викликати гемоліз еритроцитів. На відміну від парацетамолу ібупрофен не утворює токсичних метаболітів, а при передозуванні ібупрофен має меншу токсичність порівняно з парацетамолом. У роботі R.P. Beyer (2007) показано, що ібупрофен має найменшу гастро- та гепатотоксичність серед нестероїдних протизапальних засобів [10]. Отже, використання ібупрофену в педіатричній практиці є більш безпечним.
На вітчизняному фармацевтичному ринку лікарі віддають перевагу препарату ібупрофену Нурофєн® (виробник Reckitt Benckiser Healthcare International (Великобританія)), який широко використовується для лікування лихоманки та больового синдрому в педіатричній практиці. Нурофєн® доступний у таких лікарських формах: Нурофєн® для дітей, супозиторії 60 мг (з 3-місячного віку), Нурофєн®, таблетки 200 мг (з 6 років), Нурофєн® для дітей, суспензія для перорального застосування в дозуванні 100 мг/5 мл (з 3 місяців), Нурофєн® для дітей Форте, суспензія для перорального застосування в дозуванні 200 мг/5 мл (з 6 місяців).
Нашу увагу привернув Нурофєн® для дітей Форте 200 мг/5 мл, оральна суспензія з полуничним смаком у флаконах по 100 мл. Ця лікарська форма препарату забезпечує раціональне дозування для дітей більш старшого віку та застосовується у пацієнтів від 6 місяців до 12 років з масою тіла не менше від 8 кг у разовій дозі 5–10 мг/кг, максимальна добова доза 20–30 мг/кг та кратність прийому до 3 разів на добу. Показання до застосування: симптоматичне лікування гарячки та болю різного походження (включаючи гарячку після імунізації, гострі респіраторні вірусні інфекції, грип, біль при прорізуванні зубів, біль після видалення зуба, зубний біль, головний біль, біль у горлі, біль при розтягненні зв’язок та інші види болю, у тому числі запального генезу) [6].
Метою нашої роботи стало узагальнення досвіду використання препарату Нурофєн® для дітей Форте у дітей із ГРІ, що супроводжуються лихоманкою та синдромом інтоксикації.
Матеріали та методи
Під нашим спостереженням перебували 98 дітей, хворих на ГРІ. Серед них було 48 (49 %) хлопчиків та 50 (51 %) дівчаток. Середній вік хворих становив 7,1 ± 0,2 року (4–12 років).
Критеріями включення у дослідження були клінічні ознаки ГРІ вірусного походження в перші 1–2 доби від початку захворювання.
Критерії виключення із дослідження:
— 3-тя та більше доба захворювання;
— пацієнти з групи дітей, які часто хворіють;
— наявність бактеріальних ускладнень;
— підвищена чутливість до компонентів препарату Нурофєн® для дітей Форте в анамнезі;
— наявність некомпенсованих захворювань чи гострих станів, що здатні вплинути на результати дослідження (гострі та хронічні захворювання серцево-судинної системи, респіраторного тракту);
— вік дітей менше від 4 років та понад 12 років.
Хворі діти надходили під спостереження через погіршення загального стану, пов’язане з фебрильною лихоманкою (в середньому 38,7 ± 0,1 °С) та синдромом інтоксикації. Останній був виражений помірно в 1/3 пацієнтів, у 2/3 — значно і проявлявся загальною слабкістю, зниженням апетиту, відчуттям ломоти у м’язах, головним болем, негативною поведінкою дітей, що значно утруднювало встановлення контакту з медичним персоналом.
При обстеженні всі пацієнти мали катаральний синдром із залученням верхніх дихальних шляхів — закладеність носа, слизові виділення з носових ходів, дертя в горлі та болючість при ковтанні, покашлювання. Візуально було виявлено гіперемію слизової оболонки носа, піднебінних дужок, задньої стінки глотки з наявністю зернистості. Аускультативна картина була без особливостей. Усім дітям було проведено загальний аналіз крові: у 67 (68 %) дітей змін не спостерігалося, а в 31 (32 %) пацієнта був виявлений відносний лімфоцитоз.
На основі отриманих даних пацієнтам було встановлено діагноз «гостра респіраторна вірусна інфекція: гострий назофарингіт» та призначено противірусну терапію, деконгестанти за потребою. В усіх випадках із жарознижувальною метою був призначений ібупрофен (суспензія Нурофєн® для дітей Форте) в дозі 10 мг/кг. Використовували ібупрофен у вказаній дозі 3 рази на день, у середньому протягом 3 днів.
Для визначення ефективності ібупрофену як жарознижувального препарату нами було оцінено середнє значення температури тіла у хворих через 15 хвилин після його прийому та кількість пацієнтів із нормальною температурою тіла на 30-й хвилині, 1-й, 3-й, 6-й, 8-й годинах після застосування препарату. Нами був проведений аналіз динаміки симптомів, пов’язаних із синдромом лихоманки та інтоксикації протягом першої та другої доби прийому ібупрофену. Симптоми визначалися у балах (від 0 до 3) залежно від самопочуття дитини та оцінки її стану батьками: 3 бали — найбільший ступінь прояву симптому, 0 балів — повна відсутність. Безпечність препарату оцінювалася за виникненням побічних реакцій (диспептичні та алергічні прояви тощо). Аналіз суб’єктивної оцінки батьками реакції дитини на смакові якості препарату проводився за допомогою 10-бальної візуальної аналогової шкали (ВАШ), де оцінка в 0 балів відповідала найменш улюбленій страві з тих, що дитина вживала в минулому, 10 балів — найулюбленішій страві хворого з його раціону. Додатково ставилося питання: «Чи будете Ви приймати цей препарат в майбутньому при виникненні необхідності застосування антипіретиків?»
Результати дослідження та їх обговорення
Фебрильна лихоманка (у середньому 38,7 ± 0,1 °С), яка порушувала загальний стан, була у всіх дітей на момент госпіталізації. Пацієнти отримали першу дозу оральної суспензії відповідно до маси тіла. Для визначення ефективності ібупрофену як жарознижувального препарату нами було оцінене середнє значення температури тіла у хворих через 15 хвилин після його прийому. Вказане середнє значення становило 38,00 ± 0,07 °С проти 38,7 ± 0,1 °С до призначення препарату (р < 0,001). Отримані дані вказують, що використання ібупрофену дозволяє вірогідно знизити середні показники температури тіла у хворих з лихоманкою вже на 15-й хвилині після прийому препарату. Нам також було оцінено кількість пацієнтів із нормальною температурою тіла на 30-й хвилині, 1-й, 3-й, 6-й, 8-й годинах після прийому ібупрофену. Дані наведені в табл. 1.
Дані табл. 1 показують, що в усіх пацієнтів антипіретичний ефект препарату спостерігався протягом 6 годин, а в переважній більшості випадків (90 %) нормотермія підтримувалася протягом 8 годин після прийому ібупрофену.
Динаміка симптомів, пов’язаних із синдромом лихоманки та інтоксикації протягом першої та другої доби прийому ібупрофену, подана в табл. 2.
При аналізі динаміки симптомів, пов’язаних із синдромом лихоманки та інтоксикації, на фоні комплексного лікування нами було виявлено вірогідне (р < 0,001) зниження середнього показника вираженості загальної слабкості, зниження апетиту, негативної поведінки та відчуття ломоти в м’язах вже на першу добу прийому ібупрофену, при цьому вказаний ефект прогресивно збільшувався на другу добу. Призначення ібупрофену, призводячи до покращення загального самопочуття, сприяло зменшенню негативної поведінки, що, у свою чергу, збільшувало комплайєнс хворих до отримання медичної допомоги. Побічних реакцій при прийомі ібупрофену не було виявлено в жодної дитини.
Суб’єктивна оцінка батьками реакції дитини на смакові якості препарату Нурофєн® для дітей Форте у вигляді суспензії, визначена за 10-бальною візуальною аналоговою шкалою, становила 7,6 бала. Тобто препарат Нурофєн® для дітей Форте має добрі органолептичні властивості, що в педіатричній практиці є вкрай важливим для збереження прихильності пацієнта та його батьків до терапії (рис. 1).
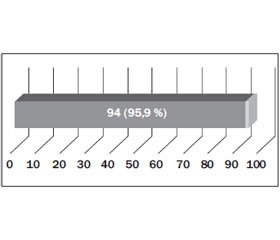
У 94 випадках із 98 отримано позитивну відповідь на запитання: «Чи будете Ви приймати цей препарат в майбутньому при виникненні необхідності застосування антипіретиків?» (рис. 2).
Висновки
Отже, згідно з даними огляду літератури та особистих спостережень, ібупрофен є безпечним та ефективним препаратом першої лінії для купірування лихоманки в дітей, особливо при поєднанні останньої з больовим та вираженим інтоксикаційним синдромами. Проведене нами дослідження показало, що Нурофєн® для дітей Форте вже через 15 хвилин застосування вірогідно знижує середні показники температури тіла в групі пацієнтів, що вказує на швидкий початок дії. Нормалізація температури тіла після прийому препарату забезпечується протягом 6 годин у всіх пацієнтів, а в переважній більшості випадків триває до 8 годин. Застосування ібупрофену дозволяє також вірогідно зменшити вираженість симптомів, пов’язаних із синдромом лихоманки та інтоксикації (загальна слабкість, зниження апетиту та відчуття ломоти в м’язах). Крім того, дія препарату сприяла зменшенню проявів негативної поведінки, внаслідок чого покращувався контакт із медичним персоналом. Побічних реакцій при прийомі ібупрофену не було виявлено в жодної дитини, що вказує на високий профіль безпеки використання препарату в дітей. При цьому оральна суспензія має добрі органолептичні властивості, завдяки чому забезпечується високий комплайєнс до терапії. Налаштування абсолютної більшості батьків на застосування препарату в майбутньому свідчить про прихильність до терапії суспензією Нурофєн® для дітей Форте.
На основі наведених даних препарат ібупрофену Нурофєн® для дітей Форте може бути рекомендований для застосування в педіатричній практиці для дітей дошкільного та шкільного віку з лихоманкою.
Список литературы
1. Баранов А.А. Педиатрия: Национальное руководство: В 2 т. — М.: ГЭОТАР-Медиа, 2009.
2. Ведення пацієнтів з болем у горлі та показання до тонзилектомії: Рекомендації SIGN // Дитячий лікар. — 2010. — № 4. — С. 66-68.
3. Вельтищев Ю.Е., Шаробаро В.Е. Неотложные состояния у детей: Справочник. — М.: Бином, 2013. — С. 222-227.
4. Геепе Н.А. Лихорадка у детей. Причины развития и методы лечения / Н.А. Геепе, А.Б. Малахов // Здоровье ребенка. — 2009. — № 1(16).
5. Знаменская А.А. Лечение и профилактика острых респираторных инфекций у часто болеющих детей / А.А. Знаменская, В.Л. Фомина, В.Ф. Учайкин и др. // Лечащий врач. — 2011. — № 1.
6. Інструкції з використання препарату Нурофєн для дітей Форте.
7. Крамарев С.О. Оцінка ефективності рекомбінантного інтерферону альфа для профілактики та лікування гострих респіраторних вірусних інфекцій у дітей / С.О. Крамарев, В.В. Євтушенко // Здоров’я України. — 2008. — № 18/1. — С. 49-50.
8. Наказ МОЗ України від 16.07.2014 № 499 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при грипі та гострих респіраторних інфекціях».
9. Печінка А.М. Гострі респіраторні захворювання: питання клінічної діагностики та лікування / А.М. Печінка, М.І. Дземан // Укр. мед. часопис. — 2010. — № 5(79). — С. 94-103.
10. Beyer R.P. Multicenter study of acetaminophen hepatotoxicity reveals the importance of biological endpoints in genomic analyses / R.P. Beyer // Toxicological Sciences. — 2007. — Vol. 99, № 1. — P. 326-337.
11. Сhiappini E. Management of fever in children: summary of the Italian Pediatric Society guidelines / E. Chiappini, N. Principi, R. Longhi, P.A. Tovo, P. Becherucci et al. // Clin. Ther. — 2009. — Vol. 31, № 8. — P. 1826-1843.
12. Craig J.C. The accuracy of clinical symptoms and signs for the diagnosis of serious bacterial infection in young febrile children: prospective cohort study of 15781 febrile illnesses / J.C. Craig, G.J Williams, M. Jones, M. Codarini // BMJ. — 2010. — Vol. 340.
13. Hay A.D. Paracetamol and ibuprofen for the treatment of fever in children: the PITCH randomised controlled trial / A.D. Hay, N.M. Redmond, C. Costelloe, A.A. Montgomery, M. Fletcher et al. // Health Technology Assessment. — 2009. — Vol. 13 (27). — P. 1-163.
14. Kanabar D. A review of ibuprofen and acetaminophen use in febrile children and the occurrence of asthma-related symptoms / D. Kanabar, S. Dale , M. Rawat // Clin. Ther. — 2007. — Vol. 29, № 12. — P. 2716-2723.
15. Nijman R.G. Clinical prediction model to aid emergency doctors managing febrile children at risk of serious bacterial infections: diagnostic study / R.G. Nijman, Y. Vergouwe, M. Thompson, M. van Veen // BMJ. — 2013. — 346. doi: http://dx.doi.org/10.1136/bmj.
16. Pelen F. Treatment of fever: Monotherapy with ibuprofen. Multicentre acceptability study conducted in hospital / F. Pelen, F. Verriere // Ann. Pediatr. — 1998. — Vol. 45(10). — P. 719-728.
17. Perrott D.A. Efficacy and safety of acetaminophen vs ibuprofen for treating children's pain or fever: a meta-analysis / D.A. Perrott, T. Piira, B. Goodenough, G.D. Champion // Arch. Pediatr. Adolesc. Med. — 2004. — Vol. 158(6). — P. 521-526.
18. Rainsford K.D. Ibuprofen: pharmacology, efficacy and safety / K.D. Rainsford // Inflammopharmacology. — 2009. — Vol. 17, № 6. — P. 275-342.

/36.jpg)
/37.jpg)