Статтю опубліковано на с. 73-77
Вступ
Неонатальна жовтяниця є однією з актуальних проблем у неонатології. У наш час спостерігається тенденція до зростання частоти цієї патології та більш тривалого перебігу захворювання з високим рівнем непрямого білірубіну в сироватці крові. У світовій медицині важливим також є питання щодо чинників розвитку пролонгованої кон’югаційної жовтяниці, уточнення ризиків і ускладнень для здоров’я дітей [1–3]. Залишається дискусійним питання щодо критичного рівня білірубіну, що токсично впливає на різні органи та системи організму. На сьогодні недостатньо вивчене питання впливу як високих, так і середніх концентрацій сироваткового білірубіну на нервову систему новонародженого, особливо при затяжному перебігу даного стану.
Причинами зростання частоти пролонгованої неонатальної жовтяниці можуть бути: погіршення стану екології та, як наслідок, погіршення стану здоров’я матерів; збільшення частоти супутньої екстрагенітальної патології; патологічного перебігу вагітності та пологів і призначення цим через це лікувальних препаратів (антибіотиків, гормональних, противірусних, протизапальних препаратів) як матерям, так і новонародженим. Важливими факторами ризику розвитку затяжної кон’югаційної жовтяниці у новонароджених є наявність соматичної й інфекційної патології матері під час вагітності, тобто анемії різного ступеня тяжкості, цукровий діабет, носійство TORCH-інфекції, гіпертонічна хвороба, автоімунний тиреоїдит, вегетативна дисфункція й інші захворювання серцево-судинної системи, хронічні захворювання органів травлення. Встановлено, що більш затяжному перебігу кон’югаційної жовтяниці сприяє акушерська патологія (стрімкі пологи, кесарів розтин, обвиття пуповиною, слабкість пологової діяльності, передчасне вилиття навколоплідних вод) [4–6]. За даними багатьох досліджень відомо, що жовтяниця частіше виникає в новонароджених, які народилися від матерів з обтяженою генетичною спадковістю, які хворіли на гострі респіраторні інфекції під час вагітності, отримували лікування під час вагітності, а також яким призначались препарати для стимуляції пологової діяльності [5–7].
На сьогодні відомо, що суттєвими факторами ризику розвитку пролонгованого перебігу неонатальної жовтяниці є патологічна втрата маси тіла понад 10 % після народження, часті зригування та блювання, дисбіоз кишечника. Сприяє розвитку гіпербілірубінемії у новонароджених відходження меконію пізніше 8–12 годин після народження, затримка перетискання пуповини. Діти, народжені з різноманітною перинатальною патологією, такою як асфіксія в пологах, крововиливи в головний мозок, кефалогематоми, внутрішньоутробні інфекції, недоношеність, затримка внутрішньоутробного розвитку, схильні до розвитку пролонгованої кон’югаційної жовтяниці внаслідок зниження функціональної активності гепатоцитів і гепатотоксичної дії інтенсивної терапії. Значний вплив на перебіг жовтяниці у новонароджених має гіпоксія та асфіксія, під впливом яких затримується дозрівання глюкуронілтрансферазної системи, спостерігається дисоціація комплексу «білірубін — альбумін», підвищується проникність судин і гематоенцефалічного бар’єра [8, 9]. Хронічна внутрішньоутробна гіпоксія викликає посилення еритропоезу, що призводить до поліцитемії, підвищеного згортання крові, порушення мікроциркуляції в судинах, розвитку сладж-синдрому. Через погіршення мікроциркуляції в тканинах знижується інтенсивність гліколізу, зростають процеси перекисного окислення та накопичення вільних радикалів, посилюється ацидоз, що, в свою чергу, руйнує мембрану еритроцитів. Під впливом хронічної гіпоксії на плід включається компенсаторний механізм, спрямований на забезпечення повноцінної оксигенації життєво важливих органів — головного мозку, серця та наднирникових залоз. У той же час знижується кровонаповнення та необхідна оксигенація печінки, нирок і кишечника плода, що супроводжується затримкою дозрівання ферментативних систем, зниженням функціональної активності цих органів у неонатальному періоді. Хронічна гіпоксія плода викликає розвиток метаболічного ацидозу, накопичення молочної кислоти, внаслідок чого порушуються білковий, ліпідний обмін, електролітний баланс. Такі зміни метаболізму підсилюють гіпоксію в тканинах і сприяють виникненню органної патології. Внаслідок дії хронічної гіпоксії відбувається активація процесів перекисного окислення ліпідів з утворенням проміжних кислих метаболітів, кетонових тіл, що призводить до посилення ацидозу [7–9, 11, 12].
У дітей, які перенесли хронічну внутрішньоутробну гіпоксію, спостерігається зниження білково-синтезуючої функції печінки, що призводить до зниження рівня альбуміну в сироватці крові. Як відомо, альбумін синтезується гепатоцитами печінки, тому визначення його рівня в сироватці крові є тестом функціонального стану печінки. Зв’язуюча здатність альбуміну залежить не лише від його кількості, але й від якості та ефективної концентрації альбуміну в сироватці крові. Фетальний альбумін відрізняється від альбуміну дорослого якісними та кількісними показниками. При зниженні рівня альбуміну в сироватці крові збільшується токсичність білірубіну, отже, токсичну властивість має не зв’язаний з альбуміном непрямий білірубін, змінюється стан мембран гепатоцитів, через що порушується адгезія білірубін-альбумінових комплексів. На концентрацію білка та його фракцій у крові новонароджених дітей суттєво впливає стан здоров’я матері під час вагітності. Доведено, що у дітей, які народилися від матерів, які мали пізні гестози, спостерігається гіпопротеїнемія та диспротеїнемія — гіпоальбумінемія та гіперглобулінемія (підвищена кількість α1-, α2-, β-глобулінів) [8, 9].
Мета роботи — дослідити особливості анамнезу, антропометричних даних та окремих функцій печінки у дітей із пролонгованою кон’югаційною жовтяницею.
Матеріали та методи
Під час дослідження обстежені 111 дітей з пролонгованою жовтяницею віком від 3 тижнів до 3 місяців. Умовою відбору дітей до групи спостереження була наявність непрямої гіпербілірубінемії, що виникла з 3–4-го дня від народження. Виключалися з групи дослідження діти з аномаліями розвитку, хворобою Дауна, аномалією жовчовивідних шляхів, гемолітичною хворобою, гіпотиреозом, пілоростенозом, різними інфекційними захворюваннями. У дослідження не включали також дітей, у матерів яких під час вагітності були виявлені носійство TORCH-інфекції та HbsAg. У всіх дітей групи спостереження був ретельно зібраний анамнез життя, захворювання, акушерсько-гінекологічний анамнез матері, проведені лабораторні (загальний аналіз крові, загальний аналіз сечі, біохімічний аналіз крові: визначення рівня загального білірубіну та фракцій, загального білка, альбуміну, глюкози) й інструментальні обстеження (ультразвукове дослідження органів черевної порожнини, нейросонографія головного мозку, електрокардіограма).
Після встановлення діагнозу «кон’югаційна жовтяниця з пролонгованим перебігом» усі діти отримували терапію згідно з протоколом лікування жовтяниці новонароджених МОЗ України [10]. Усі діти отримували фототерапію, сорбенти, гепатопротектори. Частині дітей (n = 65) додатково до фототерапії був доданий препарат левокарнітин у дозі по 100 мг 2 рази на день, курсом лікування 3 тижні. Ефективність терапії оцінювали на підставі динаміки змін основних клінічних симптомів жовтяниці: зменшення жовтяничного забарвлення шкіри та склер дитини шляхом оцінки за шкалою Крамера, покращення апетиту та загального стану дитини, дослідження в динаміці біохімічного аналізу крові — рівень загального білірубіну та його фракцій, загального білка, альбуміну, аспартатамінотрансферази й аланінамінотрансферази.
Результати та обговорення
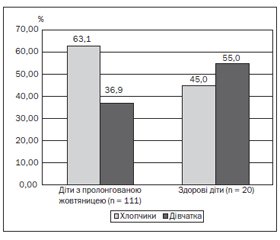
Усього було обстежено 111 дітей із пролонгованою неонатальною жовтяницею, серед них 70 хлопчиків (63,1 %) та 41 дівчинка (36,9 %), і 20 здорових дітей без жовтяниці, серед яких 9 хлопчиків (45 %) та 11 дівчаток (55 %). Дані наведені на рис. 1.
Новонароджені, залучені до дослідження, народилися в матерів у термін гестації від 35-го до 41-го тижня. Доношених новонароджених було 102 (91,9 %) дитини, недоношених — 9 (8,1 %). Отже в групах спостереження переважна більшість дітей були доношеними, між групами не було вірогідних відмінностей за цими ознаками (рис. 2).
Дослідження строку появи жовтяниці у новонароджених показало, що жовтяниця з’явилась на третю добу після народження у 82 (73,9 %) дітей, на четверту добу — у 29 (26,1 %) дітей. Переважна більшість дітей з пролонгованою жовтяницею (n = 90; 81,08 %) були на винятково грудному вигодовуванні, на змішаному — 16 (14,41 %) дітей, на штучному — 5 (4,5 %) дітей. У групі здорових дітей без жовтяниці 17 (85 %) були на виключно грудному вигодовуванні та 3 (15 %) дитини — на змішаному вигодовуванні. Отже, за типом харчування група дітей з пролонгованою жовтяницею статистично вірогідно не відрізнялась від групи здорових дітей.
Аналіз фізичного розвитку дітей на момент народження показав, що діти з пролонгованою жовтяницю статистично вірогідно не відрізнялись за показниками маси тіла, довжини тіла, окружністю голови та окружністю грудної клітки від групи здорових дітей. Серед дітей з пролонгованою жовтяницею у 50 % дітей маса тіла при народженні становила: Ме = 3440 г (Q1 = 3195; Q3 = 3680), середнє значення маси тіла — 3397,69 г (min = 1980, max = 4500). Серед здорових дітей у 50 % дітей маса тіла при народженні становила: Ме = 3485 г (Q1 = 3225; Q3 = 3610), середнє значення — 3450,75 г (min = 2750, max = 4140). Зріст при народженні серед дітей із затяжною жовтяницею у 50 % випадків був у межах: Ме = 52 см (Q1 = 51; Q3 = 54), середнє значення зросту — 52,26 см (min = 43, max = 57), серед здорових дітей зріст у 50 % дітей був 52,50 см (Q1 = 51,25; Q3 = 53,75), середнє значення — 52,45 см (min = 50, max = 56). Окружність голови при народженні у 50 % дітей із пролонгованою жовтяницею становила: Ме = 36 см (Q1 = 35; Q3 = 36), середнє значення — 35,45 см (min = 32, max = 37), серед здорових дітей: у 50 % Ме = 36 см (Q1 = 35; Q3 = 36), середнє значення — 35,55 см (min = 32, max = 37). Окружність грудної клітки при народження у 50 % дітей з пролонгованою жовтяницею знаходилась в межах: Ме = 35 см (Q1 = 34; Q3 = 35), середнє значення становило 34,42 см (min = 29, max = 37), а в групі здорових дітей: Ме = 35 см (Q1 = 34; Q3 = 35), середнє значення — 34,4 см (min = 30, max = 36). Отже, це дає можливість порівняти групу дітей із пролонгованою неонатально ю жовтяницею та групу здорових дітей і зробити висновок, що ці групи за основними показниками фізичного розвитку при народженні не мають статистично вірогідних відмінностей (р > 0,05).
При вивченні взаємозв’язку між розвитком затяжної кон’югаційної жовтяниці та послідовністю вагітності відзначено, що частіше жовтяниця мала затяжний перебіг у дітей, які народились від I вагітності — 60 (54,1 %); від II вагітності народились 27 (24,3 %) дітей; від III — 12 (10,8 %) дітей; від IV вагітності та більше — 12 (10,8 %) дітей.
За даними багатьох досліджень, супутня патологія матері та обтяжений акушерсько-гінекологічний анамнез впливають на виникнення та перебіг жовтяниці новонароджених. Щоб дослідити цей вплив, у всіх матерів дітей з груп дослідження був ретельно зібраний анамнез. Дослідження стану здоров’я матерів дітей обох груп спостереження показало, що здоровими були 43 (38,7 %) матері, з екстрагенітальною патологією було 68 (61,3 %) матерів.
При вивченні стану соматичного здоров’я матерів під час вагітності виявлено такий розподіл частоти та різноманітності супутньої патології матері: загроза переривання вагітності відзначена у 36 (32,4 %) матерів, анемія I–II ступеня — 33 (29,7 %), пієлонефрит і сечосольовий діатез — 20 (18 %), гестози — 9 (8,1 %); гостру респіраторну вірусну інфекцію під час вагітності мали 8 (7,2 %) матерів, прееклампсію — 2 (1,8 %).
Аналіз перебігу пологів матерів дітей із пролонгованою жовтяницею показав, що фізіологічні пологи спостерігались у 68 (61,3 %) матерів, пологи шляхом кесаревого розтину — у 25 (22,5 %), передчасні пологи були у 9 (8,1 %), слабкість пологової діяльності — у 5 (4,5 %), обвиття пуповиною під час пологів — у 7 (6,3 %) матерів.
За рівнем загального білірубіну в сироватці крові до початку лікування діти з пролонгованою жовтяницею були розподілені так: I група — до 100 мкмоль/л, II група — від 101 до 150 мкмоль/л, III група — від 151 до 200 мкмоль/л, IV група — від 201 до 250 мкмоль/л та V група — понад 251 мкмоль/л. Аналіз даного показника свідчив про те, що у дітей з пролонгованою неонатальною жовтяницею до початку лікування статистично вірогідно частіше рівень білірубіну знаходився в межах 101–150 мкмоль/л у 54 (48,6 %) дітей; рівень загального білірубіну — 151–200 мкмоль/л мали 26 (23,4 %) дітей; рівень загального білірубіну в сироватці крові до 100 мкмоль/л та 201–250 мкмоль/л мали однакова кількість дітей — 14 (12,6 %). Рівень загального білірубіну вище 251 мкмоль/л спостерігався лише у 3 (2,7 %) дітей.
Відомо, що трансферазні ферменти печінки — аланінамінотрансфераза (АлАТ) та аспартатамінотрансфераза (АсАТ) — є показниками ушкодження клітин печінки, їх рівень збільшується при цитолізі та внутрішньопечінковому холестазі. При вивченні цих показників виявлено, що рівень АлАТ у 50 % дітей був у межах: Ме = 35 Од/л (Q1 = 28 Од/л; Q3 = 42 Од/л). Рівень АсАТ у 50 % дітей був у межах: Ме = 28 Од/л (Q1 = 23,2 Од/л; Q3 = 32 Од/л). Отже, трансферазні ферменти печінки у дітей з пролонгованою жовтяницею знаходились на рівні верхньої межі вікової норми.
Печінка виконує білково-синтетичну функцію, зокрема, в ній утворюються фібриноген, альбуміни, протромбін. Ця функція печінки оцінюється завдяки визначенню кількості різних білків та їх фракцій у сироватці крові, рівня загального білка, фібриногену та альбуміну. При дифузних ушкодженнях печінки спостерігається гіпопротеїнемія переважно внаслідок зниження концентрації альбумінів у сироватці крові. Наші дані показали, що медіана рівня загального білка у дітей з пролонгованою жовтяницею до початку лікування становила: Ме = 52,3 г/л (Q1 = 51 г/л; Q3 = 55 г/л); рівень альбуміну в сироватці крові у дітей з жовтяницею до початку лікування був у межах: Ме = 37,9 г/л (Q1 = 36,8 г/л; Q3 = 40,2 г/л). Отже, в обстежуваних нами дітей з пролонгованою жовтяницею до початку лікування спостерігали статистично вірогідну гіпопротеїнемію та гіпоальбумінемію. Рівень альбуміну до лікування мав сильний зворотний кореляційний зв’язок із рівнем загального білірубіну до початку лікування (р < 0,01) та кореляційний зв’язок середньої сили виявлено між рівнем непрямого білірубіну до лікування та альбуміном у сироватці крові до лікування (р < 0,05). Відзначено, що чим вищим був рівень загального білірубіну та непрямого білірубіну, тим нижчим був рівень альбуміну крові, що свідчить про зниження білково-синтезуючої функції печінки при пролонгованому перебігу неонатальної жовтяниці. Вивчення рівня глюкози в крові обстежуваних дітей показало, що рівень глюкози знаходився в межах: Ме = 3,8 ммоль/л (Q1 = 3,4 ммоль/л; Q3 = 4,1 ммоль/л) та відповідав віковій нормі.
Висновки
Переважна більшість дітей із пролонгованою жовтяницею народилися доношеними та були на винятково грудному вигодовуванні.
Показники фізичного розвитку при народженні (маса тіла, довжина тіла, окружність голови, окружність грудної клітки) у дітей із пролонгованою жовтяницею та у здорових дітей не мали статистично вірогідних відмінностей.
У дітей, які народились від I вагітності (n = 60; 54,1 %), жовтяниця найчастіше мала затяжний перебіг.
Серед матерів дітей із пролонгованою жовтяницею загроза переривання вагітності спостерігалась у 36 (32,4 %) матерів, анемія I–II ступеня — 33 (29,7 %), у той час як у матерів дітей, які не мали пролонгованої жовтяниці, загроза переривання вагітності спостерігалась у 5 (25 %), анемія — у 6 (30 %) матерів.
Рівень загального білірубіну серед дітей із пролонгованою неонатальною жовтяницею до початку лікування дорівнював 101–150 мкмоль/л у 54 (48,6 %) дітей.
Вищий рівень загального та непрямого білірубіну у дітей із пролонгованою жовтяницею супроводжувався нижчим рівнем альбуміну в сироватці крові, що свідчить про зниження білково-синтезуючої функції печінки при пролонгованому перебігу жовтяниці.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.

/75.jpg)