Резюме
Мета роботи — встановити можливі причини неефективності алергенспецифічної імунотерапії (АСІТ) пилковими алергенами (бур’янів) у дітей із сезонним алергічним ринітом і/або бронхіальною астмою на підставі вивчення гіперчутливості до алергенів, аналізу анамнестичних даних. Матеріали та методи. Проведено алерготестування 192 дітей. 52 пацієнтам проведене анамнестичне опитування з акцентом на перехресну алергію та супутню патологію верхніх дихальних шляхів, а також на ефективність АСІТ. Статистична обробка результатів проведена в програмі Statistica for Windows 6.0. Результати. Серед хворих на поліноз переважала гіперчутливість до амброзії (56 %), циклахени (46 %) та соняшника (58 %). До злакових рослин (райграс, грястиця, вівсяниця) чутливі 10—20 % пацієнтів. 23 % дітей мають сенсибілізацію до 5 та більше алергенів (в середньому до 3,3 ± 0,4). 52 % дітей мають супутню харчову алергію, 15 % — синдром оральної алергії, третина дітей — аденоїдні вегетації, гіпертрофію глоткових мигдалин, у 13 % алергічний риніт ускладнювався синуситом. Незадовільний клінічний ефект АСІТ пилковими алергенами асоціювався з наявністю поєднаної пилково-грибкової сенсибілізації, перехресної харчової та пилкової алергії, із сенсибілізацією до 4 та більше пилкових алергенів, з полівалентною алергією, а також спостерігався при поєднанні алергічного риніту із синуситом (р < 0,05). Висновки. Перед початком АСІТ дітям із полінозами необхідно визначити групу ризику стосовно можливої неефективності цього методу терапії та рекомендувати їм визначення специфічних імуноглобулінів класу Е до мажорних та мінорних алергенів для прогнозування ефективності АСІТ.
Цель работы — установить возможные причины неэффективности аллергенспецифической иммунотерапии (АСИТ) пыльцевыми аллергенами у детей с сезонным аллергическим ринитом и/или бронхиальной астмой на основании изучения гиперчувствительности к аллергенам, анализа анамнестических данных. Материалы и методы. Проведено аллерготестирование 192 детей. 52 пациентам проведен анамнестических опрос с акцентом на перекрестную аллергию и сопутствующую патологию верхних дыхательных путей, а также эффективность АСИТ. Статистическая обработка результатов проведена в программе Statisticа for Windows 6.0. Результаты. Среди больных поллинозом преобладала повышенная чувствительность к амброзии (56 %), циклахене (46 %) и подсолнечнику (58 %). К злаковым (райграс, ежа, овсяница) чувствительны 10–20 % пациентов. 23 % детей имеют сенсибилизацию к 5 и больше аллергенам (в среднем к 3,3 ± 0,4). 52 % детей имеют сопутствующую пищевую аллергию, 15 % — синдром оральной аллергии, треть детей — аденоидные вегетации, гипертрофию глоточной миндалины, у 13 % аллергический ринит осложнялся синуситом. Неудовлетворительный клинический эффект АСИТ пыльцевыми аллергенами ассоциировался с наличием сочетанной пыльцово-грибковой сенсибилизации, перекрестной пищевой и пыльцевой аллергии, с сенсибилизацией к 4 и более пыльцевым аллергенам, с поливалентной аллергией, а также наблюдался при сочетании аллергического ринита с синуситом (р < 0,05). Выводы. Перед началом АСИТ детям с поллинозами необходимо определить группу риска возможной неэффективности этого метода терапии и рекомендовать им определение специфических иммуноглобулинов класса Е к мажорным и минорным аллергенам для прогнозирования эффективности АСИТ.
Background. Allergen-specific immunotherapy as elimination procedures is the only method of treatment and prevention of allergic disorders formation and exacerbation of clinical symptoms. One of the approaches to molecular diagnosis is choice of allergen for allergen-specific immunotherapy (ASIT). The purpose of our study was to identify possible reasons of failure of ASIT with pollen allergens (predominantly weeds) in children with seasonal allergic rhinitis (hay fever) and/or bronchial asthma based on studying hypersensitivity to the allergens, analysis of anamnestic data. Materials and methods. Allergy skin prick tests were conducted to 192 children (middle age 9.8 ± 2.7 years) with the seasonal symptoms of rhinitis and/or bronchial asthma according to standard methodology with pollen allergens of Immunolog Ltd (Vinnytsia). We evaluated positive results as 5 mm and higher diameter of papula/hyperemia. The anamnestic survey was carried out in 52 patients by means of the questionnaire that contained questions about cross allergy (pollen-food, oral allergy syndrome), concomitant pathology of upper respiratory tract and effectiveness of АSІТ, which is elaborated by us. Results. The skin prick tests show that in 192 patients, who have hay fever, ragweed, sunflower sensibilization predominates (56 and 58 %, correspondingly). About 10–20 % of children are sensitive to cereals (ryegrass, fescue). To the allergens of poplar, acacia, couch-grass, oak, mint, nettle, walnut, the positive reactions of prick tests were observed in 3–7 children, that is 1.5–3.6 %. According to our results, 23 % of patients had sensibilization to 5 and more pollen allergens. 52 % of children had concomitant food allergy, 15 % of patients have reactions of the lips, oral cavity when using certain products, mostly tomatoes, nuts, seeds (they were diagnosed oral allergy syndrome). Also, one third of children have varying degrees of adenoid hypertrophy, tonsils hypertrophy, allergic rhinitis is complicated by sinusitis in 13 % of cases. Children received 3 to 4 courses of preseason subcutaneous ASIT (December to May) according to classic scheme. The vast majority of children got mixed extracts of ragweed, cyclachaena, mugwort, quinoa, sunflower (90 %). One allergen (ragweed or sunflower) has been used only in 6 children (10 %). We detected that 1/5 children had no clinical effect, the symptoms of hay fever were not diminished or changed their temporal frames. 82 % of patients without effect of ASIT had cross plant-food allergy (oral allergy syndrome). Conclusion. Before the beginning of АSІТ in children with hay fever, the doctor must define a high-risk group in relation to its possible ineffectiveness. We suggest taking into account children with sensitization to 4 and more pollen allergens, with the presence of oral allergic syndrome, concomitant pathology of ENT organs, in particular, adenoid hypertrophy, chronic sinusitis. Such children are recommended to make a profile of molecular allergy diagnostics to determine the specific immunoglobulines Е to the major and minor allergens. Component resolved molecular allergy diagnostics maybe also helpful in estimation the risk of systemic (anaphylactic) reactions in children with cross reactivity (pollen-food allergy) and in improvement of preventive measures, in particular, in patients with oral allergy syndrome.
Вступ
Згідно з Постановою Європейської асоціації алергологів та клінічних імунологів ЕААСІ (2011 рік), поряд із елімінаційними заходами (уникненням контакту з алергеном) застосовується етіопатогенетичний захід лікування та профілактики алергічних захворювань — алергенспецифічна імунотерапія (АСІТ) [7]. При цьому саме АСІТ є методом медичного втручання, що може потенційно впливати на природний перебіг захворювання; запобігати прогресуванню алергічних хвороб, наприклад приєднанню бронхіальної астми до симптоматики алергічного риніту (АР). За результатами лонгітудинальних досліджень, АСІТ не лише ефективно полегшує симптоми алергії, а й забезпечує тривалу дію після завершення лікування. Під впливом АСІТ спостерігається зміна співвідношення Т-хелперів у бік активації Т-клітин 1-го типу та пригнічення Т-хелперів 2-го типу, зниження продукції ІЛ-4, підвищення рівнів ІЛ-10, ІЛ-12, гамма-інтерферону. Індукція регуляторних Т-клітин та формування периферичної Т-клітинної імунологічної толерантності є основними механізмами АСІТ. FOXP3+CD4+CD25+ регуляторні та IL-10 і TGF-β-продукуючі клітини 1-го типу Treg (TR1) можуть запобігати розвитку алергічних захворювань і відіграють важливу роль у досягненні ефективності АСІТ [1, 2, 6, 10].
Julia M. Kim та співавтори у 2013 році провели систематичний метааналіз 13 рандомізованих клінічних досліджень з ефективності підшкірної АСІТ, 18 рандомізованих клінічних досліджень з ефективності сублінгвальної імунотерапії та трьох робіт, присвячених порівнянню цих двох методів введення алергену для АСІТ. Виявилось, що доказова база є сильнішою для сублінгвальної АСІТ. Однак обидва методи ефективні в зниженні клінічної симптоматики риніту та астми (рівень доказовості А), менше впливають на очні симптоми, використання препаратів базисної терапії астми та якість життя при симптомах риніту (рівень доказовості В та С) [8].
Первинна ціль АСІТ полягає насамперед у редукції клінічної симптоматики алергії. P.M. Matricardi (2011) та колеги провели огляд досліджень з оцінки ефективності підшкірної АСІТ у дітей із сезонним алергічним ринітом. Було показано, що вже протягом першого сезону палінації пацієнти, які отримували АСІТ, відмічали зменшення вираженості симптоматики полінозу та/або спостерігали зниження потреби у фармакотерапії (ранній вплив АСІТ на клінічну симптоматику) [11]. Це стосувалося навіть тяжкого риніту, що впливав на якість життя хворих. При цьому якщо пацієнти мали сенсибілізацію до інших алергенів, окрім пилкових, ефективність АСІТ у них не була нижчою. Імунотерапія алергенами має декілька рівнів ефективності згідно з рекомендаціями Європейської організації ліків (The European Medicines Agency) у протоколі щодо розробки продуктів для АСІТ Guideline on the clinical development of products for specific immunotherapy for the treatment of allergic diseases. Вище описаний первинний ефект. Подальший ефект АСІТ полягає в покращенні симптоматики/потреби в медикаментах + зниженні шкірної гіперчутливості та симптомів пізньої фази алергічної реакції; персистуючий ефект — вищеописані ефекти відмічаються після завершення лікування; превентивний ефект АСІТ проявляється в запобіганні приєднанню інших видів сенсибілізації [9].
Для підбору алергену для проведення АСІТ необхідно точно ідентифікувати алерген, що провокує клінічні симптоми. XXI століття ознаменувалося розвитком молекулярної алергодіагностики, відкриттям мажорних та мінорних алергенів, паналергенів, що зумовлюють перехресні реакції між спорідненими видами рослин та/або харчових продуктів. Пацієнти, які мають позитивні результати прик-тестів із багатьма пилковими алергенами, можливо, мають сенсибілізацію до паналергенів або мінорних алергенів. Показано, що використання методів молекулярної діагностики змушує змінити АСІТ, підібрану за результатами шкірних прик-тестів, більше ніж в 50 % випадків, а отже, у групі пацієнтів з полівалентною сенсибілізацією висока ймовірність неправильного призначення АСІТ. Наприклад, АСІТ амброзійним алергеном буде ефективною при наявності сенсибілізації до головного алергену Amb a 1, Amb a 3 та неефективною при сенсибілізації до мінорних алергенів Amb a 6 (ліпідтранспортуючий білок, гомологічний алергену полину Art a 3), Amb a 8 (профілін), Amb a 9 та 10 (полькальцин) (http://fooke.ru/production/molekulyarnaya-allergodiagnostika. html) [5, 12, 13].
На сьогодні алергологи в Україні використовують як підшкірний метод введення алергену (переважно в умовах стаціонару), так і сублінгвальний та пероральний, що мають перевагу серед пацієнтів завдяки неінвазивності, безболісності та можливості отримувати лікування в домашніх умовах. У м. Запоріжжі в обласному алергологічному відділенні КУ «Запорізька міська багатопрофільна дитяча лікарня» проводиться підшкірна АСІТ пилковими, кліщовими алергенами. У ході підшкірної АСІТ рослинними алергенами зсув у бік Th1-хелперів та підвищення рівня інтерферону альфа спостерігалися після 12 місяців лікування (кінцевими точками також були 3, 6, 9 місяців). За даними літератури, найбільш високий ефект АСІТ досягається при полінозі й становить 80–90 %. Однак, згідно з нашими спостереженнями, близько 15–20 % дітей, хворих на поліноз, та їх батьків відмічають незадовільний ефект від АСІТ пилковими алергенами [3, 4].
Тому метою нашої роботи було встановити можливі причини неефективності АСІТ пилковими алергенами (бур’янів) у дітей із сезонним алергічним ринітом та/або бронхіальною астмою на підставі вивчення гіперчутливості до алергенів, аналізу анамнестичних даних.
Матеріали та методи
Проведено алерготестування 192 дітей (середній вік 9,8 ± 2,7 року), хворих на сезонні прояви алергічного риніту та/або бронхіальної астми, прик-методом за стандартною методикою пилковими алергенами ТОВ «Імунолог» (м. Вінниця). За позитивний результат вважали діаметр папули/гіперемії 5 мм та більше. 52 пацієнтам проведене анамнестичне опитування за допомогою розробленої нами анкети, що містила питання стосовно перехресної алергії (пилково-харчової, синдрому оральної алергії), супутньої патології верхніх дихальних шляхів, а також щодо ефективності АСІТ. Статистична обробка результатів проведена в програмі Statisticа for Windows 6.0 із використанням описової статистики, кореляційного аналізу (коефіцієнту рангової кореляції Спірмана).
Результати
При аналізі результатів алерготестування 192 пацієнтів, хворих на поліноз, було виявлено, що переважала гіперчутливість до амброзії, циклахени та соняшника. До злакових рослин (райграс, грястиця, вівсяниця) чутливі 10–20 % пацієнтів (табл. 1).
До алергенів тополі, акації, пирію, тимофіївки, дубу, м’яти, кропиви, волоського горіху позитивні реакції прик-тестів спостерігалися у 3–7 дітей, що становило 1,5–3,6 %.
Цікаво, що 23 % дітей мають сенсибілізацію до 5 та більше алергенів рослин (табл. 2). У середньому діти із сезонною алергією чутливі до 3,3 ± 0,4 пилкового алергену.
За результатами опитування та анкетування 52 % дітей мають супутню харчову алергію, 15 % пацієнтів відмічають реакції губ, ротової порожнини (у вигляді свербіння, короткочасної гіперемії та висипу) при вживанні певних продуктів, найчастіше томатів, горіхів, насіння (синдром оральної алергії). Також третина дітей мають різного ступеня тяжкості аденоїдні вегетації, гіпертрофію глоткових мигдалин, у 13 % АР ускладнювався синуситом.
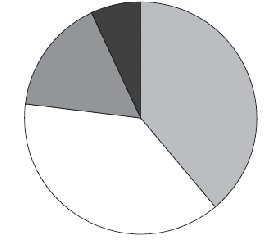
Опитані діти отримали від 3 до 4 курсів передсезонної АСІТ (з грудня по квітень — травень) підшкірним методом алергенами бур’янів. Абсолютній більшості дітей АСІТ проводили декількома алергенами у формі міксту: амброзія, циклахена, полин, лобода, соняшник. АСІТ 1 алергеном (амброзія або соняшник) отримувало лише 6 дітей (10 %).
Алергени для проведення АСІТ для кожного пацієнта були обрані за результатами прик-тестів у взаємозв’язку з клінікою сезонних проявів алергії та концентрацією загального IgE, рідше — специфічного IgE до бур’янистих рослин. Виявилося, що 1/5 дітей відзначали відсутність клінічного ефекту, симптоми полінозу в них зберігалися або змінювали свої часові рамки. При цьому у 82 % з них спостерігалася наявність перехресної пилково-рослинної алергії. За результатами аналізу таблиць спряженості незадовільний клінічний ефект АСІТ пилковими алергенами асоціювався з наявністю поєднаної пилково-грибкової сенсибілізації, перехресною харчовою та пилковою алергією, сенсибілізацією до 4 та більше пилкових алергенів, спостерігався частіше при поєднанні АР із синуситом, а також за наявності в дитини полівалентної алергії (р < 0,05).
Вважаємо, що становитиме інтерес клінічний випадок анафілактичного шоку (АШ) у дівчинки Т., 17 років, в аспекті перехресної алергії.
Пацієнтка була доставлена бригадою швидкої допомоги у відділення реанімації та невідкладної терапії КУ «Запорізька міська багатопрофільна дитяча лікарня № 5» о 21:15 зі скаргами на незначне запаморочення, оніміння нижньої губи та язика, утруднене дихання через ніс. З анамнезу відомо, що через кілька хвилин після вживання халви приблизно о 20:15 пацієнтка відчула оніміння нижньої губи та язика, з’явилися неприємні відчуття за грудиною, утруднення носового дихання. Через 10 хвилин відмічалися приливи жару, набряк обличчя, вух, генералізована висипка за типом кропив’янки, запаморочення, короткочасно втратила свідомість. Мати зробила внутрішньом’язово ін’єкцію дексаметазону 4 мг та відразу викликала швидку медичну допомогу, що приїхала через 10 хвилин. При вимірюванні артеріальний тиск становив 80/50 мм рт.ст. Були введені адреналін, дексаметазон, дівчинка госпіталізована. Раніше дівчинка мала неприємні відчуття набряку язика та губ після вживанні насіння соняшника та арахісу. Також має сильну місцеву реакцію при укусах комарів. З 15 років страждає від полінозу, переважно в травні та серпні. Мати дівчинки хвора на сезонний алергічний риніт.
При об’єктивному обстеженні в умовах відділення невідкладної допомоги стан пацієнтки стабільний, артеріальний тиск 115/70 мм рт.ст. Шкіра блідо-рожева, достатньої вологості, незначний набряк верхніх повік, одиничні уртикарні елементи на тулубі. Над легенями перкуторно ясний легеневий звук, хрипи не вислуховуються. Тони серця ритмічні, шумів немає, частота серцевих скорочень 90/хв. Живіт м’який, при пальпації безболісний.
У сироватці спостерігається підвищення рівня загального IgE, триптази, специфічних IgE до соняшника, амброзії (табл. 2). При цьому до мажорних алергенів амброзії та берези пацієнтка не сенсибілізована. Повний профіль компонентної алергодіагностики –дівчинка не пройшла з матеріальних причин.
Обговорення
Переважна сенсибілізація до пилкових алергенів у м. Запоріжжя підтверджує невщухаючий інтерес до проблеми сезонної алергії. На сучасному етапі розвитку наукових знань технології молекулярної алергодіагностики стають невід’ємною частиною клінічної практики. Особливо актуальні вони при виборі алергену для АСІТ та пошуку відмінностей істинної сенсибілізації від перехресної внаслідок сенсибілізації до мінорних алергенів та полівалентної алергії.
Згідно з результатами нашої роботи, близько 20 % пацієнтів, які отримували АСІТ пилковими алергенами, відмітили недостатній ефект або його відсутність взагалі. Ми помітили, що ці діти переважно мали гіперчутливість до 4 та більше алергенів, які були включені до міксту смітникових трав для проведення АСІТ. Можливо, ці діти мають сенсибілізацію до мінорних алергенів, що зумовило позитивні результати алергопроб до кількох бур’янистих трав, а справжня сенсибілізація присутня тільки до алергенів амброзії, які перехресно реагують з іншими бур’янами, соняшником, березою. Але, як видно з рис. 2, 90 % пацієнтів отримували АСІТ мікстами бур’янів та лише 10 % — моноалергеном.
/62-1.gif)
Харчові алергени горіхів (насамперед арахісу) належать до термостабільних алергенів, що зберігають свої алергенні властивості в шлунково-кишковому тракті під впливом кислот. У дівчини з вищенаведеним прикладом АШ спостерігається сенсибілізація до головних алергенів горіхів, що належать до ліпід-транспортуючих або запасних білків (lipid-transferproteins, storageproteins) (табл. 3).
У пацієнтки є справжня алергія до термостабільних алергенів арахісу й насіння соняшника, що належать до групи неспецифічних білків-переносників ліпідів і запасних білків. Вдруге розвинулася пилкова алергія на зразок «насіння соняшника — соняшник-амброзія». Тому дана дитина належить до групи високого ризику виникнення тяжких алергічних реакцій, і проведення АСІТ їй не показане.
Використання компонентної алергодіагностики, на жаль, обмежується фінансовими можливостями пацієнта, тому практикуючому лікареві необхідно проаналізувати індивідуальний профіль шкірної сенсибілізації та клінічну симптоматику кожного пацієнта й виділити дітей, яким показана молекулярна алергодіагностика, з метою удосконалення лікування та профілактики алергії.
Висновки
Перед початком АСІТ дітям із полінозами необхідно визначити групу ризику стосовно можливої неефективності цього методу терапії. До неї слід віднести дітей із сенсибілізацією до 4 та більше пилкових алергенів, наявністю орального алергічного синдрому, супутньою патологією лор-органів, зокрема аденоїдними вегетаціями, хронічним синуситом. Таким дітям рекомендоване визначення специфічних імуноглобулінів класу Е до мажорних та мінорних алергенів. За допомогою молекулярної діагностики також можливо оцінити ризик виникнення системних (анафілактичних) реакцій у дітей із перехресною харчовою алергією та покращити профілактичні заходи, зокрема, у пацієнтів із оральним алергічним синдромом.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Аллерген-специфическая иммунотерапия у детей с поллинозом / Р.М. Торшхоева, Л.С. Намазова-Баранова, О.И. Мурадова // Вопросы современной педиатрии. — 2014. — Т. 13, № 1. — С. 155-161.
2. Балаболкин И.И. Аллерген-специфическая иммунотерапия детей с аллергическими заболеваниями / И. И. Балаболкин // Фарматека. — 2014. — № 4. — С. 22-26.
3. Беш О.М. Алерген-специфічна імунотерапія та її місце в лікуванні бронхіальної астми: сучасний стан проблеми / О.М. Беш, О.М. Радченко // Експериментальна та клінічна фізіологія і біохімія. — 2014. — № 3. — С. 77-85.
4. Гришило П.В. Алерген-специфічна імунотерапія: стандартні підходи та сучасні погляди // Клінічна імунологія, алергологія, інфектологія. — 2011. — № 6–7 (45–46). — С. 25-28.
5. Консенсус WAO-ARIA-GA2 LEN по молекулярной диагностике аллергии / G. Walter Canonica, Ignacio J. Ansotegui, Ruby Pawankar // Аллергология, иммунология. — 2014. — Т. 15, № 1. — С. 6-15.
6. Корицька І.В. Алерген-специфічна імунотерапія: сучасні рекомендації та практичні аспекти / І.В. Корицька // Клінічна імунологія, алергологія, інсектологія. — 2012. — № 58 (9). — С. 15-18.
7. Allergen immunotherapy: A practice parameter third update / L. Cox, H. Nelson, R. Lockey [et al.] // Journal of allergy and clinical immunology. — 2011. — Vol. 127(1). — P. 289-331.
8. Allergen-Specific Immunotherapy for Pediatric Asthma and Rhinoconjunctivitis: A Systematic Review / Julia M. Kim, Sandra Y. Lin, Catalina Suarez-Cuervo [et al.] // Pediatrics. — 2013. — Vol. 131(6). — P. 1155-1167.
9. Committee for Medicinal Products for Human Use. Guideline on the Clinical Development of Products for Specific Immunotherapy for the Treatment of Allergic Diseases. European Medicines Agency. 2008. — http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2009/09/WC500003605.pdf
10. Mechanisms of allergen-specific immunotherapy / Hiroyuki Fujita, Michael B. Soyka, Mübeccel Akdis [et al.] // Clinical and Translational Allergy. — 2012. — Vol. 2. — P. 22-28.
11. Subcutaneous immunotherapy and pharmacotherapy in seasonal allergic rhinitis: A comparison based on meta-analyses / Matricardi P.M., Kuna P., Panetta V. [et al.] // J. Allergy ClinImmunol. — 2011. — Vol. 128. — P. 791-799.
12. Vaccine development for allergen-specific immunotherapy based on recombinant allergens and synthetic allergen peptides: Lessons from the past and novel mechanisms of action for the future / R. Valenta, R. Campana, M. Focke-Tejkl // Journal of Allergy and Clinical Immunology. — 2016. — Vol. 137, Issue 2. — P. 351-357.
13. Zeinab A. El-Sayed Allergen-specific immunotherapy in children / Zeinab A. El-Sayed, Ola G. El-Farghali // Egypt J. Pediatr. Allergy Immunology. — 2012. — Vol. 10(2). — P. 55-67.

/61-1.gif)
/62-1.gif)
/63-1.gif)