Вступ
Хвороби органів травлення надійно посіли провідне місце в загальній структурі захворювань у дітей, причому серед хронічних захворювань вони, безсумнівно, утримують першість [1, 2]. Цифри досить красномовні: близько 1 млн дітей в Україні страждають від хвороб травної системи. До 75 % у структурі захворювань органів травлення в дітей припадає на патологію верхніх відділів травної системи — гастродуоденальної зони (ГДЗ). Причини такого поширення патології саме верхніх відділів травного каналу численні й різноманітні [1, 3]. Деякий час вважали, що основним чинником, який сприяє розвитку гастродуоденальної патології, є порушення балансу факторів агресії (перш за все мова йде про секрецію соляної кислоти й пепсину) та факторів захисту слизових оболонок шлунково-кишкового тракту (найбільш значущою в даному випадку є роль слизово-бікарбонатного бар’єра, повноцінного кровопостачання, регенерації епітелію, імунного захисту та простагландинів, що забезпечують захист слизових від пошкодження). Серед численних факторів, що призводять до розвитку хронічних захворювань верхнього відділу травного тракту, одним з основних у даний час вважається інфекційний, асоційований із Helicobacter pylori (Hp) [4–6]. Останніми роками ми спостерігаємо значне омолодження гастродуоденальної патології в дітей, збільшення частоти деструктивних, атрофічних процесів із несприятливим, часто рецидивуючим перебігом, ускладненнями, швидким прогресуванням морфологічних змін. Багато дослідників пов’язують ці процеси саме з патогенністю Hp [4, 6, 7]. Різноманітні шляхи передачі, вплив соціально-побутових і матеріальних факторів, сімейний характер інфікування дозволяють розглядати хелікобактеріоз як інфекційне захворювання, що набуває характеру епідемії. Хелікобактерна інфекція є причиною гастритів у 50–96 % випадків, виразкова хвороба (ВХ) шлунка та дванадцятипалої кишки обумов-
лена хелікобактеріозом у 70–100 %, а розвиток карциноми шлунка і В-клітинної лімфоми шлунка пов’язаний із Нр в 70–80 % випадків. Однак дана статистика справедлива в основному для країн із низьким рівнем соціально-економічного розвитку (у тому числі, на жаль, і країн Східної Європи), тоді як у країнах Західної Європи, Північної Америки, де інфікованість населення Нр істотно (більше ніж у 2 рази) нижча, до 30–40 % дуоденальних виразок і 40–50 % шлункових виразок є Нр-негативними, причому різке зниження поширеності Нр-інфекції більш виражене серед дітей, ніж серед дорослих. Багаторічні дослідження, проведені в нашій країні, свідчать про те, що останніми роками змінилися частота і структура Hp-асоційованих форм захворювань дитячого населення України [3, 8]. Так, у дітей віком до 10 років, які страждають від захворювань ГДЗ, Hp-позитивні варіанти патології виявляються в 56–58 % випадків. У пацієнтів старшої вікової групи цей показник становить 67–75 %. Інфікованість дітей вірогідно збільшується з наростанням тяжкості процесу й тривалості захворювання, однак загальні цифри Hp-позитивних форм у зіставленні з аналогічними показниками 7–10-літньої давнини виявилися нижчими. При поверхневих змінах слизової оболонки шлунка й дванадцятипалої кишки (ДПК) (еритематозна гастродуоденопатія) Hp виявляється в 52–54 % випадків, причому ступінь обсіменіння Hp невисокий; при нодулярних формах Hp-позитивні — 57–64 %, переважно середнього і високого ступеня обсіменіння; при ерозивних гастродуоденітах Hp-позитивні форми зустрічаються в 71–82 % дітей, в основному високого ступеня інфікування; при виразковій хворобі Нp-асоційовані форми становлять 82–89 %. Причому необхідно відзначити, що при повторних рецидивах ерозивно-виразкових процесів відсоток Hp-позитивних форм ще більше знижується. Так, при виразковій хворобі ДПК повторні загострення лише в 54–57 % випадків були асоційовані з Hp [2, 8]. Подібні тенденції відзначають і багато інших дослідників проблем хелікобактеріозу в педіатрії [4, 6, 9].
Метою лікування хелікобактерної інфекції є повна ерадикація мікроорганізму (як вегетативної, так і кокової форми в шлунку та ДПК), що супроводжується незначною частотою реінфекції. Тимчасова відсутність мікроорганізму відразу після лікування називається кліренсом пригнічення. Про успішну ерадикацію можна говорити при наявності двох негативних результатів різних діагностичних тестів, виконаних не раніше ніж через 4–6 тижнів після закінчення терапії.
Протягом останніх років питання використання препаратів у схемах ерадикаційної терапії, їх обґрунтування, оптимізація термінів призначення та доз постійно перебувають в центрі уваги фахівців, переглядаються та доповнюються (Маастрихтські консенсуси: І — 1996 р., ІІ — 2000 р., ІІІ — 2005 р., IV — 2010 р., V — 1015 р.) [7, 10]. Відомі в даний час погоджувальні документи з діагностики й лікування в дорослих пацієнтів (Maastricht IV/V Florence Consensus Report Європейської групи з вивчення Helicobacter pylori й рекомендації American College of Gastroenterology) [5, 7, 10] не можуть механічно переноситись на існуючі реалії і повною мірою використовуватись у педіатричній практиці. Причиною цього є і різна частота інфікованості Нр у дитячій і дорослій популяціях і різниця в існуючих нозологіях і частоті атрофічних гастритів і малігнізації, а також у відповіді на ерадикаційну терапію (зокрема, велика частота антибіотикорезистентності в дитячій популяції порівняно з дорослою до основних препаратів антихелікобактерної терапії (АХТ) першої лінії — метронідазолу й кларитроміцину). На сьогодні обов’язковими компонентами сучасних ерадикаційних схем терапії є інгібітори протонної помпи (ІПП) і/або препарати вісмуту (Ві) й не менше від двох антибактеріальних препаратів [6, 7, 10].
Відповідно до Маастрихтських консенсусів (IV — 2010 р.; V — 2015 р. ) режим антихелікобактерної терапії повинен формуватися згідно з критеріями доказової медицини, а саме враховувати рівень доказовості й ступінь рекомендацій, прийнятих експертами за всіма пунктами угоди [7, 10].
Згідно з останніми погоджувальними документам, у тому числі Маастрихтського угодою (IV, 2010 р.), ІПП рекомендуються як основний засіб для лікування як кислотозалежних захворювань, так і Нр-інфекції. З урахуванням зростання резистентності до основних препаратів антихелікобактерної терапії першої лінії (метронідазол, кларитроміцин) ряд схем ерадикаційної терапії був модифікований шляхом включення в них препаратів, що так само відзначаються антихелікобактерною активністю, — нітрофуранів (зокрема, ніфурателу, що на сьогодні є найбільш вивченим для використання в схемах ерадикації Нр). Можливість застосування нітрофуранових препаратів не є новиною для педіатрів — уже тривалий час препарати цієї групи широко використовуються в ерадикаційних схемах терапії першої лінії разом з препаратами вісмуту (ESPGHAN). Включення в схему ерадикації препаратів вісмуту підвищує ефективність антихелікобактерної терапії на 20 %. Так, комбінація «колоїдний субцитрат вісмуту + ніфурател + амоксицилін» приводила до ерадикації Hp у 92 % випадків, комбінація «омепразол + амоксицилін + ніфурател + колоїдний субцитрат вісмуту» — в 98,2 %, а використання комбінації «колоїдний субцитрат вісмуту + рабепразол + ніфурател + амоксицилін» забезпечувало практично 100% ерадикацію. Крім того, при призначенні ніфурателу спостерігається високий комплаєнс [6, 7, 11].
Тему Hp-асоційованих захворювань поки ще рано вважати закритою. У цій галузі ще залишається багато питань та проблем. До таких спірних пунктів відносять схеми ерадикації, багато з яких при високій ефективності погано переносяться, викликають численні побічні ефекти від гіркоти в роті до розвитку дисбіозу кишечника, медикаментозного гепатиту, пліснявки тощо. Останні дослідження продемонстрували, що прогресуючі процеси атрофії слизової оболонки шлунка, пов’язані зі зміною його кислотопродукуючої функції, здатні впливати на ступінь диверсифікації шлункової мікробіоти та її кількісний склад, а тривале застосування ІПП може негативно впливати на стан шлункової й кишкової мікробіоти [4, 12, 13]. Крім того, зростає кількість антибіотикорезистентних штамів Hp, що обмежує поширення й використання антихелікобактерної терапії. Саме тому в усьому світі проводять-ся пошук, розробка та випробування нових схем ерадикаційної терапії, у яких перелічені недоліки зводилися б до мінімуму. На сьогодні міжнародними консенсусами визначені чіткі вимоги до схем ерадикаційної терапії: вони повинні бути ефективними, безпечними, забезпечувати добрий комплаєнс (рівень ерадикації повинен бути не нижчим за 80 %; схема не повинна викликати вимушеної відміни терапії внаслідок побічних ефектів (допустимі менше ніж 5 %); схема повинна бути ефективною при тривалості курсу не більше ніж 7–14 днів) [6, 7, 10].
Однак, враховуючи особливості дитячого організму, перебігу основних нозологічних форм, асоційованих з Hp-інфекцією у дітей, вікові обмеження та протипоказання для застосування тих чи інших препаратів в ерадикаційних схемах, після кожного міжнародного консенсусу з хелікобактеріозу у світі приймались уточнення та роз’яснення Європейської педіатричної групи з вивчення Hp (ESPGHAN) щодо лікування дітей з Hp-асоційованими захворюваннями. Тому особливо наголошуємо: неможливо використовувати дорослі схеми ерадикаційної терапії в дітей, тому що вони не адаптовані для використання в дитячому віці, а призначати слід тільки ті схеми, що рекомендовані педіатричними групами з вивчення Hp, бажано з урахуванням регіональних особливостей резистентності до препаратів [3, 6, 11]. Уточнення показань щодо проведення ерадикаційної анти-Нp-терапії в дитячому віці (на основі міжнародного консенсусу Маастрихт ІІІ–V, рекомендацій ESPGHAN): виразкова хвороба шлунка та ДПК; хронічний хелікобактерний гастрит/гастродуоденіт у періоді загострення; функціональна диспепсія (якщо в родині є випадки виразкової хвороби та раку шлунка) в регіонах з високим ступенем поширеності H.pylori-інфекції (більше ніж 20 %); гастроезофагеальна рефлюксна хвороба (при наявності H.pylori та вираженого гастриту в корпусі шлунка); залізодефіцитна анемія (у випадках неясного генезу та за відсутності всіх інших явних причин для її розвитку); ідіопатична тромбоцитопенія; тривала терапія нестероїдними протизапальними препаратами [6, 14–16].
Ефективність лікування дітей з Hp-асоційова-ними захворюваннями верхніх відділів травного каналу залежить не тільки від коректно проведеної ерадикації збудника, але і від комплексу наступних реабілітаційних заходів, що потребують набагато більше часу. Під час реабілітаційної терапії необхідно вирішити такі питання: ліквідувати або зменшити явища дисбіозу кишок, провести корекцію вітамінного балансу, нормалізувати моторику шлунково-кишкового тракту, нормалізувати вегетативний статус дитини, зняти психосоматичні нашарування тощо.
Зростання стійкості Нp до антибактеріальних препаратів, що потребує подовження терміну прийому (до 10–14 діб) і викликає збільшення побічних ефектів ерадикаційної терапії, свідчить про необхідність розробки альтернативних методів лікування й способів профілактики [6, 8, 10]. Ряд досліджень показали, що пробіотики можуть використовуватися й посилювати ефект ерадикаційної терапії, а також підвищувати комплаєнс. Передбачаються такі ефекти пробіотиків: покращення переносимості антибактеріальної терапії та зменшення її побічних ефектів, підвищення рівня завершеності терапії, імуномодулюючий, антибактеріальний ефекти [12, 17–19]. Вказуються можливі ефекти лактобацил: посилення захисного бар’єра, зниження адгезії й інгібування росту Нp за рахунок вироблення лактату, бактеріоцинів; деякі штами здатні пригнічувати уреазу Нp [20, 21]. Отже, пробіотики доцільно призначати при проведенні ерадикаційної терапії Нp і з профілактичною метою, і в разі появи діареї. Точний механізм антидіарейної дії пробіотиків не встановлено. Дані метааналізу досліджень ефективності пробіотиків, проведених в 2011–2013 рр., показали, що застосування цієї групи препаратів значно прискорює одужання пацієнтів при лікуванні діареї різного генезу [22, 23].
Можливість застосування пробіотиків у схемах ерадикації разом з антибіотиками як засобів ад’ювантної терапії відображена й у Маастрихтських угодах (IV і V консенсуси) [7, 10]. За умови кислотостійкості штаму (доведено для Saсcharomyces boulardii, Lactobacillus ramnosus GG, L.reuteri, Lactobacillus acidophilus) пробіотики можуть мати прямий антагоністичний ефект щодо Нp, конкурувати з ним за поживні речовини й рецептори адгезії, виробляти метаболіти, що пригнічують ріст Нp (леткі жирні кислоти, молочну кислоту, перекис водню, піроглутамат). Багато штамів пробіотичних культур виробляють антибактеріальні субстанції, що інгібують зростання інших мікроорганізмів; Lactobacilli і Bifidobacteria виділяють бактеріоцини, здатні пригнічувати ріст Нp і зменшувати його адгезію до епітеліоцитів шлунка. Крім того, пробіотики відіграють важливу роль у стабілізації бар’єрної функції шлунка й зменшують запалення його слизової оболонки [12, 17, 23]. Наведене вище дає підстави для оптимізму щодо можливості використання препаратів із симбіотичною активністю для оптимізації ерадикації Hp у пацієнтів дитячого та підліткового віку.
Мета дослідження: оцінити клінічну ефективність симбіотика Лактіалє (Protexin Health Care) як ад’ювантної терапії в рамках ерадикаційних схем у дітей різного віку з Hp-асоційованою патологією верхніх відділів травного каналу.
Матеріали та методи
Під спостереженням перебували 70 дітей із Hp-асоційованою патологією верхніх відділів травного каналу віком від 5 до 18 років (середній вік 12,70 ± ± 2,42 року). Хворі проходили обстеження й лікування в гастроентерологічному відділенні клінічної бази (МДКЛ № 19 м. Харкова) кафедри педіатричної гастроентерології та нутриціології. За віком хворі розподілилися так: 5–10 років — 43 %, старше від 10 років — 57 % дітей. У групі до 10 років переважали дівчата — 65 %, а в групі старших — хлопчики — 67,5 %. Для верифікації діагнозу детально вивчали скарги, анамнез захворювання й життя, виконували клініко-параклінічні та інструментальні дослідження згідно з протоколом [11]. З метою діагностики, а також для оцінки ефективності проведеної терапії проводився збір скарг та анамнезу за допомогою спеціально розробленої індивідуальної реєстраційної карти пацієнта. Інструментальні методи дослідження: фіброезофагогастродуоденоскопія (фіброскоп Р10 OLYMPUS, Японія), ендоскопічна інтраезофагогастральна рН-метрія (ацидогастрограф АГ-1pH-M, ТОВ «Старт», м. Вінниця), дихальний уреазний «Хелік-тест» та біоптатний уреазний «Хелпіл-тест») (ТОВ «Асоціація медицини та аналітики», м. Санкт-Петербург), випорожнення-тест для визначення антигенів Нр у копрофільтратах (CITO TEST H.pylori Ag, Farmasco; СerTest Biotec, SL, Іспанія), морфологічне дослідження фрагментів (біоптатів) слизової оболонки antrum.
Залежно від віку пацієнти були розподілені на 2 групи. Перша група (40 пацієнтів) — діти віком понад 10 років із коморбідною запально-деструктивною патологією (хронічний гастродуоденіт (ХГД) та виразкова хвороба ДПК у поєднанні з гастроезофагеальною рефлюксною хворобою (ГЕРХ)). Другу групу становили діти до 10 років — 30 пацієнтів із функціональними розладами верхніх відділів травного каналу, основний діагноз — функціональна диспепсія (ФД).
У кожній віковій групі проводився розподіл на підгрупи (основна та порівняльна) залежно від отриманої терапії. У групі до 10 років до основної підгрупи увійшли 20 пацієнтів, до підгрупи порівняння — 10. У групі старших від 10 років основну та підгрупу порівняння становили по 20 пацієнтів. Групи пацієнтів були тотожними за основними критеріями. Обов’язковою умовою було дотримання рекомендацій щодо лікування, харчування, режиму та дотримання здорового способу життя (повноцінний комплаєнс).
Пацієнти з основної підгрупи дітей, старших від 10 років, отримували разом зі стандартними ерадикаційними схемами (потрійна: ІПП/Вi + амоксицилін + ніфурател чи квадротерапія: ІПП + Bi + амоксицилін + ніфурател/кларитроміцин) симбіотик Лактіалє протягом 10 днів по 1 пакетику (109 КУО) 1 раз на добу після основного прийому їжі з рекомендаціями щодо подальшого прийому до 4 тижнів. Пацієнти групи порівняння отримували лише стандартну ерадикаційну терапію згідно з протоколами [3].
Пацієнти з основної підгрупи дітей, молодших від 10 років, отримували терапію, альтернативну стандартним схемам ерадикації: подвійну терапію (Bi + Лактіалє) протягом 10 днів з включенням препаратів вісмуту цитрату/субсаліцилату по 120 мг двічі на добу та Лактіалє двічі на добу по 1 пакетику (загальна доза 2 • 109 КУО) після основного прийому їжі з подальшою рекомендацією продовжити прийом симбіотика до 4 тижнів. Пацієнти з підгрупи порівняння отримували стандартну потрійну терапію першої лінії на основі вісмуту цитрату/субсаліцилату (Bi + амоксицилін + ніфурател).
Симбіотик Лактіалє призначали з метою підвищення ефективності ерадикації Hp, зменшення побічних дій стандартних анти-Hp-схем та покращення стану й захисних (репаративних) властивостей слизової оболонки ГДЗ у дітей та підлітків із Нр-позитивним ХГД та ВХ ДПК та як можливу альтернативу стандартним схемам ерадикації в дітей молодшого віку з Нр-позитивним статусом при функціональних розладах (ФД), враховуючи доведені властивості симбіотика [17, 24].
Симбіотик Лактіалє (для компанії «Фармак» препарат виробляє компанія Protexin Health Care, Великобританія) містить 7 корисних штамів пробіотичних мікроорганізмів (Lactobacillus casei, Lactobacillus rhamnosus, Streptococcus thermophylus, Bifidobacterium breve, Lactobacillus acidophylus, Bifidobacterium infantis, Lactobacillus bulgaricus (присутні в нормі в мікрофлорі кишечника здорової людини)) та пребіотик — фруктоолігосахариди. Лактіалє має паспорт безпеки, що дуже важливо для його використання в дитячому віці, який засвідчує якість (підтверджено сертифікатами GMP, RPSGB, FEMAS, ISO 9001). Лактіалє відповідає всім вимогам до пробіотиків (табл. 1).
/45-1.gif)
Вдало підібрана комбінація біфідобактерій, лактобактерій і молочнокислого стрептокока дозволяє потенціювати біологічну бактерицидну дію кожної бактерії, що входить до складу Лактіалє, для ерадикації патогенних та умовно-патогенних бактерій, що заселяють кишечник, усунення симптомів захворювань, викликаних активізацією патогенної мікрофлори (діарея, запор, метеоризм), а також зменшення інтоксикації; дозволяє швидко й адекватно відновити рівновагу мікрофлори в дітей та дорослих без ризику посилення активності патогенної флори.
Крім того, склад Лактіалє обумовлює покращені адгезивні якості позитивної мікрофлори до стінок кишечника, що дозволяє підвищити не тільки просвітний, а й пристінковий імунітет, а це означає пролонгацію позитивного лікувального ефекту пробіотика. Спеціально підібране співвідношення лакто- і біфідобактерій у Лактіалє дозволяє в короткі терміни підвищити не тільки місцевий, а й загальний імунітет за рахунок специфічної взаємодії бактерій Лактіалє з імунокомпетентними клітинами слизової кишечника, інгібування синтезу запальних цитокінів шляхом впливу на природні механізми захисту слизової кишечника (стимуляція фагоцитарної активності нейтрофілів (L.acidophylus, Str.thermophylus, L.casei, L.rhamnosus), посилення синтезу IL-10, ФНП-α, зниження синтезу IgE, посилення синтезу sIgА, формування імунологічної толерантності (В.longum, B.іnfantis)), препарат також чинить протизапальний вплив на епітелій шлунково-кишкового тракту [19, 23, 24].
Оцінку ефективності терапії за динамікою клінічних показників проводили одразу після закінчення ерадикаційної терапії (на 7–10-й день) та через 4 тижні під час оцінки ефективності анти-Hp-лікування. Проводилась статистична обробка результатів дослідження. Кількісні й порядкові показники подавалися як середнє значення ± стандартне відхилення. Якісні показники подавалися у вигляді абсолютного числа спостережень і частки (у відсотках) від загального числа хворих у вибірці в цілому або відповідній групі. Вірогідність відмінностей порівнюваних величин визначали за критерієм Стьюдента, розходження вважали вірогідними при р < 0,05.
Результати та обговорення
Пацієнти обох підгруп із 1-ї групи спостереження на початку лікування мали майже однакові скарги, що стосувалися перш за все основної патології — проявів запально-деструктивних процесів ГДЗ та стравоходу (рис. 1).
Абдомінальний біль, відрижку, печію, астеноневротичні прояви мали більшість пацієнтів з ХГД, ВХ ДПК та ГЕРХ. Супутні скарги (метеоризм, діарея) мали окремі пацієнти. При динамічному спостереженні після закінчення антихелікобактерної терапії на 10-й день клінічні прояви і характер скарг значно відрізнялись у пацієнтів основної підгрупи й підгрупи спостереження, про що свідчать дані діаграми (рис. 1).
Так, у пацієнтів основної підгрупи, які отримували симбіотик разом з потрійною чи квадротерапією, на момент її закінчення відзначали виражену позитивну динаміку як за основними скаргами, так і щодо супутньої патології, особливо астеноневротичних проявів, і покращання якості життя. Пацієнти з групи порівняння теж мали позитивну динаміку щодо основних скарг (перш за все больового синдрому), але значно менш виражену, а диспептичні скарги (відрижка, гіркота у роті, неприємний запах, печія) не тільки не зменшились, а в деяких випадках зросли чи навіть з’явилися вперше. Крім того, виникли скарги, пов’язані з негативними наслідками ерадикації, а саме: метеоризм (35 %), діарея (35 %), гіркота в роті (45 %), печія (90 %), алергічні прояви (15 %), значно посилились і збільшились прояви астеноневротичного синдрому. Дані прояви погіршували якість життя пацієнтів та потребували корекції.
Подальший аналіз результатів спостереження (через 1 місяць після закінчення АХТ) виявив однозначну позитивну динаміку майже всіх скарг і клінічних проявів захворювання в основній підгрупі. Усі пацієнти мали гарне самопочуття, добре оцінювали якість свого життя, комплаєнс в лікуванні. У пацієнтів з підгрупи порівняння за цей період теж спостерігалися позитивні зміни, але диспептичні скарги й астеноневротичні прояви трималися довше й на момент огляду мали місце в 20–70 % хворих.
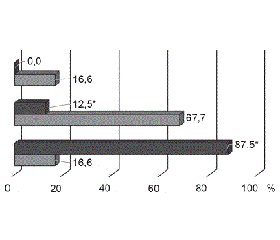
Оцінюючи ефективність ерадикаційної терапії, проведеної неінвазивними методами (уреазний дихальний та випорожнення-тест), констатували задовільний результат в обох підгрупах, що за міжнародними стандартами (80 % і більше [6, 7, 25]) дає право на позитивну оцінку.
Але ефективність в основній підгрупі була на 10 % більшою, ніж у підгрупі порівняння (рис. 2). Це дає можливість позитивно оцінити використання симбіотика Лактіалє як ад’ювантної терапії в рамках ерадикації Hp.
Посиленням протизапальної дії симбіотика можна пояснити й значну позитивну динаміку проявів морфологічних ознак запалення слизової оболонки шлунка у пацієнтів основної підгрупи з ВХ ДПК, що подано на рис. 3.
Отже, результати використання симбіотика Лактіалє у пацієнтів 1-ї групи як ад’ювантної терапії в рамках стандартних педіатричних схем ерадикації Hp дають можливість говорити про доцільність і високу ефективність такого лікування. Про це свідчать не тільки позитивна динаміка скарг, відсутність побічних ефектів і гарна переносимість препаратів на фоні прийому симбіотика, але і збільшення на 10 % ефективності ерадикації порівняно зі стандартними схемами, що збігається з результатами інших досліджень [17, 25]. Окремо треба відзначити позитивний вплив симбіотика на процеси якісного загоєння виразок (рис. 4) та значне посилення протизапального ефекту, що спостерігали в динаміці лікування в пацієнтів основної підгрупи з ВХ ДПК.
/47-1.gif)
Пацієнти молодшого віку з 2-ї групи спостереження теж мали однотипні скарги, але з переважанням різноманітних суб’єктивних проявів, що є характерним для функціональних порушень ШКТ (ФД), які мали місце в дітей в обох підгрупах, у тому числі проявів супутньої патології кишечника (метеоризм, запор та інші — 40–70 %), ще до початку лікування. Динаміка клінічних проявів і скарг у пацієнтів основної підгрупи і підгрупи порівняння була різнонаправленою і значно відрізнялась вже одразу після закінчення АХТ, про що свідчить діаграма (рис. 5). Якщо в пацієнтів основної підгрупи динаміка скарг і клінічних проявів була однозначно позитивною, то більшість пацієнтів з підгрупи порівняння скаржились не тільки на погіршення самопочуття, але й на маніфестацію ознак побічної дії, погану переносимість стандартних схем ерадикації, у результаті 3 пацієнти відмовились продовжувати лікування. І через місяць після скасування ерадикаційних схем у половини пацієнтів самопочуття залишалось порушеним, вірогідно частіше зберігались скарги на диспептичні прояви, больовий і аcтеноневротичний синдроми.
/48-1.gif)
Оцінку ефективності ерадикаційної терапії також проводили неінвазивними методами (уреазний дихальний та випорожнення-тест) через місяць після відміни анти-Hp-схем. Результати, подані на рис. 6, свідчать про неефективність схем ерадикаційної терапії в пацієнтів обох підгруп за міжнародними стандартами (результати нижче від 80 %). І хоча в основній підгрупі з використанням альтернативної схеми подвійної терапії з препаратом Bi і Лактіалє ефективність була на 5 % вище, ніж при використанні стандартних схем, результат не можна вважати задовільним.
/49-1.gif)
Такий низький результат ерадикації, отриманий нами в пацієнтів 2-ї групи з функціональними розладами і Hp-позитивним статусом, можна вважати прогнозованим. Про це свідчать і останні міжнародні консенсуси (Маастрихт IV та V) та погоджувальні висновки експертів [7, 10, 15] — низький відсоток ефективності ерадикації в пацієнтів з функціональною диспепсією (не більше від 15–30 %), що збігається з отриманими результатами. Але безпека, добра переносимість, антимікробні, протизапальні імуномодулюючі та інші властивості пробіотичних штамів, що входять до складу Лактіалє, дають можливість говорити про ерадикаційну перспективність використання даного симбіотика в лікуванні дітей з хелікобактер-асоційованими захворюваннями верхніх відділів шлунково-кишкового тракту.
Висновки
1. Сучасні проблеми лікування хелікобактер-асоційованих захворювань у дітей пов’язані з багатьма чинниками, серед яких антибіотикорезистентність та незадовільна переносимість стандартних ерадикаційних схем унаслідок побічних реакцій і незадовільного комплаєнсу є найчастішими причинами неефективності ерадикації.
2. Використання симбіотика Лактіалє як ад’ювантної терапії в рамках ерадикаційних схем у дітей різного віку з Hp-асоційованою патологією верхніх відділів травного каналу є доцільним, тому що суттєво підвищує ефективність ерадикації.
3. Включення симбіотика Лактіалє до схем лікування одночасно з ерадикаційною терапією дозволило значно покращити переносимість анти-Hp-препаратів і, відповідно, прихильність пацієнтів до дотримання лікування й рекомендацій.
4. Ад’ювантна терапія із симбіотиком Лактіалє позитивно вплинула й на віддалені результати, а саме на процеси якісного загоєння виразок та значне посилення протизапального ефекту, що спостерігали в динаміці лікування в пацієнтів із ВХ ДПК.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Белоусова О.Ю. Еще раз о факторах риска развития патологии верхних отделов пищеварительного тракта и об оптимизации схем эрадикационной терапии в педиатрической практике / О.Ю. Белоусова // Здоров’я України. — Вересень 2016. — № 3(38). — С. 24-26.
2. Белоусова О.Ю. Сочетанная патология верхних отделов пищеварительного канала у детей: современные тенденции / О.Ю. Белоусова, Н.В. Павленко, Л.Г. Волошина [и др.] // Лікарська справа. — 2014. — № 11. — С. 85-88.
3. Шадрин О.Г. Нelicobacter рylori у детей: современные подходы к диагностике и пути оптимизации терапии / О.Г. Шадрин // Современная педиатрия. — 2014. — № 5(61). — С. 119-127.
4. Alarcon T., Jose Martinez-Gomez M., Urruzuno P. Helicobacter pylori in pediatrics // Helicobacter. — 2013 Sep. — 18, Suppl. 1. — 52-7. doi:10.1111/hel.12070.
5. Chey W.D., Wong B.C. American College of Gastroenterology guideline on the management of Helicobacter pylori infection // Am. J. Gastroenterol. — 2007. — 102. — 1808-1825. DOI: 10.1111/j.1572-0241.2007.01393.x.
6. Koletzko S., Jones N.L., Goodman K.J. et al. Evidence-based guidelines from ESPGHAN and NASPGHAN for Helicobacter pylori infection in children // J. Pediatr. Gastroenterol. Nutr. — 2011 Aug. — 53(2). — 230-43. doi: 10.1097/MPG.0b013e3182227e90.
7. Malfertheiner P. et al. The European Helicobacter Study Group (EHSG). Management of Helicobacter pylori infection — the Maastricht IV/Florence Consensus Report // Gut. — 2012. — 61. — 646-664. doi:10.1136/gutjnl-2012-302084.
8. Фадеенко Г.Д. Вікові особливості перебігу захворювань шлунково-кишкового тракту, асоційованих з Нelicobacter pylori, та їх раціональна корекція / Г.Д. Фадеенко, О.Ю. Бєлоусова, Н.В. Павленко [ та ін.]; Метод. рек. — К., 2015. — 32 с.
9. Ford A.C., Marwaha A., Sood R., Moayyedi P. Global prevalence of, and risk factors for uninvestigated dyspepsia: a meta-analysis // Gut. — 2014. doi: 10.1136/gutjnl-2014-307843.
10. Malfertheiner P et al. Management of Helicobacter pylori infection — the Maastricht V/Florence Consensus Report // Gut. — 2016 Oct 5. — http://dx.doi.org/10.1136/gutjnl-2016-312288.
11. Про затвердження уніфікованих клінічних протоколів медичної допомоги дітям із захворюваннями органів травлення: Наказ МОЗ України від 29.01.2013 № 59 [Електронний документ]. — Режим доступу: http:www.moz.gov.ua — назва з екрана.
12. Bahrami B., Macfarlane S., Macfarlane G.T. Induction of cytokine formation by human intestinal bacteria in gut epithelial cell lines // J. Appl. Microbiol. — 2011 Jan. — 110(1). — 353-63. doi: 10.1111/j.1365-2672.2010.04889.x.
13. Hurduc V., Plesca D., Dragomir D., Sajin M., Vandenplas Y. A randomized, open trial evaluating the effect of Saccharomyces boulardii on the eradication rate of Helicobacter pylori infection in children // Acta Paediatric. — 2009 Jan. — 98(1). — 127-31. doi: 10.1111/j.1651-2227.2008.00977.x.
14. Boeckxstaens G., El-Serag H.B., Smout A., Kahrilas P. Symptomatic reflux disease: the present, the past and the future // BMJ. — 2014. — 63(7). — 1185-1193. — http://dx.doi.org/10.1136/gutjnl-2013-306393.
15. Sugano K., Tack J., Kuipers E.J. et al. Kyoto global consensus report on Helicobacter pylori gastritis // Gut. — 2015. — 64. — 1353-67. doi: 10.1136/gutjnl-2015-309252.
16. Vakil N., van Zanten S.V., Kahrilas P., Dent J., Jones R. The Montreal definition and classification of gastroesophageal reflux disease: a global evidence-based consensus // Am. J. Gastroenterol. — 2006. — 101. — 1900-1920. — http://dx.doi.org/10.1111/j.1572-0241.2006.00630.x
17. Goel A., Aggarwal R. Probiotics as adjunctive therapy for eradication of Helicobacter pylori infection (Protocols) // Cochrane Database of Systematic Reviews. — 2013. — Issue 10. — Art. No CD010776. doi: 10.1002/14651858.CD010776.
18. Hsieh P.S., Tsai Y.C., Chen Y.C., The S.F., Ou C.M., King V.A. Eradication of Helicobacter pylori infection by the probiotic strains Lactobacillus johnsonii MH-68 and L. salivarius ssp. Salicinius AP-32 // Helicobacter. — 2012 Dec. — 17(6). — 466-77. doi: 10.1111/j.1523-5378.2012.00992.x.
19. Rizzelo V., Bonaccorsi I., Dongarra M.N. et al. Role of natural killer and dendritic cell crosstalk in immunomodulation by commensal bacteria probiotics // J. Biomed. Biotechnol. — 2011. — 2011. — 473097. doi: 10.1155/2011/473097.
20. Shenderov B.A. Metabolics: novel idea or natural development of probiotic conception // Microb. Ecol. Health. Dis. — 2013 Apr 12. — 24. doi: 10.3402/mehd.v24i0.20399.
21. Szajewska H., Albrecht P., Topczewska-Cabanek A. Rando-mized, double-blind, placebo-controlled trial: effect of lactobacillus GG supplementation on Helicobacter pylori eradication rates and side effects during treatment in children // J. Pediatr. Gastroenterol. Nutr. — 2009 Apr. — 48(4). — 431-6. doi: 10.1097/MPG.0b013e318182e716.
22. Le Moal V.L., Fayol-Messaoudi D., Servin A.L. Compound(s) secreted by Lactobacillus casei strain Shirota YIT9029 irreversibly and impair the swimming motility of Helicobacter pylori and Salmonella enterica serovar Typhimurium, respectively // Microbiology. — 2013 Sep. — 159(Pt9). — 1956-71. doi: 10.1099/mic.0.067678-0.
23. Yoon S.S., Sun J. Probiotics, nuclear receptor signaling, and anti-inflammatory pathways // Gastroenterol. Res. Pract. — 2011. — 2011. — 971938. doi: 10.1155/2011/971938.
24. Efrati C., Nicilini G., Cannaviello C., O’Sed N.P., Valabrega S. Helicobacter pylori eradication: sequential therapy and Lactobacillus reuteri supplementation // World J. Gastroenterol. — 2012. — Nov. 21. — 18(43). — 6250-4. doi: 10.3748/wjg.v18.i43.6250.
25. Yuan Y, Ford A.C., Khan K.J. Optimum duration of regimens for Helicobacter pylori eradication // Cochrane Data base Syst. Rev. — 2013. — 12. — CD008337. doi: 10.1002/14651858.CD008337.pub2.

/45-1.gif)
/46-1.gif)
/47-1.gif)
/48-1.gif)
/49-1.gif)