Дослідження є фрагментом кафедральної планової науково-дослідної роботи «Клініко-патофізіологічні аспекти анестезіологічного забезпечення оперативних втручань та інтенсивної терапії у хворих із порушенням гомеостазу».
Цукровий діабет (ЦД) набув характеру епідемії в усьому світі. Частота ЦД 2-го типу швидко зростає серед представників усіх вікових груп та рас. Станом на 2017 рік у США він діагностований у 22 мільйонів осіб [4, 20], а це близько 6,9 % населення країни [22], а ще в понад 8 мільйонів людей він не діагностований [28]. Американське Національне дослідження здоров’я й харчування (NHANES) вказує на те, що майже 13 % пацієнтів віком понад 20 років мають ЦД, і 40 % цих випадків є недіагностованими [26]. Тому лікарі амбулаторної хірургії повинні враховувати той факт, що кожен десятий пацієнт потенційно може мати ЦД.
Під терміном «предіабет», або «дисглікемія», розуміють зростання рівня глюкози в плазмі крові понад 100 мг/дл (5,6 ммоль/л), але менше від 125 мг/дл (6,94 ммоль/л), порушення толерантності до глюкози в крові (рівень від 140 мг/дл (7,8 ммоль/л) до 199 мг/дл (11,0 ммоль/л) через 2 години після перорального прийому 75 г глюкози) або збільшення рівня глікозильованого гемоглобіну А1с (HbA1c) від 5,7 до 6,4 % [6]. HbA1c використовується для приблизного визначення концентрації глюкози в плазмі пацієнта протягом попередніх 3 місяців. HbA1c — це відсоток гемоглобіну, зв’язаного з глюкозою (глікозильований), що наростає при збільшенні глікемії (табл. 1).
Американська асоціація з діабету запропонувала формулу, за якою середній рівень глюкози (мг/дл) може бути розрахований із показника HbA1c для порівняння з добовими показниками глюкози, отриманими за допомогою глюкометра [6, 28]: (показник HbA1c × 28,7) – 46,7 = середній рівень глюкози в плазмі (мг/дл) (поділити 18 — для переводу мг/дл у ммоль/л).
Результати перерахунку подано в табл. 2.
Оскільки кожна третя особа має предіабет, визначено, що понад 40 % амбулаторних пацієнтів можуть мати базову дисглікемію. Тому при її виявленні, часто через хірургічний стрес, логічно припустити, що більшість амбулаторних хірургічних пацієнтів перебуватимуть у стані предіабету [26, 27].
Поширеність ЦД серед людей похилого віку дуже висока — приблизно 26 % осіб у віці 65 років і старших. Очікується, що до 2025 року в цій віковій групі кількість діабетиків зросте майже вдвічі. Цікавим є той факт, що представники расових/етнічних меншин у США страждають від ЦД при більш високих показниках глюкози [20, 28]. У світі налічується 422 мільйони діабетиків, і цьому відповідає 1,5 мільйона випадків смертей на рік [10]. ЦД посідає 7-ме місце серед основних причин смертності населення, зокрема, діабет 1-го типу скорочує тривалість життя на 20 років, а діабет 2-го типу — на 10 років [23].
Цукровий діабет — це нездатність правильно метаболізувати білки, жири й вуглеводи через повну відсутність чи недостатню кількість інсуліну, секретованого β-клітинами підшлункової залози: нечутливість тканин або руйнування інсуліну, перш ніж він досягає пункту призначення [11].
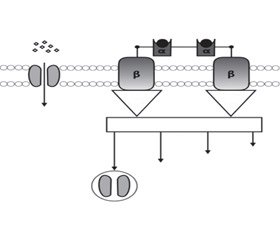
У нормі вуглеводи розщеплюються до глюкози й транспортуються через клітинні мембрани. Інсулін зв’язується з α-ланцюгом рецептора інсуліну на поверхні клітини-мішені, викликаючи фосфорилювання трансмембранної β-субодиниці, яка активує внутрішньоклітинну тирозинкіназу. Тирозинкіназа активує субстрати інсулінового рецептора, що беруть участь у низці важливих функцій, зокрема синтезі глікогену, жирів, білків, і найвагомішою з них є стимуляція руху молекул транспорту глюкози до поверхні клітини. Після приєднання до клітинної мембрани молекули переносу глюкози відкривають трансмембранний канал, через який глюкоза проникає в цитоплазму клітини [17]. Основним джерелом енергії клітинного метаболізму є фосфорильована внутрішньоклітинна глюкоза (рис. 1).
/90-2.jpg )
Підшлункова залоза складається з 2 різних типів тканин: панкреатичного ацинуса (екзокринні клітини) та острівців Лангерганса (ендокринні клітини). Ацинуси становлять близько 80 % панкреатичної маси, там відбувається секреція травних ферментів, бікарбонатних іонів і води у дванадцятипалу кишку через панкреатичний канал. Приблизно 20 % підшлункової залози складається з 1–2 мільйонів острівців, які вивільняють гормони (глюкагон, інсулін, амілін, соматостатин та панкреатичний пептид) безпосередньо в кровотік [11].
При ЦД 1-го типу підшлункова залоза не здатна виділяти достатню кількість інсуліну через знищення β-клітин в острівцях Лангерганса, що обумовлено автоімунними розладами чи вірусними інфекціями й може спостерігатися при всіх видах ЦД (зазвичай діагностується в дітей і підлітків) [23].
ЦД 2-го типу, як правило, зустрічається в людей, старших за 30 років, однак цей вид діабету стрімко молодшає [11, 20]. Найбільш ймовірно, що існує пряма кореляція між збільшенням кількості дітей і підлітків з ожирінням і розвитком ЦД 2-го типу в людей, молодших за 20 років [11, 17, 26]. Насправді ожиріння є основним фактором ризику розвитку діабету 2-го типу. Вважається, що збільшення маси тіла приводить до утворення меншої кількості рецепторів інсуліну в печінці, жировій та м’язових тканинах. Порушення чи хибні ненормальні сигнальні шляхи між існуючими рецепторами інсуліну й певними клітинними реакціями також мають важливе значення при діабеті, пов’язаному з ожирінням [11]. Серед інших причин інсулінорезистентності, які можуть привести до ЦД 2-го типу, виділяють гестаційний діабет, синдром полікістозних яєчників, надлишок гормону росту, синдром Кушинга й гемохроматоз.
Інсулінорезистентність, пов’язана з ЦД 2-го типу, спричиняє надзвичайно високий рівень глікемії. Прийнятний рівень глюкози крові натще — менше від 100 мг/дл (5,6 ммоль/л) (110 мг/дл (6,1 ммоль/л) — верхня межа норми), а нормальний рівень HbA1c — менше від 5,7 % [6]. У діабетиків часто глікемія перевищує 125 мг/дл (6,9 ммоль/л). Гострий, небезпечний для життя гіпересмолярний стан, коли глікемія перевищує 600 мг/дл (33,3 ммоль/л), є свідченням ускладнень ЦД 2-го типу [17].
NHANES дійшло висновку, що лише 14 % діабетиків не мають супутніх захворювань [24]. Серед найпоширеніших супутніх захворювань ЦД — ожиріння, серцево-судинні захворювання (ССЗ), гіпертонія, дисліпідемія й ураження нирок. Також часто зустрічаються депресія, розлади сну й рак [18]. Саме тому амбулаторним анестезіологам важливо розуміти зв’язок між ЦД 2-го типу та супутніми станами й ускладненнями, що можуть виникнути під час седації й загальної анестезії.
Дослідження NHANES показало, що близько 90 % пацієнтів із ЦД 2-го типу мали надмірну вагу або ожиріння (індекс маси тіла > 25 кг/м2) [18]. Ожиріння є додатковою проблемою при анестезії, включаючи труднощі з диханням, вентиляцією, оксигенацією, обструктивне нічне апное, гастро–езофагеальну рефлюксну хворобу, проблему з точним дозуванням та сповільненою дією препаратів.
Основною причиною смерті у хворих на ЦД 2-го типу є ССЗ та атеросклеротичні захворювання, зокрема гостре порушення мозкового кровообігу й ішемічна хвороба серця [18]. Інсулінова стимуляція синтезу тригліцеридів і гальмування їх розпаду погіршується через відсутність інсуліну або інсулінорезистентність і є основною причиною вищевказаних ускладнень. Погано переноситься тахікардія, фіксується 10-кратне збільшення смертності при поєднанні із захворюванням коронарної артерії, при яких постійна ЧСС перевищує 105 уд/хв упродовж 5 хвилин і довше після операції. Оскільки пацієнти із ССЗ зазвичай приймають антитромбоцитарну терапію, вони, відповідно, мають високий ризик періопераційної кровотечі. Ліпідні розлади значно підвищують ризик розвитку ССЗ і пов’язаних із ними захворюваннями. Дослідження NHANES показало, що майже 50 % хворих на ЦД 2-го типу мають підвищений рівень ліпідів [2].
Близько 70 % пацієнтів із ЦД 2-го типу страждають від гіпертонії [18], що підвищує ризик періопераційного інфаркту міокарда, цереброваскулярних катастроф і мікросудинних захворювань (ретинопатія, вегетативна й сенсорна нейропатія). Американська асоціація діабету рекомендує утримувати в пацієнтів артеріальний тиск нижче від 140/80 мм рт.ст. [20]. Ретельний контроль тиску матиме більш безпосередній і значущий вплив на захворюваність і смертність, ніж контроль над глікемією або ліпідами [30].
До 40 % діабетиків мають хронічні захворювання нирок та мікросудинні ураження [21]. Інсулінозалежні пацієнти мають підвищений ризик гіпоглікемії, оскільки хронічні хвороби нирок впливають на фармакокінетику інсуліну [18]. Багато пероральних антидіабетичних препаратів, включаючи бігуаніди (метформін), сульфонілсечовину й інгібітори α-глюкозидази, не можна застосовувати у хворих із цією супутньою патологією [29].
Важливо знати допустимий рівень глюкози чи HbA1c, коли планується провести анестезію та хірургічне втручання. Чи рівень гіперглікемії не є занадто високим для проведення операції? Коли фактори ризику, пов’язані з неконтрольованим діабетом, визначають, що хірургічне втручання має бути скасоване або перенесене? Триває багато суперечок стосовно того, який рівень глікемії вважається безпечним і наскільки строгий глікемічний контроль слід застосовувати для діабетиків, яким планується операція.
На початку ХХІ століття багато практикуючих анестезіологів виступали за курс лікування хворих на ЦД, який називався «жорстким глікемічним контролем» з посиланням на захворюваність та смертність при інтенсивній терапії [5]. Жорсткий глікемічний контроль — це швидке зниження глікемії з метою досягнення рівня HbA1c < 6 % [17]. Однак подальше дослідження показало, що такий метод тільки збільшив ризик смертності, пов’язаної з гіпоглікемією. Насправді дослідження ACCORD 2008 року було зупинено через високий рівень смертності його учасників, які пройшли жорсткий режим глікемії [26]. Дослідження NICE-SUGAR 2009 року також показало збільшення смертності хворих на ЦД, які зазнали різкого зниження гіперглікемії [29]. На сьогодні існує понад 7 різних рекомендацій від авторитетних джерел, що пропонують різні стратегії глікемічного контролю, однак загальний консенсус — уникнення різких коливань глюкози [19, 31]. Літературні джерела вказують на те, що контроль за змінами рівня глюкози в крові може бути настільки ж важливим, як і керування гіперглікемією, і що смертність залежить більше від коливань глюкози, ніж від її середніх величин [3, 17].
Товариство амбулаторної анестезії підготувало консенсусне твердження щодо періопераційного лікування глікемії в діабетиків. У рекомендаціях зазначено, що до операції анестезіолог повинен знати останні показники рівня глюкози і HbA1c [1, 19]. Це пов’язано з тим, що пацієнти з гострою гіперглікемією мають більше пері- та післяопераційних ускладнень, включаючи дегідратацію, кетоацидоз, гіперосмолярний гіперглікемічний стан, затримку загоєння операційної рани та її інфікування [26]. Рішення скасувати або відстрочити хірургічне втручання повинно прийматися спільно з хірургом і має враховувати терміновість операції, ґрунтуватися на усвідомленні ризиків і переваг [13]. На сьогодні немає даних про оптимальний рівень глюкози в крові у хворих на ЦД. Товариство амбулаторної анестезії стверджує, що для пацієнтів із добре контрольованим діабетом періопераційний рівень глюкози повинен підтримуватися на рівні нижче від 180 мг/дл (10,0 ммоль/л). Пацієнтам із погано контрольованим діабетом, як зазначено раніше, слід підтримувати вихідний рівень глюкози в крові [1].
Контроль рівня глікемії повинен проводитись до і після операції. Якщо хірургічне втручання заплановане менше ніж на 2 години, то в інтраопераційному тестуванні немає потреби. Однак при тривалих операціях доцільно проводити моніторинг глюкози кожні 1–2 години [15, 19]. Застосування портативних глюкометрів є прийнятним способом визначення рівня глюкози в крові. Проте слід розуміти, що Управління з контролю за харчовими продуктами та лікарськими засобами приймає похибку вимірювання на рівні 20 % для апаратів, що читають величини > 100 мг/дл (5,6 ммоль/л), та 15 % похибки для рівнів, менших від 100 мг/дл [1, 13]. Якщо потрібно знати точний рівень глюкози в крові, слід при можливості зробити аналіз в лабораторії.
ЦД вагомо впливає на організм людини, що ускладнює застосування анестезії. Наприклад, у пацієнтів часто спостерігається високий рівень необоротного глікованого колагену й неефективна колагеназна активність, що приводить до наростання колагену й муцину в кінцівках [25]. Цей склеротичний стан шкіри, відомий як діабетична склеродермія, робить епідерміс верхніх кінцівок жорстким, задубілим, і тому дуже складно провести внутрішньовенне канюлювання.
Глікований колаген може також накопичуватися в суглобах діабетиків, викликаючи їх обмежену рухливість. Часто жорсткий суглобовий синдром визначає нездатність правильно відображати «знак молитви»: коли пацієнт поєднує свої долоні, пальці не наближаються [7]. Діабетичний синдром жорсткого суглоба викликає занепокоєння анестезіолога, оскільки це може серйозно обмежувати рух атланто-потиличного суглоба або (рідше, тимчасово) нижньощелепного суглоба, що робить проведення звичайної ларингоскопії практично неможливим.
Гастропарез, або «діабетичний шлунок», виникає, коли вегетативна нейропатія, спричинена хронічним підвищенням рівня глюкози в плазмі, впливає на блукаючий нерв. При його пошкодженні порушується моторика шлунка й кишки із затримкою евакуації їжі та іншого вмісту шлунка [9, 29]. Неправильно перетравлена їжа не рухається по кишці, і утворюються безоари, що можуть спричинити непрохідність шлунка й збільшити ризик нудоти та блювання [8]. Гастроезофагеальний рефлюкс є ще одним поширеним побічним ефектом гастропарезу. Анестезіолог повинен бути добре обізнаним із цими потенційними проблемами, пов’язаними з порушенням моторики, оскільки може виникнути аспірація вмісту шлунка під час індукції чи протягом операції. Рух прозорих рідин не порушується, однак вони можуть потрапляти за 2 години перед анестезією [8, 9].
Ще одне з найпоширеніших і серйозних ускладнень діабетичної нейропатії, від якої страждає понад 20 % пацієнтів із ЦД 2-го типу, — це серцево-судинна вегетативна нейропатія [33]. Глікозилювання ендоневральних кровоносних судин може викликати нейроіндукцію, що призводить до дисфункції вегетативних нервів серця: тахікардії в спокої, ортостатичної гіпотензії й непереносимості фізичних вправ. Діабетики із серцево-судинною вегетативною нейропатією, що підтверджується варіабельністю серцевого ритму, вдвічі частіше страждають від німої ішемії міокарда [33]. Використовується термін «німа ішемія міокарда», оскільки такий же процес нервової дисфункції, що виникає при вегетативній нейропатії, зустрічається в сенсорних нервах. Це проявляється як оніміння в різних ділянках тіла (наприклад, серця) чи як біль, зазвичай поколювання чи пекучі відчуття в недерматомному патерні. Таким пацієнтам призначають інгібітори зворотного захоплення серотоніну й норадреналіну для лікування болю, що може привести до небажаного збільшення гемодинамічного ефекту від адреналіну, який входить до складу місцевих анестетиків.
Порівняно із загальною популяцією діабетики мають більш високий рівень захворювань печінки: безалкогольний жировий гепатоз, гепатоцелюлярна карцинома, гемохроматоз, гепатит В та C [12, 16]. Тому анестезіологи повинні переглянути останні біохімічні маркери стану печінки пацієнта. Аланін–амінотрансфераза (АЛТ) та аспартатамінотрансфераза (АСТ) — показники гострого пошкодження гепатоцитів, визначають кількість внутрішньоклітинних ферментів печінки, які циркулюють у крові через пошкодження чи загибель клітин (при нормі АЛТ 7–56 Од/л; АСТ 10–40 Од/л). При рості цих трансфераз (> 3 разів) понад 6 місяців ушкодження печінки приводить до порушення метаболізму ліків, що зазвичай використовуються при анестезії. Захворювання печінки є однією з основних причин смерті в пацієнтів із ЦД 2-го типу.
Хронічне захворювання нирок є в більшості хворих із ЦД, і власне креатинін плазми використовують для оцінки їх функції. Рівень креатиніну 2 мг/дл зазвичай означає втрату приблизно 50 % нефронів, а рівень 4,8 мг/дл свідчить про втрату 75 % нефронів [34]. Мікроальбумінурія, як правило, вказує на ранні стадії захворювання нирок [14, 32].
Отже, ризики, пов’язані із седацією й загальною анестезією, у діабетиків є значними. Лікар-анесте–зіо–лог при анестезіологічному забезпеченні в амбулаторних умовах зобов’язаний розуміти патофізіологію захворювання й загальні супутні захворювання. –Потрібно з належною увагою підійти до вибору ефективної й безпечної анестезії для хворих на ЦД при хірургічному втручанні в амбулаторних умовах.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Aldam P., Levy N., Hall G.M. Perioperative management of diabetic patients: new controversies // Br. J. Anaesth. — 2014. — 113(6). — 906-909.
2. American Diabetes Association. Standards of medical care in diabetes — 2013 // Diabetes Care. — 2013. — 36. — S11-S66.
3. Cefalu W.T. Glycemic targets and cardiovascular di–sease // N. Engl. J. Med. — 2008. — 358(24). — 2633-2635.
4. Centers for Disease Control and Prevention. Diabetes public health resource. — Atlanta, GA: Centers for Disease Control and Prevention, 2016. — Available from: www.cdc.gov/diabetes/statistics/prev/national/figpersons.html. — Accessed: June 2016.
5. Cryer P.E. Hypoglycemia, functional brain failure, and brain death // J. Clin. Invest. — 2007. — 117. — 868-870.
6. Diagnosing diabetes and learning about prediabetes. — Ale–xandria, VA: American Diabetes Association, 2014. — Availa–ble from: http://www.diabetes.org/are-you-at-risk/prediabetes/. — Accessed: June 2016
7. Erden V., Basaranoglu G., Delatioglu H., Hamzaoglu N.S. Relationship of difficult laryngoscopy to long-term non-insulin-dependent diabetes and hand abnormality detected using the ‘prayer sign’ // Br. J. Anaesth. — 2003. — 91(1). — 159-160.
8. Gastroparesis. — Alexandria, VA: American Diabetes Association, 2014. — Available from: http://www.diabetes.org/living-with-diabetes/complications/gastroparesis.html. — Accessed: August 2016.
9. Gastroparesis: introduction. — Baltimore, MD: Johns Hopkins Medicine, 2013. — Available from: http://www.hopkinsmedicine.org/gastroenterology_hepatology/pdfs/esophagus_stomach/gastroparesis.pdf. — Accessed: August 2016.
10. Global report ON DIABETES. — Washington, DC: World Health Organization, January 2016. — Available from: http://www.who.int/diabetes/global-report/en/. — Accessed: June 2016.
11. Hall J.E. Guyton and Hall Textbook of Medical Physio–logy. — 12th ed. — Philadelphia, PA: Saunders Elsevier, 2011.
12. Harris E.H. Elevated liver function tests in type 2 diabetes // Clin. Diabetes. — 2005. — 23(3). — 115-119.
13. Joshi G.P., Chung F., Vann M.A. et al. Society for Ambulatory Anesthesia consensus statement on preoperative blood glucose management in diabetic patients undergoing ambulatory surgery // Anesth. Anal. — 2010. — 11(6). — 1378-1387.
14. Koroshi A. Microalbuminuria, is it so important? // Hippokratia. — 2007. — 113. — 105-107.
15. Korpman T. Society of Ambulatory Anesthesia (SAMBA) on preoperative blood glucose management in diabetic patients undergoing ambulatory surgery; review of the consensus statement and additional commentary // CSA Bull. — 2010. — 58-62.
16. Liver function. — Charlottesville, VA: Johns Hopkins Medicine, 2015. — Available from: http://www.hopkinsguides.com/hopkins/view/Johns_Hopkins_Diabetes_Guide/547086/all/Liver_function. — Accessed: August 2016.
17. Longnecker D.E., Brown D.L., Newman M.F., Zapol W.M. Anesthesiology. — 2nd ed. — New York, NY: McGraw Hill Medical, 2012.
18. Management of common comorbidities of diabetes. — Jacksonville, FL: American Association of Clinical Endocrinologists, AACE Diabetes Resource Center, 2016. — Available from: http://outpatient.aace.com/type-2-diabetes/management-of-common-comorbidities-of-diabetes. — Accessed: June 2016.
19. Mathioudakis N., Golden S.H. A comparison of inpatient glucose management guidelines: implications for patient safety and quality // Curr. Diabetes Rep. — 2015. — 15. — 13.
20. National Center for Chronic Disease Prevention and Health Promotion, Division of Diabetes Translation. National diabetes statistics report, 2014. Estimates of diabetes and its burden in the United States. — Atlanta, Ga: Centers for Disease Control and Prevention, 2014. — Available from: www.cdc.gov/diabetes/pubs/statsreport14/national-diabetes-report-web.pdf. — Accessed: June 1, 2016.
21. Plantinga L.C., Crews D.C., Coresh J. et al. Prevalence of chronic kidney disease in US adults with undiagnosed diabetes or prediabetes // Clin. J. Am. Soc. Nephrol. — 2010. — 5. — 673-682.
22. Population estimates. — Washington, DC: US Department of Commerce, United States Census Bureau, 2016. — Avai–lable from: www.census.gov. — Accessed: June 2016.
23. Roberstshaw H.J., Hall G.M. Diabetes mellitus: anaesthetic management // Anaesthesia. — 2006. — 61. — 1187-1190.
24. Saha D.C., Choia I.S., Plauschinat C., Kwon J., Baron M. Impact of comorbid conditions and race/ethnicity on glycemic control among the US population with type 2 diabetes, 1988–1994 to 1999–2004 // J. Diabetes Complicat. — 2010. — 24(6). — 382-391.
25. Scleredema. — Alphen aan den Rijn, the Netherlands: UpToDate, 2015. — Available from: http://www.uptodate.com/contents/scleredema. — Accessed: August 2016.
26. Sheehy AM, Gabbay RA. An overview of preoperative glucose evaluation, management, and perioperative impact // J. Diabetes Sci Technol. — 2009. — 6. — 1261-1269.
27. So… do І have prediabetes? — New York, NY: Ad Council, 2016. — Available from: https://doihaveprediabetes.org/index.html. — Accessed: June 2016.
28. Statistics about diabetes. — Alexandria, VA: American Diabetes Association, 2016. — Available from: www.diabetes.org/diabetes-basics/statistics/?loc=db-slabnav. — Accessed: June 2016.
29. The NICE-SUGAR Study Investigators. Intensive versus conventional glucose control in critically ill patients // N. Engl. J. Med. — 2009. — 360(13). — 1283-1297.
30. UK Prospective Diabetes Study Group. Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38 // BMJ. — 1998. — 317. — 703-713.
31. Vann M.A. Perioperative management of ambulatory surgical patients with diabetes mellitus // Curr. Opin. Anaesthesiol. — 2009. — 22. — 718-724.
32. Venkat K.K. Proteinuria and microalbuminuria in adults: significance, evaluation, and treatment // South Med. J. — 2004. — 97(10). — 969-979.
33. Vink A.I., Maser R.E., Mitchell B.D., Freeman R. Diabetic autonomic neuropathy // Diabetes Care. — 2003. — 26. — 1553-1579.
34. Waikar S.S., Bonventre J.V. Creatinine kinetics and the definition of acute kidney injury // J. Am. Soc. Nephrol. — 2009. — 20(3). — 672-679.

/90-1.jpg )
/90-2.jpg )