Резюме
Актуальність. Стаття присвячена актуальній проблемі — вивченню вікових особливостей структурних змін печінки при хронічних запальних захворюваннях кишечника (ХЗЗК). Мета роботи: вивчити вікові особливості структурних змін печінки при неспецифічному виразковому коліті (НВК) та хворобі Крона (ХК). Матеріали та методи. Проведено обстеження 40 пацієнтів за допомогою неінвазивних методів дослідження — стеатометрії та зсувнохвильової еластометрії (ЗХЕ), у тому числі 27 хворих на НВК, 13 — на ХК. Усі хворі були розподілені на групи залежно від віку (відповідно до класифікації Всесвітньої організації охорони здоров’я: від 25 до 44 років — молодий вік, 45–59 років — середній вік). В обстеження включено 29 пацієнтів молодого та 11 пацієнтів середнього віку. Результати. Встановлено, що зміни печінки мали вікові відмінності. Так, за результатами стеатометрії печінки виявлені зміни, характерні для стеатозу печінки за шкалою NAS, у 32,5 % хворих на ХЗЗК, причому у пацієнтів середнього віку стеатоз печінки виявлявся в 1,8 раза частіше порівняно з хворими молодого віку. За даними ЗХЕ, виявлено зміни жорсткості паренхіми печінки у 14 (35 %) у хворих на ХЗЗК, у вигляді І і ІІІ стадії фіброзу — у 25 та 10 % відповідно. У пацієнтів середнього віку у 2,6 раза частіше зустрічалася І та ІІІ стадія фіброзу печінки. Висновки. Враховуючи отримані дані, хворим на ХЗЗК старшої вікової групи доцільно включати в стандарт діагностики проведення ультразвукового дослідження печінки з зсувнохвильовою еластометрією та стеатометрією, що дозволить своєчасно виявити ознаки жирового переродження печінки та визначити раціональну тактику ведення пацієнта, що буде сприяти зниженню ризику розвитку ускладнень захворювань.
Актуальность. Статья посвящена актуальной проблеме — изучению возрастных особенностей структурных изменений печени при хронических воспалительных заболеваниях кишечника (ХВЗК). Цель работы: изучить возрастные особенности структурных изменений печени при неспецифическом язвенном колите (НЯК) и болезни Крона (БК). Материалы и методы. Проведено обследование 40 пациентов с помощью неинвазивных методов исследования — стеатометрии и сдвиговолновой эластометрии (СВЭ), в том числе 27 больных НЯК, 13 — болезнью Крона. Все больные были разделены на группы в зависимости от возраста (согласно классификации Всемирной организации здравоохранения: от 25 до 44 лет — молодой возраст, 44–60 лет — средний возраст). В обследование включены 29 пациентов молодого и 11 пациентов среднего возраста. Результаты. Установлено, что изменения печени имели возрастные различия. Так, по результатам стеатометрии печени обнаружены изменения, характерные для стеатоза печени, по шкале NAS у 32,5 % больных ХВЗК, причем у пациентов среднего возраста стеатоз печени встречался в 1,8 раза чаще по сравнению с больными молодого возраста. По данным СВЭ, выявлены изменения жесткости паренхимы печени у 14 (35 %) больных воспалительными заболеваниями кишечника, в виде І и ІІІ стадии фиброза — у 25 и 10 % соответственно. У пациентов среднего возраста в 2,6 раза чаще встречалась I и III стадия фиброза печени. Выводы. Учитывая полученные данные, больным ХВЗК старшей возрастной группы целесообразно включать в стандарт диагностики проведение ультразвукового исследования печени со сдвиговолновой эластометрией и стеатометрией, что позволит своевременно выявить признаки жирового перерождения печени и определить рациональную тактику ведения пациента, будет способствовать снижению риска развития осложнений заболеваний.
Background. The article deals with the topical issue — studying age features of structural changes in the liver in chronic inflammatory bowel diseases (IBD). Our purpose was to study the age features of structural changes in the liver with ulcerative colitis and Crohn’s disease. Materials and methods. Forty patients, including 27 individuals with ulcerative colitis and 13 — with Crohn’s disease, were examined by non-invasive methods — steatometry and shear wave elastography. All patients were divided into groups depending on the age (according to the World Health Organization classification: from 25 to 44 years — young age, 44–60 years — middle age). The examination included 29 patients of young and 11 patients of middle age. Results. It was found that liver changes had age differences. Therefore, according to the results of liver steatometry, changes characteristic of hepatic steatosis on the nonalcoholic fatty liver disease activity score were observed in 32.5 % of patients with IBD, and in patients of middle age, liver steatosis was 1.8 times more frequent as compared to the persons of young age. According to shear wave elastography, changes in the stiffness of liver parenchyma were revealed in 14 (35.0 %) patients with IBD in the form of fibrosis stages I and III — in 25.0 and 10.0 % of cases, respectively. In patients of middle age, stages I and III of liver fibrosis were 2.6 times more frequent. Conclusions. Given the obtained data, for patients with IBD in the older age group, it is expedient to include into the diagnosis standard the ultrasound examination of the liver with shear wave elastography and steatometry, which will allow timely detection of signs of fatty degeneration of the liver and determine the rational management of the patient that help reduce the risk of developing complications of diseases.
Вступ
Ураження печінки є одними з найбільш частих позакишкових проявів хронічних неспецифічних захворювань кишечника та виявляються у більш ніж третини пацієнтів. Деякі патологічні стани печінки, що виникають при неспецифічному виразковому коліті (НВК) та хворобі Крона (ХК), виходять на перший план у клінічній картині цих нозологій і визначають їх подальший несприятливий прогноз [1–4]. В роботах, присвячених питанню гепатобіліарної патології при хронічних запальних захворюваннях кишечника (ХЗЗК), не існує єдиної думки щодо механізму виникнення ураження печінки у таких хворих, чітко не визначені їх нозологічні форми. Ураження печінки пов’язано не стільки з тяжкістю захворювань кишечника, скільки з їх хронічним безперервним перебігом, який супроводжується порушенням обмінних процесів [5–8].
Найчастіше у хворих на ХЗЗК виявляється стеатоз печінки, який може бути пов’язаний з синдромом –мальабсорбції, парентеральним харчуванням, використанням глюкокортикостероїдних препаратів. Можливі неалкогольний стеатогепатит, значно рідше — гранулематоз печінки, автоімунний гепатит, первинний склерозуючий холангіт, первинний біліарний цироз печінки і зовсім рідко — аденокарцинома жовчних проток [9, 10].
Останніми роками за мірою вдосконалення діагностичних методів визначається зростання захворюваності і поширеності неалкогольної жирової хвороби печінки (НАЖХП) як серед населення в цілому, так і серед пацієнтів з ХЗЗК [11]. Вважається, що стеатоз печінки, пов’язаний із запальними захворюваннями кишечника, як правило, відрізняється стабільним перебігом і сприятливим прогнозом.
Золотим стандартом діагностики НАЖХП є пункційна біопсія печінки, оскільки дозволяє провести диференціальну діагностику між різними її стадіями, оцінити стадію фіброзу або виключити інші причини ураження печінки [12]. Проте обмеженість спостереження за патологічним процесом в динаміці, а також інвазивність методу, що може стати причиною серйозних ускладнень, унеможливлюють використання біопсії в широкій клінічній практиці. Це мотивувало до пошуку нових неінвазивних методів діагностики НАЖХП. Серед інструментальних найбільш перспективними на сьогодні для визначення жорсткості паренхіми печінки є зсувнохвильова еластографія (ЗХЕ), а для оцінки ступеня стеатозу печінки — стеатометрія [12, 13].
Стеатометрія — ультразвуковий (УЗ) метод оцінки ступеня стеатозу печінки, при якому у В-режимі оцінюють звукопровідність паренхіми печінки або згасання ультразвуку за товщиною печінки в передньозадньому напрямку за критеріями М. Hamaguchi. На однаковій глибині вимірюють величину коефіцієнта затухання ультразвуку (КЗУ) у паренхімі печінки, виконують УЗ-стеатографію та стеатометрію за 2D-технологією кількісного вимірювання концентрації жирових крапель у режимі реального часу [14]. Визначення ступеня стеатозу за результатами УЗ-стеатометрії проводили за шкалою затухання ультразвуку, запропонованою M. Sasso et al. і валідизованою за морфологічною шкалою жирової інфільтрації NAS [15]:
1) S0 відповідає нормі (частка гепатоцитів з жиром становить від 0 до 5 %): від 1,0 до 2,19 дБ/см;
2) S1 відповідає легкому ступеню стеатозу (частка гепатоцитів з жиром становить 6–33 %): від 2,20 до 2,29 дБ/см;
3) S2 відповідає помірному ступеню стеатозу (частка гепатоцитів з жиром становить 34–66 %): від 2,30 до 2,90 дБ/см;
4) S3 відповідає тяжкому ступеню стеатозу (частка гепатоцитів з жиром становить > 66 %): > 2,90 дБ/см.
Еластографія — ультразвукова методика оцінки жорстко-еластичних властивостей паренхіматозних органів. Для проведення дослідження використовуються датчики для В-режиму, інформація обробляється в реальному часі. Ультразвук використовується для створення карти деформації м’яких тканин. Результат відображається на еластограмі [16–19].
Мета роботи: вивчити вікові особливості структурних змін печінки при неспецифічному виразковому коліті та хворобі Крона.
Матеріали та методи
Обстежено 40 хворих на ХЗЗК віком від 19 до 59 років, в середньому (37,85 ± 1,80) року, в тому числі 27 хворих на НВК, 13 — на ХК. У 18 випадках при НВК та 8 випадках при ХК спостерігався перебіг середнього ступеня тяжкості, у решти 9 хворих на НВК та 5 хворих на ХК хвороба мала тяжкий перебіг. Серед обстежених хворих були 23 жінки (57,5 %) та 17 чоловіків (42,5 %). Більшість пацієнтів знаходилися в молодому працездатному віці — від 25 до 50 років (65 %). Середній вік хворих на НВК був (35,70 ± 2,27) року, на ХК — (42,40 ± 3,38) року.
Усі хворі були розподілені на групи залежно від віку (відповідно до класифікації Всесвітньої організації охорони здоров’я: від 25 до 44 років — молодий вік, 45–59 років — середній вік). В обстеження включено 29 пацієнтів молодого та 11 пацієнтів середнього віку.
Хворим проводили ультразвукове дослідження паренхіми печінки В-методом з одночасною зсувнохвильовою еластографією на апараті Ultima PA Expert® (фірма «Радмир», м. Харків, Україна) датчиком конвексного формату на частотах 2–5 МГц на глибині 10–50 мм від капсули. Кількість успішних вимірювань становила не менше 3. Після чого з зазначених вимірів визначали медіану, яка характеризувала жорсткість паренхіми печінки (ЖПП) у кілопаскалях (кПа).
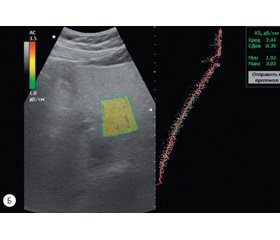
Розраховували показник інтерквартильного розмаху (IQR), що характеризує однорідність отриманих даних і є інтервалом з центром в точці медіани, в який вкладаються результати 50 % вимірів (від 25-го до 75-го квартильного значення). При цьому однорідним результат вимірювання вважався в тому випадку, якщо співвідношення IQR/медіана становив менше 30 %. Для оцінки стадії фіброзу використовували порогові значення за G. Ferraioli et al. [14, 19]: F 0–І стадія — до 6,5 кПа; F ІІ стадія — до 7,1 кПа; F ІІІ стадія — до 8,7 кПа; F ІV стадія — 10,4 і більше за шкалою МЕTAVIR (рис. 1).
Результати та обговорення
При аналізі даних стеатометрії виявлено зміни, які характерні для стеатозу печінки, за шкалою NAS у 32,5 % хворих на ХЗЗК. У 12 (30 %) пацієнтів виявлено 1 ступінь стеатозу печінки та у 1 (2,5 %) — 2 ступінь (рис. 2).
У пацієнтів середнього віку в 1,8 раза частіше виявлявся стеатоз печінки порівняно з хворими молодого віку (рис. 3).
Частота випадків S1 і S2 в групі хворих середнього віку була вищою порівняно з молодими пацієнтами (54,6 % проти 24,1 %). Звертає увагу, що виявлення стеатозу печінки у чоловіків з ХЗЗК спостерігалось в 1,6 раза частіше порівняно з жінками (41,2 проти 26,1 %) (р > 0,05).
У хворих на ХЗЗК середньовікової групи середній показник КЗУ був вірогідно вищий в 1,2 раза порівняно з групою молодого віку: (2,06 ± 0,16) проти (1,84 ± 0,03) (р < 0,05). Дані середнього значення стеатометрії печінки залежно від вікових особливостей наведені у табл. 1.
Визначення жорсткості паренхіми печінки методом ЗХЕ як маркера прогресування фіброзу у хворих на ХЗЗК залежно від віку виявило вірогідне підвищення ЖПП у хворих з ХЗЗК середнього віку порівняно з молодим в 1,2 раза: (6,17 ± 0,53) кПа проти (5,10 ± 0,19) кПа, (1,41 ± 0,06) м/с проти (1,30 ± 0,03) м/с (р < 0,05) та ХК (5,57 ± 0,31) кПа проти (4,56 ± 0,16) кПа і (1,37 ± 0,04) м/с проти (1,23 ± 0,03) м/с (р < 0,01), імовірно, за рахунок більш тривалого анамнезу хвороби, що може сприяти прогресуванню фіброзу печінки (табл. 2). Відмічалась тенденція до підвищення ЖПП у пацієнтів з НВК середньовікової групи, але без вірогідних відмінностей порівняно з хворими молодого віку.
Фіброз печінки за даними ЗХЕ виявили у 14 (35 %) хворих на ХЗЗК, із них 10 (25 %) пацієнтів мали F І та 4 (10 %) — F ІІІ. У більшої частини хворих встановлено відсутність фіброзу (F 0) за шкалою METAVIR — 26 осіб (65,5 %) (рис. 4).
У групі середнього віку в 2,6 раза частіше зустрічався фіброз печінки І та ІІІ ступенів порівняно з молодшою (45,5 проти 17,2 % та 18,2 проти 6,9 % відповідно).
Висновки
Зміни стану печінки за даними стеатометрії та зсувнохвильової еластометрії мали вікові відмінності. Так, за результатами стеатометрії печінки виявлені зміни, характерні для стеатозу печінки, за шкалою NAS у 32,5 % хворих на ХЗЗК, причому у пацієнтів середнього віку стеатоз печінки виявлявся в 1,8 раза частіше порівняно з хворими молодого віку.
За даними ЗХЕ, виявлено зміни ЖПП у 14 (35 %) у хворих на ХЗЗК, у вигляді F І та F ІІІ — у 25 та 10 % відповідно. У пацієнтів середнього віку у 2,6 раза частіше зустрічалася І і ІІІ стадія фіброзу печінки.
Враховуючи отримані дані, хворим на ХЗЗК старшої вікової групи доцільно включати в стандарт діагностики проведення УЗД печінки з зсувнохвильовою еластометрією та стеатометрією, що дозволить своєчасно виявити ознаки жирового переродження печінки та визначити раціональну тактику ведення пацієнта, яка буде сприяти зниженню ризику розвитку ускладнень захворювань.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Кушнир И.Э. Поражение печени при воспалительных заболеваниях кишечника / И.Э. Кушнир // Здоров’я України. Тематичний номер «Гастроентерологія, гепатологія, колопроктологія». — 2016. — № 2. — С. 43-45.
2. Uko V. Liver disorders in inflammatory bowel disease / V. Uko, S. Thangada, K. Radhakrishnan // Gastroenterol. Res. Pract. — 2012. — 642923. — doi: 10.1155/2012/642923. Epub 2012 Feb 15.
3. Venkatesh P.G. Hepatobiliary disorders and complications of inflammatory bowel disease / P.G. Venkatesh, U. Navaneethan, B. Shen // J. Dig. Dis. — 2011. — № 12. — С. 245-256.
4. Григорьева Г.А. Гепатобилиарные поражения при болезни крона и методы их консервативного лечения / Г.А. Григорьева, Н.Ю. Мешалкина // Экспериментальная и клиническая гастроэнтерология. — 2013. — № 6. — С. 3-6.
5. Дорофеев А.Э. Заболевания кишечника / А.Э. Дорофеев, Т.Д. Звягинцева, Н.В. Харченко. — Горлівка: Ліхтар, 2010. — 532 с.
6. Inflammatory Bowel Disease diagnostic and therapeutic stra–tegies / G. Adler, C. Fiocchi, L.B. Lazebnik, G.I. Vorobiev. — Sprin–ger, 2007. — 237 p.
7. Румянцев В.Г. Язвенный колит: руководство для врачей / B.Г. Румянцев. — М.: Медицинское информационное агентство, 2009. — 424 с.
8. Trivedi P.J. PSC, AIH and overlap syndrome in inflammatory bowel disease / P.J. Trivedi, R.W. Chapman // Clin. Res. Hepatol. Gastroenterol. — 2012. — № 36(5). — Р. 420-36. — doi: 10.1016.
9. Saich R. Primary sclerosing cholangitis, autoimmune hepatitis and overlap syndromes in inflammatory bowel disease / R. Saich, R. Chapman // World J. Gastroenterol. — 2008. — № 14(3). — Р. 331-337.
10. Дорофеев А.Э. Поражения печени у больных неспецифическим язвенным колитом / А.Э. Дорофеев, А.А. Дорофеева // Гастроентерологія. — 2017. — № 51(2). — С. 29-34.
11. Бойко Т.И. Внекишечные проявления воспалительных заболеваний кишечника / Т.И. Бойко // Новости медицины и фармации. — 2010. — № 18(323). — С. 36-39.
12. Кушнир И.Э. Внекишечные проявления хронических воспалительных заболеваний кишечника / И.Э. Кушнир // Здоров’я України. — 2007. — № 7(1). — С. 64-67.
13. McGowan C.E. Changing shape of disease: nonalcoholic fatty liver disease in Crohn’s disease-a case series and review of the literature / C.E. McGowan, P. Jones, M.D. Long, A.S. Barritt 4th // Inflamm. Bowel. Dis. — 2012. — № 18(1). — Р. 49-54.
14. Дынник О.Б. Сдвиговолновая эластография и эластометрия паренхимы печени / О.Б. Дынник, А.В. Линская, Н.Н. Кобыляк // Променева діагностика, променева терапія. — 2014. — № 1–2. — С. 73-82.
15. Controlled Attenuation Parameter (CAP): A novel VCTE guided ultrasound attenuation measurement for the evaluation of hepatic steatosis: Preliminary study and validation in a cohort with chronic liver disease from various causes / M. Sasso, M. Beaugrand, de Ledinghen [et al.] // Ultrasound in Med. and Biol. — 2010. — Vol. 36, № 11. — P. 1825-1835.
16. Зыкин Б.И. Эластография: анатомия метода / Б.И. Зыкин, Н.А. Постнова, М.Е. Медведев // Променева діагностика, променева терапія. — 2012. — № 2–3. — С. 107-113.
17. Дынник О.Б. 6 измерений ультразвуковой диагностики диффузных заболеваний печени, или мультипараметрический ультразвук / О.Б. Дынник, А.А. Федусенко, Н.Н. Кобыляк [и др.] // Променева діагностика, променева терапія. — 2016. — № 3–4. — С. 69-84.
18. Stepanov Yu.M. Steatometry and elastometry as methods of noninvasive diagnostics of pancreatic steatosis and fibrosis in children / Yu.M. Stepanov, N.H. Gravirovska, O.Yu. Lukianenko // Gastroenterology. — 2017. — № 2(51). — Р. 20-24.
19. Ferraioli G. Point shear wave elastography method for assessing liver stiffness / G. Ferraioli, C. Tinelli, R. Lissandrin [et al.] // World J. Gastroenterol. — 2014. — Vol. 20(16). — P. 4787-4796.

/37-1.jpg)
/38-1.jpg)