Резюме
Попередньо було проведено ретроспективний аналіз результатів хірургічного лікування варикозної хвороби нижніх кінцівок у системі малої підшкірної вени (МПВ) на базі відділення судинної хірургії ЗОЗ «4-та міська клінічна лікарня імені М.Є. Савченка» м. Мінська за 2009–2014 рр. Виявлено, що при класичній флебектомії у 13,9 % пацієнтів кросектомія МПВ виконана з залишенням кукси 20–35 мм. У 13,5 % МПВ видалена до підколінної складки, але далі продовжувалась на стегно як проксимальна гілка або вена Джіакоміні з рефлюксом за останньою. У 23,6 % МПВ видалена до середньої третини гомілки, у 8,1 % — до верхньої третини гомілки. У 40,9 % пацієнтів МПВ видалена на всьому протязі. Наведено клінічний аналіз двох випадків ускладнень після флебектомії в системі малої підшкірної вени: пацієнт з тромбофлебітом кукси МПВ і флотацією тромбу в підколінну вену і пацієнт з артеріовенозною фістулою підколінної області. Викладені симптоматика, клінічний перебіг даних видів ускладнень, методи діагностики, профілактики венозного тромбоемболізму і хронічної серцевої недостатності.
Предварительно был проведен ретроспективный анализ результатов хирургического лечения варикозной болезни нижних конечностей в системе малой подкожной вены (МПВ) на базе отделения сосудистой хирургии УЗ «4-я городская клиническая больница имени Н.Е. Савченко» г. Минска за 2009–2014 гг. Выявлено, что при классической флебэктомии у 13,9 % пациентов кроссэктомия МПВ выполнена с оставлением культи 20–35 мм. У 13,5 % МПВ удалена до подколенной складки, но далее продолжалась на бедро как проксимальная ветвь или вена Джиакомини с рефлюксом по последней. У 23,6 % МПВ удалена до средней трети голени, у 8,1 % — до высшей трети голени. У 40,9 % пациентов МПВ удалена на всем протяжении. Представлен клинический анализ двух случаев осложнений после флебэктомии в системе малой подкожной вены: пациент с тромбофлебитом культи МПВ и флотацией тромба в подколенную вену и пациент с артериовенозной фистулой подколенной области. Изложены симптоматика, клиническое течение данных видов осложнений, методы диагностики, профилактики венозного тромбоэмболизма и хронической сердечной недостаточности.
Previously, we have performed the retrospective analysis based on the results of surgical treatment of varicose veins of the lower limbs in the system of the small saphenous vein (SSV) at the premises of vascular surgery department of N.E. Savchenko City Clinical Hospital 4 (Minsk) for 2009–2014. In 13.9 % of patients who underwent “classical” phlebectomy SSV crossectomy was performed leaving a stump of 20–35 mm. 13.5 % of patients had SSV removed to popliteal line, but it extended to the hip as a proximal brunch or Giacomini vein with reflux at the latter. 23.6 % of patients had SSV removed to the middle third of the tibia; 8.1 % — to the upper third of the tibia. 40.9 % of patients had SSV removed completely. A clinical analysis is performed of two cases of complications after phlebectomy in the small saphenous vein system: a patient with thrombophlebitis of the SSV stump and thrombus floating in the popliteal vein, and a patient with arteriovenous fistula of the popliteal region. The symptoms, clinical picture, diagnostic methods, prevention of venous thromboembolism and chronic heart failure are described.
Введение
Острый тромбофлебит нижних конечностей — частое острое сосудистое заболевание, характеризующееся образованием тромботических масс в просвете подкожных вен, что является потенциальным риском таких серьезных венозных тромбоэмболических осложнений, как тромбоз глубоких вен и тромбоэмболия легочной артерии (ТЭЛА). ТЭЛА — вторая по частоте причина смерти у лиц до 40 лет после несчастных случаев и третья в общей популяции после ишемической болезни сердца и острого нарушения мозгового кровообращения [1].
Тромбоз глубоких вен при тромбофлебите нижних конечностей встречается у 70 % пациентов, а при тромбофлебите малой подкожной вены (МПВ) — у 34 % [2], бессимптомная ТЭЛА — у 20–33 % пациентов и в 2–13 % случаев выявляется симптоматическая ТЭЛА [3, 4].
Несостоятельность МПВ выявляется у 20 % пациентов с варикозной болезнью нижних конечностей [5]. Флебэктомия в системе МПВ считается более сложным хирургическим вмешательством, чем на большой подкожной вене, и связана с более высоким числом рецидивов и частотой осложнений [6]. Учитывая анатомическое разнообразие сафено-поплитеального соустья, даже несмотря на пред–операционное ультразвуковое картирование данной области, адекватная интраоперационная идентификация сафено-поплитеального соустья осуществляется не всегда адекватно [7].
Тромбозы глубоких вен после оперативных вмешательств при варикозной болезни нижних конечностей довольно редки (от 0 до 1,2 %), но по-прежнему встречаются в практике и остаются наиболее значимым осложнением после оперативного вмешательства [8].
Приобретенные артериовенозные фистулы наиболее часто формируются вследствие проникающих ранений и повреждений сосудов. Ятрогенные артериовенозные фистулы описаны после выполнения различных медицинских манипуляций (катетеризация сосудов), ортопедических операций, чрескожной биопсии органов (например, печени, почек), эмболэктомии с использованием катетера Фогарти [9–11]. Длительно существующая артериовенозная фистула может приводить к развитию хронической сердечной недостаточности вследствие объемной перегрузки правых отделов сердца, увеличению преднагрузки, следовательно, к развитию гипертрофии левого желудочка и ремоделированию мио–карда левого желудочка. Основными факторами развития хронической сердечной недостаточности являются диаметр фистулы (соустья), его локализация и длительность заболевания [12, 13].
Цель работы: оценить отдаленные результаты после классической флебэктомии в системе МПВ.
Материалы и методы
Был проведен ретроспективный анализ результатов хирургического лечения варикозной болезни нижних конечностей в системе МПВ на базе отделения сосудистой хирургии учреждения здраво–охранения «4-я ГКБ им. Н.Е. Савченко» г. Минска за 2009–2014 гг. Установлено, что лишь у 40,9 % осмотренных пациентов МПВ удалена оптимально на всем протяжении до сафено-поплитеального соустья (табл. 1).
У всех пациентов было получено информированное согласие на участие в исследовании согласно Хельсинкской декларации Всемирной медицинской ассоциации (WMA Declaration of Helsinki — Ethical Principles for Medical Research Invol–ving Human Subjects, 2013). Исследование одобрено комиссией по вопросам биоэтики учреждения здравоохранения «4-я городская клиническая больница им. Н.Е. Савченко» г. Минска.
Результаты
При проведении ретроспективного анализа выявлено два существенных осложнения после флеб–эктомии по Бэбкокку в системе МПВ.
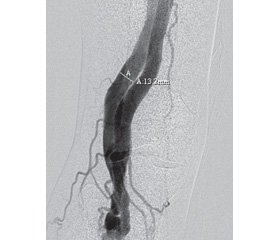
Клинический случай 1. Женщина, 53 года. Из анамнеза установлено: в течение 5 дней беспокоили отек, боль в левой голени, усиливающаяся при нагрузке. При ультразвуковом исследовании вен нижних конечностей у пациентки выявлено: культя МПВ слева диаметром 8 мм, длиной 30 мм, тромбирована. Тромботические массы распространялись в подколенную вену на 13 мм с флотацией тромба. Фрагмент флотирующего участка — 27 мм (рис. 1).
В этот же день по экстренным показаниям с целью предупреждения ТЭЛА выполнена пликация поверхностной бедренной вены.
В раннем послеоперационном периоде пациентка получала раствор надропарина кальция в лечебной дозировке 5 дней, затем переведена на прием дабигатрана этексилата в лечебной дозировке постоянно и ношение компрессионного трикотажа 2-го класса компрессии.
Через 6 месяцев после операции при ультразвуковом исследовании вен нижних конечностей отмечена частичная реканализация культи МПВ слева, глубокие вены проходимы, рефлюкса нет. Пациентка отмечала отсутствие отека левой нижней конечности и исчезновение болей при нагрузке. Пациентка продолжала прием дабигатрана этексилата 150 мг 2 раза в день в течение 6 месяцев после оперативного лечения, венотоников, содержащих в составе диосмин и гесперидин, и ношение компрессионного трикотажа 2-го класса компрессии.
При ультразвуковом контроле вен нижних конечностей через 18 месяцев отмечалась полная реканализация культи МПВ слева, глубокие вены и зона пликации поверхностной бедренной вены проходимы, отека левой нижней конечности нет.
Клинический случай 2. Мужчина, 62 года. Из анамнеза отмечено: в течение года беспокоили чувство тяжести, периодические отеки правой голени. При объективном осмотре правая голень была увеличена в объеме, окружность ее была больше на 2 см по сравнению с левой. При пальпации подколенной области определялось систолическое дрожание, при аускультации выслушивался непрерывный сосудистый шум, усиливающийся во время систолы. Точка максимальной интенсивности шума находилась на 1 см ниже подколенной складки (область после–операционного рубца). Выполнено ультразвуковое исследование вен и артерий нижних конечностей: артериовенозная фистула подколенной артерии и подколенной вены справа; состояние после флеб–эктомии МПВ (рис. 2).
/150-2.jpg)
Пациент госпитализирован с диагнозом «артериовенозная фистула правой подколенной области». Выполнены общеклинические обследования, эхокардиография (миокард не утолщен, сократительная функция левого желудочка не нарушена, давление в легочной артерии в норме), артериография правой нижней конечности: поверхностная бедренная артерия — контур четкий, ровный, без стенозирования, диаметр 10–11 мм; подколенная артерия — контур ровный, диаметр 8–10 мм, фистула с подколенной веной; передняя большеберцовая, межберцовые артерии не визуализируются, задняя большеберцовая артерия — слабое заполнение, визуализируется на всем протяжении, без значимого стенозирования (рис. 3).
Выполнено оперативное лечение: разобщение артериовенозной фистулы правой подколенной области.
В послеоперационном периоде пациент получал раствор надропарина кальция в профилактической дозировке 7 дней.
Через 7 дней выполнено контрольное ультразвуковое исследование магистральных артерий и вен нижних конечностей: состояние после разобщения артериовенозной фистулы правой подколенной области, неокклюзирующий тромбоз суральной вены, без убедительных признаков флотации.
На амбулаторном этапе пациент принимал варфарин в лечебной дозировке и осуществлял ношение компрессионного трикотажа 2-го класса компрессии.
Через три месяца было выполнено ультразвуковое исследование магистральных артерий и вен нижних конечностей: признаки перенесенного флеботромбоза подколенно-берцового сегмента справа с частичной реканализацией и умеренной клапанной недостаточностью, и компьютерная артериография: расширение общей и поверхностной бедренных артерий, подколенной артерии справа. Артериовенозных фистул не выявлено.
Пациент отмечал отсутствие отека левой нижней конечности и исчезновение тяжести при нагрузке. Продолжил принимать варфарин в лечебной дозировке в течение 3 месяцев после оперативного лечения, венотоники, содержащие в составе диосмин и гесперидин, и ношение компрессионного трикотажа 2-го класса компрессии.
Обсуждение
Большинство артериовенозных фистул являются бессимптомными и обнаруживаются случайно [14]. Вероятнее всего, причиной артериовенозной фистулы явилось ранее перенесенное оперативное вмешательство в подколенной ямке. На современном этапе лечения данных поражений сосудов предпочтение отдается эндоваскулярным вмешательствам ввиду меньшей травматичности. Учитывая расположение артериовенозной фистулы в рубцовой ткани, вследствие проведенного хирургического вмешательства риск интраоперационного массивного кровотечения и повреждения прилегающих нервов возрастает в несколько раз в связи с наличием сети компенсаторных коллатералей и нарушений анатомо-топографического расположения сосудисто-нервного пучка [14, 15]. Однако в данном клиническом случае открытое хирургическое вмешательство явилось более предпочтительным ввиду расположения артериовенозной фистулы в области крупного сустава и наличия широкого дефекта артериовенозного соустья. Во время оперативного вмешательства наблюдался выраженный рубцовый процесс в послеоперационной области. Развитая сеть коллатералей и неоваскулогенеза потребовали тщательного гемостаза. В результате с техническими трудностями удалось лигировать артериовенозную фистулу, не прибегая к дополнительным реконструкциям на артериальной и венозной системе подколенной области.
В ходе ретроспективного анализа результатов флебэктомии МПВ по Бэбкокку установлено (клинически и с помощью ультразвукового обследования), что кроссэктомия МПВ выполнена оптимально менее чем у 50 % пациентов. Данный результат является следствием большой вариабельности строения сафено-поплитеального соустья и стремления хирургов выполнить оперативное вмешательство мини-инвазивно, что не всегда позволяет надлежащим образом визуализировать сафено-поплитеальное соустье и его притоки. В конечном итоге малотравматичный доступ приводит к неадекватному лигированию сафено-поплитеального соустья, оставлению части ствола МПВ и развитию столь грозных осложнений, как тромбоз культи с угрозой ТЭЛА и формирование артериовенозной фистулы, способствующей развитию хронической сердечной недостаточности.
Выводы
Классическая флебэтомия является распространенным методом лечения варикозной болезни нижних конечностей. Однако эффективность данного вмешательства, в частности при удалении МПВ, является недостаточной. Лишь у 41 % пациентов флебэктомия МПВ выполнена оптимально. У остальной части пациентов выявлены ультразвуковые признаки длинной культи или части ствола МПВ, что может привести к рецидиву и редким, но грозным осложнениям.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи. Финансовой поддержки со стороны компаний-производителей лекарственных препаратов авторы не получали.
Список литературы
1. Баешко А.А. Послеоперационный тромбоз глубоких вен нижних конечностей и тромбоэмболия легочной артерии: Эпидемиология. Этиопатогенез. Профилактика. — М.: Триада-Х, 2000. — 136 с.
2. Сабадош Р.В. Роль малой подкожной вены в развитии тромбоза глубоких вен при остром варикотромбофлебите нижних конечностей // Новости хирургии. — 2014. — Т. 22, № 2. — С. 184-190.
3. Decousus H. еt al. POST (Prospective Observational Thrombophlebitis) Study Group. Superficial venous thrombosis and Venous thromboembolism: a large, prospective epidemiologic study // Ann. Intern. Med. — 2010. — 152. — Р. 218-24.
4. Galanaud J.-P. et al. Predictive factors for concureent deep-vein thrombosis and symptomatic venous thromboembolic recurrence in case of superficial vein thrombosis. The OPTIMEV study // Thromb. Haemost. — 2011. — 105. — Р. 31-9.
5. Tellings S.S., Ceulen R.P., Sommer A. Surgery and endovenous techniques for the treatment of small saphenous varicose veins: a review of the literature // Phlebology. — 2011. — № 26(5). — Р. 179-84.
6. Perrin M.R., Labropoulos N., Leon L.R. Jr. Presentation of the patient with recurrent varices after surgery (REVAS) // J. Vasc. Surg. — 2006. — 43. — Р. 327-34.
7. Золотухин И.А. Физикальное определение состояния проксимального отдела малой подкожной вены // Флебология. — 2008. — 1. — 77.
8. Boersma D., Kornmann V.N., van Eekeren R.R., Tromp E., Ünlü Ç., Reijnen M.M., de Vries J.P. Treatment Modalities for Small Saphenous Vein Insufficiency: Systematic Review and Meta-analysis // Journal of Endovascular Therapy. — 2016 Feb. — № 23(1). — Р. 199-211.
9. Lee C.H. Stent graft repair of iatrogenic femoral arteriovenous fistula with acute bleeding after hemodialysis catheter insertion // Hemodial. Int. — 2016 Oct. — № 20(4). — Р. 497-500. — doi: 10.1111/hdi.12431. Epub 2016 May 5.
10. Wooster B.M., Grimm N.L., DeOrio J.K., Mithani S.K. Iatrogenic Arteriovenous Fistula With Associated Pseudoaneurysm of Posterior Tibial Artery After Revision Total Ankle Arthroplasty: A Case Report // J. Foot Ankle Surg. — 2017 Jan-Feb. — № 56(1). — Р. 75-77. — doi: 10.1053/j.jfas.2016.09.014.
11. Kurian J. Mylankal, Brian Johnson and Duncan F. Ettles. Iatrogenic Arteriovenous Fistula as a Cause for Leg Ulcers: A Case Report // Ann. Vasc. Dis. — 2011. — № 4(2). — Р. 139-142.
12. Thavarajan D., Bakran A. Iatrogenic arteriovenous fistula in the groin presenting as cardiac failure // NDT Plus. — 2009 Feb. — № 2(1). — Р. 46-8. — doi: 10.1093/ndtplus/sfn190. Epub 2008 Dec 15.
13. Чернуха Л.М., Никульников П.И., Каширова Е.В., Влайков Г.Г., Альтман И.В., Гуч А.А., Матящук А.С. Посттравматические артериовенозные фистулы. Опыт лечения // Новости хирургии. — 2011. — № 19(3). — С. 63-69.
14. Suknaic S., Erdelez L., Skopljanac A., Sef D., Novacic K. Chronic ischaemic leg ulcer as a late complication of post-traumatic arteriovenous fistula // Phlebology. — 2012. — 27. — Р. 124-127.
15. Tetik O., Ergunes K., Yurekli I. et al. Surgical treatment of a giant external-iliac-vein aneurysm in a patient with a post-traumatic femoral arteriovenous fistula // Tex. Heart Inst. J. — 2011. — 38. — Р. 187-190.

/150-1.jpg)
/150-2.jpg)
/151-1.jpg)