Вступ
Задньобічний поперековий спондилодез є одним з ефективних методів хірургічного лікування дегенеративних захворювань хребта. Водночас відсутність кісткового зрощення в зоні спондилодезу реєструється в 5–35 % спостережень [1, 2], а в деяких випадках біомеханічно ідеальна фіксація не забезпечує формування кісткового блока [3, 4]. Це спонукає до створення нових біоматеріалів, які покращують остеогенні, остеоіндуктивні й остеокондуктивні властивості кістковопластичних матеріалів, що застосовують у хірургії хребта і прискорюють репаративні процеси в зоні спондилодезу.
Мета роботи: дослідити формування кісткового зрощення за умов експериментального задньобічного спондилодезу з використанням кісткових ало- та місцевих автотрансплантатів та збагаченого тромбоцитами автологічного фібрину.
Матеріали та методи
Експерименти виконано на 42 статевозрілих самцях кролів (віком 4–5 міс. на початку експерименту) із дотриманням вимог Європейської конвенції про захист хребетних тварин, яких використовують для дослідних та інших наукових цілей, і вимог закону України «Про захист тварин від жорстокого поводження» [5] після ухвалення комітетом з біоетики при ДУ «ІПХС ім. проф. М.І. Ситенка НАМН» (протокол № 151 від 18.01.2016).
Хірургічні втручання проводили в умовах асептики в операційній експериментально-біологічної клініки під внутрішньовенною анестезією комбінацією препаратів ксилазину (5 мг/кг) і кетаміну (35 мг/кг). У процесі виконання міжпоперечного спондилодезу всім кролям виконували двобічну декортикацію поперечних відростків тіл хребців LIV та LV, на яких медіально розміщували трансплантаційний матеріал залежно від групи експерименту (по 7 кролів у кожній): 2 — автотранс-плантати, 3 — автотрансплантати в поєднанні зі збагаченим тромбоцитами фібрином (platelet rich fibrin, PRF), 4 — алотрансплантати з крила клубової кістки, 5 — алотрансплантати з крила клубової кістки в поєднанні з PRF, 6 — PRF. У тварин контрольної групи 1 трансплантати не використовували. Кролів виводили з експерименту через 8 тижнів після операції шляхом введення летальної дози тіопенталу натрію (90 мг/кг).
Місцеві кісткові автотрансплантати являли собою фрагменти резектованих інтраопераційно остистих відростків LIV і LV хребців (на рівні спондилодезу).
Ліофілізовані алотрансплантати, отримані з гребеня клубової кістки виведених з експерименту кролів, підготовлені на базі відділення трансплантології ДУ «ІПХС ім. проф. М.І. Ситенка НАМН», зареєстрованого МОЗ України (сертифікат № UA.TR. 101-06/ПП-2015 від 30.11.2015).
Підготовлені для спондилодезу авто- і алотрансплантати являли собою кірково-спонгіозні кісткові фрагменти розмірами 0,1–0,2 см на 0,1–0,5 см; кожному кролю імплантували 2 г авто- або алокістки. Вибір розміру трансплантатів обумовлений тим, що дрібніші кісткові фрагменти утворюють більш гомогенні спондилодезні маси, швидше досягаючи біомеханічної зрілості [6].
PRF отримували безпосередньо перед операцією: кров з вушної вени кроля в кількості 7,0 мл забирали в пробірку без коагулянту та негайного центрифугували зі швидкістю 3000 обертів на 1 хвилину (приблизно 400 g) протягом 10 хв. Отримані 3,0 мл збагаченого тромбоцитами автологичного фібрину ділили на 2 пор-ції по 1,5 мл для виконання двостороннього задньобічного спондилодезу.
Для гістологічного дослідження виділяли фрагменти поперекового відділу хребта (LIV та LV). Матеріал фіксували у 10% розчині нейтрального формаліну, декальцинували в 10% розчині мурашиної кислоти, зневоднювали в спиртах висхідної концентрації та заливали в целоїдин [7]. Гістологічні зрізи виготовляли на санному мікротомі Reichert, забарвлювали гематоксиліном Вейгерта й еозином, а також пікрофуксином за Ван Гізоном. Аналізували гістологічні препарати у світловому мікроскопі BX-63 (Olympus, Японія). Для фотографування використано цифрову фотокамеру DP73 (Olympus) та програмне забезпечення Cell Sens Dimention 1.8.1 (Olympus, 2013).
Морфометричні дослідження виконували лише в тих випадках, коли клінічно та рентгенологічно було встановлено утворення кісткового блока (хоча б з одного боку хребта). Напівкількісне оцінювання якості спондилодезу виконували два незалежних морфологи. Від кожної тварини аналізували по 5 сагітальних зрізів на рівні поперечних відростків з обох боків поперекового відділу хребта у мікроскопі Olympus BX-63 (Японія) з об’єктивом ×2. Визначали якість утвореного спондилодезу з наданням балів залежно від виявлених у цій зоні тканин (окремо кісткової, хрящової та сполучної — загалом) за A.R. Gezici і співавт. [8] у власній модифікації. Найбільшу кількість балів (4) надавали, якщо в зоні спондилодезу утворилася лише кісткова тканина, найменшу (0) — коли її не спостерігали. Переважання кісткової тканини над сполучною та хондроїдом відповідало 3 балам, дорівнювання цих тканин — 2, менший вміст кісткової тканини — 1.
Ширину регенерату, який утворився між попереч-ними відростками вздовж двох суміжних каудально та краніально розташованих тіл хребців, вимірювали за допомогою програмного забезпечення Cell Sens Dimention 1.8.1 (Olympus, 2013) для мікроскопа Olympus ВХ63.
Статистичний аналіз. Отримані числові показники обробляли за допомогою прикладної програми IBM SPSS Statistics 20.0.0.2. Результати подавали у вигляді M ± m, де М — середнє значення, m — похибка середнього арифметичного. Визначали значущість відмінностей між групами з використанням апостеріорного тесту Дункана. Рівень значущості прийнятий p < 0,05.
Результати
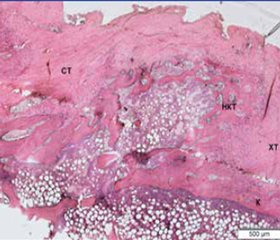
Гістологічні дослідження. У кролів групи 1 (конт-роль) у зоні спондилодезу спостерігали розростання пластинчастої кісткової тканини у вигляді нашарувань потовщених кісткових трабекул на поперечних відростках. Проте формування з’єднання ані між відростками, ані між тілами хребців не виявлено (рис. 1).
У кролів, яким при виконанні поперекового міжпоперечного спондилодезу як кістково-пластичний матеріал були використані автотрансплантати (самостійно або в комбінації з PRF — групи 2 та 3 відповідно), у зоні спондилодезу визначали фіброретикулярну, хрящову, сполучну та кісткову тканини із переважанням кісткової пластинчастої. На поверхні новоутворених кісткових трабекул містилися яскраво забарвлені остеоцити, а за периметром — функціонально активні остеобласти. Щільність і товщина зазначених трабекул була більшою порівняно з тими, що розташовувалися в тілі хребця. У міжтрабекулярних просторах виявлено червоний і жовтий кістковий мозок.
У кролів, яким як остеопластичний матеріал використано автотрансплантати в поєднанні з PRF (група 3), у зоні спондилодезу відмічено формування компактної кісткової тканини з судинними каналами різного діаметра, що відображує більшу зрілість кісткового регенерату.
Автотрансплантати у вигляді відокремлених невеликих фрагментів кісткового матриксу без остеоцитів розташовувалися між тканинами регенерату. Кісткова тканина формувалася безпосередньо на їх поверхні, межу між цими структурами простежували за наявністю різкого базофільного забарвлення по крайовій поверхні автотрансплантатів. На незначних територіях навколо них спостерігали щільну сполучну тканину (рис. 2).
Слід зазначити, що процес перебудови автотранс-плантатів ще тривав. На їх крайовій поверхні визначено резорбційні порожнини — порожні та такі, де містилися остеокласти, які беруть безпосередню участь у руйнуванні кісткового матриксу. Між новоутвореною кістковою тканиною та автотрансплантатом у цих зонах виявляли тонкий прошарок фіброретикулярної тканини остеогенного типу зі значною кількістю кровоносних капілярів, клітин остеобластичного та фібробластичного диферонів (рис. 3). Це дає змогу припустити заміщення автотрансплантаів кістковою тканиною в подальшому.
Вогнища сполучної тканини в ділянці спондилодезу складалися зі щільних пучків колагенових волокон, спрямованих паралельно осі новоутворених кісткових трабекул. Між ними спостерігали кровоносні судини та фібробласти з подовженою цитоплазмою та великим гіпохромним ядром.
У кролів, яким під час виконання поперекового міжпоперечного спондилодезу використовували алотранс-плантати самостійно або в поєднанні з PRF (групи 4 та 5 відповідно), під час мікроскопічного дослідження між поперечними відростками виявлено регенерат, представлений кістковою, фіброретикулярною, сполучною та хрящовою тканинами (рис. 4).
Новоутворена кісткова тканина була пластинчастої структури і побудована з кісткових трабекул різної ширини. Наявність на їх крайовій поверхні функціонально активних остеобластів характерної структури, як і у випадку застосування автотрансплантатів, відображувала активність репаративного остеогенезу. Також кісткові трабекули безпосередньо контактували з остеопластичним матеріалом.
У центральних ділянках регенерату містилися осередки сполучної тканини різного ступеня зрілості. Щільність клітин фібробластичного диферону в цій ділянці була високою. Найменшу територію займала хрящова тканина, осередки якої виявлено в товщі сполучної. Вона характеризувалася незначною базофілією матриксу та значною кількістю хондробластів круглястої форми.
Фрагменти алотрансплантатів різного розміру розподілялися по всій досліджуваній зоні. Деякі з них були оточені сполучною тканиною, інші — щільно з’єднані з кістковими трабекулами. На поверхні фрагментів алотрансплантатів, розташованих у кістковій тканині, відмічено остеокласти, що свідчить про їх резорбцію, та нашарування остеоїду. Крім того, зафіксовано проростання в них кровоносних судин, що також є ознакою перебудови алотранс-плантатів (рис. 5).
У групі тварин, у яких як остеопластичний матеріал використано PRF, мікроскопічно між поперечними відростками вздовж кортексу суміжних тіл хребців виявляли утворення регенерату, який складався з кісткової тканини, розташованої переважно поблизу материнської кістки та з’єднаної з нею, осередків хрящової та сполучної тканин. Новоутворена кісткова тканина за структурою була порівнянна з кістковою тканиною тіла хребця. Її кісткові трабекули характеризувались значною щільністю остеоцитів та функціонально активних остеобластів; міжтрабекулярні простори були заповнені червоним і жовтим кістковим мозком. Між кістковими трабекулами розміщувалася новоутворена щільна сполучна тканина, яка містила розширені судини, значну кількість клітин фібробластичного диферону. Крім того, у регенераті візуалізували осередки хрящової тканини з високою щільністю клітин, у неї проростали кровоносні капіляри, навколо яких формувалася кісткова тканина (рис. 6).
/18-2.jpg)
Морфометричний аналіз. Визначено, що найменше кісткової тканині в ділянці спондилодезу утворилось у випадку використання PRF самостійно. Показник за напівкількісною гістологічною шкалою, де максимальна кількість балів (4) відповідала наявності лише кісткової тканини в регенераті, у цих тварин виявився вірогідно (р < 0,001) меншим порівняно з іншими групами експерименту: застосування алотрансплантатів — в 1,78 раза, алотрансплантатів у поєднанні з PRF — в 1,89; автотрансплантатів самостійно або з PRF — у 2,06. Найбільше новоутвореної кісткової тканини зафіксовано, відповідно, у разі застосування кісткових автотрансплантатів самостійно або з PRF. Переважання в ділянці спондилодезу кісткової тканини дає змогу стверджувати про вищі характеристики міцності зони зрощення в такому випадку (табл. 1).
/19-1.jpg)
Ширина зони спондилодезу також варіювала в групах кролів (табл. 2). Найширший регенерат виявлено у випадку використання автотрансплантатів у поєднанні з PRF: в 1,9 раза порівняно з PRF самостійно, в 1,14–1,16 — порівняно з іншими групами (р < 0,001). Відповідно, найменшу ширину регенерату, як і найменшу кількість кісткової тканини в ньому, визначено в разі застосування лише PRF.
Таким чином, у результаті морфологічного дослідження встановлено формування регенерату, який розташовувався між поперечними відростками та з’єднував суміжні тіла хребців, у всіх тварин, де використано остеопластичні матеріали. За складом усі регенерати були однотипними — містили пластинчасту кісткову, сполучну та хрящову тканини. У кролів контрольної групи визначено розростання кісткової тканини поперечних відростків унаслідок їх декортикації, проте з’єднання ані між ними, ані між тілами суміжних хребців не відбулося.
Якість утвореного регенерату залежала від використаного для пластики матеріалу. Зокрема, найбільшу кількість кісткової тканини спостерігали у разі застосування кісткових автотрансплантатів самостійно або в поєднанні з PRF. При цьому слід зазначити, що в кролів, яким як остеопластичний матеріал використано автотрансплантати в поєднанні з PRF, у зоні спондилодезу відмічено формування компактної кісткової тканини з судинними каналами різного діаметру, що відображує більшу зрілість кісткового регенерату. Міцність утвореного між тілами хребців з’єднання у випадку застосування автотрансплантатів самостійно або з PRF підвищувала також односпрямованість пучків колагенових волокон у новоутвореній сполучній тканині та кісткових трабекул — у кістковій.
На якість утвореного спондилодезу також впливає ширина регенерату, оскільки недостатня міцність зновсформованих тканин на ранніх етапах компенсується їх значним обсягом. Найширший регенерат виявлено у випадку використання автотрансплантатів у поєднанні з PRF порівняно з іншими групами (р < 0,001). Відповідно, найменшу ширину регенерату, як і найменшу кількість кісткової тканини в ньому, визначено в разі застосування лише PRF.
Ало- та автотрансплантати, які використано в експерименті, повністю не заміщувалися новоутвореними тканинами, а процес їх перебудови тривав.
Найменше кісткової тканини, як і найменший за шириною регенерат, у ділянці спондилодезу утворилось у випадку використання PRF самостійно.
Обговорення
Одним із найчастіше використовуваних кістково-пластичних матеріалів у хірургії хребта є ало- та місцеві автотрансплантати. Місцеві автотрансплантати є кращим біоматеріалом, оскільки містять мезенхімальні стовбурові, остеопрогеніторні й остеогенні клітини [9, 10], остеоіндуктивні білки [11]. Завдяки значній кількості мезенхімальних стовбурових клітин автотранс-плантати зберігають остеогенний потенціал, незважаючи на ішемію, яка розвивається після їх вилучення [12]. Цим можна пояснити, що в нашому дослідженні найбільшу кількість кісткової тканини в зоні спондилодезу ми спостерігали у разі застосування кісткових автотрансплантатів самостійно або в поєднанні з PRF. Використання автотрансплантатів не спричинює імунних реакцій, що сприяє його вростанню в кістку реціпієнта [13], а їх отримання не призводить до хвороби донорського кісткового ложа [14]. Одним із суттєвих недоліків місцевих автотрансплантатів є їх недостатній обсяг, особливо в разі полісегментарного спондилодезу [15, 16], що може уповільнювати формування кісткового блоку або призводити до незрощення [17].
Алотрансплантати мають певні остеоіндуктивні й остеокондуктивні властивості, але їх остеогенний потенціал нижчий порівняно з автотрансплантатами [18]. Крім того, у випадку використання кісткових алотрансплантатів є ризик трансмісії бактеріальної інфекції та вірусних захворювань (ВІЛ, гепатити В і С), виникнення імунологічних реакцій аж до відторгнення трансплантата [19, 20]. Точний механізм імунної відповіді кісткової тканини реципієнта невідомий. Вважають, що він ініціюється активацією антигенів гістосумісності [21]. Для зниження зазначених ризиків трансплантації застосовують свіжозаморожені та ліофілізовані кісткові алотрансплантати, які додатково обробляють гамма-опроміненням, етиленоксидом або гіпотонічним розчином. Проте вказане опрацювання погіршує остеокондуктивні й остеоіндуктивні характеристики та суттєво обмежує остеогенні властивості ліофілізованих алотрансплантатів [9], пролонгуючи репаративні процеси [22]. Зазначене знайшло відображення й в отриманих нами результатах: у випадку застосування алотрансплантатів зафіксовано в 1,15 раза менше (p < 0,01) кісткової тканини в зоні спондилодезу порівняно з використанням автотрансплантатів. Крім цього, у процесі ліофілізації знижується механічна міцність алотрансплантата [22], що може призводити до зниження опороспроможності оперованого сегмента, надлишкової його рухомості з розвитком псевдоартрозу.
Підвищення остеогенного потенціалу кісткових ало- та місцевих автотрансплантатів може бути досягнуто шляхом поєднаного їх застосування зі збагаченим тромбоцитами автологічним фібрином. За даними P.M. Sethi і співавт. [24], за умов обмеженого обсягу автотрансплантата застосування PRF дозволяє поліпшити біомеханічні властивості спондилодезованого сегмента, причому частота спондилодезу, який визначено біомеханічно та візуалізовано на рентгенограмах, корелювала в 70 % спостережень. Поєднання PRF з ліофілізованим кістковим алотрансплантатом підвищує механічну міцність біоматеріалу, прискорює клітинну міграцію та проліферацію в фібриновому матриксі [24] зі збільшенням тривалості життя тромбоцитарних цитокінів [25], стимулюючи репаративні процеси в зоні спондилодезу. У наведеній роботі в ділянці поперекового міжпоперечного спондилодезу найбільше новоутвореної кісткової тканини та найбільший за обсягом регенерат зафіксовано в разі застосування кісткових авто- ті алотрансплантатів у поєднанні з PRF.
Остеокондуктивні й остеоіндуктивні властивості PRF пов’язані з архітектонікою фібринового матриксу. Останній являє собою гнучку та міцну тривимірну мережу [26], яка містить значну кількість тромбоцитарних і лейкоцитарних цитокінів, які поступово вивільняються [27] і здатні стимулювати клітинну міграцію та проліферацію в матриксі фібрину, ініціюючи неоангіогенез і васкуляризацію трансплантата, забезпечуючи його виживання [25, 28]. У фібриновому каркасі прискорюється диференціація мезенхімальних стовбурових клітин [29], що разом із постійним вивільненням факторів росту сприяє процесу регенерації тканин [30]. Кісткові морфогенетичні білки, які містяться в PRF, мають ангіогенні й остекондуктивні властивості [31]. Наявність лейкоцитарних цитокінів у PRF потенціює пригнічення інфекційних і запальних процесів у післяопераційній рані [30]. У результаті експериментального дослідження встановлено, що введення в дірчастий дефект тіла хребця кролів збагаченого тромбоцитами фібрину сприяє прискоренню кісткоутворення через 14 діб та 1 міс. після травми [32]. Проте в цій роботі ми виявили найменшу кількість кісткової тканини в зоні спондилодезу в разі застосування лише PRF порівняно з використанням інших остеопластичних матеріалав, що, імовірно, пов’язано з недостатнім об’ємом PRF і відсутністю його обмеження кістковою тканиною.
Висновки
Використання пластичних матеріалів (PRF, ало- та автотрансплантати самостійно й у поєднанні з PRF) під час поперекового міжпоперечного спондилодезу сприяло формуванню зони зрощення на рівні операції.
Найбільше новоутвореної кісткової тканини в зоні спондилодеза зафіксовано у разі застосування кісткових автотрансплантатів самостійно або з PRF (3,70 ± 0,06 бала) та кісткових алотрансплантатів у поєднанні з PRF (3,40 ± 0,11 бала).
Найширший регенерат сформувався у випадку використання автотрансплантатів з PRF — 6160,00 ± 155,75 мкм. Ширина регенерату в разі застосування автотрансплантатів, алотрансплантатів самостійно та в поєднанні з PRF була порівняною — 5420,70 ± 226,82; 5371,80 ± 200,81 та 5308,40 ± 189,33 мкм відповідно. Найменшу кількість кісткової тканини в зоні спондилодезу виявлено в разі застосування лише PRF — 3219,30 ± 157,15 мкм (р < 0,001).
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Lumbar pseudarthrosis: a review of current diagnosis and treatment / S. Danielle, B.A. Chun, K.C. Baker, W.K. Hsu // Neurosurg. Focus. — 2015. — Vol. 39. — P. 1-8. — doi: 10.3171/2015.7.FOCUS15292.
2. Affective disorders in uence clinical out- comes after revision lumbar surgery in elderly patients with symptomatic adjacent-segment disease, recurrent stenosis, or pseudarthrosis: clinical article / O. Adogwa, T. Verla, P. Thompson [et al.] // J. Neurosurg. Spine. — 2014. — Vol. 21. — P. 153-159. — doi: 10.3171/2014.4.SPINE12668.
3. Revision surgery for lumbar pseudarthrosis / O. Dede, D. Thuillier, M. Pekmezci [et al.] // Spine J. — 2015. — Vol. 15. — P. 977-982. — doi: 10.1016/j.spinee.2013.05.039.
4. West J.L. Results of spinal arthrodesis with pedicle screw fixation / J.L. West, D.S. Bradford, J.W. Ogilvie // J. Bone Joint Surg. — 1991. — Vol. 73-A. — P. 1179-1184.
5. Європейська конвенція про захист хребетних тварин, що використовуються для дослідних та інших наукових цілей. Страсбург, 18 березня 1986 року: офіціальний переклад [Електронний ресурс] / Верховна Рада України. Офіційний веб-сайт. (Міжнародний документ Ради Європи). — Режим доступу до документу: електронний ресурс: [http:// zakon.rada.gov.ua/cgi-bin/laws/main.cginreg=994_137].
6. Boden S.D. Volvo Award in basic sciences. The use of an osteoinductive grows factor for lumbar spinal fusion. Part II: Study of dose, carrier and species / S.D. Boden, J.H. Schimandle, W.C. Hutton // Spine. — 1995. — Vol. 20(24). — P. 2633-2644.
7. Саркисов Д.С. Микроскопическая техника / Д.С. Саркисов, Ю.Л. Перов. — М.: Медицина, 1996. — 542 с.
8. The effect of risedronate on posterior lateral spinal fusion in a rat model / A.R. Gezici, R. Ergun, K. Gurel [et al.] // J. Korean Neurosurg. Soc. — 2009. — Vol. 46. — P. 45-51. — DOI: 10.3340/jkns.2009.46.1.45.
9. Bone regenerative medicine: classic options, novel strategies, and future directions [web source] / A. Oryan, S. Alidadi, A. Moshiri, N. Maffulli // J. Orthop. Surg. Res. — 2014. — Vol. 9. — Article 18. — Access mode: http://www.josr-online.com/content/9/1/18. doi: 10.1186/1749-799X-9-18.
10. Bone regeneration: Current concepts and future directions [web source] / R. Dimitriou, E. Jones, D. McGonagle, P.V. Giannoudis // BMC Med. — 2011. — 10 p. — Access mode: https://bmcmedicine.biomedcentral.com/track/pdf/10.1186/1741-7015-9-66. doi:10.1186/1741-7015-9-66.
11. Brydone A.S. Bone grafting, orthopaedic biomaterials, and the clinical need for bone engineering / A.S. Brydone, D. Meek, S. Maclaine // Proc. Inst. Mech. Eng. H. — 2010. — Vol. 224. — P. 1329-1343. — doi: 10.1243/09544119JEIM770.
12. Bhatt R.А. Bone graft substitutes / R.A. Bhatt, T.D. Rozental // Hand Clin. — 2012. — Vol. 12. — P. 457-468. — Doi.org/10.1016/j.hcl.2012.08.001.
13. Janicki P. What should be the characteristics of the ideal bone graft substitute? Combining scaffolds with growth factors and/or stem cells / P. Janicki, G. Schmidmaier // Injury. — 2011. — Vol. 42. — P. S77-S81. — doi: 10.1016/j.injury.2011.06.014.
14. Orthopaedic applications of bone graft and graft substitutes: a review / S.K. Nandi, S. Roy, P. Mukherjee [et al.] // Indian J. Med. Res. — 2010. — Vol. 132. — P. 15-30.
15. The use of coralline hydroxyapatite with bone marrow, autogenous bone graft, or osteoinductive bone protein extract for posterolateral lumbar spine fusion / S.D. Boden, G.J. Martin, M. Morone [et al.] // Spine. — 1999. — Vol. 24. — P. 320-327.
16. Factors influencing arthrodesis rates in a rabbit posterolateral spine model with iliac crest autograft / J.H. Ghodasra, E.L. Daley, E.L. Hsu, W.K. Hsu // Eur. Spine J. — 2014. — Vol. 23. — P. 426-434. — doi: 10.1007/s00586-013-3074-0.
17. Reliability of the rabbit postero-lateral spinal fusion mo–del: A meta-analysis / A.M. Riordan, R. Rangarajan, J.W. Balts [et al.] // J. Orthop. Res. — 2013. — Vol. 8. — P. 1261-1269. — doi:10.1002/jor.22359.
18. Zimmermann G. Allograft bone matrix versus synthetic bone graft substitutes / G. Zimmermann, A. Moghaddam // Injury. — 2011. — Vol. 42. — P. S16-S21. — doi: 10.1016/j.injury.2011.06.199.
19. Oryan A. Current concerns regarding healing of bone defects [web source] / A. Oryan, S. Alidadi, A. Moshiri // Hard Tissue. — 2013. — Vol. 2. — 13 p. — Access mode: http://www.oapublishinglondon.com/article/374.
20. Moshiri A. Role of tissue engineering in tendon reconstructive surgery and regenerative medicine: current concepts, approaches and concerns [web source] / A. Oryan, A. Moshiri // Hard Tissue. — 2012. — Vol. 1. — 11 p. — Access mode: http://www.oapublishinglondon.com/article/291.
21. Stevenson S. The response to bone allografts / S. Stevenson, M. Horowitz // J. Bone Joint Surg Am. — 1992. — Vol. 74(6). — P. 939-950.
22. Wang W. Bone grafts and biomaterials substitutes for bone defect repair: A review / W. Wang, K.W.K. Yeung // Bioactive Materials. — 2017. — Vol. 2. — P. 224-247. — doi.org/10.1016/j.bioactmat.2017.05.007.
23. Effect of storage temperature on allograft bone / C. Folsch, W. Mittelmeier, U. Bilderbeek [et al.] // Transfus. Med. Hemother. — 2012. — Vol. 39(1). — P. 36-40. — doi: 10.1159/000335647.
24. Evaluation of autologous platelet concentrate for intertransverse process lumbar fusion / P.M. Sethi, J.J. Miranda, S. Kadiyala [et al.] // Am. J. Orthop. — 2008. — Vol. 37(4). — P. E84-E90.
25. Regenerative potential of platelet rich fibrin in dentistry: literature review / V. Gupta, V.K. Bains, G.P. Singh [et al.] // Asian J. Oral Health & Allied Sci. — 2011. — Vol. 1(1). — P. 22-28.
26. Mosesson M.W. Structure and biological features of fibrinogen and fibrin / M.W. Mosesson, K.R. Siebenlist, D.A. Meh // Ann. NY Acad. Sci. — 2001. — Vol. 936. — P. 11-30. — doi: 10.1111/j.1749-6632.2001.tb03491.
27. Slow release of growth factors and thrombospondin-1 in Choukroun’s platelet-rich fibrin (PRF): A gold standard to achieve for all surgical platelet concentrates technologies / D.M. Dohan Ehrenfest, de G.M. Peppo, P. Doglioli, G. Sammartino // Growth Factors. — 2009. — Vol. 27. — P. 63-69. — doi: 10.1080/08977190802636713.
28. Introducing Choukroun’s platelet rich fibrin (PRF) to the reconstructive surgery milieu / M. Toffler, N. Toscano, D. Holtzclaw [et al.] // J. Implant Advanced Clin. Dent. — 2009. — Vol. 1. — P. 21-32. — DOI: 10.13140/2.1.2586.2086.
29. Platelet-rich fibrin (PRF): a second-generation platelet concentrate. Part IV: Clinical effects on tissue healing / J. Choukroun, A. Diss, A. Simonpieri [et al.] // Oral Surg., Oral Med., Oral Path., Oral Radiol. & Endodont. — 2006. — Vol. 101(3). — P. E56-E60. — doi: 10.1016/j.tripleo.2005.07.011.
30. Khiste S.V. Platelet-rich fibrin as a biofuel for tissue regeneration / S.V. Khiste, R. Naik Tari // ISRN Biomaterials. — 2013. — Vol. 2013. — Article ID: 627367. doi: 10.5402/2013/627367.
31. Kawamura M., Urist M.R. Human fibrin is a physiologic delivery system for bone morphogenetic protein // Clin. Orthop. Rel. Res. — 1988. — Vol. 235. — P. 302-310.
32. Попсуйшапка К.О. Визначення ролі збагаченого тромбоцитами фібрину в процесі регенерації дефекту тіла хребця (експериментальне дослідження) / К.О. Попсуйшапка, Н.О. Ашукіна, В.О. Радченко // Ортопедия, травматология и протезирование. — 2017. — № 3(608). — С. 32-38. — doi: http://dx.doi.org/10.15674/0030-59872017332-38.

/17-1.jpg)
/17-2.jpg)
/18-1.jpg)
/18-2.jpg)
/19-1.jpg)