Вступ
Кашель у дитини є найчастішою скаргою, з якою звертаються батьки на прийом до сімейного лікаря чи педіатра. Близько 55 % всіх дітей (50–70 % молодшого віку, 30–60 % дітей шкільного віку), батьки яких звертаються за медичною допомогою, скаржаться саме на кашель [5].
Правильна інтерпретація та диференціація цього симптому дає можливість вчасно встановити діагноз і провести ефективне лікування. Стикаючись з проблемою кашлю, лікар перш за все повинен вирішити, яке значення має цей симптом для конкретного пацієнта — захисне фізіологічне чи патологічне. Фізіологічна сутністю кашлю — пристосувальна захисна реакція, спрямована на видалення сторонніх речовин і патологічного секрету з дихальних шляхів, тобто кашель — це фізіологічний процес, без якого нормальне функціонування органів дихання є неможливим [4]. Цей механізм кашлю спрацьовує в ситуації, коли неефективним стає мукоциліарний кліренс, що виконує дві основні функції: забезпечує евакуацію секрету з повітроносних шляхів і захищає їх від аспірації чужорідних тіл. Відомо, що протягом доби у здорової дитини в бронхах утворюється близько 50–80 мл слизу, який за допомогою клітин війчастого епітелію рухається вгору до гортані, звідки потрапляє в глотку і проковтується. Такий рух слизу забезпечується не тільки адекватним функціонуванням війок епітелію дихальних шляхів, але й нечастим покашлюванням. Саме тому короткі кашльові поштовхи спостерігаються й у здорових дітей [4, 10].
У фізіологічних умовах слизова оболонка верхніх дихальних шляхів успішно справляється з агресивним впливом навколишнього середовища завдяки факторам захисту. Важливим захисним механізмом є утворення трахеобронхіального секрету, який є продуктом секреторної діяльності келихоподібних клітин епітелію залоз трахеї і бронхів. Одним з основних захисних механізмів слизової оболонки є мукоциліарний кліренс. Війки миготливого епітелію дихальних шляхів забезпечують постійний рух секрету в напрямку порожнини рота та видалення надлишку слизу, сторонніх часток, мікроорганізмів [3]. Причому оптимальна робота війок миготливого епітелію можлива лише при нормальній реології секрету слизової оболонки (в’язкості, еластичності, адгезивності). До складу слизу слизової оболонки дихальних шляхів входять імуноглобуліни та ферменти (лізоцим, лактоферин), що забезпечують бактерицидний ефект [7].
У разі розвитку запалення респіраторних шляхів значно збільшується секреція бронхіальних залоз і келихоподібних клітин, уміст у бронхіальному секреті продуктів розпаду клітин, метаболітів життєдіяльності та розпаду мікроорганізмів, ексудату. Встановлено, що одночасно з гіперпродукцією слизу змінюється і склад секрету — зменшується питома вага води та підвищується концентрація муцинів [10]. Густий і в’язкий секрет, що застоюється в дихальних шляхах, призводить до вентиляційних порушень і сприяє розмноженню бактерій. Крім цього, зміна в’язкості слизу супроводжується суттєвими якісними змінами його складу: зниженням вмісту секреторного IgA, інтерферону, лактоферину, лізоциму — основних компонентів місцевого імунітету, що мають противірусну та протимікробну активність [3, 6]. Це призводить до підвищеної адгезії патогенних мікроорганізмів на слизовій оболонці респіраторного тракту і створює умови для їх розмноження. Водночас збільшення продукції слизу є захисною реакцією слизової оболонки на вторгнення патогенних агентів. Однак гіперпродукція слизу із захисного процесу під час хвороби перетворюється на патологічний. Виникає хибне коло — адгезія тригерів призводить до розвитку запальної реакції з боку слизової оболонки, збільшується продукція та змінюється реологія слизу, порушується мукоциліарний кліренс, що сприяє контамінації мікроорганізмів і розвитку патологічного процесу [1, 4]. Отже, виникає запалення в дихальних шляхах, що призводить до пошкодження миготливого епітелію і зміни реологічних властивостей мокротиння, яке супроводжується зниженням мукоциліарного кліренсу. Недостатній рівень мукоциліарного кліренсу не дозволяє адекватно звільняти дихальні шляхи від мокротиння. При цьому основним механізмом очищення дихальних шляхів стає кашель [2, 3, 8].
Визначення характеристик кашлю дає можливість проводити диференційну діагностику та добирати найбільш раціональну схему фармакотерапії. Характер кашлю може бути дуже різноманітним. Зокрема, сухий (непродуктивний) кашель виникає зазвичай у дебюті запалення слизових оболонок респіраторного тракту або при фіброзних відкладеннях у трахеї; гавкаючий — при ларингітах; гучний, «як у діжку» — при трахеїтах; бітональний — низький, а потім високий тон — патогномонічна ознака захворювань, які призводять до подразнення місця біфуркації трахеї; вологий кашель виникає при гострих, рекурентних бронхітах, бронхоектатичній хворобі, пневмоніях, у післяприступному періоді при загостренні бронхіальної астми; нападоподібний кашель із репризами — при кашлюку тощо [6].
Розглядаючи проблему кашлю, доцільно виділяти гострий і хронічний кашель. Протягом багатьох років у світовій педіатричній літературі дискутується проблема визначення тривалості періоду переходу кашлю у хронічну фазу. Зокрема, рекомендації британських учених визначають кашель хронічним після восьмого тижня з моменту його появи, австралійські та американські — після четвертого тижня [2]. Водночас практичний лікар потребує чітких рекомендацій із цього приводу. На сьогодні в Україні гострим прийнято вважати кашель, який триває не більше 3 тижнів, підгострим — від 3 до 8 тижнів, хронічним — понад 8 тижнів [2, 4].
Кашель часто зумовлює погіршення якості життя не лише пацієнта, але й його родини. Він може виснажувати та значно впливати на сон дитини, її шкільну успішність і фізичну активність. Водночас кашель може також порушувати сон інших членів сім’ї, спричиняти серйозну тривогу батьків [9].
Вибираючи тактику лікування дитини з кашлем, педіатр насамперед повинен з’ясувати причини його виникнення, природу захворювання, оцінити продуктивність, тривалість та інтенсивність, ступінь впливу кашлю на загальний стан і самопочуття хворої дитини, оцінити характер бронхіального секрету, наявність або відсутність бронхоспазму. Алгоритм лікування кашлю повинен складатися винятково індивідуально і розпочинатися зі створення оптимальних умов для адекватного функціонування органів дихання. Перш за все необхідно забезпечити вільне носове дихання, зволоження повітря, адекватну регідратацію пацієнта (часте, тепле пиття). Нерідко використання саме цих заходів дає можливість вирішити проблему кашлю, і питання про застосування медикаментів просто не стоїть. У разі потреби фармакотерапії можливе застосування медикаментів із різними механізмами дії, а саме: засоби для покращення дренажної функції бронхів і відновлення адекватного мукоциліарного кліренсу; протикашльові препарати за чіткими показаннями; антибактеріальна терапія лише за умови доведеної бактеріальної інфекції [7].
Важливим патогенетичним механізмом, що призводить до порушення прохідності дихальних шляхів, є утворення в’язкої мокроти. Розрідження і видалення цього патологічного секрету займає суттєве місце в терапії захворювань органів дихання у дітей. Ліки, що впливають на розрідження мокротиння й очищення трахеобронхіального дерева від скупчення бронхіального секрету, слизу, гною, складають велику групу відхаркувальних (мукоактивних) засобів. Основний механізм їхньої дії полягає у зміні якості мокротиння, що починає краще відходити. Призначення терапії дитині з кашлем повинно ґрунтуватися на глибокому знанні механізмів дії цих лікарських засобів, що дозволяє забезпечити раціональний вибір лікувальної тактики залежно від характеру патології, віку дитини, індивідуальних особливостей її організму. Найпоширенішими щодо застосування в педіатрії мукоактивними засобами є амброксол, карбоцистеїн, ацетилцистеїн (табл. 1).
Згідно з даними різних педіатричних шкіл України, сьогодні у практиці найчастіше використовуються як муколітики препарати амброксолу або карбоцистеїну, а також комбінація даних лікарських речовин.
Відомо, що амброксол є активним метаболітом бромгексину, належить до муколітичних препаратів нового покоління та за своєю фармакологічною дією є муколітичним препаратом із вираженою відхаркувальною, протизапальною і навіть імуномодулюючою дією [6]. Він збільшує секрецію залоз дихальних шляхів, підсилює синтез легеневого сурфактанту в альвеолярних пневмоцитах і зменшує його розпад, стимулює циліарну активність, внаслідок чого полегшується виділення слизу та його виведення (мукоциліарний кліренс). Результатом дії препарату є активація секреції рідини та збільшення мукоциліарного кліренсу, що значно полегшує виділення мокротиння, покращує відхаркування, полегшує дихання [5, 7].
Місцевий протизапальний і протинабряковий ефект амброксолу обумовлений пригніченням вивільнення гістаміну, лейкотрієнів, цитокінів із лейкоцитів та тучних клітин, а також пригніченням продукції медіаторів запалення мононуклеарами (інтерлейкіну-1 та фактора некрозу пухлини α). Препарат також стимулює місцевий імунітет, сприяючи збільшенню активності тканинних макрофагів і підвищенню концентрації секреторного імуноглобуліну А (ІgА) [9].
Амброксол — відома молекула, перевірена часом. Він ефективно розріджує мокротиння, практично не збільшуючи його об’єму і сприяючи адекватному виведенню. При застосуванні цього препарату не розвивається синдром «затоплення» легень і бронхообструкції. Слід також зазначити існуючі дані про те, що амброксол підвищує ефективність антибіотикотерапії, сприяє збільшенню концентрації амоксициліну, цефуроксиму, макролідів і доксицикліну в бронхолегеневому секреті, що полегшує перебіг захворювання при бактеріальних інфекціях дихальних шляхів.
Амброксол, виступаючи в ролі секретомоторика, активує рух війок внаслідок дії сурфактанта, і як муколітик знижує в’язкість секрету через зміну хімізму його мукополісахаридів. Активація війок миготливого епітелію бронхів і перистальтики бронхіол у поєднанні з покращенням реологічних властивостей бронхіального секрету призводить до ефективної санації дихальних шляхів, допомагаючи хворому легше відхаркувати мокротиння [2].
На особливе місце в лікуванні кашлю заслуговують мукорегулятори, що регулюють вироблення слизу залозистими клітинами і нормалізують їх секреторну функцію, поліпшують мукоциліарний кліренс шляхом нормалізації в’язкості та реологічних властивостей слизу незалежно від вихідного патологічного стану. Найбільш відомим препаратом цієї групи є карбоцистеїн, який походить від цистеїну, але водночас має окремі характеристики, що принципово відрізняють його від ацетилцистеїну. Зокрема, він не впливає безпосередньо на структуру слизу, як це робить ацетилцистеїн, і, як наслідок, не сприяє розвитку синдрому «затоплення» легень. Карбоцистеїн стимулює активность сіалілтрансферази, збільшує синтез сіаломуцинів, оптимізуючи баланс сіаломуцинів і фукомуцинів, відновлює еластичні властивості мокротиння (в’язкість) [6]. Карбоцистеїн виявляє не лише муколітичний ефект, але й відновлює нормальну активність секреторних (келихоподібних) клітин слизової оболонки дихальних шляхів, підвищує продукцію sIgA [3].
Перспективними в лікуванні кашлю є комбіновані препарати (амброксол + карбоцистеїн). Амброксол і карбоцистеїн мать два різних та незалежних механізми дії і, впливаючи на різні патогенетичні ланки мукогенезу, діють комплексно та більш ефективно розріджують і виводять в’язке мокротиння з трахеобронхіального дерева. Іншими словами, комбінація амброксолу та карбоцистеїну внаслідок ефективної і безпечної дії кожного препарату визначає оптимальну корекцію найбільш важливих порушень у секретоутворенні бронхіальних залоз, забезпечує нормалізацію складу секрету, відновлення адекватності дренажних функцій дихальних шляхів. Існують дані про те, що комбіноване застосування амброксолу і карбоцистеїну сприяє підвищенню ефективності терапії гострих і хронічних захворювань дихальних шляхів [8]. Зокрема, комбіновані препарати показані для широкого застосування в педіатричній практиці при гострих і хронічних бронхолегеневих захворюваннях, пов’язаних із порушеннями бронхіальної секреції та утрудненим просуванням слизу (трахеїти, бронхіти, пневмонії, бронхіальна астма, бронхоектатична хвороба тощо). Більше того, сьогодні існують переконливі дані про те, що антибіотикотерапія, що доволі часто призначається у разі респіраторної патології у дітей, суттєво підвищує в’язкість мокротиння, а отже, на її фоні виникає потреба в застосуванні препаратів, які покращують реологічні властивості мокротиння і забезпечують його ефективне відходження [5]. У контексті антибіотикотерапії варто згадати і про здатність амброксолу та карбоцистеїну підвищувати проникність окремих антибіотиків, підвищуючи їх концентрацію у вогнищі інфекції, що також дозволяє говорити про здатність комбінованого муколітика Пектолван Ц підвищувати ефективність антибіотикотерапії. Викладена вище ситуація визначила актуальність і мету нашого дослідження.
Мета: підвищення ефективності лікування кашлю у дітей шляхом вибору оптимальної мукоактивної терапії.
Матеріали та методи
Ми провели порівняння ефективності трьох мукоактивних препаратів — амброксолу, карбоцистеїну та їх комбінації — в лікуванні гострих трахеїту і бронхіту, які супроводжувалися виділенням в’язкого мокротиння, що важко відкашлювалося. Окрім мукоактивної терапії діти отримували у разі потреби симптоматичну терапію (антипіретики).
Критеріями включення в дослідження були: вік дитини 2–6 років; симптоми гострої респіраторної вірусної інфекції (температура тіла вище 37,5 °С, –астенія, явища інтоксикації); продуктивний кашель із в’язким мокротинням, що важко відділяється; відповідна аускультативна картина (дихання з подовженим видихом, вологі різнокаліберні хрипи тощо); згода батьків на участь дитини у дослідженні.
Критерії виключення: бактеріальна етіологія захворювання; застосування антибіотикотерапії; індивідуальна непереносимість амброксолу, карбоцистеїну чи інших компонентів муколітичних засобів; приєднання бактеріальної флори; виникнення побічних реакцій у відповідь на муколітичну терапію, що вимагає відміни муколітичного препарату; інші ускладнення, що потребують зміни тактики лікування.
Дослідження проводилося у трьох групах, кожна з яких включала 30 дітей. Розподіл дітей до певної групи був випадковим. Спостереження за дітьми проводилося в умовах Львівського міського дитячого алергологічного центру. Основна група становила 30 пацієнтів, які як мукоактивну терапію отримували препарат Пектолван Ц, до складу якого входять амброксол і карбоцистеїн. Діти віком 2–6 років отримували препарат по 2,5 мл 2–3 рази на добу. У групу порівняння «А» увійшли 30 пацієнтів, у яких муколітична терапія передбачала застосування сиропу амброксолу. Діти віком 2–5 років отримували препарат по 2,5 мл 3 рази на добу, діти віком 6 років — по 5 мл 2–3 рази на добу. Група порівняння «К» складалася з 30 пацієнтів, які отримували мукоактивну терапію із застосуванням карбоцистеїну. Діти віком 2–5 років отримували по 5 мл препарату 2–3 рази на добу, діти віком 5 та 6 років — по 5 мл 3 рази на добу.
Відомо, що призначення мукоактивної терапії потребує дотримання правильного режиму застосування препаратів. Категорично заборонялося застосування ліків безпосередньо перед сном, оскільки лежаче положення сприяє активному відходженню мокротиння, появі кашлю, що, у свою чергу, погіршує сон і впливає на якість життя дитини. Діти, які брали участь у дослідженні, отримували препарати з таким розрахунком, щоб останній прийом був найпізніше за 3 години до сну.
Моніторинг перебігу хвороби здійснювали на підставі оцінки кашлю, фізикальних змін (дані аускультації) та якості життя пацієнтів.
Вираженість клінічних симптомів оцінювали в балах: кашель (0 — відсутній, 1 — слабо виражений, 2 — помірно виражений, 3 — інтенсивний), дані аускультації (0 — хрипів немає, 1 — поодинокі вологі хрипи, 2 — вологі хрипи у помірній кількості, 3 — множинні вологі хрипи).
Результати
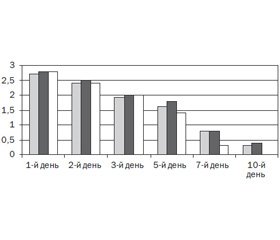
Динаміка кашлю під впливом лікування показана на рис. 1.
Отже, можна стверджувати, що кашель досить швидко регресував в усіх трьох групах обстежених, однак найменшою виявилася тривалість кашлю у дітей, які отримували Пектолван Ц.
Дані, наведені на рис. 2, ілюструють фізикальні зміни, що дозволили зареєструвати найвищу ефективність комбінованого препарату.
Таким чином, отримані результати дозволяють вважати препарат Пектолван Ц дуже перспективним мукоактивним лікарським засобом.
Обговорення
Сьогодні, оцінюючи ефективність будь-яких способів лікування, піддають аналізу не лише об’єктивні показники, але й суб’єктивну оцінку впливу хвороби на життя дитини. Суб’єктивний показник задоволення власних потреб у житті прийнято визначати як якість життя. Якість життя із загального поняття перетворилася на предмет наукових досліджень і визначає ступінь комфортності людини. Ми провели спеціальне тестування і виявили, що застосування всіх трьох препаратів позитивно вплинуло на якість життя наших маленьких пацієнтів. Діти легше переносили хворобу та швидко відновлювали нормальний активний спосіб життя.
Безпечність і переносимість препаратів ми оцінювали за наявністю чи відсутністю побічних ефектів. Серйозні побічні ефекти, які б вимагали відміни препаратів, не були виявлені.
Отже, діагностичний пошук причин кашлю у дітей потребує виваженого підходу з визначенням індивідуального вектора фармакотерапії. Ще з давніх-давен відомим є вислів, що кашель — це сторожовий пес людського організму. Тому лікар перш за все повинен вирішити, яке значення має цей симптом для конкретного пацієнта — захисне фізіологічне чи патологічне, і лише після цього за потреби проводити відповідну корекцію. Раціональний вибір і своєчасне призначення мукоактивних препаратів у комплексній терапії гострих трахеїту і бронхіту значно підвищує ефективність лікування та сприяє швидшому одужанню маленького пацієнта.
Висновки
Результати дослідження довели доцільність та обґрунтованість використання комбінованого лікарського засобу Пектолван Ц з метою мукоактивної терапії при гострих трахеїті та бронхіті у дітей віком 2–6 років. Окремі критерії ефективності вказали на позитивну перевагу комбінації амброксолу та карбоцистеїну над застосуванням даних лікарських речовин окремо.
Конфлікт інтересів. Не заявлений.

/36-1.jpg)