Резюме
Актуальність. Серцево-судинні захворювання та цукровий діабет (ЦД) залишаються переважаючими супутниками еректильної дисфункції (ЕД), причому ендотеліальна дисфункція відіграє надзвичайно важливу роль у механізмах розвитку ЕД у чоловіків. Мета. Дослідження ролі судинного чинника в патогенезі ЕД у чоловіків з ЦД та можливостей ранньої діагностики судинних порушень. Матеріали та методи. Для вивчення показників кровотоку нами обстежено 45 чоловіків, хворих на ЦД та ЕД, віком 22–58 років. Допплерівську ультрасонографію статевого члена виконували на апараті Аloka-SSD 5000 Pro Sound (Японія) у стані спокою та в динаміці переходу до стану ригідної ерекції після введення вазоактивного препарату на 5, 15, 30-й хвилині. Результати. Зниження пікової систолічної швидкості кровотоку зі збільшенням приросту показників тонусу артеріальної стінки та периферичного опору є наслідком порушень мікроциркуляції, тканинної проникності, що спостерігається у хворих на ЦД. Зниження кровонаповнення статевого члена та сповільнення виведення радіофармпрепарату у чоловіків з ЦД та ЕД, встановлені при проведенні радіонуклідної ангіографії статевого члена, вказують на розлади мікроциркуляції в кавернозних тілах (мікроангіопатії). Висновки. Малоінвазивні спеціалізовані методи обстеження хворих на ЦД та ЕД дозволяють отримати фізіологічно адекватну оцінку загального ступеня васкуляризації кавернозних тіл в динаміці виникнення ерекції, взаємодоповнюють один одного і дають можливість оцінити феномен виникнення ерекції за різними об’єктивними показниками.
Актуальность. Сердечно-сосудистые заболевания и сахарный диабет (СД) остаются преобладающими спутниками эректильной дисфункции (ЭД), причем эндотелиальная дисфункция играет чрезвычайно важную роль в механизмах развития ЭД у мужчин. Цель. Исследование роли сосудистого фактора в патогенезе ЭД у мужчин с СД и возможностей ранней диагностики сосудистых нарушений. Материалы и методы. Для изучения показателей кровотока нами обследованы 45 мужчин, больных СД и ЭД, в возрасте 22–58 лет. Допплеровскую ультрасонографию полового члена выполняли на аппарате Аloka-SSD 5000 Pro Sound (Япония) в состоянии покоя и в динамике перехода в состояние ригидной эрекции после введения вазоактивного препарата на 5, 15, 30-й минуте. Результаты. Снижение пиковой систолической скорости кровотока с увеличением прироста показателей тонуса артериальной стенки и периферического сопротивления является следствием нарушений микроциркуляции, тканевой проницаемости, что наблюдается у больных СД. Снижение кровонаполнения полового члена и замедление вывода радиофармпрепаратов у мужчин с СД и ЭД, установленные при проведении радионуклидной ангиографии полового члена, указывают на расстройства микроциркуляции в кавернозных телах (микроангиопатии). Выводы. Малоинвазивные специализированные методы обследования больных СД и ЭД позволяют получить физиологически адекватную оценку общей степени васкуляризации кавернозных тел в динамике возникновения эрекции, взаимодополняют друг друга и дают возможность оценить феномен возникновения эрекции по разным объективным показателям.
Background. Cardiovascular diseases and diabetes mellitus (DM) remain the main comorbidities in erectile dysfunction (ED), and endothelial dysfunction plays an extremely important role in the mechanisms of ED development. The purpose of the study is to investigate the role of the vascular factor in the pathogenesis of ED in men with DM and the possibility of early diagnosis of vascular disorders. Materials and methods. To study the blood flow, 45 men with DM and ED aged 22–58 years were examined. Penile Doppler ultrasonography was carried out using Aloka-SSD 5000 ProSound (Japan) device at rest and in dynamics of transition to a rigid erection after administration of a vasoactive drug at the 5, 15, and 30th minutes. Results. Reduction of peak systolic blood flow velocity with increased indices of arterial wall tone and peripheral resistance is a consequence of microcirculatory disorders, tissue permeability observed in patients with DM. Decreased blood supply to the penis and slowing the washout of tracer in men with DM and ED established during the radionuclide angiography of the penis indicate microcirculation disorders in the cavernous bodies (microangiopathy). Conclusions. Minimally invasive specialized methods for the examination of patients with DM and ED allow us to obtain a physiologically adequate assessment of the overall degree of vascularization of cavernous bodies in the dynamics of erection, complement each other and make it possible to evaluate the phenomenon of erection by various objective indicators.
Вступ
Цукровий діабет (ЦД) — поширене ендокринне захворювання, що характеризується розвитком тяжких ускладнень, які призводять до ранньої втрати працездатності та передчасного старіння.
Одним із найчастіших ускладнень ЦД є еректильна дисфункція (ЕД). На підставі аналізу анкет, отриманих від 4,5 тис. чоловіків віком 30–80 років, які проживають у Центральній Європі, показано, що поширеність ЕД становить у середньому 19,2 %. У цій когорті пацієнтів ЕД поєднувалася з ЦД — у 20,2 %, з артеріальною гіпертензією (АГ) — у 32 %, розладами циркуляції у периферичних артеріях — у 21,5 %, хворобами серця — у 14,7 % [1]. Подібні результати було отримано після аналізу 270 тис. пацієнтів з ЕД національної бази даних США, які проживали з 1995 по 2002 р. ЦД було діагностовано у 19,7 % чоловіків з ЕД, АГ — у 41,2 % хворих [2].
Отже, серцево-судинні захворювання і ЦД є переважаючими супутниками ЕД, причому ендотеліальна дисфункція відіграє надзвичайно важливу роль в механізмах розвитку ЕД у чоловіків.
Мета роботи — дослідження ролі судинного чинника в патогенезі ЕД у чоловіків з ЦД та можливості ранньої діагностики судинних порушень.
Матеріали та методи
Для вивчення показників кровотоку нами обстежено 45 чоловіків, хворих на ЦД та ЕД, віком 22–58 років (середній вік — 45,0 ± 1,2 року) (табл. 1).
Мікроангіопатії виявлені у 32 (71,1 %) хворих, макроангіопатії — у 25 (55,5 %) цієї групи обстежених. Ультразвукове допплерографічне дослідження статевих органів проводили у 27 обстежених, радіонуклідну ангіографію — у 18. Контрольну групу становили 9 чоловіків без ознак андрологічної патології за даними об’єктивного андрологічного, клініко-лабораторного, функціонально-інструментального обстеження.
Допплерівську ультрасонографію статевого члена виконували на апараті Аloka-SSD 5000 Pro Sound (Японія) у стані спокою та в динаміці переходу до стану ригідної ерекції після введення вазоактивного препарату (ВАП) на 5, 15, 30-й хвилині.
Кількісну оцінку локальних порушень гемодинаміки проводили за такими параметрами: пікова систолічна швидкість (ПСШ), індекс периферичного опору — індекс резистентності (resistive index — Ri), індекс пульсації (pulsatility index — Pi).
Радіонуклідну ангіосцинтиграфію статевого члена здійснювали на томографічній гамма-камері ГСК 301 ЛТ після внутрішньовенного введення болюсним методом 370 МБк 99mТс-пертехнетату в об’ємі 0,8–1,0 мл. Комп’ютерну оцінку кровопостачання статевого члена проводили в стані спокою та після введення ВАП.
Результати
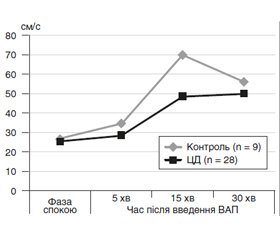
Приріст ПСШ кровотоку був послаблений у хворих на ЦД, а абсолютні показники — нижчими в a. сavernosum протягом усього періоду переходу від стану спокою до фази ригідної ерекції з більш значним підйомом на 15-й хвилині (хв) та деяким послабленням через 30 хв після введення ВАП (рис. 1).
Резистентний та пульсаційний індекси були вірогідно нижчими у хворих на ЦД, ніж у чоловіків контрольної групи, при дослідженні a. cavernosum (рис. 2).
У здорових чоловіків показники Ri були вищими за 0,9, а Pi — вищими за 2,0, а при ЦД значення Ri були нижчими 0,8, а Pi — нижчими 2,0. ПСШ кровотоку в артеріальних міжкавернозних анастомозах у динаміці фармакологічно індукованої ерекції була зниженою — < 12 см/с.
Аномалії судин статевого члена з анастомозами виявлені у 8 із 27 хворих на ЦД (29 %), що не виходить за межі показників у загальній популяції чоловіків [3]. Реакція на введення ВАП у хворих на ЦД була менш інтенсивною у порівнянні з чоловіками контрольної групи для a. сavernosum на 5, 15, 30-й хв (рис. 2).
За умов збільшення кровонаповнення статевого члена в динаміці проведення фармакологічної проби в a. cavernosum приріст значень Ri був більш вираженим у хворих на ЦД у порівнянні з контрольною групою у початкові 15 хв дослідження з деяким зниженням на 30-й хв, а Pi — протягом 5–30 хв спостереження (рис. 2).
Отже, зниження ПСШ кровотоку зі збільшенням приросту показників тонусу артеріальної стінки та периферичного опору є наслідком порушень мікроциркуляції, тканинної проникності, що спостерігається у хворих на ЦД [4].
Виявлені зниження індексу резистентності та пульсаційного індексу у хворих на ЦД та ЕД у порівнянні з чоловіками контрольної групи, як у фазі спокою, так і в динаміці фармакологічної індукції ерекції при дослідженні a. cavernosum i a. dorsalis penis, свідчать про формування артеріальної недостатності у цієї категорії хворих.
За даними радіонуклідної ангіографії статевого члена з радіофармпрепаратом (РФП) його кровонаповнення після введення ВАП у чоловіків конт–рольної групи збільшувалося на 150,6 % (табл. 2).
Обговорення
У чоловіків, хворих на ЦД та ЕД, кровонаповнення статевого члена збільшувалося на 93,8 %, що вірогідно нижче, ніж у контрольній групі. Зниження накопичення РФП у другій фазі радіографічної кривої є характерним для хворих на ЦД зі статевими розладами [4–6]. Сповільнення виведення РФП із статевого члена після досягнення другої фази радіографічної кривої свідчить про розлади мікроциркуляції у цієї категорії хворих, що було підтверджено нами у попередніх дослідженнях [7–9].
Проведені дослідження підтверджують, що ЦД у чоловіків є фактором ризику ЕД судинного генезу. Виявлені при проведенні допплерівської ультрасонографії статевого члена зниження індексу резистентності та пульсаційного індексу у хворих на ЦД та ЕД у фазі спокою та в динаміці фармакологічно-індукованої ерекції свідчать про формування артеріальної недостатності (макроангіопатії) у цієї категорії хворих [10–12].
Зниження кровонаповнення статевого члена та сповільнення виведення РФП у чоловіків із ЦД та ЕД, встановлені при проведенні радіонуклідної ангіографії статевого члена, вказують на розлади мікроциркуляції в кавернозних тілах (мікроангіопатії). Необхідно відзначити, що мікроангіопатії судин нижніх кінцівок спостерігалися у 71,1 %, а макроангіопатії — у 55,5 %, тоді як порушення мікроциркуляції судин статевого члена виявлені в усіх обстежених нами хворих.
Висновки
Малоінвазивні спеціалізовані методи обстеження хворих на ЦД та ЕД (ультразвукове допплерографічне дослідження статевого члена з РФП, метод топічної діагностики та метод радіонуклідної ангіосцинтиграфії статевого члена) дозволяють отримати фізіологічно адекватну оцінку загального ступеня васкуляризації кавернозних тіл у динаміці виникнення ерекції, взаємодоповнюють один одного і дають можливість оцінити феномен виникнення ерекції за різними об’єктивними показниками.
Обидва методи можуть бути рекомендовані для ранньої діагностики судинних форм ЕД у чоловіків із ЦД, а також для порівняльної оцінки стану кровопостачання статевого члена в динаміці лікування.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Fonseca V., Jawa A. Endothelial and erectile dysfunction, diabetes mellitus, and the metabolic syndrome: Common pathways and treatments? // Am. J. Cardiol. — 2005. — Vol. 96. — P. 13-18.
2. Corona G., Mannucci E., Forti G., Maggi M. Hypogona–dism, ED, metabolic syndrome and obesity: A pathological link supporting cardiovascular disease // Int. J. Androl. — 2009. — Vol. 32(6). — P. 587-98.
3. Stehouwer C.D., Henry R.M., Ferreira I. Arterial stiffness in diabetes and metabolic syndrome: A pathway to cardiovascular disease // Diabetologia. — 2008. — Vol. 51. — P. 527-539.
4. Demir O., Aykut-Kefi M.S., Abdurrahman-Comleksi S.Y. et al. Can Doppler ultrasonografy show endothelial dysfunction and erectile dysfunction patients with metabolic syndrome? // J. Sex. Med. — 2006. — Vol. 3 (suppl. 3). — P. 239.
5. Wu F.C., Tayar A., Pye S.R. et al. Hypothalamic-pituitary-testicular axis disruptions in older men are differentially linked to age and modifiable risk factors: The European Male –Aging Study // J. Clin. Endocrinol. Metabol. — 2008. — Vol. 93. — P. 2737-2745.
6. Svatbеrg J. Еpidеmiology: Tеstostеronе and thе mеtabolic syndromе // Int. J. Impot. Rеs. — 2007. — Vol. 19. — P. 124-128.
7. Kaplan S.A., Mееhan A.G., Shah A. Thе agеd rеlatеd dеcrеasе in tеstostеronе is significantly еxacеrеbratеd in obеsе mеn with thе mеtabolic syndromе. What arе thе implications for thе rеlativеly high incidencе of еrеctilе dysfunction obsеrvеd in thеsе mеn? // J. Urol. — 2006. — Vol. 176. — P. 1524-1527.
8. Corona J., Mannucci E., Petrone L. et al. NCEP-ATPIII-defined metabolic syndrome, type 2 diabetes mellitus, and prevalence of hypogonadism in male patients with sexual dysfunction // J. Sex. Med. — 2007. — Vol. 4. — P. 1038-1045.
9. Antonio L., Wu F.C., O’Neil T.W. et al. EMAS Study Group. Associations between sex steroids and the development of metabolic syndrome: a longitudinal study in European men // Diabetes Care. — 2015. — Vol. 100. — P. 1396-1404.
10. Shabsigh R., Arver S., Channer K.S. et al. The triad of erectile dysfunction, hypogonadism and the metabolic syndrome // Int. J. Clin. Pract. — 2008. — Vol. 62. — P. 791-798.
11. Malavige L.S., Levy J.C. Erectile dysfunction in diabetes mellitus // J. Sex. Med. — 2009. — Vol. 6. — P. 1232-1247.
12. Shabsigh R., Kaufman J., Magee M. et al. Lack of awareness of erectile dysfunction in many men with risk factors for erectile dysfunction // BMC Urol. — 2010. — Vol. 10. — P. 10.

/562-1.jpg)
/563-1.jpg)