Журнал "Гастроэнтерология" Том 52, №4, 2018
Вернуться к номеру
Агрегационная способность тромбоцитов у пациентов с гипертонической болезнью в сочетании с неалкогольной жировой болезнью печени на фоне ожирения
Авторы: Баженова Н.М.
Национальный медицинский университет имени А.А. Богомольца, г. Киев, Украина
Киевская клиническая больница на железнодорожном транспорте № 2 филиала «Центр здравоохранения» публичного акционерного общества «Украинская железная дорога», г. Киев, Украина
Рубрики: Гастроэнтерология
Разделы: Клинические исследования
Версия для печати
Актуальність. Активація тромбоцитів і їх агрегації є важливими процесами в патофізіології ішемічної хвороби серця. Залежність смертності від серцево-судинної захворюваності може поглиблюватися наявністю інших супутніх серцево-судинних факторів ризику, у тому числі гіпертонічною хворобою (ГХ), ожирінням, неалкогольною жировою хворобою печінки (НАЖХП). Мета роботи: вивчити наявність тромбофілічних змін крові у пацієнтів з гіпертонічною хворобою з супутнім ожирінням і неалкогольною жировою хворобою печінки шляхом визначення функціональної активності тромбоцитів. Матеріали та методи. Обстежено 91 пацієнта. Середній вік — (57,9 ± 9,4) року. Виділено три групи: I — 36 хворих із ГХ II стадії з супутньою НАЖХП, II — 28 пацієнтів із НАЖХП без ГХ, III група — 27 пацієнтів із ГХ II стадії без супутньої НАЖХП. Результати. Виявлено вірогідне збільшення ступеня спонтанної агрегації в пацієнтів у всіх групах: у пацієнтів із ГХ II ст. — у 3 рази (р < 0,05), у пацієнтів із НАЖХП — у 4,2 раза (р < 0,001), у пацієнтів із НАЖХП + ГХ II ст. — у 7 разів (р < 0,01). Ступінь АДФ-індукованої агрегації тромбоцитів вірогідно зростав в усіх групах пацієнтів: у групі ГХ II ст. збільшувався на 116 % (р < 0,05), у групі НАЖХП + ГХ II ст. — на 93 % (р < 0,001), при самостійній НАЖХП — на 71,7 % (р < 0,05). Ступінь агрегації, індукованої арахідоновою кислотою, вірогідно знижувався на 8,3 % (р < 0,05) у групі пацієнтів з НАЖХП + ГХ II ст. Висновки. При ГХ спостерігалося збільшення функціональної активності тромбоцитів, ступінь якої значно зростав при приєднанні НАЖХП. У пацієнтів з ізольованою НАЖХП також спостерігалося статистично значуще посилення спонтанної агрегації тромбоцитів, що дозволяє розглядати НАЖХП як один із факторів ризику тромбофілічних змін первинної ланки гемостазу.
Актуальность. Активация тромбоцитов и их агрегации являются важнейшими процессами в патофизиологии ишемической болезни сердца. Зависимость смертности от сердечно-сосудистой заболеваемости может усугубляться присутствием других сопутствующих сердечно-сосудистых факторов риска, в том числе гипертонической болезнью (ГБ), ожирением, неалкогольной жировой болезнью печени (НАЖБП). Цель работы: изучить наличие тромбофилических изменений крови у пациентов с гипертонической болезнью и сопутствующим ожирением и неалкогольной жировой болезнью печени путем определения агрегационной способности тромбоцитов. Материалы и методы. Обследован 91 пациент. Средний возраст — (57,9 ± 9,4) года. Выделено три группы пациентов: I — 36 больных ГБ II стадии с сопутствующей НАЖБП, II — 28 пациентов с НАЖБП без ГБ, III группа — 27 пациентов с ГБ II стадии без сопутствующей НАЖБП. Результаты. Выявлено достоверное увеличение степени спонтанной агрегации у пациентов во всех группах по сравнению с группой контроля: у пациентов с ГБ II ст. — в 3 раза (p < 0,05), у пациентов с НАЖБП — в 4,2 раза (p < 0,001), у пациентов с НАЖБП + ГБ II ст. — в 7 раз (p < 0,01). Степень АДФ-индуцированной агрегации тромбоцитов достоверно возрастала во всех группах пациентов: в группе ГБ II ст. увеличивалась на 116 % (p < 0,05), в группе НАЖБП + ГБ II ст. — на 93 % (р < 0,001), при самостоятельной НАЖБП — на 71,7 % (p < 0,05). Степень агрегации, индуцированной арахидоновой кислотой, достоверно снижалась на 8,3 % (p < 0,05) в группе пациентов с НАЖБП + ГБ II ст. Выводы. При гипертонической болезни наблюдалось увеличение функциональной активности тромбоцитов, выраженность которой значительно возрастала при присоединении НАЖБП. У пациентов с изолированной НАЖБП также наблюдалось статистически значимое усиление спонтанной агрегации тромбоцитов, что позволяет рассматривать НАЖБП как один из факторов риска тромбофилических изменений первичного звена гемостаза.
Background. Activation of platelets and their aggregation are central processes in the pathophysiology of coronary heart disease. The relationship between mortality and cardiovascular morbidity varies depending on the presence of other concomitant cardiovascular risk factors. Materials and methods. Ninety one patients were examined. Their average age was (57.9 ± 9.4) years. Three groups of patients were identified: I — 36 persons with stage 2 hypertension and non-alcoholic fatty liver disease (NAFLD), II — 28 patients with NAFLD without hypertension, group III — 27 patients with stage 2 hypertension without NAFLD. Results. A significant increase of spontaneous aggregation degree was revealed in all groups: in patients with stage 2 hypertension — threefold (p < 0.05), in group with NAFLD — by 4.2 times (p < 0.001), in group with stage 2 hypertension and NAFLD — sevenfold (p < 0.01). The degree of adenosine diphosphate-induced platelet aggregation increased in all patients: with stage 2 hypertension — by 116 % (p < 0.05), NAFLD and stage 2 hypertension — by 93 % (p < 0.001), with NAFLD alone — by 71.7 % (p < 0.05). The degree of arachidonic acid-induced platelet aggregation decreased by 8.3 % (p < 0.05) in the group of NAFLD with stage 2 hypertension. Conclusions. An increase of the functional activity of platelets is observed in hypertension, the severity of which increases significantly in combination with NAFLD. Patients with NAFLD alone had also significant increase in spontaneous platelet aggregation. It allows us to consider NAFLD as one of the risk factors for thrombophilic changes in the primary link of hemostasis.
неалкогольна жирова хвороба печінки; агрегація тромбоцитів; гіпертонічна хвороба; ожиріння
неалкогольная жировая болезнь печени; агрегация тромбоцитов; гипертоническая болезнь; ожирение
non-alcoholic fatty liver disease; platelet aggregation; hypertension; obesity
Введение
Повышенное артериальное давление (АД) является важнейшей причиной роста сердечно-сосудистой заболеваемости (ССЗ) во всем мире, так как способствует развитию ишемических и геморрагических повреждений органов-мишеней. Величина АД имеет положительную корреляцию с риском развития инсультов и ишемической болезнью сердца, значительно влияя на общую смертность [1].
Зависимость смертности от ССЗ может усугубляться присутствием других сопутствующих сердечно-сосудистых факторов риска, а высокое АД часто сопровождается наличием метаболических нарушений [2].
Ожирение — одна из главных модифицируемых причин развития патологии сердечно-сосудистой системы, обусловливает ее быстрое прогрессирование, более тяжелое течение и высокую частоту осложнений [5].
Развитие артериальной гипертензии (АГ) тесно связано с приростом массы тела, при этом более значимым является повышенное содержание висцеральной жировой ткани, которое также сопряжено с рядом других метаболических факторов риска ССЗ. Корреляция между ожирением и АГ была подтверждена Фрамингемским исследованием, в котором было показано, что при увеличении массы тела значительно возрастает распространенность АГ независимо от возрастной категории и пола пациентов.
Ожирение представляет собой наиболее значимый фактор, связанный с неалкогольной жировой болезнью печени (НАЖБП). Согласно многочисленным исследованиям, увеличение индекса массы тела является независимым предиктором формирования жировой инфильтрации печени [7].
Распространенность НАЖБП в различных странах Европы составляет 10–24 %, из них у 57–74 % — среди людей с ожирением [6–8].
Принято считать, что НАЖБП сочетается с ожирением, но в большинстве случаев степень ожирения не коррелирует со степенью жирового гепатоза [8].
По данным рекомендаций 2016 года Американской ассоциации клинических эндокринологов и Американского колледжа эндокринологии по клинической практике для комплексной медицинской помощи больным с ожирением, скрининг НАЖБП следует проводить всем пациентам с избыточным весом или ожирением, сахарным диабетом 2 типа или с метаболическим синдромом. Начальный этап скрининга — определение лабораторных показателей функции печени. В случае повышения уровня аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы — провести ультразвуковое исследование печени или использовать другой метод визуализации. В то же время у всех пациентов с НАЖБП следует оценивать наличие избыточного веса или ожирения [4, 9].
В соответствии с обновленными в 2018 году рекомендациями Американского колледжа гастроэнтерологии по диагностике и ведению НАЖБП, снижение верхней границы нормы для показателя АЛТ будет способствовать росту количества пациентов с незначительным повышением уровня АЛТ, что приведет к раннему выявлению НАЖБП, и может быть ассоциировано с хорошим прогнозом заболевания [9, 10].
Абдоминальный тип ожирения — признак, наиболее свойственный НАЖБП и метаболическому синдрому, который часто сопровождается развитием сердечно-сосудистых заболеваний, в том числе тромбофилических изменений крови, которые способствуют возникновению тромбоза в коронарных артериях, артериях головного мозга.
Активация тромбоцитов и их агрегации являются важнейшими процессами в патофизиологии ишемической болезни сердца [11].
Треть населения планеты имеет НАЖБП, и у большинства больных присутствуют сердечно-метаболические факторы риска, такие как абдоминальное ожирение, сахарный диабет 2 типа и другие компоненты метаболического синдрома.
На базе медицинской школы при университете в городе Дюздже в Турции авторами Н. Ozhan, М. Aydin и др. проводилось исследование, целью которого было изучение среднего объема тромбоцитов у пациентов, которые имели НАЖБП. Проведено сравнение среднего объема тромбоцитов у пациентов с НАЖБП и у пациентов без жировой болезни печени. Было показано, что пациенты с НАЖБП имеют более высокие показатели среднего объема тромбоцитов, а также имели более низкое количество тромбоцитов. Так как средний объем тромбоцитов является показателем их активации, это может иметь прогностическое значение для пациентов с НАЖБП и указывает на возможное увеличение риска сердечно-сосудистых заболеваний [14, 15].
Несмотря на большое количество работ, посвященных НАЖБП, много принципиально важных вопросов остаются неизученными. Проведен ряд исследований, которые изучали связь количества тромбоцитов со стадией НАЖБП, с развитием фиброза и прогнозом НАЖБП [16–18]. Также изучалось влияние НАЖБП на средний объем тромбоцитов как косвенный показатель их активности, но непосредственно агрегационная способность тромбоцитов у пациентов с НАЖБП не была изучена.
Цель работы: изучить наличие тромбофилических изменений крови у пациентов с гипертонической болезнью (ГБ) и сопутствующим ожирением и неалкогольной жировой болезнью печени путем определения агрегационной способности тромбоцитов.
Материалы и методы
Проведено обследование 91 пациента (41 мужчины и 50 женщин). Средний возраст пациентов (57,9 ± 9,4) года. Пациенты были распределены на три группы: I — 36 больных ГБ II стадии с сопутствующей НАЖБП, II — 28 пациентов с НАЖБП без ГБ, III группа — 27 пациентов, у которых обнаружена ГБ II стадии без сопутствующей НАЖБП. Все пациенты имели различную степень ожирения. Группа контроля — 15 здоровых лиц, сопоставимых по возрасту и полу. Больным проводили общеклинические исследования; для верификации НАЖБП — ультразвуковое исследование органов брюшной полости, исследование на «Фиброскане».
Для достижения поставленной цели проводилось исследование агрегационной способности тромбоцитов с помощью лазерного анализатора 230-LA (НПФ «Биола»).
Исследование выполнено в плазме венозной крови, взятие которой проводили из локтевой вены после 12-часового голодания, с соблюдением всех требований, выдвигаемых для коагулологических исследований: забор крови выполняли полистироловым шприцем в полистироловые центрифужные градуированные пробирки с пробкой, содержащие 1 объем стабилизатора (3,8% раствора натрия цитрата), куда добавляли 9 объемов крови. Период инкубации крови при комнатной температуре — 25–30 минут.
Исследование проводили в богатой и бедной тромбоцитами плазме. Богатую тромбоцитами плазму получали путем центрифугирования цитратной крови в течение 3 минут на скорости 1000 оборотов в 1 минуту, бедную тромбоцитами плазму получали путем центрифугирования цитратной крови в течение 20 минут при скорости 3000 оборотов в 1 минуту (1500 g), что является общепринятым для коагулологических исследований.
Изучали спонтанную и индуцированную агрегацию тромбоцитов с использованием индукторов фирмы «НПО-Ренам»: аденозин-5-дифосфат (АДФ), арахидоновая кислота (АК), коллаген, адреналин. Для исследования агрегации тромбоцитов использовали турбидиметрический метод, который основан на регистрации изменений светопропускания обогащенной тромбоцитами плазмы. Получение информации в виде кривых агрегации с автоматическим расчетом показателей осуществляли с помощью компьютера, сопряженного с агрегометром. При этом светопропускание обедненной тромбоцитами плазмы анализатор автоматически принимал за 100 %, богатой плазмы — за 0 %. По кривой светопропускания рассчитывались показатели степени и скорости агрегации тромбоцитов. Степень агрегации определялась как максимальный прирост светопропускания после добавления индуктора и измерялась в процентах [19, 20].
Статистическая обработка данных проводилась с использованием статистического пакета Portable Statistica 10, StatSoft, Inc., США. Критический уровень значимости при проверке статистических гипотез принимался равным 0,05. Для анализа показателей тромбоцитарного гемостаза применялись непараметрические методы статистики: критерий Манна — Уитни, критерий Краскела — Уоллиса, так как использовались малые объемы выборок, а значения в группах не подчинялись закону нормального распределения.
Результаты и обсуждение
Для определения статистически значимых различий между значениями спонтанной и индуцированной агрегации изучаемых выборок применен критерий Краскела — Уоллиса. Достоверные различия имели группы пациентов по уровню спонтанной агрегации (р = 0,0002), агрегации, индуцированной АДФ (р < 0,05), коллагеном (р < 0,05). В дальнейшем для сравнения двух групп пациентов по каждому из показателей агрегации использовался критерий Манна — Уитни.
Спонтанная агрегация тромбоцитов
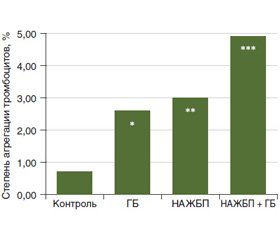
Было выявлено достоверное увеличение степени спонтанной агрегации у пациентов во всех группах по сравнению с группой контроля: у пациентов с ГБ II ст. — в 3 раза (р < 0,05), у пациентов с НАЖБП — в 4,2 раза (p < 0,001), у пациентов с ГБ II ст. и сопутствующей НАЖБП — в 7 раз (p < 0,01) (рис. 1). При этом сравнение с группой ГБ II ст. показало, что степень спонтанной агрегации была достоверно выше в группе пациентов с НАЖБП, сочетанной с ГБ II ст., на 88 % (p < 0,01) и на 13 % выше — у пациентов с изолированной НАЖБП (p < 0,05).
Индуцированная агрегация тромбоцитов
Степень АДФ-индуцированной агрегации тромбоцитов достоверно возрастала во всех группах пациентов в сравнении с контрольной когортой. Более высокие показатели среди пациентов с гипертонией: в группе ГБ II ст. агрегация увеличивалась на 116 % (р < 0,05), в группе НАЖБП + ГБ II ст. — на 93 % (р < 0,001), при самостоятельной НАЖБП степень АДФ-индуцированной агрегации увеличивалась на 71,7 % (р < 0,05).
Степень АК-индуцированной агрегации тромбоцитов была выше в группе пациентов с гипертонией и в группе с НАЖБП, но достоверные изменения наблюдали лишь у пациентов с НАЖБП + ГБ II ст., при этом степень агрегации снижалась на 8,3 % (р < 0,05).
Коллаген-индуцированная агрегация уменьшалась с присоединением как ГБ, так и НАЖБП. При этом достоверное и более выраженное уменьшение наблюдалось при сравнении контрольной выборки с группой ГБ II ст. на 23,3 % (р < 0,05), а в группе НАЖБП, сочетанной с ГБ II ст., отмечали уменьшение степени коллаген-индуцированной агрегации на 11,2 % (р < 0,05).
Агрегация тромбоцитов, индуцированная адреналином, более выражена в группах с ГБ, но достоверные отличия от контрольной группы имели только пациенты с изолированной ГБ II ст. — увеличение степени агрегации в 2,2 раза (р < 0,01) (рис. 2).
Выводы
1. У больных ГБ наблюдалось повышение агрегационной способности тромбоцитов, выраженность которой значительно прогрессировала при присоединении НАЖБП.
2. У пациентов с изолированной неалкогольной жировой болезнью печени прослеживалось статистически достоверное увеличение спонтанной агрегации тромбоцитов, что позволяет рассматривать НАЖБП как один из факторов риска тромбофилических изменений первичного звена гемостаза.
3. Для пациентов с ГБ характерно повышение адреналин-индуцированной агрегации, в отличие от других исследуемых групп, и может быть объяснено ролью симпатической нервной системы в патогенезе ГБ.
4. Наличие НАЖБП сопровождалось значительным увеличением реакции тромбоцитов на АДФ, что необходимо учитывать при выборе антитромбоцитарной терапии, так как АДФ-индуцированная агрегация отражает чувствительность к лечению клопидогрелем.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов при подготовке данной статьи.
Информация о финансировании. Научно-исследовательская работа выполнялась на базе Киевской клинической больницы на железнодорожном транспорте № 2 филиала «Центр здравоохранения» публичного акционерного общества «Украинская железная дорога».
1. Poulter N.R. Hypertension / N.R. Poulter, D. Prabhakaran, M. Caulfield // The Lancet. — 2015. — Vol. 386, № 9995. — P. 801-812. doi: 10.1016/S0140-6736(14)61468-9.
2. Lackland D.T. Global burden of cardiovascular disease and stroke: hypertension at the core / D.T. Lackland, M.A. Weber // Canadian Journal of Cardiology. — 2015. — Vol. 31, № 5. — P. 569-571. doi: 10.1016/j.cjca.2015.01.009.
3. National, regional, and global trends in body-mass index since 1980: systematic analysis of health examination surveys and epidemiological studies with 960 country-years and 91 million participants / M.M. Finucane, G.A. Stevens, M.J. Cowan [et al.] // The Lancet. — 2011. — Vol. 377, № 9765. — P. 557-567. doi: 10.1016/S0140-6736(10)62037-5.
4. American association of clinical endocrinologists and american college of endocrinology comprehensive clinical practice guidelines for medical care of patients with obesity / W.T. Garvey, J.I. Mechanick, E.M. Brett [et al.] // Endocrine Practice. — 2016. — Vol. 22 (Suppl. 3). — P. 1-203. doi: 10.4158/EP161365.GL.
5. Машура Г.Ю. Оптимізація діагностики і лікування хворих на неалкогольну жирову хворобу печінки у поєднанні з гіпертонічною хворобою з урахуванням смакової чутливості до хлориду натрію: Дис… канд. мед. наук / Г.Ю. Машура. — Ужгород, 2017. — 220 с.
6. Raziel A. Current solutions for obesity-related liver disorders: non-alcoholic fatty liver disease and non-alcoholic steatohepatitis / A. Raziel, N. Sakran, A. Szold, D. Goitein // The Israel Medical Association journal. — 2015. — Vol. 17, № 4. — P. 234-8.
7. Rinella M.E. Nonalcoholic fatty liver disease / M.E. Rinella // JAMA. — 2015. — Vol. 313, № 22. — P. 2263. doi: 10.1001/jama.2015.5370.
8. Распространенность неалкогольной жировой болезни печени у пациентов амбулаторно-поликлинической практики в Российской Федерации: результаты исследования DIREG 2 / В.Т. Ивашкин, О.М. Драпкина, И.В. Маев [и др.] // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2015. — Т. 25, № 6. — С. 31-41.
9. The diagnosis and management of nonalcoholic fatty liver disease: practice guidance from the american association for the study of liver diseases / N. Chalasani, Z. Younossi, J.E. Lavine [et al.] // Hepatology. — 2018. — Vol. 67, № 1. — P. 328-357. doi: 10.1002/hep.29367.
10. Kwo P.Y. ACG clinical guideline: evaluation of abnormal liver chemistries / P.Y. Kwo, S.M. Cohen, J.K. Lim // American Journal of Gastroenterology. — 2017. — Vol. 112, № 1. — P. 18-35. doi: 10.1038/ajg.2016.517.
11. Сиволап В.В. Показники АДФ-індукованої агрегації тромбоцитів у хворих на гіпертонічну хворобу, що ускладнена ішемічним півкульним інсультом / В.В. Сиволап, С.П. Жеманюк // Запорожский медицинский журнал. — 2017. — Т. 19, № 5(104). — С. 534-539. doi: 10.14739/2310-1210.2017.5.110080.
12. Баженова Н.М. Функциональная активность тромбоцитов у больных гипертонической болезнью в сочетании с неалкогольной жировой болезнью печени / Н.М. Баженова, Л.А. Дидковская // Евразийский кардиологический журнал. — 2017. — № 3. — С. 70.
13. EASL-EASD-EASO clinical practice guidelines for the management of non-alcoholic fatty liver disease / Journal of Hepatology. — 2016. — Vol. 64, № 6. — P. 1388-1402. doi: 10.1016/j.jhep.2015.11.004.
14. Platelet mean volume, distribution width, and count in type 2 diabetes, impaired fasting glucose, and metabolic syndrome: a meta-analysis / F. Zaccardi, B. Rocca, D. Pitocco [et al.] // Diabetes/Metabolism Research and Reviews. — 2015. — Vol. 31, № 4. — P. 402-410. doi: 10.1002/dmrr.2625.
15. Mean platelet volume in patients with non-alcoholic fatty liver disease / H. Ozhan, M. Aydin, M. Yazici [et al.] // Platelets. — 2010. — Vol. 21, № 1. — P. 29-32. doi: 10.3109/09537100903391023.
16. Garjani A. Association between platelet count as a noninvasive marker and ultrasonographic grading in patients with nonalcoholic fatty liver disease / A. Garjani, A. Safaeiyan, M. Khoshbaten // Hepatitis monthly. — 2015. — Vol. 15, № 1. — P. 1-16. doi: 10.5812/hepatmon.24449.
17. Nonalcoholic fatty liver disease may cause thrombocytopenia / G.J. Ruiz-Argüelles, S. Velazquez-Sanchez-De-Cima, G. Zamora-Ortiz [et al.] // Acta Haematologica. — 2014. — Vol. 132, № 2. — P. 159-162. doi: 10.1159/000357934.
18. Higher platelet counts are associated with metabolic syndrome independent of fatty liver diagnosis / K.C. Fang, Y.L. Cheng, C.W. Su [et al.] // Journal of the Chinese Medical Association. — 2017. — Vol. 80, № 3. — P. 125-132. doi: 10.1016/j.jcma.2016.07.003.
19. Медведев И.Н. Агрегационные свойства форменных элементов крови и сосудистый контроль над ними у больных артериальной гипертонией с дислипидемией / И.Н. Медведев, И.А. Скорятина // Российский кардиологический журнал. — 2015. — № 4. — С. 18-22. doi: 10.15829/1560-4071-2015-4-18-22.
20. Самойлова С.О. Стан коагулянтної активності крові та тромбоцитарного гемостазу у хворих на гіпертонічну хворобу в поєднанні із ХОЗЛ / С.О. Самойлова // Вісник морської медицини. — 2016. — № 2. — С. 105-116.

/35-1.jpg)
/35-2.jpg)
/36-1.jpg)