Журнал «Травма» Том 21, №1, 2020
Вернуться к номеру
Препараты гиалуроновой кислоты в системе реабилитационного лечения повреждений хряща после артроскопических операций на коленном суставе
Авторы: Болховитин П.В., Белостоцкий А.И., Болховитин Н.П.
МЦ «Кинезио», г. Харьков, Украина
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
У статті наведено дослідження ефективності препарату гіалуронової кислоти proFLEX INTRA при проведенні реабілітаційних заходів після артроскопічних втручань у пацієнтів із пошкодженням суглобового хряща колінного суглоба. У дослідженні взяли участь чоловіки і жінки віком від 18 до 70 років з артрозом колінного суглоба 1–2-ї стадії за Kellgren — Lawrence і пошкодженням хряща 2–4-го ступеня за R. Outerbridge, яким із різних причин були проведені артроскопічні оперативні втручання. Пацієнти були випадковим чином розподілені в основну (30 осіб) і контрольну (30 осіб) групи. Пацієнтам основної групи на 14-й день після артроскопічного втручання на колінному суглобі внутрішньосуглобово вводили 3 мл proFLEX INTRA («Дельта Медікел Промоушнз АГ», Швейцарія), 20 мг/мл. Встановлено, що досліджуваний препарат має значний терапевтичний ефект при пошкодженнях суглобового хряща, що проявляється в зменшенні вираженості больового синдрому за візуальною аналоговою шкалою; відновленні функції ушкодженого суглоба, оціненої за часом проходження дистанції 30 м і індексом за шкалою Лекена; у послабленні запальних і дистрофічних проявів у біохімічному аналізі крові.
В статье представлено исследование эффективности препарата гиалуроновой кислоты proFLEX INTRA при проведении реабилитационных мероприятий после артроскопических вмешательств у пациентов с повреждением суставного хряща коленного сустава. В исследовании приняли участие мужчины и женщины в возрасте от 18 до 70 лет с артрозом коленного сустава 1–2-й стадии по Kellgren — Lawrence и повреждением хряща 2–4-й степени по R. Outerbridge, которым по различным причинам были проведены артроскопические оперативные вмешательства. Пациенты были случайным образом распределены в основную (30 человек) и контрольную (30 человек) группы. Пациентам основной группы на 14-й день после артроскопического вмешательства на коленном суставе внутрисуставно вводили 3 мл proFLEX INTRA («Дельта Медикел Промоушнз АГ», Швейцария), 20 мг/мл. Установлено, что исследуемый препарат оказывает значительный терапевтический эффект при повреждениях суставного хряща, что проявляется в уменьшении выраженности болевого синдрома по визуальной аналоговой шкале; восстановлении функции поврежденного сустава, оцененной по времени прохождения дистанции 30 м и индексу по шкале Лекена; в уменьшении выраженности воспалительных и дистрофических проявлений в биохимическом анализе крови.
The article presents the study on the effectiveness of proFLEX INTRA, a hyaluronic acid preparation, during rehabilitation after arthroscopic interventions in patients with damage to the articular cartilage of the knee joint. The study involved men and women aged 18–70 with Kellgren-Lawrence grade 1–2 knee osteoarthritis and cartilage lesions degree 2–4 according to R. Outerbridge; they underwent arthroscopic surgeries for various reasons. Patients were randomly assigned to the main (30 people) and control (30 individuals) groups. Patients of the main group on the 14th day after arthroscopic surgery on the knee joint received intraarticular injections of proFLEX INTRA (Delta Medical Promotions AG, Switzerland), 20 mg/ml 3 ml. It was found that the studied drug has a significant therapeutic effect in case of damage to the articular cartilage, which is manifested in a decrease in the severity of pain according to visual analogue scale; restoration of the function of the damaged joint evaluated by the time taken to cover a distance of 30 m and the Lequesne index; in reducing the severity of inflammatory and dystrophic manifestations in a biochemical blood test.
гіалуронова кислота; ушкодження хряща; артроскопія; реабілітаційне лікування; остеоартроз; колінний суглоб
гиалуроновая кислота; повреждения хряща; артроскопия; реабилитационное лечение; остеоартроз; коленный сустав
hyaluronic acid; cartilage damage; arthroscopy; rehabilitation treatment; osteoarthritis; knee joint
Введение
Повреждения суставного хряща занимают ведущее место в структуре поражений коленного сустава различного генеза. Поражение суставов происходит как одномоментно, так и хронически, при различных патологических состояниях. Возникновение остеоартроза (ОА) является одной из наиболее частых причин стойкой утраты трудоспособности. Повреждение суставного хряща коленного сустава является основным звеном патогенеза раннего посттравматического, диспластического и других видов остеоартроза. Адекватность лечебно-профилактических мероприятий на ранних стадиях заболевания является залогом успеха при лечении патологии коленного сустава.
С внедрением в клиническую практику современных артроскопических технологий появилась возможность раннего выявления повреждений хряща. Следовательно, стало возможным раннее адекватное и эффективное лечение данной патологии.
Наиболее применимы с этой целью препараты симптоматического действия (с быстрым или медленным эффектом) и препараты структурно-модифицирующего действия. Подобная дифференциация существует [1–4] вне зависимости от пути введения препарата (внутрь, в полость сустава или местно).
Внутрисуставное введение препаратов гиалуроновой кислоты (ГК) в настоящее время находится на пике популярности. Одни производители предлагают препараты ГК с высокой концентрацией и молекулярной массой (которые, по мнению ряда авторов, обладают высокой эффективностью при остеоартрозе) [6–10]. Другие настаивают на эффективности препаратов с низкой концентрацией и молекулярной массой.
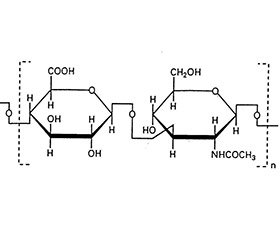
ГК является важным компонентом синовиальной жидкости и хрящевой ткани. Это полисахарид с высокой молекулярной массой, состоящий из длинных, не содержащих серы прямых цепочек дисахаридов различной длины, состоящих из N-ацетилглюкозамина. ГК играет важную роль в трофике хряща и регуляции среды в полости сустава. При ОА происходят изменения в свойствах нативной ГК. Существуют препараты ГК с различной концентрацией и молекулярной
массой.
Рекомендации по лечению ОА опубликовали Американский колледж ревматологии (ACR) и Европейская лига против ревматизма (EULAR, 2013), в которых указывалось на эффективность применения препаратов ГК [11–14]. В связи с этим были подробно изучены физиологические и фармакологические свойства ГК [6–10]. В результате этого исследовательского процесса возникла новая концепция.
Вискосуплементация
Концепция вискосуплементации базируется на механических свойствах ГК, которые, в свою очередь, зависят от молекулярной массы и концентрации [11, 12]. Под идеальными свойствами данная концепция подразумевает молекулярную массу и концентрацию гиалуроновой кислоты в нормальной синовиальной жидкости. Эта концепция корректна исключительно с биомеханической точки зрения. Хотя в настоящее время клинические данные о том, что благоприятный эффект ГК при симптомах ОА связан с ее молекулярной массой, являются дискуссионными [9]. Отсутствие единой точки зрения на молекулярную массу и концентрацию привело к созданию различных препаратов ГК.
С этой точки зрения применение ГК имеет смысл исключительно при 1–2-й стадии остеоартроза коленного сустава, когда дистрофические изменения не столь значительны. Различные исследования подтверждают эффективность ГК, что может расцениваться как верификация вязкоэластичной концепции [23–25].
Данные литературы позволяют критично отнестись к первоначальной концепции вязкоэластичности ГК как единственного объяснения механизма ее действия [11, 12, 30–37], так как одного этого свойства недостаточно для объяснения долгосрочных клинических эффектов подобной терапии. Кроме того, было показано, что ГК обладает множественными биологическими эффектами [7]. Более того, как было сказано ранее, гипотеза о том, что высокая молекулярная масса ГК является ключевым фактором ее клинической эффективности, недавно была поставлена под сомнение [9]. Aviad и Houpt выдвинули гипотезу о том, что концентрация ГК более важна, чем ее молекулярная масса [6].
Вискоиндукция
Эндогенное введение гиалуроновой кислоты с высокой молекулярной массой и концентрацией повышает амортизационные свойства синовиальной жидкости и препятствует дальнейшим дистрофическим изменениям суставного хряща и других внутрисуставных структур. Однако стимулирующим воздействием на синтез эндогенной ГК преимущественно обладают как раз препараты с низкой (1 %) концентрацией и низкой молекулярной массой (500–750 кДа) [19].
Стимулирование синтеза нативной ГК препаратами с высокой молекулярной массой и высокой концентрацией ставится под сомнение многими учеными. Если же к высокой молекулярной массе и высокой концентрации добавлена перекрестно-сшитая модификация, то эти препараты часто дают воспалительные реакции [25, 26, 37]. Возникает парадоксальная ситуация, когда препараты с высокой концентрацией, молекулярной массой и объемом обеспечивают вискосуплементацию, а препараты с низкой концентрацией, молекулярной массой и объемом обеспечивают вискоиндукцию [24, 27–29].
Вискомодификация
Модификация патологического процесса (защита хрящевой ткани или структурная модификация [2, 3]) при ОА становится все более реалистичной, так как в исследованиях подобная активность была показана у некоторых препаратов, применяющихся для лечения ОА. Тем не менее путь к доказательству структурно-модифицирующего действия при ОА у человека не является прямым [1, 3, 20–37]. Проспективное контролируемое рандомизированное пилотное исследование длительностью 1 год было проведено Listrat и соавт. [19] среди 39 пациентов с варусным ОА коленного сустава. После лаважа полости сустава (2 л физиологического раствора) при артроскопии все пациенты были разделены на 2 группы. В первой группе пациенты прошли 3 курса внутрисуставного введения ГК (1 курс — 3 инъекции ГК), во второй группе пациенты получали традиционную терапию ОА. Оценка результатов лечения проводилась по визуальной аналоговой шкале (ВАШ), функциональной шкале Lequesne's index, также применялась оценка качества жизни: arthritis impact measurement scale (AIMS2) [19].
Структурный эффект терапии оценивался по степени сужения суставной щели (при рентгенографии в переднезадней проекции) коленного сустава при нагрузке и при артроскопической оценке. Использовались три метода оценки: общая оценка исследователем повреждения хряща по ВАШ 100 мм, оценка при обзоре и оценочная система Французского общества артроскопии (FSA). Результаты показали наличие меньшего количества патологических изменений структурных параметров в группе ГК по сравнению с контрольной группой, со статистически значимыми различиями между группами при общей оценке повреждения хряща, оценке по ВАШ и оценке по FSA (+5,1 ± 12,7 мм в сравнении с 16,7 ± 18,3 мм; р = 0,016 и +3,7 ± 7,3 в сравнении с 9,0 ± 11,5; р = 0,05).
Frizziero и соавт. [20] изучали структурный эффект пяти еженедельных инъекций препарата ГК у 40 пациентов в открытом пилотном исследовании. Изучение результатов лечения проводилось путем микроартроскопической оценки и морфологического анализа биопсийного материала, полученного исходно и через 6 месяцев. Все образцы гистологически анализировались методом слепого контроля. Через 6 месяцев, по данным микроартроскопической оценки, у 60 % пациентов изменений не отмечалось, у 32,5 % пациентов отмечались улучшения степени и/или выраженности поражения хряща, у 7,5 % пациентов было отмечено ухудшение. Параллельно наблюдалось значимое снижение синовиального воспаления. Эти результаты были подтверждены морфологической оценкой. Клинически отмечалось снижение боли в покое и при нагрузке, улучшалась подвижность сустава и снижалось количество выпота начиная с 35-х суток до окончания наблюдения.
Pasquali-Ronchetti с соавт. [21] в своем исследовании оценивали во время артроскопии синовиальные мембраны 48 пациентов с ОА коленного сустава (по критериям ACR).
Для микроскопического анализа выполнялась биопсия. Пациенты рандомизировались в группы с пятью еженедельными инъекциями ГК или тремя еженедельными инъекциями метилпреднизолона. Оба препарата приводили к значимому уменьшению признаков воспаления в синовиальной мембране от исходного до окончательного осмотра (6 месяцев). Guidolin и соавт. [18] провели гистоморфометрическое исследование у 24 пациентов с первичным ОА коленного сустава, включенных в предыдущее исследование. 11 пациентов получали ГК, 13 — метилпреднизолона ацетат. Через шесть месяцев после начала терапии у пациентов, которые получали ГК, отмечалось выраженное восстановление поверхностного слоя и улучшение плотности и метаболизма хондроцитов (на что указывало увеличение размеров структур, участвующих в синтезе, и митохондрий).
Для подтверждения гипотезы о том, что ГК может являться структурно-модифицирующим препаратом, эти предварительные морфологические исследования должны быть подтверждены более крупными, плацебо-контролируемыми двойными слепыми исследованиями. Подобное исследование недавно было выполнено Jubb и соавт. [22]. Пациенты с ОА коленного сустава включались в исследование и распределялись в группы трех курсов по три инъекции ГК или плацебо с интервалом в три месяца. Структурная оценка результатов выполнялась посредством рентгенологического исследования исходно и через один год. Всего было включено 408 пациентов, исследование завершили 319 пациентов, данные рентгенографии были получены у 273. Хотя между группами терапии в общей популяции различий выявлено не было, среднее снижение ширины суставной щели было значительно меньше в группе ГК, чем в группе плацебо: –0,13 ± 1,1 мм по сравнению с –0,55 ± 1,0 мм соответственно (р = 0,02) у пациентов с большим средним размером суставной щели исходно (то есть с исходным размером суставной щели, превышающим медиану). Как ранее было отмечено в пилотном исследовании Listrat и соавт. [19], данные результаты подтверждают, что внутрисуставное введение ГК с молекулярной массой 500–730 кДа при ОА коленного сустава может оказывать структурное действие.
Назрела проблемная ситуация, когда нужен компромисс в угоду концепции вискомодификации. Вискомодификация возможна исключительно в случае объединения вискоиндукции и вискосуплементации, помноженной на продолжительность жизни молекулы, которая может быть достигнута путем более прочной перекрестно-сшитой стабилизации ГК. Поиск идеального препарата ГК продолжается. На основании результатов исследований, изучающих применение различных видов ГК, мы выдвигаем рабочую гипотезу концепции вискомодификации, основанную на применении препарата ГК со следующими характеристиками:
— концентрация: в интервале от 1 до 2 % гиалуроната натрия — это та концентрация, которая может обес-печить вискоиндуктивный эффект;
— молекулярный вес: от 2000 до 3000 кДа, этого будет достаточно для вискосуплементации, молекулы будут достаточно стабильными и не смогут вызывать воспалительные реакции при внутрисуставном введении;
— количество: от 2 до 3 мл гиалуроната натрия будут оптимальными для вискосуплементации;
— стабилизация за счет перекрестно-сшитой технологии получения молекулы для получения более длительного эффекта.
Интересной для клинического применения является инновация от компании «Дельта Медикел Промоушнз АГ» (Швейцария). Это новый имплантат синовиальной жидкости proFLEX INTRA — вязкоэластичный гель гиалуроната натрия, структурированный уникальным современным методом «энзим кросс-линк» (enzymes cross-linked) для стойкого, длительного клинического эффекта на 9–12 месяцев. На данный момент proFLEX INTRA представлен в 3 концентрациях — 10 мг/мл 2 мл, 12 мг/мл 2,5 мг и 20 мг/мл 3 мл. Этот ортопедический имплантат синовиальной жидкости может стать реальным и революционным структурно-модифицирующим решением в системе лечения остеоартроза за счет сочетания различных концепций.
Концентрация 1; 1,2; 2 % геля гиалуроната натрия может обеспечить вискоиндуктивный эффект.
Молекулярный вес 2100 кДа, 2600 кДа, 3200 кДа и количество 2,0 мл/20 мг, 2,5 мл/30 мг, 3,0 мл/60 мг гиалуроната натрия будут оптимальными для вискосуплементации.
Стабилизация молекулы за счет запатентованной системы «Enzymes cross-linked» обеспечит (по данным производителя) до 9–12 месяцев жизни молекулы ГК внутрисуставно.
Цель исследования: объективная оценка комплексного заместительного, хондропротекторного и восстановительного эффекта внутрисуставного гиалуроната натрия в форме геля, модифицированного enzyme cross-linked, proFLEX INTRA в качестве базисного препарата в системе восстановительного лечения повреждений хряща при раннем артрозе коленного сустава.
Задачи исследования включали:
— изучение эффективности proFLEX INTRA при проведении реабилитационных мероприятий после артроскопических вмешательств у пациентов с повреждением суставного хряща коленного сустава в сравнении с контрольной группой по таким показателям:
– изменения болевого синдрома по визуальной аналоговой шкале;
– воспалительные и дистрофические изменения суставов по биохимическому анализу крови (сиаловые кислоты, гликопротеины, С-реактивный белок, хондроитинсульфаты);
– восстановление функции сустава по изменению времени прохождения дистанции 30 м, индексов по шкале Лекена и шкале EuroQul-5D;
— изучение переносимости и возможных побочных эффектов proFLEX INTRA.
Материалы и методы
В исследовании приняли участие мужчины и женщины в возрасте от 18 до 70 лет с артрозом коленного сустава 1–2-й стадии по Kellgren — Lawrence и повреждением хряща 2–4-й степени по R. Outerbridge, которым по различным причинам были проведены артроскопические оперативные вмешательства. Все пациенты проходили реабилитационное лечение, включающее в себя физиопроцедуры, массаж, ЛФК, механотерапию и/или гидрокинезотерапию. Исследование включало в себя следующие этапы: скрининг и период лечения с регистрацией субъективных данных и результатов объективных клинических и лабораторных исследований, систематизация и анализ полученных результатов.
Все пациенты случайным образом были распределены по 30 человек на основную и контрольную группы.
Пациенты основной группы получали внутрисуставной ортопедический имплантат синовиальной жидкости proFLEX INTRA («Дельта Медикел Промоушнз АГ», Швейцария) 20 мг/мл 3 мл на 14-й день после артроскопического вмешательства на коленном суставе.
Общая характеристика включенных в исследование пациентов (возраст, пол, масса тела) представлена в табл. 1, из которой видно, что по данным показателям основная и контрольная группы были однородными.
Всем пациентам выполнялись дополнительные исследования в виде рентгенографии, УЗИ, МРТ. Рентгенография давала возможность исключить костную патологию. При ультразвуковом исследовании обращали внимание на гематомы, наличие выпота, повреждения связок, сухожилий и хряща. МРТ позволяла определить поражение хряща до артроскопии. При артроскопическом исследовании сустава верифицировалось повреждение гиалинового хряща, проводились эндоскопические манипуляции (резекция разрушенного хряща, высокочастотная абляция пораженных участков хряща, мезенхимальная стимуляция хондрорепарации и другие по показаниям). Результаты позволяли включать пациентов в группу исследования. Наиболее частой патологией были: остеоартроз, диспластический синдром нарушения нагружения надколенника, повреждение менисков, изолированное повреждение суставного хряща и повреждение свободными внутрисуставными телами.
В ходе клинического исследования каждый пациент проходил обследование. Результаты оценивали с использованием следующих методов.
Методы оценки общего клинического статуса:
— оценка общего состояния с регистрацией артериального давления и частоты сердечных сокращений;
— опрос и клинический осмотр с целью выявления жалоб и возможных побочных реакций.
Специальные методы оценки степени клинической выраженности воспалительных изменений в коленном суставе:
— оценка выраженности болевого синдрома по визуальной аналоговой шкале: на отрезке прямой в 10 см больной отмечает интенсивность боли, где 0 см — полное отсутствие боли, 0–2 см — незначительная боль, 2–4 см — слабая боль, 4–6 см — умеренная боль, 6–8 см — выраженная боль, 8–10 см — нестерпимая боль, вызывающая страдания;
— оценка степени восстановления функции сустава при помощи критерия изменения времени прохождения дистанции 30 м, индексов по шкале Лекена и шкале EuroQul-5D.
Оценка функции пораженных суставов с помощью индекса Лекена (Lequesne M.G., 1997) производилась исследователем на основании опроса пациентов по степени тяжести нарушений функциональных показателей (табл. 2).
Индекс тяжести нарушений функции пораженных суставов оценивается по сумме баллов: 1–4 балла — слабовыраженные нарушения, 5–7 — средняя степень тяжести, 8–10 — выраженные нарушения, 11–12 — значительно выраженные нарушения, > 12 — резко выраженные нарушения.
Оценка функции пораженных суставов по времени прохождения дистанции 30 м производилась исследователем.
Оценка качества жизни по шкале EuroQоl-5D производилась больным по сумме количественной выраженности субъективных ощущений (табл. 3).
Заполнение требует около 3 минут после краткого инструктажа исследователем. Выраженность признака определяется в баллах: 0 — отсутствие трудностей, 1 — умеренная степень выраженности, 2 — значительная степень выраженности. Максимальное количество баллов, которое может набрать пациент, составляет 10, минимальное — 0. Вывод об эффективности проводимой терапии делается на основании уменьшения суммарного количества баллов.
Лабораторные методы:
— общий анализ крови (эритроциты, гемоглобин, цветовой показатель, лейкоциты, скорость оседания эритроцитов — СОЭ);
— общий анализ мочи (плотность, рН, белок, сахар, лейкоциты, эритроциты, цилиндры, эпителиальные клетки);
— биохимический анализ крови (сиаловые кислоты, гликопротеины, хондроитинсульфаты).
Результаты и обсуждение
Эффективность внутрисуставного ортопедического имплантата синовиальной жидкости proFLEX INTRA («Дельта Медикел Промоушнз АГ», Швейцария) в качестве базисного препарата при лечении повреждений хряща оценивали по влиянию на динамику вышеперечисленных показателей, характеризующих степень клинической выраженности воспалительных явлений и функциональное состояние суставов.
Статистическую обработку проводили с использованием методов параметрической статистики. Рассчитывали средние значения показателей, их стандартную ошибку. Достоверность различий определяли по критерию Стьюдента на уровне значимости не менее 95 % (р = 0,05).
Влияние на выраженность болевого синдрома по ВАШ
До начала лечения 1 пациент (3,3 %) основной группы оценивал выраженность боли как нестерпимую, вызывающую страдания (8–10 см), а 29 пациентов (96,7 %) — как выраженную. В контрольной группе 2 пациента (6,7 %) зафиксировали нестерпимую, вызывающую страдания боль, 28 пациентов (93,3 %) — выраженную боль (табл. 4). Таким образом, до лечения у большинства пациентов обеих групп болевой синдром соответствовал выраженной степени.
На 15-й день после операции и следующий день после внутрисуставной инъекции исследуемого препарата в основной группе результаты практически не отличались. Этот эффект также был замечен и на 21-й день. На 29-й день в основной группе не отмечались клинически значимые болезненные ощущения, а в контрольной группе 5 пациентов отметили слабую боль, а 1 — умеренную. Данные представлены в табл. 4.
Влияние на функцию поврежденного сустава по индексу Лекена
У всех пациентов наблюдались нарушения функции суставов различной степени тяжести, минимальные из которых соответствовали средней степени тяжести.
Уже к 21-му дню исследования у большинства пациентов функция суставов значительно улучшилась. К окончанию исследования нормализация функции сустава отмечена у всех пациентов основной группы и у 24 пациентов контрольной (табл. 5).
Влияние на функцию коленного сустава по времени прохождения дистанции 30 метров
Важным показателем с нашей точки зрения в контексте спортивной реабилитации является динамика изменения скорости прохождения расстояния 30 метров. Результаты изучения этого показателя представлены в табл. 6.
Лучшие показатели к 29-му дню отмечены в основной группе. Однако следует заметить, что в дальнейшем, после окончания исследования, ограничения ходьбы регрессировали у всех пациентов как в основной, так и в контрольной группе.
Влияние на качество жизни по шкале EuroQol-5D
Мы провели изучение группы клинических наблюдений по изменению показателя по шкале EuroQol-5D. К 29-му дню лучшие результаты были отмечены в основной группе. Результаты оценки качества жизни в динамике представлены в табл. 7.
Исследование показателей воспаления по биохимическому анализу крови
Нами были изучены такие показатели, как сиаловые кислоты, гликопротеины, хондроитинсульфаты.
Изучена и представлена в табл. 8 сравнительная характеристика исследуемых групп по среднему значению изучаемого признака.
В результате проведенного исследования изменений биохимических показателей в крови выяснилось, что степень выраженности изменений ниже в основной группе по всем изученным показателям.
Осмотр и опрос пациентов основной и контрольной групп в ходе настоящего клинического исследования не выявил каких-либо жалоб, неожидаемых побочных реакций, осложнений или явлений непереносимости внутрисуставного ортопедического имплантата синовиальной жидкости proFLEX INTRA.
Ни один из пациентов не предъявлял жалоб и не испытывал каких-либо неприятных ощущений, которые можно было бы связать с действием изучаемого препарата.
Исследуемый препарат не оказал отрицательного влияния на артериальное давление и частоту сердечных сокращений, являющиеся основными показателями сердечной деятельности и гемодинамики: по завершении клинического исследования у больных не отмечено достоверных изменений этих показателей по сравнению с исходным уровнем до лечения. Клинический анализ крови у всех пациентов был в пределах нормы.
Выводы
1. Внутрисуставной ортопедический имплантат синовиальной жидкости proFLEX INTRA оказывает выраженный терапевтический эффект при повреждениях суставного хряща, который состоит в уменьшении выраженности болевого синдрома по ВАШ; восстановлении функции поврежденного сустава, оцененной по времени прохождения дистанции 30 м и индексу по шкале Лекена; уменьшении выраженности воспалительных и дистрофических проявлений в биохимическом анализе крови (сиаловые кислоты, гликопротеины, хондроитинсульфаты).
2. Введение внутрисуставного гиалуроната натрия в форме геля proFLEX INTRA у исследуемой категории пациентов позволяет быстрее достичь желаемых результатов реабилитации после артроскопических вмешательств.
3. Основные клинические и лабораторные показатели нормализуются у большинства пациентов спустя 4 недели после операции.
4. Внутрисуставной имплантат синовиальной жидкости proFLEX INTRA хорошо переносится больными и на протяжении трехнедельного курса лечения ни у кого из включенных в исследование пациентов не вызвал каких-либо ожидаемых или неожидаемых побочных эффектов.
5. Назначение препарата позволяет существенно улучшить качество жизни пациентов, что подтверждается положительной динамикой показателей шкалы EuroQul-5D.
6. Проведенное исследование позволяет рекомендовать внутрисуставной ортопедический имплантат синовиальной жидкости proFLEX INTRA («Дельта Медикел Промоушнз АГ», Швейцария) для широкого практического применения в качестве базисного препарата при реабилитации пациентов с повреждениями гиалинового хряща различной этиологии.
Конфликт интересов. Не заявлен.
1. Lequesne M., Brandt K., Bellamy N. et al. Guidelines for testing slow acting an disease modifying drugs in osteoarthritis. J. Rheumatol. 1994. 21 (Suppl. 41). 65-71.
2. Group for the Respect of Ethics and Excellence in Science (GREES: osteoarthritis section): recommendations for the registration of drugs in the treatment of osteoarthritis. Ann. Rheum. Dis. 1996. 55. 552-557.
3. Altman R.D., Brandt K., Hochberg M. et al. Design and conduct of clinical trials in patients with osteoarthritis: recommendations from a task force of Osteoarthritis Research Society. Results of a workshop. Osteoarthritis Cartillage. 1996. 4. 217-243.
4. Bellamy N., Kirwan J., Altman R.D. et al. Recommendations for a core set of outcome measures for future phase III clinical trials in knee, hip and hand osteoarthritis: consensus development in OMERACT III. J. Rheumatol. 1997. 24. 799-802.
5. Desmarais M.H.L. Value of intra-articular injections in osteoarthritis. Ann. Rheum. Dis. 1952. 11. 277-281.
6. Aviad A.D., Houpt J.B. The molecular weight of therapeutic hyaluronan (sodium hyaluronate): how significant is it? J. Rheumatol. 1994. 21. 297-301.
7. Abantangelo G., O’Regan M. Hyaluronan: biological role and function in articular joints. Eur. J. Rheumatol. Inflam. 1995. 15. 9-16.
8. George E. Intra-articular hyaluronan treatment for osteoarthritis. Ann. Rheum. Dis. 1998. 57. 637-640.
9. Brandt K.D., Smith G.N., Simon L.S. Intraartricular injections of hyaluronan as treatment for knee osteoarthritis: what is the evidence? Arthritis Rheum. 2000. 43. 1192-1203.
10. Emmanuel Maheu, MD, François Rannou, MD, PhDb, Jean-Yves Reginster, MD, PhDc: Efficacy and safety of hyalu-ronic acid in the management of osteoarthritis: Evidence from real-life setting trials and surveys, Seminars in Arthritis and Rheumatism. 2016. 45. S28-S33.
11. Adams M.E., Lussier A.J., Peyron J.G. A risk-benefit assessment of injections of hyaluronan and it’s derivates in the treatment of osteoarthritis of the knee. Drug Saf. 2000. 23. 115-130.
12. Balazs E.A., Denlinger J.L. Viscosupplementation: a new concept in the treatment of osteoarthritis. J. Rheumatol. 1993. 20 (Suppl. 39). 3-9.
13. Waddell D.D. Viscosupplementation with hyaluronans for osteoarthritis of the knee: clinical efficacy and economic implications. Drugs Aging. 2007. 24. 629-642.
14. Altman R.D., Hochberg M.C., Moskowitz R.W., Schnitzer T.J., members of the ACR subcommittee on osteoarthritis guidelines. Recommendations for the medical management of osteoarthritis of the hip and knee: 2000 update. Arthritis Rheum. 2000. 43. 1905-1915.
15. Fernandes L., Hagen K.B., Bijlsma J.W., Andreassen O., Christensen P., Conaghan P.G. et al. EULAR recommendations for the non-pharmacological core management of hip and knee osteoarthritis. Ann. Rheum. Dis. 2013. 72. 1125-1135.
16. Akmal M., Singh A., Anand A., Kesani A., Aslam N., Goodship A., Bentley G. The effects of hyaluronic acid on articular chondrocytes. J. Bone Joint. Surg. Br. 2005. 87. 1143-1149.
17. Conrozier T., Balblanc J.C., Richette P., Mulleman D., Maillet B., Henrotin Y., Rannou F., Piroth C., Hilliquin P., Mathieu P., Walliser-Lohse A., Rousselot I., Plattner V., Maillefert J.F., Vignon E., Chevalier X. Early effect of hyaluronic acid intra-articular injections on serum and urine biomarkers in patients with knee osteoarthritis: An open-label observational prospective study. J. Orthop. Res. 2012. 30. 679-685.
18. Moreland L.W. Intra-articular hyaluronan (hyaluronic acid) and hylans for the treatment of osteoarthritis: mechanisms of action. Arthritis Res. Ther. 2003. 5. 54-67.
19. Guidolin D.D., Pasquali-Ronchetti I., Lini E. et al. Morphological analysis of articular cartilage biopsies from a randomized, clinical study comparing the effects of 500–730 kDa sodium hyaluronate (Hyalgan) and methylprednisolone acetate on primary osteoarthritis of the knee. Osteoarthritis Cartilage. 2001. 9. 371-381.
20. Listrat V., Ayral X., Patarnello F., Bonvarlet J.P., Simonnet J., Amor B., Dougados M. Arthroscopic evaluation of potential structure modifying activity of hyaluronan (Hyalgan) in osteoarthritis of the knee. Osteoarthritis Cartilage. 1997. 5. 153-160.
21. Ghosh P., Guidolin D. Potential mechanism of action of intra-articular hyaluronan therapy in osteoarthritis: are the effects molecular weight dependent? Semin. Arthritis Rheum. 2002. 32 (1). 10-37.
22. Frizziero L., Govoni E., Bacchini P. Intra-articular hyaluronic acid in the treatment of osteoarthritis of the knee: clinical and morphological study. Clin. Exp. Rheumatol. 1998. 16. 441-449.
23. Pasquali-Ronchetti I., Guerra D., Taparelli F., Boraldi F., Bergamini G., Mori G., Zizzi F., Frizziero L. Morphological analysis of knee synovial membrane biopsies from a randomized controlled clinical study comparing the effects of sodium hyaluronate (Hyalgan) and methylprednisolone ace-tate (Depomedrol) in osteoarthritis. Rheumatology. 2001. 40. 158-169.
24. Jubb R., Piva S., Beinat L. et al. Structure modifying study of hyaluronan (500–750 kDa, Hyalgan) on osteoarthritis of the knee. Arthritis Rheum. 2001. 44 (Suppl.). S155.
25. Disla E., Infante R., Fahmy A. et al. Recurrent acute calcium pyrophosphate dihydrate artritis following hyaluronate injection. Arthritis Rheum. 1999. 42. 1302-1303.
26. Lussier A., Cividino A.A., McFarlane C.A. et al. Viscosupplementation with hylan for the treatment of osteoarthritis: findings from clinical practice in Canada. J. Rheumatol. 1996. 23. 1579-1585.
27. Pullman-Mooar S., Mooar P., Sieck M. et al. Are there distinctive inflammatory flares of synovitis after Hylan GF intraarticular injections? Arthritis Rheum. 1999. 42 (9 Suppl.). S295.
28. Martens P.B. Bilateral symmetric inflammatory reaction to hylan G-F 20 injection. Arthritis Rheum. 2001. 44. 978-979.
29. Peyron J.G. A new approach to the treatment of ostheoarthritis: viscosupplementation. Osteoarthritis Cartillage. 1993. 1. 85-87.
30. Dougados M., Nguyen M., Listrat V., Amor B. High molecular weight sodium hyaluronate (hyalectin) in osteoarthritis of the knee: a 1 year placebo-controlled trial. Osteoarthritis Cartilage. 1993. 1. 97-103.
31. Henderson E.B., Smith E.C., Pegley F., Blake Dr. Intra-articular injections of 750 kD hyaluronan in the treatment of osteoarthritis: a randomised single centre double-blind placebo-controlled trial of 91 patients demonstrating lack of efficacy. Ann. Rheum. Dis. 1994. 53. 529-53.
32. Altman R.D. et al. The mechanism of action for hyalu-ronic acid treatment in the osteoarthritic knee: a systematic review. BMC Musculoskelet Disord. 2015. 16. 321.
33. Xu X. et al. Hyaluronic acid-based hydrogels: from a Natural Polysaccharide to Complex Networks. Soft Matter. 2012. 8 (12). 3280-3294.
34. Fakhari A. Biomedical application of hyaluronic acid nanoparticles. PhD thesis. 2012.
35. Burdick J.A., Prestwich G.D. Hyaluronic acid hydrogels for biomedical applications. Adv. Mater. 2011. 23 (12). H41-H56
36. Collins M.N., Birkinshaw C. Hyaluronic acid based sca olds for tissue engineering: A review. Carbohyd. Polym. 2013. 92 (2). 1262-1279.
37. Yoshioka K. et al. Pharmacological e ects of novel cross-linked hyaluronate, Gel-200, in experimental animal models of osteoarthritis and human cell lines. Osteoarthr. Cartil. 2014 22 (6). 879-887
38. Sun S.F. et al. Comparison of single intra-articular injection of novel hyaluronan (HYA-JOINT Plus) with synvisc-one for knee osteoarthritis: a Randomized, Controlled, Double-Blind Trial of Ecacy and Safety. J. Bone Joint. Surg. Am. 2017. 99 (6). 462-471
39. Hangody L. et al. Intraarticular injection of a cross-linked sodium hyaluronate combined with triamcinolone hexacetonide (cingal) to provide symptomatic relief of osteoarthritis of the knee: A Randomized, Double-Blind, Placebo-Controlled Multicenter Clinical Trial. Cartilage. 2017. 1947603517703732.

/24-1.jpg)
/25-1.jpg)
/26-1.jpg)
/27-1.jpg)
/28-1.jpg)