Резюме
Актуальність. У статті розглядаються питання взаємозв’язків структурних змін печінки з показниками імунологічного статусу у хворих із хронічним вірусним гепатитом С (ХГС). Мета: визначити особливості змін імунологічного статусу та вуглеводного обміну у хворих на ХГС залежно від стадії фіброзу. Матеріали та методи. Обстежені 94 пацієнти з хронічним гепатитом С, середній вік яких становив (49,91 ± 11,23) року. Виконане морфологічне дослідження в 42 хворих, зсувно-хвильову еластографію печінки (ЗХЕ), оцінку коефіцієнта затухання ультразвуку. Для вивчення асоціацій імунологічного статусу та вуглеводного обміну із структурними змінами печінки усіх хворих розподілено на групи: з помірним (FІ + FІІ) та вираженим фіброзом (FІІІ + FIV) за шкалою METAVIR. Визначали субпопуляційний склад лімфоцитів, циркулюючих імунних комплексів, проводили оцінку імунного статусу. Здійснили оцінку інсулінорезистентності за допомогою індексу HOMA-IR. Статистичну обробку отриманих результатів проводили за допомогою пакета прикладних програм Statistica 6.1 (серійний номер AGAR909 E415822FA). Результати. У 73,4 % хворих на ХГС знижено відносний вміст СD3+-лімфоцитів. Медіана відносного вмісту СD4+-лімфоцитів була нижчою в 1,4 раза (р < 0,05) порівняно з контролем. У хворих на ХГС СD4+-клітини стимулюють продукцію антитіл В-лімфоцитами (r = 0,56, р < 0,01) й активують СD8+ Т-клітини (r = 0,59, р < 0,01), специфічні для вірусінфікованих клітин. Порушення (зниження) індексу імунорегуляції встановлено в 79,8 % хворих. Визначений негативний вірогідний зв’язок між вмістом Т-хелперів та ЗХЕ печінки (r = –0,26, р < 0,05). За результатами SWE серед обстежених у 66 (70,2 %) хворих на ХГС діагностовано помірний фіброз, у 28 (29,8 %) пацієнтів виявлено виражений фіброз. Визначено збільшення вмісту інсуліну у хворих на ХГС із вираженим фіброзом відносно його рівня в групі контролю у 2,3 раза (р < 0,05) та хворих із помірним фіброзом в 1,3 раза (р < 0,05), установлений зв’язок цього показника з жорсткістю печінки за даними SWE (r = 0,43, р < 0,05). У хворих на ХГС встановлений зв’язок між рівнем ІЛ-6 та SWE печінки (r = 0,68, р < 0,01), ступенем фіброзу (за METAVIR) (r = 0,57, р < 0,01). Окремі імунологічні показники (вміст В-лімфоцитів, Т-хелперів, TNF-α, ІЛ-6 та інсуліну) можуть бути використані для розробки неінвазивної діагностики помірного та вираженого фіброзу печінки у хворих на ХГС. Висновки. У хворих на ХГС прогресування фіброзу печінки супроводжується виснаженням клітинної ланки імунітету, підвищенням рівня прозапальних цитокінів та порушенням вуглеводного обміну залежно від вираженості фіброзної трансформації.
Актуальность. В статье рассматриваются вопросы взаимосвязей структурных изменений печени с показателями иммунологического статуса у больных с хроническим вирусным гепатитом С (ХГС). Цель: определить особенности изменений иммунологического статуса и углеводного обмена у больных ХГС в зависимости от стадии фиброза. Материалы и методы. Обследованы 94 пациента с хроническим гепатитом С, средний возраст которых составил (49,91 ± 11,23) года. Выполнили морфологическое исследование у 42 больных, сдвиговолновую эластографию печени (СВЭ) и оценку коэффициента затухания ультразвука. Для изучения ассоциаций иммунологического статуса и углеводного обмена со структурными изменениями печени всех больных разделили на группы: с умеренным (FI + FII) и выраженным фиброзом (FIII + FIV) по шкале METAVIR. Определяли субпопуляционный состав лимфоцитов, циркулирующих иммунных комплексов, проводили оценку иммунного статуса. Осуществили оценку инсулинорезистентности с помощью индекса HOMA-IR. Статистическую обработку полученных результатов проводили с помощью пакета прикладных программ Statistica 6.1 (серийный номер AGAR909 E415822FA). Результаты. У 73,4 % больных ХГС снижено относительное содержание СD3+-лимфоцитов. Медиана относительного содержания СD4+-лимфоцитов была ниже в 1,4 раза (р < 0,05) по сравнению с контролем. У больных ХГС СD4+-клетки стимулируют продукцию антител В-лимфоцитами (r = 0,56, р < 0,01) и активируют СD8+ Т-клетки (r = 0,59, р < 0,01), специфические для вирусинфицированных клеток. Нарушение (снижение) индекса иммунорегуляции установлено у 79,8 % больных. Определены отрицательные корреляционные связи между содержанием Т-хелперов и СВЭ печени (r = –0,26, р < 0,05). Определено увеличение содержания инсулина у больных ХГС с выраженным фиброзом относительно его уровня в группе контроля в 2,3 раза (р < 0,05) и больных с умеренным фиброзом в 1,3 раза (р < 0,05), установлена связь этого показателя с жесткостью печени по данным СВЭ (r = 0,43, р < 0,05). Выявлена связь между уровнем ИЛ-6 и СВЭ печени (r = 0,68, р < 0,01), степенью фиброза (по METAVIR) (r = 0,57, р < 0,01). Отдельные иммунологические показатели (содержание В-лимфоцитов, Т-хелперов, TNF-α, ИЛ-6 и инсулина) могут быть использованы для разработки неинвазивной диагностики умеренного и выраженного фиброза печени у больных с ХГС. Выводы. У больных с ХГС прогрессирование фиброза печени сопровождается истощением клеточного звена иммунитета, повышением уровня провоспалительных цитокинов и нарушением углеводного обмена в зависимости от выраженности фиброзной трансформации.
Background. The article deals with the relationship between structural changes in the liver and immunological parameters in patients with chronic hepatitis C virus (HCV). The purpose of the study is to define the peculiarities of changes in the immune status and carbohydrate metabolism in patients with chronic HCV depending on the stage of fibrosis. Materials and methods. The research involved 94 patients with chronic HCV who were undergoing treatment at the Department of Liver and Pancreatic Diseases of the State Institution “Institute of Gastroenterology of the National Academy of Medical Sciences of Ukraine”. The diagnosis was verified on the basis of a thorough analysis of complaints, medical history, serological methods, ultrasound results, shear wave elastography, liver steatometry and morphological studies, in accordance with the recommendations of international consensus. Then these measurements were used to determine the average values that characterized the liver stiffness in kilopascals. Forty-two patients underwent a morphological examination. To study the associations of immunological status and carbohydrate metabolism with structural liver changes, all patients were divided into groups: moderate (FI + FII) and severe fibrosis (FII + FIV) according to METAVIR score. The subpopulation composition of lymphocytes was determined using the monoclonal antibodies (Sorbent TM) to molecules CD3, CD19, CD4, CD8, CD16. The immune status assessment was performed according to the guidelines of R.V. Petrov (1992). The level of circulating immune complexes was determined by the method of V. Haskov (1977). During the investigation, sets of reagents of Vector-BEST company were used to measure the amount of tumor necrosis factor α (TNF-α), interleukins (IL) 6 and 10, and those manufactured by DRG (Germany) — to measure insulin in the blood serum. The enzyme-linked immunosorbent assay was performed using Stat Fax 303 Plus analyzer (USA). The insulin resistance was evaluated using the homeostasis model assessment. Statistical processing of the results was performed using the software package Statistica 6.1 (serial number AGAR909 E415822FA). Results. According to shear wave elastography results, moderate fibrosis was diagnosed in 66 (70.2 %) patients with chronic HCV, and 28 (29.8 %) patients demonstrated severe fibrosis. As a result of the investigation performed, the obtained data showed that in 73.4 % (69 of 94 cases) of patients with the chronic HCV, the content of CD3+ lymphocytes reduced relatively. The median of the relative CD4+ lymphocyte content decreased significantly — by 1.4 times (p < 0.05) as compared to the control group. The results of the correlation study showed that in patients with chronic HCV, CD4+ cells stimulated the production of antibodies by B-lymphocytes (r = 0.56, p < 0.01) and activated CD8+ T-cells (r = 0.59, p < 0.01) specific to virus-infected cells. The immunoregulatory index impairment (decrease) was found in 79.8 % of cases (75 of 94 patients). Individuals with chronic HCV were found to have a negative plausible correlation between T-helper content and liver stiffness (r = –0.26, p < 0.05). In addition, a probable increase in insulin content was found in chronic HCV patients with severe fibrosis, by 2.3 times in relation to its level in the control group (p < 0.05), and in patients with moderate fibrosis — by 1.3 times (p < 0.05). According to shear wave elastography data, a correlation was reported between this index and liver stiffness (r = 0.43, p < 0.05). Thus, in patients with chronic HCV, a correlation was established between IL-6 and: the liver stiffness according to shear wave elastography (r = 0.68, p < 0.01), the fibrosis stage according to METAVIR score (r = 0.57, p < 0.01). These data indicate that certain immunological indicators (B-lymphocyte, T-helper, TNF-α, IL-6 and insulin contents) can be used to develop non-invasive diagnosis of moderate and severe liver fibrosis in patients with chronic HCV. Conclusions. In patients with chronic HCV, the progression of liver fibrosis is accompanied by the depletion of the cellular immune system, increased levels of proinflammatory cytokines and impaired carbohydrate metabolism depending on the severity of fibrotic transformation.
Вступ
Основний шлях прогресування хронічних захворювань печінки, що призводить до дифузних уражень печінкової паренхіми, — це процес активації фіброгенезу. Причиною дифузних захворювань печінки часто є хронічний вірусний гепатит, що асоційований із вірусом С (ХГС) [1, 2].
Гепатит С є одною з найбільш небезпечних хвороб печінки вірусної етіології, поширеність якої щорічно зростає. За оцінками Всесвітньої організації охорони здоров’я, 130–150 млн осіб інфіковані вірусом гепатиту С, що становить 2,0–2,5 % від загальної чисельності у світі [3]. У 2015 р. у світі 71 млн осіб страждали від хронічної інфекції, HCV; у 2016 р. близько 1,75 млн осіб набули HCV-інфекцію (23,7 випадку інфікування на 100 тис. осіб у глобальних масштабах).
У значної частини інфікованих HCV осіб розів’ється цироз печінки (ЦП) або гепатоцелюлярна карцинома (ГЦК), і щороку від пов’язаних із HCV-інфекцією захворювань печінки (головним чином ЦП і ГЦК) вмирають приблизно 399 тис. осіб [4, 5].
Стеатоз печінки є загальною гістологічною особливістю серед пацієнтів із хронічними захворюваннями печінки, зокрема в кожного другого із ХГС. Жирова дистрофія печінки при ХГС асоційована з такими проблемами, як інсулінорезистентність, швидке прогресування фіброзу, низька відповідь на лікування та зростання ризику ГЦК. Стеатоз зазвичай є оборотним, але може бути передвісником тяжкого стану в умовах розвитку запалення — стеатогепатиту [6].
У наш час проводяться численні дослідження, в яких вивчається роль імунної системи при захворюваннях органів травлення, зокрема, встановлено тісний зв’язок між порушеннями в імунному статусі й формуванням патології гепатобіліарної системи [7–9]. Доведено, що імунна система може бути пригнічена в результаті інтоксикації організму, причини якої різноманітні: токсини мікроорганізмів, які викликають запальний процес, токсична дія застосованих для лікування антибактеріальних препаратів [10].
Нині вважається встановленим, що висока частота формування хронічних форм і розвитку ускладнень обумовлена «вислизанням» вірусу від імунного нагляду. Механізми цього до кінця не визначені. Вважається, що центральну роль в елімінації вірусу гепатиту С відіграє Т-клітинна ланка імунітету. Суттєве значення в підтримці патологічного процесу у хворих має недостатність CD4+ Т-хелперів і дисбаланс цитокінів [11, 12]. Відомо, що в розвитку та прогресуванні ХГС активну участь беруть прозапальні цитокіни, серед яких велику роль відіграє інтерлейкін-6 (ІЛ-6) та фактор некрозу пухлини альфа (TNF-α). Існують роботи, в яких доведено, що ступінь підвищення вмісту TNF-α в сироватці крові корелює з тяжкістю захворювання [14]. Відомо, що TNF-α є медіатором деструкції тканин. Рівень ІЛ-6 у сироватці крові прямо пропорційний їх концентрації в печінці, який показує активність її запалення [15, 16]. Останнім часом вченими всього світу ведеться клінічна валідація різних методів еластографії щодо встановлення стадії фіброзу печінки. Проте на сьогодні в сучасних публікаціях недостатньо приділяється уваги висвітленню взаємозв’язків показників SWE й імунологічного стану у хворих на ХГС.
Отже, механізми, що лежать в основі прогресування структурних змін печінки при ХГС, досі потребують уточнення, у зв’язку з чим питання ролі імунного статусу в посиленні фібротичних процесів залишається актуальним.
Мета дослідження: визначити особливості змін імунологічного статусу та вуглеводного обміну у хворих на ХГС залежно від стадії фіброзу.
Матеріали та методи
У дослідження були залучені 94 пацієнти з ХГС, що перебували на лікуванні у відділенні захворювань печінки та підшлункової залози ДУ «Інститут гастроентерології НАМНУ». Серед обстежених чоловіків було 50 (53,2 %), жінок — 44 (46,8 %), середній вік яких становив (49,91 ± 11,23) року. Контрольну групу становили 30 практично здорових осіб. Усі пацієнти надали згоду на участь у дослідженні. Подані для публікації матеріали не суперечать положенням біоетики.
Верифікація діагнозу здійснювалась на підставі ретельного аналізу скарг, даних анамнезу, серологічних методів, результатів УЗД, зсувно-хвильової еластометрії, стеатометрії печінки та морфологічного досліджень згідно з рекомендаціями міжнародних консенсусів. Морфологічне дослідження виконане 42 хворим. При аналізі даних окремо по стадіях фіброзу вірогідних відмінностей показників SWE печінки не виявлено; при поєднанні FІ та FІІ і FІІІ з FIV ми отримали вірогідну різницю жорсткості печінки. Для вивчення асоціацій імунологічного статусу та вуглеводного обміну зі структурними змінами печінки усіх хворих розподілено на групи: з помірним (FІ + FІІ) та вираженим фіброзом (FІІІ + FIV) за шкалою METAVIR.
Зсувно-хвильову еластографію виконано усім хворим на апараті Soneus P7 (Україна, Швейцарія) датчиком конвексного формату 2–5 МГц на глибині 10–50 мм від капсули. Після цього із зазначених вимірів визначали середні значення, які характеризували жорсткість паренхіми печінки в кілопаскалях (кПа). Для оцінки стадії фіброзу використовували порогові значення G. Ferraioli: F0–1 ст. — до 6,5 кПа; F2 ст. — до 7,1 кПа; F3 ст. — до 8,7 кПа; F4 ст. — 10,4 і більше за шкалою METAVIR. Крім того, на цьому ж апараті визначали коефіцієнт затухання ультразвуку в дБ/см — метод кількісної оцінки ступеня стеатозу печінки.
Субпопуляційний склад лімфоцитів визначали за допомогою моноклональних антитіл фірми «Сорбент ТМ» до молекул СD3, СD19, СD4, СD8, СD16. Мононуклеарні клітини виділяли з периферичної венозної крові пацієнтів у градієнті щільності 1,077 г/см. Оцінку імунного статусу проводили згідно з рекомендаціями Р.В. Петрова (1992).
Циркулюючі імунні комплекси (ЦІК) визначали за методом V. Haskova (1977). У роботі використовували набори реактивів фірми «Вектор-БЕСТ» для визначення кількості TNF-α, ІЛ-6, ІЛ-10 та фірми DRG (Німеччина) для визначення інсуліну в сироватці крові. Імуноферментний аналіз проводили за допомогою аналізатора Stat Fax 303 Plus (США).
Визначення показника інсулінорезистентності проводили за допомогою індексу HOMA-IR, що розраховували за формулою:
HOMA-IR = глюкоза натще (ммоль/л) × інсулін натще (мкОд/мл)/22,5.
Статистичну обробку отриманих результатів проводили за допомогою пакета прикладних програм Statistica 6.1 (серійний номер AGAR909 E415822FA). Для опису даних застосовували медіану (Me), нижній (Q1) та верхній (Q2) квартилі. Порівняння здійснювали за допомогою непараметричного критерію Манна — Уїтні. Статистичну значущість оцінювали на рівні не нижче, ніж 95,0 % (р < 0,05). Ступінь взаємозв’язків між змінними оцінювали за допомогою значущих коефіцієнтів кореляції Спірмена (r).
Результати
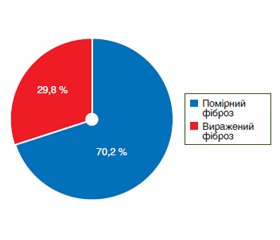
За результатами SWE серед обстежених у 66 (70,2 %) хворих на ХГС діагностовано помірний фіброз, у 28 (29,8 %) пацієнтів виявлено виражений фіброз (рис. 1).
Результати отриманих даних роботи показали, що в 73,4 % хворих на ХГС було знижено відносний вміст СD3+-лімфоцитів (табл. 1). Враховуючи, що клітинний імунітет здійснюється сенсибілізованими Т-лімфоцитами, а у хворих на ХГС вміст Т-клітин вірогідно знижений, можна вважати, що в них імунна відповідь має депресивний характер.
У 85,1 % (80 із 94 хворих) спостерігаємо значне зниження Т-хелперної субпопуляції. Медіана відносного вмісту СD4+-лімфоцитів була вірогідно зниженою в 1,4 раза (р < 0,05) порівняно з контрольною групою.
Слід зазначити, що імунна відповідь організму на деструкцію тканин ніколи не розвивається за типом клітинної реакції в чистому вигляді. Паралельно з розвитком клітинних реакцій завжди відбувається синтез антитіл, активується продукція цитокінів, які можуть модифікувати клітинну відповідь. Результати кореляційного дослідження показали, що у хворих на ХГС СD4+-клітини стимулюють продукцію антитіл В-лімфоцитами (r = 0,56, р < 0,01) й активують СD8+ Т-клітини (r = 0,59, р < 0,01), специфічні для вірусінфікованих клітин.
Цитотоксична імунна відповідь повинна вмикати неспецифічну ланку — СD16+ і антигеннеспецифічну ланку — цитотоксичні лімфоцити, що повинно забезпечувати захист організму від внутрішньоклітинних патогенів, у тому числі від вірусів. У хворих встановлено вірогідне зниження відносного вмісту СD16+-лімфоцитів у 1,6 раза (р < 0,05) відносно групи контролю. Отже, активація В-лімфоцитів у 38,3 % (36 із 94 хворих) хворих вказує на активацію гуморальної ланки імунітету, що, однак, не призводить до елімінації патогену у хворих на ХГС. Надлишок антитіл сприяє посиленню цитотоксичних реакцій і призводить до імунокомплексного ураження печінки. Ліпопротеїнові мембрани гепатоцитів можуть набути властивості чужорідного антигена, що індукує атаку Т-кілерів, що закінчується лізисом клітин-мішеней, тобто паренхіми печінки. Важливе прогностичне значення в перебігу процесу має співвідношення рівня лімфоцитів СD4+/СD8+ та імунорегуляторного індексу. Порушення (зниження) індексу імунорегуляції встановлено в 79,8 % (75 із 94 хворих) хворих.
У хворих на ХГС установлений позитивний вірогідний зв’язок між рівнем Т-хелперів та вмістом Т-кілерів (r = 0,43, р < 0,01). Крім того, у цих хворих установлений зв’язок між рівнем Т-супресорів та ІЛ-6 (r = –0,29, р < 0,01).
Виявлене в результаті дослідження зниження відносних показників СD3+, СD4+, СD4+/СD8+ свідчить про недостатність клітинного імунітету у хворих на ХГС, що, можливо, сприяє формуванню фіброзу.
У хворих на ХГС визначений негативний вірогідний зв’язок між рівнем Т-хелперів та жорсткістю селезінки та печінки (r = –0,26, р < 0,05).
У 85,1 % (80 із 94 хворих) хворих на ХГС рівень ЦІК був вірогідно підвищений (р < 0,05) відносно рівня контролю.
Вірогідну відмінність між відносним вмістом СD8+- (підвищення в 1,4 раза, р < 0,05), СD19+-лімфоцитів (підвищення в 1,4 раза, р < 0,05), СD16+-клітин (зниження в 1,3 раза, р < 0,05), рівнем ЦІК (підвищення в 1,5 раза, р < 0,05) установлено у хворих із вираженим фіброзом порівняно з помірним (табл. 1).
У хворих на ХГС установлене вірогідне збільшення рівня інсуліну в 1,9 раза (р < 0,05) порівняно із значенням контрольної групи (табл. 2). Крім того, установлено вірогідне збільшення вмісту інсуліну у хворих на ХГС із вираженим фіброзом відносно його рівня в групі контролю в 2,3 раза (р < 0,05) та хворих із помірним фіброзом у 1,3 раза (р < 0,05). Установлено кореляційний зв’язок даного показника з жорсткістю печінки за даними SWE (r = 0,43, р < 0,05) та зі ступенем фіброзу (за шкалою METAVIR) (r = 0,43, р < 0,05).
Значення індексу HOMA-IR у хворих були вище 3,0 і вірогідно відрізнялись від даних у групі контролю. Ці зміни були більш виражені у хворих із вираженим фіброзом у 2,6 раза (р < 0,05), що вказує на порушення вуглеводного обміну.
Проведені дослідження показали, що медіана концентрації ІЛ-6 була вірогідно вищою в 1,7 раза (р < 0,05) у хворих на ХГС порівняно з групою контролю. Установлене підвищення рівня ІЛ-6 у сироватці крові вказує на прогресування запальних процесів та сприяє розвитку стеатогепатиту та фіброзу у хворих на ХГС. На це вказує і вірогідне збільшення даного показника в 53,2 % хворих (50 із 94) із вираженим фіброзом — у 1,8 раза (р < 0,05) порівняно із значенням при помірному фіброзі. Так, у хворих на ХГС установлений зв’язок між рівнем ІЛ-6 та жорсткістю печінки за даними SWE (r = 0,68, р < 0,01), ступенем фіброзу (за шкалою METAVIR) (r = 0,57, р < 0,01).
Концентрація TNF-α у хворих на ХГС була вірогідно вищою (у 9,2 раза, р < 0,05) порівняно з групою контролю. У хворих із вираженим фіброзом визначено вірогідне збільшення медіани рівня TNF-α (у 3,0 та у 21,8 раза, р < 0,05) відповідно порівняно з його рівнем у хворих із помірним фіброзом та контрольною групою.
Підвищення TNF-α/ІЛ-10 в 1,4 раза (р < 0,05) установлено у хворих на ХГС, у 1,5 раза (р < 0,05) — у хворих із вираженим фіброзом порівняно зі значеннями групи контролю.
Разом із цим розвиток фіброзної трансформації печінки, ймовірно, відбувається на тлі вираженого запалення, про що свідчать установлені позитивні кореляційні зв’язки показника жорсткості печінки за даними SWE із рівнем TNF-α (r = 0,51, р < 0,05) та співвідношенням прозапальних та протизапальних цитокінів (r = 0,43, р < 0,05).
Обговорення
Отримані дані свідчать про те, що зміна імунного статусу при різних ступенях фіброзу визначається, наімовірніше, тривалістю перебігу захворювання. На більш пізніх стадіях (виражений фіброз) спостерігається тенденція до виснаження імунної системи у хворих із ХГС. Установлені зниження відносних показників СD3+, СD4+ та збільшення коефіцієнта СD4+/СD8+ на фоні вираженості фіброзної трансформації печінки у хворих на ХГС. При цьому залишається високою експресія активаційних антигенів, що побічно вказує на порушення в проведенні сигналів у клітинах імунної системи. Недостатність енергетичного потенціалу лімфоцитів, порушення дозрівання і диференціювання субпопуляцій імунорегуляторних клітин супроводжуються різкою зміною кількісних і функціональних показників імунокомпетентних клітин, що є головною ланкою в патогенезі вторинних імунодефіцитних станів при прогресуванні фіброзу у хворих на ХГС [12], що підтверджується встановленим негативним вірогідним кореляційним зв’язком між рівнем Т-хелперів та жорсткістю печінки (r = –0,26, р < 0,05).
Підвищений рівень TNF-α впродовж тривалого часу пригнічує активність Т-хелперів 1 типу, а отже, і клітинну імунну відповідь. З одного боку, TNF-α є необхідним для проліферації гепатоцитів і запобігання їх апоптозу при регенерації печінки, з іншого — є медіатором гепатотоксичності при бактеріальних, вірусних і токсичних впливах. До того ж ступінь підвищення вмісту TNF-α в сироватці крові корелює з тяжкістю захворювання [14]. В обстежених нами пацієнтів із ХГС із прогресуванням фіброзу баланс між прозапальними та протизапальними цитокінами порушується на користь перших, що перешкоджає контролю над запаленням і фіброгенезу. Установлено високий кореляційний зв’язок між рівнем TNF-α та даними SWE, що збігається з даними інших досліджень [1].
Отже, виснаження клітинної ланки імунітету та підвищення рівня інсуліну, ІЛ-6, TNF-α у сироватці крові у хворих на ХГС пов’язані з погіршенням структурних змін печінки і вірогідно сприяє прогресуванню фіброзу. За результатами нашого дослідження встановлено, що окремі імунологічні показники (вміст В-лімфоцитів, Т-хелперів, TNF-α, ІЛ-6 та інсуліну) можуть бути використані для включення до алгоритму скринінгу помірного та вираженого фіброзу печінки у хворих на ХГС.
Висновки
У хворих на ХГС прогресування фіброзу печінки супроводжується виснаженням клітинної ланки імунітету, підвищенням рівня прозапальних цитокінів та порушенням вуглеводного обміну залежно від вираженості фіброзної трансформації.
Перспективи подальших досліджень. Перспективним і важливим науковим напрямом вважаємо розробку алгоритму скринінгу вираженого фіброзу печінки у хворих на ХГС з урахуванням показників імунологічного стану.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів і власної фінансової зацікавленості при підготовці даної статті.
Інформація про фінансування. Дослідження виконано в рамках держбюджетної НДР № 5 «Вивчити особливості формування і прогресування стеатозу та фіброзу в пацієнтів із хронічними дифузними захворюваннями печінки залежно від етіологічних факторів», номер держреєстрації 0115U007179.
Список литературы
1. Булатова И.А., Щекова А.П., Насибуллина Н.И., Щекова В.В., Падучева С.В. Определение стадии фиброза печени с использованием комплекса биомаркеров, включающего фактор некроза опухолей. Новости «Вектор-Бест». 2016. 1(79). С. 1-6.
2. Bracht Т., Mölleken С., Ahrens М., Poschmann G., Schlosser A., Eisenacher M. et al. Evaluation of the biomarker candidate MFAP4 for non-invasive assessment of hepatic fibrosis in hepatitis C patients. J. Transl. Med. 2016. 14. Р. 201. doi: 10.1186/s12967-016-0952-3. PubMed PMID: 27378383. PMCID: PMC4932744.
3. Еналеева Д.Ш., Фазылов В.Х., Созинов А.С. Хронические вирусные гепатиты В, С и D: Руководство для врачей. Москва: ГЭОТАР-Медиа, 2015. 192 с.
4. Сергєєва Т.А. Гепатит С в Україні: епідеміологічна характеристика та оцінка тягаря. Київ: Центр громадського здоров’я, 2018. С. 111. https://www.phc.org.ua/sites/default/files/uploads/files/VGC-2018.pdf
5. World Health Organization. Global Hepatitis Report, 2017. Geneva: WHO, 2017. http://apps.who.int/iris/bitstream/handle/10665/255017/WHO-HIV-2017.06-eng.pdf?sequence=1
6. Grace Lai-Hung Wong Transient elastography: Kill two birds with one stone? World J. Hepatol. 2013, May 27. 5(5). С. 264-274. doi: 10.4254/wjh.v5.i5.264 PMID: 23717737. PubMed Central PMCID: PMC3664284.
7. Татарчук О.М., Діденко В.І., Меланіч С.Л., Кудрявцева В.Є. Імунологічна реактивність у хворих на хронічні дифузні захворювання печінки. Гастроентерологія. 2018. 4(52). С. 222-226. doi: https://doi.org/10.22141/23082097.52.4.2018.154142.
8. Сляднев С.А. Медиаторы межклеточных взаимодействий при неалкогольной жировой болезни печени. Вестник молодого ученого. 2015. 3(10). С. 3-8.
9. Останин А.А., Старостина Н.М., Меледина И.В. и др. Мультиплексный анализ 26 цитокинов, секретируемых клетками крови больных циррозом печени. Медицинская иммунология. 2015. 6(17). Р. 539-552. https://doi. org/10.15789/1563-0625-2015-6-539-552.
10. Bellot P., Frances R., Such J. Pathological bacterial translocation in cirrhosis: pathophysiology, diagnosis and clinical implications. Liver Int. 2013. 1(33). Р. 31-39.
11. Сахарова Д.А., Терешков П.П., Витковский Ю.А. Клеточный иммунитет у больных хроническим вирусным гепатитом С. Дальневосточный медицинский журнал. 2013. 4. С. 21-24. https://elibrary.ru/item.asp?id=21181062
12. Ивашкин В.Т. Иммунная система и повреждения печени при хронических гепатитах В и С. РЖГГК. 2009. 6. С. 4-10.
13. Wong V.W., Vergniol J., Wong G.L. et al. Diagnosis of fibrosis and cirrhosis using liver stiffness measurement in nonalcoholic fatty liver disease. Hepatology. 2010 Feb. 51(2). Р. 454-62. doi: 10.1002/hep.23312. PubMed PMID: 20101745.
14. Шадрін О.Г., Чернега Н.Ф., Марушко Р.В., Брюзгіна Т.С. Стан жирно-кислотного спектру крові у дітей із захворюваннями печінки та його зв’язок з показниками цитокінового статусу. Вісник проблем біології та медицини. 2015. 1(117). С. 193-198.
15. Oh H., Jun D.W., Saeed W.K., Nguyen M.H. Non-alcoholic fatty liver diseases: update on the challenge of diagnosis and treatment. Clin. Mol. Hepatol. 2016. 22(3). Р. 327-335. doi: 10.3350/cmh.2016.0049.
16. Wieckowska A., Papouchado B.G., Li Z., Lopez R., Zein N.N., Feldstein A.E. Increased hepatic and circulating interleukin-6 levels in human nonalcoholic steatohepatitis. 2008. 103(6). Р. 1372-9. doi: 10.1111/j.1572-0241.2007.01774.x.
/29.jpg)

/29_2.jpg)
/30.jpg)