Журнал "Гастроэнтерология" Том 54, №3, 2020
Вернуться к номеру
Якість життя дітей з неалкогольною жировою хворобою печінки
Авторы: Степанов Ю.М., Завгородня Н.Ю., Завгородня О.Ю.
ДУ «Інститут гастроентерології НАМН України», м. Дніпро, Україна
Рубрики: Гастроэнтерология
Разделы: Клинические исследования
Версия для печати
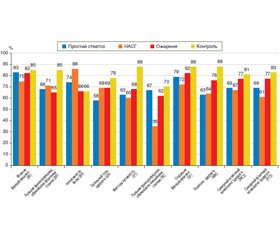
Актуальність. Неалкогольна жирова хвороба печінки (НАЖХП) обіймає провідні позиції серед хронічних захворювань печінки в педіатричній популяції. Незважаючи на малосимптомний перебіг захворювання, у дітей із НАЖХП спостерігається значна частота виявлення психоемоційних розладів, порушення соціальної адаптації, низька толерантність до фізичних навантажень, що призводить до погіршення якості життя хворих. Мета: проаналізувати зміни якості життя дітей із НАЖХП залежно від стадії захворювання (простий стеатоз, неалкогольний стеатогепатит (НАСГ)) за опитувальником Short Form-36 (SF-36) та визначити вплив клінічних проявів захворювання на параметри якості життя. Матеріали та методи. В обстеження включено 170 пацієнтів віком від 6 до 17 років (середній вік — (12,15 ± 2,51) року). Пацієнти були розподілені на 4 групи: 1 групу становили 53 пацієнти з простим стеатозом печінки, 2 групу — 37 пацієнтів з неалкогольним стеатогепатитом, 3 групу — 65 пацієнтів з надмірною вагою та ожирінням без стеатозу печінки, 4 групу (контрольну) — 15 пацієнтів з нормальною вагою. Оцінка якості життя проводилась за допомогою скороченої форми опитувальника якості життя Medical Outcomes Study — Short Form-36. Результати. Незалежно від стадії захворювання у дітей із НАЖХП спостерігалось вірогідне зниження сумарних показників, що характеризують як психічний, так і фізичний компонент здоров’я. Аналіз фізичної складової здоров’я за окремими шкалами продемонстрував, що діти з НАЖХП (простим стеатозом) були найбільш незадоволеними за шкалою загального стану здоров’я (р < 0,05). У дітей із НАЖХП оцінка рольового функціонування, пов’язаного з фізичним станом, виявила тенденцію до зниження (р > 0,05). Інтенсивність больового синдрому незначно впливала на загальну характеристику фізичного компонента здоров’я дітей із НАЖХП і вірогідно відрізнялась від групи контролю лише у пацієнтів із НАСГ (р < 0,05). Аналіз психічної складової здоров’я у дітей із НАЖХП продемонстрував обмеження життєвої активності та значуще погіршення показників психічного здоров’я порівняно з дітьми з нормальною вагою (р < 0,05). Прогресування НАЖХП супроводжувалось погіршенням сумарних рівнів фізичного та психічного компонентів здоров’я. Провідною причиною значущого погіршення психічного компонента здоров’я у дітей із НАСГ стала психоемоційна дезадаптація: показник оцінки за шкалою рольового функціонування, обумовленого емоційним станом, продемонстрував значно нижчий рівень порівняно з дітьми з простим стеатозом печінки (р < 0,05). Причиною погіршення фізичного компонента здоров’я дітей із НАСГ було зростання частоти виявлення клінічної симптоматики, пов’язаної з супутніми захворюваннями (стеатоз підшлункової залози, гастроезофагеальна рефлюксна хвороба, синдром надмірного бактеріального росту). Якість життя дітей із НАЖХП негативно корелювала з наявністю інтестинальних розладів за шкалами соціального та фізичного функціонування, інтенсивністю больового синдрому, обумовленого супутньою патологією біліарного тракту, кишечника, підшлункової залози. Висновки. Вивчення якості життя дітей із НАЖХП за допомогою опитувальника SF-36 показало, що захворювання негативно впливає на фізичний та психічний компоненти здоров’я вже на етапі простого стеатозу, якість життя погіршується у хворих із НАСГ внаслідок зростання нестабільності психоемоційної сфери. Під час прогресування НАЖХП спостерігається збільшення частоти виявлення коморбідних станів, що накладає негативний відбиток на показники якості життя й вимагає своєчасної їх корекції.
Актуальность. Неалкогольная жировая болезнь печени (НАЖБП) в последние годы лидирует среди хронических заболеваний печени в педиатрической популяции. Несмотря на малосимптомное течение заболевания, у детей с НАЖБП достаточно часто наблюдаются психоэмоциональные расстройства, нарушения социальной адаптации, низкая толерантность к физическим нагрузкам, что приводит к ухудшению качества жизни пациентов. Цель: проанализировать изменения качества жизни детей с НАЖБП в зависимости от стадии заболевания (простой стеатоз, неалкогольный стеатогепатит (НАСГ)) с помощью опросника Short Form-36 (SF-36) и исследовать влияние клинических проявлений заболевания на параметры качества жизни. Материалы и методы. В обследование включены 170 пациентов в возрасте от 6 до 17 лет, средний возраст составил (12,15 ± 2,51) года. Пациенты были распределены на 4 группы: 1 группу составили 53 пациента с простым стеатозом печени, 2 группу — 37 пациентов с неалкогольным стеатогепатитом, 3 группу — 65 пациентов с избыточным весом и ожирением без стеатоза печени, 4 группу (контрольную) — 15 пациентов с нормальным весом. Оценка качества жизни проводилась с помощью сокращенной формы опросника качества жизни Medical Outcomes Study — Short Form-36. Результаты. Независимо от стадии заболевания у детей с НАЖБП наблюдалось достоверное снижение суммарных показателей, характеризующих как психический, так и физический компонент здоровья. Анализ физической составляющей здоровья по отдельным шкалам показал, что дети с НАЖБП (простым стеатозом) имели наиболее низкие показатели при оценивании по шкале общего состояния здоровья (р < 0,05). У детей с НАЖБП оценка ролевого функционирования, связанного с физическим состоянием, продемонстрировала тенденцию к снижению (р > 0,05). Интенсивность болевого синдрома незначительно влияла на общую характеристику физического компонента здоровья детей с НАЖБП и достоверно отличалась от группы контроля только у пациентов с НАСГ (р < 0,05). Анализ психической составляющей здоровья у детей с НАЖБП продемонстрировал ограничение жизненной активности и значимое ухудшение показателей психического здоровья по сравнению с детьми с нормальным весом (р < 0,05). Прогрессирование НАЖБП сопровождалось ухудшением суммарных уровней физического и психического компонентов здоровья. Ведущей причиной значительного ухудшения психического компонента здоровья у детей с НАСГ стала психоэмоциональная дезадаптация: показатель оценки по шкале ролевого функционирования, обусловленного эмоциональным состоянием, продемонстрировал значительно более низкий уровень по сравнению с детьми с простым стеатозом печени (р < 0,05). Причиной ухудшения физического компонента здоровья детей с НАСГ был рост частоты выявления клинической симптоматики, связанной с сопутствующими заболеваниями (стеатоз поджелудочной железы, гастроэзофагеальная рефлюксная болезнь, синдром избыточного бактериального роста). Качество жизни детей с НАЖБП негативно коррелировало по шкалам социального и физического функционирования с наличием интестинальних расстройств, интенсивностью болевого синдрома, обусловленного сопутствующей патологией билиарного тракта, кишечника, поджелудочной железы. Выводы. Изучение качества жизни детей с НАЖБП с помощью опросника SF-36 показало, что заболевание негативно влияет на физический и психический компоненты здоровья уже на этапе простого стеатоза, качество жизни снижается у больных НАСГ за счет нарастания нестабильности психоэмоциональной сферы. При прогрессировании НАЖБП наблюдается увеличение частоты выявления коморбидных состояний, что накладывает негативный отпечаток на показатели качества жизни и требует своевременной их коррекции.
Background. Nonalcoholic fatty liver disease (NAFLD) in recent years is the main cause of chronic liver disease in the pediatric population. Despite the generally asymptomatic course of NAFLD in children, there is a significant frequency of psycho-emotional disorders, impaired social adaptation, low tolerance to physical activity among these patients, which leads to a deterioration in the quality of life. The purpose of the study was to analyze the changes in the quality of life in children with NAFLD depending on the stage of the disease (simple steatosis, nonalcoholic steatohepatitis (NASH)) according to the SF-36 questionnaire and to determine the impact of clinical manifestations on the quality of life. Materials and methods. The study included 170 patients aged 6 to 17 years, the mean age was (12.15 ± 2.51) years. The fatty liver was determined on transient elastography (FibroScan® 502 Touch F6015, Echosens, France) with the controlled attenuation parameter (CAP) measurement. Patients were divided into 4 groups according to the presence of hepatic steatosis (as determined by CAP), overweight and obesity (by body mass index), nonalcoholic steatohepatitis (by gender-specific alanine aminotransferase levels): group 1 consisted of 53 patients with simple hepatic steatosis, group 2 included 37 patients with nonalcoholic steatohepatitis, group 3 enrolled 65 overweight and obese patients without hepatic steatosis, group 4 (control) consisted of 15 patients with normal weight. Quality of life assessment was performed using the Medical Outcomes Study — Short Form-36 questionnaire. The calculation was based on 8 scales, 1–4 of which reflect the physical component of health, and 5–8 scales — the mental component of health. The total score of each scale ranged from 0 to 100 points, with fewer points corresponding to a poorer quality of life. Physical component summary and mental component summary were calculated. Statistical processing of research results was carried out by variation statistics methods, implemented by the standard application package SPSS 13.0 for Windows. Results. Regardless of the stage of the disease, children with NAFLD demonstrated a significant reduction in the total levels of both mental and physical components of health. Analysis of the physical component of health on separate scales showed that children with simple steatosis had the lowest level on the scale of general health (p < 0.05). In children with NAFLD, there were no significant changes in the assessment on the scale of physical functioning, but the assessment of role functioning associated with the physical condition showed a tendency to decrease (p > 0.05). The pain intensity had a small effect on the general characteristics of the physical component of the health in children with NAFLD and differed significantly from the control group only in patients with NASH (p < 0.05). The analysis of the mental component of health showed that in children with NAFLD the vital activity was limited and mental health values decreased significantly compared to children with normal weight (p < 0.05). The most common symptoms that impaired the quality of life of the examined children with NAFLD were fatigue, sleep disturbances, and sadness. NAFLD progression was accompanied by a worsening of both physical and mental component summary levels. The leading cause of significant deterioration in the mental health component in children with NASH was role-emotional dysfunction such as psycho-emotional dysadaptation, which manifested itself in the range of interests restriction, limited participation in everyday activities, impaired ability to concentrate in various activities: this rate showed significantly lower levels compared to children with simple hepatic steatosis (p < 0.05).The quality of life of children with NAFLD negatively correlated with the presence of intestinal disorders on the scales of social and physical functioning, the pain intensity caused by comorbid pathology of the biliary tract, intestine, pancreas. Conclusions. Thus, a study of the quality of life in children with NAFLD using the MOS SF-36 questionnaire showed that the disease negatively affects both physical and mental components of health already at the stage of simple steatosis, the quality of life deteriorates in patients with NASH due to increasing instability of psycho-emotional sphere. With NAFLD progression, there is an increase in the frequency of clinical symptoms, probably associated with comorbidity, which has a negative impact on the quality of life and requires timely correction.
якість життя; неалкогольна жирова хвороба печінки; діти
качество жизни; неалкогольная жировая болезнь печени; дети
quality of life; nonalcoholic fatty liver disease; children
Вступ
Матеріали та методи
Результати
Обговорення
Висновки
- Di Sessa A., Marzuillo P., Guarino S. et al. When a secondary form of pediatric non-alcoholic fatty liver disease should be suspected? Expert Review of Gastroenterology & Hepatology. 2019. P. 519-521. doi: 10.1080/17474124.2019.1605290.
- Paglia L.The sweet danger of added sugars. Eur. J. Paediatr. Dent. 2019. Vol. 20(2). P. 89. doi: 10.23804/ejpd.2019.20.02.01.
- Clemente M.G., Mandato C., Poeta M. et al. Pediatric non-alcoholic fatty liver disease: Recent solutions, unresolved issues, and future research directions. World Journal of Gastroenterology. 2016. Vol. 22(36). P. 8078.
- Goldner D., Lavine J.E. Nonalcoholic Fatty Liver Disease in Children: Unique Considerations and Challenges. Gastroenterology. 2020. Vol. 158(7). P. 1967-1983. doi: 10.1053/j.gastro.2020.01.048.
- Forlano R., Mullish B.H., Nathwani R. et al. Non-Alcoholic Fatty Liver Disease and Vascular Disease. Curr. Vasc. Pharmacol. 2020. Mar 17 [published online ahead of print]. doi: 10.2174/1570161118666200318103001.
- Benedict M., Zhang X. Non-alcoholic fatty liver disease: An expanded review. World Journal of Hepatology. 2017. Vol. 9(16). P. 715. doi: 10.4254/wjh.v9.i16.715.
- Pacifico L., Perla F.M., Andreoli G. et al. Nonalcoholic Fatty Liver Disease is Associated with Low Skeletal Muscle Mass in Overweight/Obese Youths. Front Pediatr. 2020. vfd
- Assimakopoulos K., Karaivazoglou K., Tsermpini E.E. et al. Quality of life in patients with nonalcoholic fatty liver disease: A systematic review. Journal of Psychosomatic Research. 2018. Vol. 112. P. 73-80. doi: 10.1016/j.jpsychores.2018.07.004.
- Marcel W.M. Post Definitions of quality of life: what has happened and how to move on. Top Spinal Cord Inj Rehabil. 2014. Vol. 20(3). P. 167-180. doi: 10.1310/sci2003-167.
- Faienza M.F., Chiarito M., Molina-Molina E. et al. Childhood obesity, cardiovascular and liver health: a growing epidemic with age. World Journal of Pediatrics. 2020. Feb 4 [published online]. doi: 10.1007/s12519-020-00341-9.
- Schwimmer J.B. Clinical advances in pediatric nonalcoholic fatty liver disease. Hepatology. 2016. Vol. 63(5). P. 1718-1725. doi: 10.1002/hep.28441.
- Karaivazoglou K., Kalogeropoulou M., Assimakopoulos S. et al. Psychosocial Issues in Pediatric Nonalcoholic Fatty Liver Disease. Psychosomatics. 2019. Vol. 60(1). P. 10-17. doi: 10.1016/j.psym.2018.09.001.
- Ware J.E. SF-36 Health Survey Update. Spine. 2000. Vol. 25, № 24. P. 3130-3139. doi: 10.1097/00007632-200012150-00008.
- Kistler K.D., Molleston J., Unalp A. et al. Nonalcoholic Steatohepatitis Clinical Research Network (NASH CRN). Symptoms and quality of life in obese children and adolescents with non-alcoholic fatty liver disease. Aliment. Pharmacol. Ther. 2010. Vol. 31(3). Р. 396-406. doi: 10.1111/j.1365-2036.2009.04181.x.
- Didsbury M.S., Kim S., Medway M.M. et al. Socio-economic status and quality of life in children with chronic disease: A systematic review. J. Paediatr. Child Health. 2016. Vol. 52(12). P. 1062-1069. doi: 10.1111/jpc.13407.
- Parmar A., Vandriel S.M., Ng V.L. Health-related quality of life after pediatric liver transplantation: A systematic review. Liver Transpl. 2017. Vol. 23(3). P. 361-374. doi: 10.1002/lt.24696.
- Trevizoli I.C., Pinedo C.S., Teles V.O. et al. Autoimmune Hepatitis in Children and Adolescents: Effect on Quality of Life. J. Pediatr. Gastroenterol. Nutr. 2018. Vol. 66(6). P. 861-865. doi: 10.1097/MPG.0000000000001930.
- Vos M.B., Abrams S.H., Barlow S.E. et al. NASPGHAN Clinical Practice Guideline for the Diagnosis and Treatment of Nonalcoholic Fatty Liver Disease in Children: Recommendations from the Expert Committee on NAFLD (ECON) and the North American Society of Pediatric Gastroenterology, Hepatology and Nutrition (NASPGHAN). J. Pediatr. Gastroenterol. Nutr. 2017. Vol. 64(2). P. 319-334. doi: 10.1097/MPG.0000000000001482.
- Nobili V., Alisi A., Valenti L. et al. NAFLD in children: new genes, new diagnostic modalities and new drugs. Nat. Rev. Gastroenterol. Hepatol. 2019. Vol. 16(9). P. 517-530. doi: 10.1038/s41575-019-0169-z.
- Huber Y., Boyle M., Hallsworth K. et al. Health-related quality of life in nonalcoholic fatty liver disease associates with hepatic inflammation. EPoS Consortium Investigators. Clin. Gastroenterol. Hepatol. 2019. Vol. 17(10). P. 2085-2092.e1. doi: 10.1016/j.cgh.2018.12.016.
- Gerber L.H., Weinstein A.A., Mehta R. et al. Importance of fatigue and its measurement in chronic liver disease. World J. Gastroenterol. 2019. Vol. 25(28). P. 3669-3683. doi: 10.3748/wjg.v25.i28.3669.
- Kerkar N., D'Urso C., Van Nostrand K. et al. Psychosocial outcomes for children with nonalcoholic fatty liver disease over time and compared with obese controls. J. Pediatr. Gastroenterol. Nutr. 2013. Vol. 56(1). P. 77-82. doi: 10.1097/MPG.0b013e31826f2b8c.
- Balp M.M., Krieger N., Przybysz R. et al. The burden of non-alcoholic steatohepatitis (NASH) among patients from Europe: A real-world patient-reported outcomes study. JHEP Rep. 2019. Vol. 1(3). P. 154-161. doi: 10.1016/j.jhepr.2019.05.009.
- Younossi Z.M., Stepanova M., Lawitz E.J. et al. Patients with nonalcoholic steatohepatitis experience severe impairment of health-related quality of life. Am. J. Gastroenterol. 2019. Vol. 114(10). P. 1636-1641. doi: 10.14309/ajg.0000000000000375.
- Chawla K.S., Talwalkar J.A., Keach J.C. et al. Reliability and validity of the chronic liver disease questionnaire (CLDQ) in adults with non-alcoholic steatohepatitis (NASH). BMJ Open Gastroenterol. 2016. Vol. 3(1). https://doi.org/10.1136/bmjgast-2015-000069 e000069.
- Sayiner M., Stepanova M., Pham H. et al. Assessment of health utilities and quality of life in patients with non-alcoholic fatty liver disease. BMJ Open Gastroenterol. 2016. Vol. 3(1). e000106. doi: 10.1136/bmjgast-2016-000106.
- David K., Kowdley K.V., Unalp A. et al. NASH CRN Research Group, Quality of life in adults with nonalcoholic fatty liver disease: baseline data from the nonalcoholic steatohepatitis clinical research network. Hepatology. 2009. Vol. 49. P. 1904-1912. doi: 10.1002/hep.22868.
- Schwimmer J.B., Burwinkle T.M., Varni J.W. Health-related quality of life of severely obese children and adolescents. JAMA. 2003. Vol. 289(14). P. 1813-1819. doi: 10.1001/jama.289.14.1813.

/37.jpg)
/38.jpg)
/39.jpg)