Международный эндокринологический журнал Том 17, №2, 2021
Вернуться к номеру
Аналіз віддалених результатів комплексного лікування ішемічної хвороби серця у пацієнтів із предіабетом та явним цукровим діабетом
Авторы: Джунь Я.Ю.(1), Маньковський Г.Б.(1), Руденко Н.М.(1, 2)
(1) — ДУ «Науково-практичний медичний центр дитячої кардіології та кардіохірургії МОЗ України», м. Київ, Україна
(2) — Національний університет охорони здоров’я України імені П.Л. Шупика, м. Київ, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
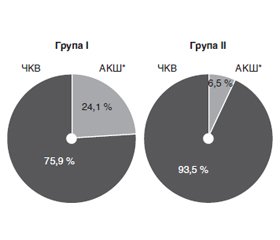
Актуальність. Попри сучасні методи діагностики та лікування порушень обміну глюкози, цукровий діабет (ЦД) залишається незалежним фактором ризику та удвічі збільшує кількість серцево-судинних подій (ішемічна хвороба серця (ІХС), ішемічний інсульт, смерть). Ефективність сучасних методів реваскуляризації міокарда у хворих з цукровим діабетом потребує подальшого вивчення. Мета: оцінка факторів ризику та віддалених результатів реваскуляризації коронарних артерій у пацієнтів із ішемічною хворобою серця та супутнім предіабетом або явним ЦД. Матеріали та методи. У ретроспективному дослідженні брали участь 120 пацієнтів із ІХС, яким було проведено реваскуляризацію коронарних артерій. Залежно від глікемічного статусу пацієнти були розподілені на дві групи: І група (основна група) — хворіли на предіабет або ЦД (n = 58); ІІ група (контрольна група) — пацієнти без порушення глікемії (n = 62). Ступінь ураження коронарних артерій визначали за результатами коронарографії. Результати лікування у пацієнтів обох груп оцінювали за наявністю прогресування атеросклерозу коронарних артерій (повторні втручання з приводу появи нових атеросклеротичних уражень або рестенозу попередньо імплантованого стента) та показниками летальності. Середній термін спостереження хворих у двох групах становить 3 роки (мінімальний — 24 місяці). Результати. У пацієнтів І групи, із предіабетом та явним ЦД, переважає трисудинне ураження коронарних артерій (43,1 vs 16,1 %, p < 0,05); хронічна оклюзія судин серця діагностується частіше, ніж у пацієнтів ІІ групи (43,1 vs 25,8 %, p < 0,05), що характеризує більш тяжчий перебіг захворювання. У хворих основної групи порівняно із групою контролю захворюваність на інфаркт міокарда (45,9 vs 33,9 %, відношення шансів (OR) 6,1 (95% довірчий інтервал (ДІ) 2,76–13,6) p < 0,05), інсульт (13,8 vs 3,2 %, OR 4,8 (95% ДІ 0,97–23,6) p < 0,05) та хронічну ниркову недостатність (10,3 vs 1,6 %, OR 7,0 (95% ДІ 0,82–60,4) p < 0,05) є вірогідно більшою. На відміну від пацієнтів без ЦД, у хворих першої групи показники систолічної функції серця вірогідно нижчі (48,9 ± 11,9 % vs 54,61 ± 7,56 %, p < 0,05). Черезшкірне коронарне втручання є методом вибору реваскуляризації коронарних артерій у пацієнтів із ІХС, проте аортокоронарне шунтування частіше застосовується за наявності ЦД (24,1 vs 6,5 %, p < 0,05). Прогресування атеросклерозу коронарних артерій переважає у пацієнтів із порушеним обміном глюкози (19,0 vs 6,5 %, OR 3,4 (95% ДІ 1,01–11,3) p < 0,05). Летальність у пацієнтів І групи є вищою (12,1 vs 1,6 %, OR 8,4 (95% ДІ 1,00–70,3) p < 0,05). Висновки. Багатосудинне ураження коронарних артерій обумовлює гірший прогноз у пацієнтів із цукровим діабетом. Розвиток повторних порушень кровообігу спостерігається частіше у хворих із порушеним обміном глюкози. Наявність даної патології вірогідно збільшує ризик розвитку інфаркту міокарда, інсульту та хронічної ниркової недостатності.
Background. Despite modern methods for the diagnosis and treatment of impaired glucose metabolism, diabetes mellitus remains an independent risk factor and doubles the number of cardiovascular events (coronary heart disease, ischemic stroke, death). The effectiveness of modern methods for myocardial revascularization in patients with diabetes mellitus needs further researches. The purpose of this study is to evaluate risk factors and long-term outcomes of coronary artery revascularization in patients with coronary heart disease and concomitant prediabetes or overt diabetes mellitus. Materials and methods. This retrospective study involved 120 individuals with coronary heart disease who underwent revascularization of coronary arteries. Patients were divided into two groups according to the glycemic status: group I (main group) — prediabetes or diabetes mellitus (n = 58); group II (controls) — individuals without impaired glycemia (n = 62). Stenosis of coronary arteries was determined by coronary angiography. Treatment outcomes in both groups of patients were assessed as a progression of coronary artery atherosclerosis (repeated interventions caused by new atherosclerotic lesions or restenosis of preimplanted stent) and mortality rates. The average follow-up of patients in two groups is 3 years (minimum of 24 months). Results. Patients of group I predominantly had triple vessel disease (43.1 vs 16.1 %, p < 0.05); chronic occlusion of the heart vessels was diagnosed more often than in group II (43.1 vs 25.8 %, p < 0.05), which characterizes more severe course of disease. Compared to the control group, in patients of the main group, the incidence of myocardial infarction (45.9 vs 33.9 %, odds ratio (OR) 6.1 (95% confidence interval (CI) 2.76–13.6), p < 0.05), stroke (13.8 vs 3.2 %, OR 4.8 (95% CI 0.97–23.6), p < 0.05) and chronic renal failure (10.3 vs 1.6 %), OR 7.0 (95% CI 0.82–60.4), p < 0.05) was significantly higher. In contrast to individuals without diabetes mellitus, patients from group I had significantly lower systolic heart function (48.9 ± 11.9 % vs 54.61 ± 7.56 %, p < 0.05). Percutaneous coronary intervention was a method of choice for coronary artery revascularization in patients with coronary heart disease, but coronary artery bypass grafting was more commonly used in the presence of diabetes mellitus (24.1 vs 6.5 %, p < 0.05). The progression of coronary artery atherosclerosis prevailed in patients with impaired glucose metabolism (19.0 vs 6.5 %, OR 3.4 (95% CI 1.01–11.3), p < 0.05). Mortality in people from group I was higher (12.1 vs 1.6 %, OR 8.4 (95% CI 1.00–70.3), p < 0.05). Conclusions. Multivascular lesions of the coronary arteries caused a worse prognosis in patients with diabetes mellitus. The development of recurrent circulatory disorders was more common in patients with impaired glucose metabolism. The presence of this pathology significantly increases the risk of myocardial infarction, stroke and chronic renal failure.
ішемічна хвороба серця; цукровий діабет; атеросклероз коронарних артерій; черезшкірне коронарне втручання; аортокоронарне шунтування
coronary heart disease; diabetes mellitus; atherosclerosis of coronary arteries; percutaneous coronary intervention; coronary artery bypass grafting
Вступ
Матеріали та методи
Результати
Обговорення
Висновки
- Benjamin Emelia J., Muntner Р., Alonso А., Marcio S. Bittencourt, Clifton W. Callaway et al. Heart Disease and Stroke Statistics — 2019 Update: A Report From the American Heart Association. Circulation. 2019. 139. e56-e528. 1. doi: 10.1161/CIR.0000000000000659.
- Coronary artery surgery study (CASS): a randomized trial of coronary artery bypass surgery. Survival data. Circulation. 1983. 68(5). 939-50. doi: 10.1161/01.cir.68.5.939.
- Kannel W.B., McGee D.L. Diabetes and glucose tolerance as risk factors for cardiovascular disease: the Framingham study. Diabetes Care. 1979. 2(2). 120-6. doi: 10.2337/diacare.2.2.120.
- Stamler J., Vaccaro O., Neaton J.D., Wentworth D. Diabetes, other risk factors, and 12-yr cardiovascular mortality for men screened in the Multiple Risk Factor Intervention Trial. Diabetes Care. 1993. 16(2). 434-44. doi: 10.2337/diacare.16.2.434.
- Shore S., Borgerding J.A., Gylys-Colwell I., McDermott K., Ho P.M., Tillquist M.N., Lowy E. et al. Association between hyperglycemia at admission during hospitalization for acute myocardial infarction and subsequent diabetes: insights from the veterans administration cardiac care follow-up clinical study. Diabetes Care. 2014. 37(2). 409-18. doi: 10.2337/dc13-1125.
- Lankisch M., Füth R., Gülker H., Lapp H., Bufe A., Haastert B., Martin S., Rathmann W. Screening for undiagnosed diabetes in patients with acute myocardial infarction. Clin. Res. Cardiol. 2008. 97(10). 753-9. doi: 10.1007/s00392-008-0674-5.
- Pajunen P., Koukkunen H., Ketonen M., Jerkkola T., Immonen-Räihä P., Kärjä-Koskenkari P., Kuulasmaa K. et al. Myocardial infarction in diabetic and non-diabetic persons with and without prior myocardial infarction: the FINAMI Study. Diabetologia. 2005. 48(12). 2519-24. doi: 10.1007/s00125-005-0019-0.
- Haffner S.M., Lehto S., Rönnemaa T., Pyörälä K., Laakso M. Mortality from coronary heart disease in subjects with type 2 diabetes and in nondiabetic subjects with and without prior myocardial infarction. N. Engl. J. Med. 1998. 339(4). 229-34. doi: 10.1056/NEJM199807233390404.
- Qin S.Y., Zhou Y., Jiang H.X., Hu B.L., Tao L., Xie M.Z. The association of diabetes mellitus with clinical outcomes after coronary stenting: a meta-analysis. PLoS One. 2013. 8(9). e72710. doi: 10.1371/journal.pone.0072710.
- Sarembock I.J. Stent restenosis and the use of drug-eluting stents in patients with diabetes mellitus. Curr. Diab. Rep. 2004. 4(1). 13-9. doi: 10.1007/s11892-004-0005-9.
- International Diabetes Federation. IDF Diabetes Atlas. 8th edition. http://diabetesatlas.org/resources/2017-atlas.html (June 14 2019).
- Emerging Risk Factors Collaboration, Sarwar N., Gao P., Seshasai S.R., Gobin R., Kaptoge S., Di Angelantonio E., Ingelsson E. et al. Diabetes mellitus, fasting blood glucose concentration, and risk of vascular disease: a collaborative meta-analysis of 102 prospective studies. Lancet. 2010. 375(9733). 2215-22. doi: 10.1016/S0140-6736(10)60484-9.
- Dauriz M., Targher G., Laroche C., Temporelli P.L., Ferrari R., Anker S., Coats A. et al.; ESC-HFA Heart Failure Long-Term Registry. Association Between Diabetes and 1-Year Adverse Clinical Outcomes in a Multinational Cohort of Ambulatory Patients With Chronic Heart Failure: Results From the ESC-HFA Heart Failure Long-Term Registry. Diabetes Care. 2017. 40(5). 671-678. doi: 10.2337/dc16-2016.
- Xie Y., Bowe B., Mokdad A.H., Xian H., Yan Y., Li T., Maddukuri G., et al. Analysis of the Global Burden of Disease study highlights the global, regional, and national trends of chronic kidney disease epidemiology from 1990 to 2016. Kidney Int. 2018. 94(3). 567-581. doi: 10.1016/j.kint.2018.04.011.
- Morgan K.P., Kapur A., Beatt K.J. Anatomy of coronary disease in diabetic patients: an explanation for poorer outcomes after percutaneous coronary intervention and potential target for intervention. Heart. 2004. 90(7). 732-8. doi: 10.1136/hrt.2003.021014.
- Barry A., Wilkinson I., Halford V., Springett K., McInnes A. A clinical study and the National Service Framework for diabetes. J. Tissue Viability. 2004. 14(4). 124-132. doi: 10.1016/s0965-206x(04)44002-9.
- Mankovsky G. Angiographic characteristics of the lesions of coronary arteries in patients with ischemic heart disease and diabetes mellitus. Ukrainian Journal of Cardiovascular Surgery. 2018. 2(31). 27-30. https://doi.org/10.30702/ujcvs/18.31/05(027-030).

/32.jpg)
/33.jpg)
/34.jpg)
/34_2.jpg)