Газета «Новости медицины и фармации» №6 (758), 2021
Вернуться к номеру
Застосування етилметилгідроксипіридину сукцинату (Лодиксем) при хронічному панкреатиті
Авторы: Черній В.І., д.м.н., професор
НПЦ профілактичної та клінічної медицини ДУС, м. Київ, Україна
Рубрики: Гастроэнтерология
Разделы: Клинические исследования
Версия для печати
Вступ
Хронічний панкреатит (ХП) — це захворювання, якому притаманне постійне або періодичне запалення підшлункової залози (ПЗ), що призводить до необоротних запальних та/або фіброзних змін паренхіми/проток підшлункової залози. Це захворювання супроводжується сильним болем, який знижує якість життя, і поступовим розвитком екзокринної та ендокринної недостатності ПЗ [6, 7, 14].
ХП належить до групи небагатьох хвороб, які мають дуже широкий спектр симптомів та ускладнень, що пов’язано насамперед з особливою комбінацією екзокринної та ендокринної функцій, які виконуються ПЗ, із продукцією травних ферментів та регуляторних пептидів, що необхідні при метаболізмі. Важливим також є те, що ПЗ знаходиться поряд з важливими паренхіматозними органами та судинними і нервовими структурами. Більшість ускладнень переважно є місцевими. Найпоширенішими з них є псевдокісти, геморагії, обструкція прилеглих структур або інфекційне ураження. Така гетерогенність зумовлює важливість підбору індивідуального диференціально-діагностичного та терапевтичного підходу до ведення ХП [7, 9, 10, 14].
Цікавими є статистичні дані щодо поширення ХП у світі. Так, захворюваність на хронічний панкреатит у країнах Європи становить 4–8 випадків на 100 тис. населення, а поширеність — 25 випадків на 100 тис. населення [6]. Щороку кількість випадків ХП зростає. Зокрема, за даними англійських дослідників, захворюваність зросла з 4,3 на 100 тис. населення на рік у 90-х роках ХХ ст. до 8,6 на 100 тис. населення на рік у 2000-х роках [8]. Американські вчені зі штату Міннесота також встановили значне зростання ХП упродовж 20 років: від 1,9 до 3,5 на 100 тис. населення [4]. У Японії показники захворюваності зросли з 2,0 на 100 тис. до 5,0–5,9 на 100 тис. населення [5]. Найвищий рівень ХП відмічений у Скандинавії, і там надалі відбувається ріст захворюваності: з 10,4 до 13,4 на 100 тис. населення на рік [12].
В Україні, за даними досліджень, рівень захворюваності на ХП суттєво перевищує світові показники і останніми роками становить 226 випадків на 100 тис., поширеність — 2471 на 100 тис. населення. Таку значну різницю в показниках з іншими країнами пояснюють гіпердіагностикою при встановленні діагнозу ХП, а також більш високим рівнем зловживання алкоголем, що є однією з основних причин розвитку ХП [6]. Дослідження довели, що алкоголь спричинює ХП у 70–90 % випадків. Крім того, значну роль у виникненні цієї хвороби відіграє неправильне харчування: вживання їжі з високим умістом жиру, переїдання.
Соціальна значущість ХП є вагомою через суттєві фінансові витрати на лікування, зменшення кількості робочих днів, а отже, і виробленої продукції чи послуг. Також значними є персональні витрати хворого, інвалідизація та зниження його якості життя. ХП обмежує звичний ритм життя і часто є причиною емоційних розладів, зокрема підвищеної тривожності й астенодепресивного синдрому. Власне тому своєчасна діагностика та лікування є надзвичайно важливими.
Лікування хронічного панкреатиту у першу чергу спрямоване на зменшення та ліквідацію болю; також необхідними є компенсація дефіциту ферментів ПЗ, корегування порушень метаболізму вуглеводів, профілактика гіпотрофії та лікування ускладнень. До лікувальних стратегій належать замісна терапія панкреатичними ферментами, поповнення дефіциту жиророзчинних вітамінів (особливо А і D) та лікування ендокринної недостатності ПЗ [6, 13].
Одним із сучасних препаратів, який почали використовувати при лікуванні ХП, є Лодиксем (діюча речовина етилметилгідроксипіридину сукцинат), який є інгібітором вільнорадикальних процесів, мембранопротектором та має антигіпоксичну, стресопротекторну, ноотропну, протисудомну та анксіолітичну дію. Даний препарат відомий тим, що підвищує резистентність організму до дії різних факторів, зокрема інтоксикації алкоголем та антипсихотичними засобами (нейролептиками). Крім того, препарат стабілізує мембранні структури клітин крові (еритроцитів і тромбоцитів), зменшує вміст загального холестерину і ліпопротеїнів низької щільності (ЛПНЩ), викликає регресування атеросклеротичних змін в артеріях (гіполіпідемічна та антиатерогенна дія), а також зменшує ферментативну токсемію та ендогенну інтоксикацію при гострому панкреатиті або при загостреннях хронічного. Протиалкогольна дія препарату проявляється у витверезному ефекті і послабленні мотивації до вживання алкоголю, що є важливим при лікуванні ХП, яке передбачає виключення споживання алкоголю.
Наведене вище обумовило проведення дослідження щодо використання етилметилгідроксипіридину сукцинату при лікуванні хронічного панкреатиту.
Мета роботи: аналіз джерел наукової літератури щодо лікувальних можливостей етилметилгідроксипіридину сукцинату (Лодиксем) у терапії хронічного панкреатиту.
Матеріали та методи
Проводився пошук літературних джерел в основних електронних базах даних доказової медицини: BMJ Clinical Evidence (http://clinicalevidence.bmj.com); The Cochrane Collaboration The Cochrane Library (http://www.cochrane.org/); Medscape from WebMD (http://www.medscape.com); Centers for Disease Control and Prevention (CDC) (https://www.cdc.gov/); National Guideline Clearinghouse (https://www.guideline.gov/); BMJ Clinical Evidence (http://clinicalevidence.bmj.com); National Institute for Health and Clinical Excellence (NICE) (https://www.nice.org.uk/); American Medical Association (AMA) (https://www.ama-assn.org/); Health-ua.com; Національній бібліотеці України ім. В.І. Вернадського за такими ключовими словами: «етилметилгідроксипіридину сукцинат», «Лодиксем», «хронічний панкреатит». Після електронного пошуку здійснювався пошук вручну, із використанням списку посилань усіх отриманих оглядових статей та первинних досліджень для виявлення інших досліджень, яких не було в первинному електронному пошуку за ключовими словами.
Результати дослідження
За даними літературного пошуку, уперше важливість включення етилметилгідроксипіридину сукцинату (Лодиксему) до схеми лікування ХП була відмічена в 2010 році вченими з Іжевська, які визначали рівень якості життя пацієнтів із ХП у відкритому контрольованому дослідженні 70 пацієнтів з діагнозом «хронічний панкреатит, стадія загострення» із тривалістю захворювання від 4 до 18 років (у середньому 9,6 ± 2,3 року). У стандартну схему лікування включили етилметилгідроксипіридину сукцинат у дозі 125 мг 2 рази на день.
Було відмічене покращення всіх складових якості життя через 4 тижні лікування, зокрема активності (переносимості фізичного навантаження), загального та психічного здоров’я. Ці зміни збереглися й через 12 тижнів після проведеного лікування. При лікуванні загострення ХП спостерігали зниження болю і показника інтенсивності болю. Також через 12 тижнів у пацієнтів знизилася ситуативна тривожність на 24,2 % (p < 0,05), тоді як у групі порівняння (контрольній), що лікувалася за стандартною схемою, — на 5,6 % (p < 0,05) (рис. 1).
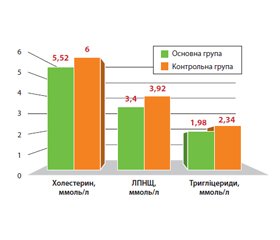
У процесі лікування відмічене покращення показників порушеного ліпідного спектра, причому знову ж таки більш значне — в основній групі. Так, до 12-го тижня відмічено зниження загального холестерину в основній групі до 5,52 ± 0,10 ммоль/л порівняно з 6,11 ± 0,15 ммоль/л у контрольній групі (р < 0,05), ЛПНЩ — до 3,40 ± 0,10 ммоль/л проти 3,92 ± 0,10 ммоль/л (р < 0,05) і тригліцеридів — до 1,98 ± 0,02 ммоль/л проти 2,34 ± 0,04 ммоль/л (р < 0,05) відповідно (рис. 2).
Наведені дані підтверджують позитивний ефект терапії із включенням препарату етилметилгідроксипіридину сукцинату до стандартної схеми лікування ХП [3].
Водночас науковці із Саранська в 2018 році досліджували ефективність етилметилгідроксипіридину сукцинату як препарату для профілактики функціональних і структурних порушень підшлункової залози, індукованих обтураційним холестазом. Дослідження проводилось на 20 наркотизованих собаках, яким з метою лікування вводили 5% розчин етилметилгідроксипіридину сукцинату. У результаті експерименту було доведено зниження вмісту екзокринних ферментів підшлункової залози до закінчення лікування: рівень α-амілази знизився в 1,8 раза (до 104 ± 8 од/л), ліпази — в 2 рази (до 81 ± 5 од/л) порівняно з вихідним рівнем. Опубліковані результати показують покращення функціональної активності підшлункової залози і відновлення її структури не тільки завдяки дезінтоксикаційній дії введеної рідини, а в основному завдяки відновленню клітинних мембран ациноцитів під впливом етилметилгідроксипіридину сукцинату [11].
Вітчизняні вчені з Дніпропетровської медичної академії МОЗ України у 2014 році опублікували результати клінічного дослідження 12 хворих з панкреатитом, яким у межах інтенсивної терапії проводили лікування препаратом етилметилгідроксипіридину сукцинат упродовж 7 діб. У дослідженні було доведено, що використання даного препарату у складі інтенсивної терапії гострого панкреатиту або загострення хронічного панкреатиту забезпечує скорочення тривалості панкреатогенної токсемії на 2 доби, швидку стабілізацію цитолізу, що дозволило обмежити деструктивні процеси у підшлунковій залозі. Зокрема, було відмічено зменшення вираженості больового синдрому до кінця першої доби (р = 0,001 до вихідного рівня): показник за візуальною аналоговою шкалою у групі з додаванням вказаного препарату був нижчим, ніж у групі зі стандартною схемою терапії (3,7 ± 0,5 бала проти 6,7 ± 0,4 бала, р = 0,024). Також було підтверджено зниження в 2 рази вже на 2-гу добу лікування кількості балів за шкалою MODS (до 1,00 ± 0,05 бала та 1,7 ± 0,5 бала відповідно).
Значення внутрішньочеревної гіпертензії 1-го ступеня на 2-гу добу лікування так само відрізнялось у групах (10,5 ± 0,6 мм рт.ст. (р = 0,009 до вихідного рівня) проти 14,7 ± 1,1 мм рт.ст. відповідно, р = 0,021), як і рівень секреторної активності підшлункової залози після проведеного лікування: динаміка значень діастази сечі щодо вихідних (р = 0,026 і р = 0,041 відповідно) на 3-тю добу терапії була більш вираженою у пацієнтів основної групи (133,6 ± 16,8 мккат/л проти 114,0 ± 26,6 мккат/л відповідно). Порушення білкового обміну у пацієнтів, які отримували лікування етилметилгідроксипіридину сукцинатом, мали відстрочений і менш виражений характер, що непрямо вказує на органопротективну дію препарату при загостренні ХП.
Таким чином, проведення інтенсивної терапії із включенням етилметилгідроксипіридину сукцинату ліквідувало больовий і диспептичний синдроми на 2 доби швидше, ефективно вплинуло на панкреатогенну токсемію, дозволило корегувати порушення вуглеводного обміну, надало органопротективний та цитостатичний ефекти і тим самим покращило якість життя пацієнтів з гострим панкреатитом та з загостренням хронічного [2].
Ще одні українські вчені з Харківського національного медичного університету під керівництвом В.І. Робак (2019) аналізували ефективність етилметилгідроксипіридину сукцинату (Лодиксем) окремо та у комбінації з пентоксифіліном у розчині Рінгера лактату (Лодиксем + Латрен) при лікуванні 120 пацієнтів з епізодом гострого панкреатиту в клінічному дослідженні. Було відмічено статистично значуще зниження рівнів лейкоцитів, індексу лейкоцитарної інтоксикації, індексу інтоксикації та вмісту С-реактивного білка в усіх групах пацієнтів на 5-й день. Оцінка тяжкості стану хворих за шкалами Ranson, Simplified Acute Physiology Score II, Acute Sepsis Severity Evaluation Scale (ASSES) довела значне зниження балів у групах хворих, які отримували дану терапію: спостерігалося значне зниження показників шкали ASSES (до 6,11 ± 0,37) та шкали Ranson (до 1,8 ± 0,9 бала) у пацієнтів із запропонованою схемою лікування, що підтвердило ефективність препарату етилметилгідроксипіридину сукцинату [1].
Висновки
За даними проведеного літературного пошуку виявлено докази терапевтичної ефективності етилметилгідроксипіридину сукцинату при лікуванні хронічного панкреатиту, особливо у період загострення. З’ясовано, що Лодиксем є ефективним у корегуванні вільнорадикального окиснення і профілактиці розвитку окисного стресу, перешкоджає розвитку в підшлунковій залозі істотних функціональних і структурних змін, забезпечує скорочення тривалості на 2 доби панкреатогенної токсемії, швидко стабілізує цитоліз, тим самим зменшуючи прояви органної дисфункції.
Відмічено позитивний ефект застосування етилметилгідроксипіридину сукцинату у поєднанні з пентоксифіліном у розчині Рінгера лактату, а саме зменшення проявів інтоксикації та стимуляцію репаративних процесів, що дозволяє рекомендувати дану комбіновану схему лікування до включення у протоколи лікування пацієнтів із хронічним панкреатитом.
Список литературы
1. Робак В.И., Евтушенко Д.В., Петюнин О.Г., Драна Л.О. Оптимизация лечебной тактики при остром панкреатите. Хирургия Украины. 2019. № 2 (70). С. 20-25.
2. Кравец О.В. Пути повышения эффективности интенсивной терапии у пациентов с острым панкреатитом. Медицина неотложных состояний. 2014. № 3 (58).
3. Samarin A.G., Pimenov L.T. Chronic pancreatitis: quality of a life and possibilities of pharmacological correction by ethylmethylhydroxypyridine succinate [In Russian]. Eksp. Klin. Gastroenterol. 2010. Vol. 6. Р. 77-81. https://pubmed.ncbi.nlm.nih.gov/20734491/
4. O’Sullivan J.N., Nobrega F.T., Morlock C.G., Brown A.L. Jr, Bartholomew L.G. Acute and chronic pancreatitis in Rochester, Minnesota, 1940 to 1969. Gastroenterology. 1972. Vol. 62. Р. 373-9.
5. Lin Y., Tamakoshi A., Matsuno S. et al. Nationwide epidemiological survey of chronic pancreatitis in Japan. J. Gastroenterol. 2000. Vol. 35. Р. 136-41.
6. Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при хронічному панкреатиті. Наказ МОЗ від 10.09.2014 № 638. https://zakon.rada.gov.ua/rada/show/v0638282-14#Text
7. Matsumura N., Ochi K., Ichimura M. et al. Study on free radicals and pancreatic fi brosis induced by repeated injections of superoxide dismutase inhibitor. Pancreas. 2001. Vol. 22. № 1. P. 53-57.
8. Tinto A., Lloyd D.A., Kang J.Y., Majeed A., Ellis C., Williamson R.C., Maxwell J.D. Acute and chronic pancreatitis — diseases on the rise: a study of hospital admissions in England 1989/90–1999/2000. Aliment. Pharmacol. Ther. 2002. Vol. 16. Р. 2097-105.
9. Lankisch P.G., Assmus C., Maisonneuve P., Lowenfels A.B. Epidemiology of pancreatic diseases in Luneburg County. A study in a defined german population. Pancreatology. 2002. Vol. 2(5). P. 469-477.
10. Маев И.В., Казюлин А.Н., Кучерявый Ю.А. Хронический панкреатит. Москва: Медицина, 2005. 504 с.
11. Беляев А.Н., Костин С.В., Беляев С.А., Тюрина Н.А. Профилактика функциональных и структурных нарушений поджелудочной железы при остром обтурационном холестазе. Медицинский альманах. 2018, март. № 1 (52). С. 59-63.
12. Jaakkola M., Nordback I. Pancreatitis in Finland between 1970 and 1989. Gut. 1993. Vol. 34. Р. 1255-60.
13. Удосконалені алгоритми діагностики та лікування гострого панкреатиту: методичні рекомендації. За ред. П.Д. Фоміна, Я.С. Березницького. Київ, 2012. 80 с.
14. Pain J. Pathophysiology of Obstructive Jaundice. Pancreatic Disease. 1991. Р. 3-17.

/10_u.jpg)