Журнал «Травма» Том 22, №3, 2021
Особенности использования аддитивных технологий в оперативной ортопедии
Авторы: Косяков А.Н.(1), Лоскутов А.Е.(2), Гребенников К.А.(1), Милосердов А.В.(1), Федин Е.М.(1), Галузинский А.А.(3), Бурбурская С.В.(3)
(1) — Киевский городской центр эндопротезирования, хирургии и реабилитации, Киевская городская
клиническая больница № 12, г. Киев, Украина
(2) — Днепровский государственный медицинский университет, г. Днепр, Украина
(3) — Лаборатория биомедицинской инженерии, г. Киев, Украина
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Резюме
Актуальність. Адитивні технології з кожним днем переходять з університетських лабораторій і високотехнологічних виробництв у рутинну клінічну практику і навіть у наш повсякденний побут. Кожен ентузіаст, маючи у своєму розпорядженні персональний комп’ютер і побутовий 3D-принтер, може створювати будь-які фізичні об’єкти — від дитячих іграшок до витворів мистецтва. Наявність на ринку широкого асортименту програмних продуктів, обладнання та витратних матеріалів у сукупності з даними сучасних методів діагностики, високим рівнем підготовки та кооперації лікарів та інженерів дають практичній медицині нові можливості. Уперше ми можемо повністю індивідуалізувати наші лікувально-діагностичні заходи: виконати прецизійне передопераційне планування, створити детальний план операції, відпрацювати втручання на повномасштабних анатомічних прототипах із використанням стандартного інструменту, провести його максимально швидко й атравматично, мінімізувати ризики, забезпечити оптимальний функціональний результат. У найтяжчих випадках — виготовити і встановити індивідуальні імплантати. Мета: запропонувати до уваги колег практичні аспекти та можливості адитивних технологій у сучасній ортопедичній практиці, ознайомити з історією та поточним станом медичного прототипування, поділитися технологічними тонкощами. Матеріали та методи. Під час написання цієї статті ми використовували дані публікацій останніх років у спеціальній вітчизняній і зарубіжній періодиці, нечисленних монографій, матеріали тематичних конференцій, результати неформальних бесід із колегами в операційних, за комп’ютером і на виробництві, а також власний досвід (понад 200 випадків прототипування). Висновки. Доступність обладнання, програмного забезпечення і витратних матеріалів дозволяє впровадити методи адитивних технологій у повсякденну практику практично кожної сучасної ортопедо-травматологічної клініки.
Актуальность. Аддитивные технологии с каждым днем переходят из университетских лабораторий и высокотехнологичных производств в рутинную клиническую практику и даже в наш повседневный быт. Каждый энтузиаст, располагая персональным компьютером и бытовым 3D-принтером, может создавать любые физические объекты — от детских игрушек до произведений искусства. Наличие на рынке широкого ассортимента программных продуктов, оборудования и расходных материалов в совокупности с данными современных методов диагностики, высоким уровнем подготовки и кооперации врачей и инженеров предоставляют практической медицине новые возможности. Впервые мы можем полностью индивидуализировать наши лечебно-диагностические мероприятия: выполнить прецизионное предоперационное планирование, создать детальный план операции, отработать вмешательство на полномасштабных анатомических прототипах с использованием стандартного инструмента, провести ее максимально быстро и атравматично, минимизировать риски, обеспечить оптимальный функциональный результат. В самых тяжелых случаях — изготовить и установить индивидуальные имплантаты. Цель: представить вниманию коллег практические аспекты и возможности аддитивных технологий в современной ортопедической практике, ознакомить с историей и текущим состоянием медицинского прототипирования, поделиться технологическими тонкостями. Материалы и методы. При написании этой статьи мы использовали данные публикаций последних лет в специальной отечественной и зарубежной периодике, немногочисленных монографий, материалы тематических конференций, результаты неформальных бесед с коллегами в операционных, за компьютером и на производстве, а также собственный опыт (более 200 случаев прототипирования). Выводы. Доступность оборудования, программного обеспечения и расходных материалов позволяет внедрить методы аддитивных технологий в повседневную практику практически каждой современной ортопедо-травматологической клиники.
Background. Additive technologies are increasingly making their way from university laboratories and high-tech industries into routine clinical practice and even into our everyday lives. Any enthusiast, having a PC and a 3D printer at his or her disposal, can create any physical object — from children’s toys to works of art. The presence on the market of a wide range of software pro-ducts, equipment, and consumables along with the data from mo-dern diagnostic methods, a high level of training and cooperation between doctors and engineers provide practical medicine with unprecedented opportunities. We are finally able to fully customize our treatment and diagnostic procedures: to perform precise preoperative planning; to draw up a detailed plan of the operation; to rehearse the intervention on full-scale anatomical prototypes using a standard tool; to conduct the surgery as quickly and atraumatically as possible; to minimize risks; to ensure the optimal functional result and to manufacture and install customized implants in the most difficult cases. The purpose was to draw the attention of our distinguished colleagues to the aspects of application of additive technologies in modern orthopaedic practice, to introduce them into the history and current state of medical prototyping, as well as to share technological nuances with them. Materials and methods. While writing this article, we incorporated the data of recent publications in specialized domestic and foreign periodicals, several monographs, materials from thematic conferences, the results of informal conversations with colleagues in the operating rooms, at the computer and production site, as well as our own experience (over 200 cases of prototyping). Conclusions. The availability of equipment, software, and consumables allows for the introduction of additive technology into the everyday practice of nearly every modern orthopaedic and trauma clinic.
Ключевые слова
адитивні технології; 3D-планування і прототипування; ендопротезування суглобів
аддитивные технологии; 3D-планирование и прототипирование; эндопротезирование суставов
additive technologies; 3D planning and prototyping; joint replacement
Введение
Технологии 3D-печати из различных материалов прочно вошли в нашу жизнь и заняли ведущее место во многих отраслях. На сегодняшний день это одна из наиболее стремительно развивающихся технологий в мире, которая позволяет решить большое количество вопросов с меньшими временными и материальными затратами. В медицине 3D-технологии оказались особенно интересны и полезны для хирургов всех направлений.
Первые попытки пространственного моделирования тканей и клеточных структур относятся к 30-м годам прошлого столетия. В 1932 году М. Кнолль и Э. Руска построили первый прототип современного электронного микроскопа. Эта работа Э. Руски в 1986 году была отмечена Нобелевской премией по физике, которую присудили ему и изобретателям сканирующего зондового микроскопа Герду Карлу Биннигу и Генриху Рореру. Использование просвечивающего электронного микроскопа для научных исследований было начато в конце 1930-х годов. В конце 1930-х — начале 1940-х годов появились первые растровые электронные микроскопы, формирующие изображение объекта при последовательном перемещении электронного зонда малого сечения по объекту. Массовое применение этих приборов в научных исследованиях началось в 1960-х годах, когда они достигли значительного технического совершенства [1].
Идея применения трехмерных медицинских изображений, а именно данных компьютерной томографии (КТ), для воссоздания физической модели впервые была предложена в 1979 году. В то время еще не существовало систем 3D-печати, однако присутствовала возможность субтрактивной обработки материалов, или фрезерования [2].
Первая анатомическая модель, созданная с использованием методов медицинской визуализации, была изготовлена в том же 1979 году: это была модель таза из полистирола. По мере того как в конце 1980-х
стали появляться образцы 3D-принтеров и все чаще стали использоваться технологии трехмерной визуализации, всерьез стал рассматриваться вопрос о применении 3D-печати в медицине. Стереолитография (Steriolithography Apparatus — SLA) — технология, в которой управляемый компьютером луч лазера применяется для отвердения жидкого полимера или смолы, послойно создавая требуемую структуру. SLA стала первой доступной технологией 3D-печати, которая была применена в медицине в 1994 году [3].
Ввиду того что принтеры в то время могли печатать только твердотельные модели, первыми областями медицины, где смогли применять прототипы, стали ортопедия, челюстно-лицевая хирургия, нейрохирургия.
Цель работы: на основе литературных данных осветить практические аспекты и возможности аддитивных технологий в современной ортопедической практике, ознакомить с историей и текущим состоянием медицинского прототипирования, поделиться технологическими тонкостями.
Материалы и методы
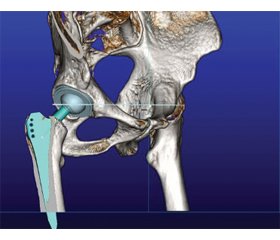
Для того чтобы получить напечатанный прототип, необходимо создание цифровой модели будущего изделия. В медицинской практике трехмерные цифровые данные, которые необходимы для создания модели, получают в основном с компьютерной, реже магнитно-резонансной томографии (МРТ) или их совмещения [4] (рис. 1, 2). При этом для 3D-печати используют и другие способы получения трехмерного изображения: КТ с коническим лучом, томографическая ангиография, МР-ангиография, позитронно-эмиссионная томография, МР-холангиопанкреатография, 3D-эхокардиография, системы лазерного сканирования и даже фотографии, сделанные при помощи смартфона [5].
/19.jpg)
Gillaspie в 2016 году совместил данные компьютерной и позитронно-эмиссионной томографии для создания моделей, демонстрирующих физиологическую активность и анатомию. Его же группа визуализировала и выполнила трехмерную печать в динамике, продемонстрировав реакцию опухоли на индукционную терапию. Авторы называют этот метод пятимерной печатью, поскольку к трехмерной модели добавлены время и физиологическая активность [6].
В медицинской сфере требуется совместная работа междисциплинарной группы, которая состоит из медицинского инженера и хирурга. Этот процесс требует относительно больших временных затрат и постоянного взаимодействия хирурга с инженером, на каждой ступени могут возникнуть вопросы, которые необходимо решать совместно.
Процесс 3D-печати начинается с разработки виртуального образа будущего объекта в 3D-редакторе или CAD-программе (3D Studio Max, AutoCAD, «Компас», SolidWorks и др.). 3D-печать для медицины имеет ряд нюансов. Во-первых, необходимо создать качественную модель анатомического объекта в натуральную величину. Существует много программ, с помощью которых получают электронные трехмерные модели по данным различных видов томографии: RadiAnt, 3D Doctor, Simplant, ScanIp, Simplewar, однако точность «чтения» электронной 3D-модели зависит от способностей специалиста к пространственному воображению [7]. Ситуацию может осложнять наличие артефактов изображения.
Поскольку анатомические объекты представляют собой совокупность сложных поверхностей, которые не всегда поддаются стандартному измерению, возможность искусственного воспроизведения по данным томографии индивидуального физического макета-прототипа позволяет снять отпечатки этих поверхностей (например, с помощью слепка или сканирования) для дальнейшего точного проектирования навигационных хирургических шаблонов, инструментов, фиксаторов и имплантатов, подбора тактики хирургического вмешательства и вида доступа [7–9]. Прототип обладает высокой точностью, что обеспечивает возможность измерения пространственного размещения определенных точек или поверхностей с помощью физических методов [10, 11].
Первым этапом создания индивидуального макета-прототипа является обработка множества двухмерных изображений, полученных с помощью лучевой диагностики (КТ- и МРТ-сканирование). Под обработкой подразумевают: анализ качества исходных изображений, очистку артефактов, сегментацию анатомических объектов в автоматическом и ручном режимах. Данная работа выполняется на каждом срезе и в трех плоскостях конкретного исследования [12].
Первый этап является ключевым в построении 3D-модели анатомических объектов. Для гарантирования высокого конечного результата необходимо обеспечить ряд условий:
1. Качество входящих данных.
1.1. Для исследования с помощью компьютерной томографии:
1.1.1. Обеспечить максимально тонкие срезы за счет уменьшения ширины рентгеновского луча (коллимирование) [13].
1.1.2. Использовать подавление артефактов от металла в случае наличия конструкций в области сканирования.
1.1.3. Минимизировать артефакты изображений (рис. 3).
1.2. Для исследования с помощью магнитно-резонансной томографии:
1.2.1. Обеспечить изотропный воксел (одинаковые размеры объемного элемента в трех измерениях).
1.2.2. Обеспечить минимальный зазор между срезами (SG).
1.2.3. Минимизировать артефакты изображений [14].
2. Высокий уровень знания анатомии у специалиста, работающего с сегментацией (в спорных случаях необходима консультация хирурга).
Для обработки двухмерных изображений используется специализированное программное обеспечение. Наиболее распространенным форматом ввода данных является DICOM, но также поддерживаются другие форматы изображений, такие как TIFF, JPEG, BMP и RAW. В автоматическом режиме программа выделяет анатомические структуры по указанной плотности. Компьютерная обработка изображения позволяет различать более ста степеней изменения плотности исследуемых тканей: от нуля — для воды и ликвора до ста и более — для костей, что дает возможность дифференцировать различия нормальных и патологических участков тканей в пределах 0,5–1 %, т.е. в 20–30 раз больше, чем на обычных рентгенограммах [15] (рис. 4).
/20.jpg)
Учитывая тот факт, что 3D-моделирование используют чаще при сложных случаях, специалист сталкивается с измененной анатомией и наличием множества артефактов плоско-параллельных изображений, например артефакты от металла, что требует ручного исправления сегментации, выполненной программой. Обработанное изображение сохраняется в любом из следующих форматов исходных файлов в зависимости от дальнейшего применения: STL, VRML, PLY и DXF. Основной формат файлов для трехмерной печати (далее — 3D-печать) — STL [16].
Вторым этапом является экспорт сохраненного файла в формате STL в программы (AutodeskNetFabb), в которых производится автоматическое и ручное исправление и редактирование 3D-модели. Поверхность объектов в этом формате представляет собой совокупность полигонов (Polygonmesh). Интеллектуальные скрипты могут автоматически анализировать поверхности, исправлять ошибки сетей, улучшать точность моделей путем повторной триангуляции, устранять пространственные коллизии и другие ошибки. Программа дает возможность спрогнозировать искажения, возникающие в изделии в ходе 3D-печати, непосредственно до запуска в производство. На основании этого инженер может скорректировать исходную модель таким образом, чтобы избежать ошибок при 3D-печати (рис. 5).
/20_2.jpg)
Третьим этапом является перевод готовой 3D-мо-дели в слайсер-программу. Это программа для преобразования трехмерной модели в понятный принтеру набор команд, называемый g-code. На этом этапе устанавливают конечные данные для 3D-печати, а именно: задают положение детали во время печати, рассчитывают тип и количество поддержек, задают плотность заполнения модели, выбирают оптимальную скорость и температуру для печати. Вышеперечисленные характеристики напрямую зависят от типа печати и материала будущей модели.
Для создания индивидуального макета-прототипа чаще используют технологию FDM (Fused Deposition Modeling) — моделирование методом наплавления. Объект формируется путем послойной укладки расплавленной нити из плавкого рабочего материала (пластик, гибкий пластик, воск). Гибкие пластики можно использовать для создания прототипов полых органов, мягкотканных анатомических объектов, опухолей, которые можно без усилий резать скальпелем и накладывать швы. Преимуществами данной технологии являются доступность, низкая стоимость, возможность использования различных материалов.
Очень важной характеристикой созданной 3D-модели является возможность ее стерилизации. 3D-прототип может быть использован не только для предоперационного планирования и проведения «операции до операции» на этапах подготовки. Эта модель может быть создана с сосудами и нервами и может быть использована в операционной как навигатор во время операции. На сегодняшний день на рынке существует большой объем материалов для 3D-печати моделей, которые повторяют тактильные, механические, эластические характеристики живых тканей и, кроме того, поддаются разным методам стерилизации.
Процесс создания и печати 3D-модели может оказаться длительным и трудоемким, что обусловлено нарушением нормальной анатомии, наличием деформаций, дефектов и артефактов в области исследования.
Экономия времени в операционной требует больших временных затрат на изготовление прототипа. Прямые преимущества для пациента: меньшее количество времени под анестезией, снижение кровопотери, лучшие результаты оперативного вмешательства [6].
В последние годы частота применения 3D-печати в медицине увеличивается, о чем свидетельствуют многочисленные публикации. Изготовление моделей с использованием аддитивных технологий может иметь несколько целей. 3D-прототипы можно использовать: для предоперационного планирования будущей операции, как систему навигации во время хирургического вмешательства и как наглядное пособие для обучения врачей, интернов, студентов, медицинских сестер.
Изучение анатомии пациента с использованием муляжа требуемых структур реального размера обладает очевидными преимуществами перед просмотром изображений на экране компьютера. В недавнем исследовании проводилось сравнение напечатанных трехмерных моделей с трехмерными изображениями для предоперационного планирования. Респондентам (хирургам-интернам) предложили разработать и сравнить виртуальные и напечатанные на принтере трехмерные модели и на их материале выработать предоперационный план. Интерны, работавшие с напечатанными 3D-моделями, составили план более высокого качества. Авторы исследования пришли к выводу о том, что использование напечатанных трехмерных моделей может повысить качество предоперационного планирования для начинающих хирургов и улучшить навыки опытных врачей за пределами операционной [17].
Группами авторов опубликованы работы по предоперационному планированию при подготовке к реконструктивным операциям и тотальному эндопротезированию тазобедренного сустава у пациентов с наличием посттравматических изменений в этой зоне. Наличие пластикового прототипа на этапах предоперационного планирования позволяет не только увидеть анатомические особенности данного пациента, но и подобрать оптимальную форму, размеры имплантатов, определить безопасное направление и длину винтов. Наличие 3D-модели позволило составить детальный план проведения оперативного вмешательства и тем самым сократить время нахождения в операционной и улучшить исход оперативного лечения [18–22].
/22.jpg)
Количество ревизионных операций по артропластике тазобедренного сустава постоянно увеличивается [23–27]. При подготовке к ревизионным операциям требуется тщательное и полноценное предоперационное планирование. Не во всех случаях его можно провести по рентгенограммам и данным компьютерной или магнитно-резонансной томографии. В ряде случаев хирурги прибегают к помощи аддитивных технологий. По результатам компьютерной томографии создается пластиковый прототип, на котором можно провести предварительную операцию и проработать возможные сценарии предстоящей ревизионной артропластики [28–30].
Несмотря на большой арсенал ревизионных конструкций, возникают ситуации, когда даже их наличие не позволяет выполнить ревизионное вмешательство. К этой группе относятся пациенты после многочисленных вмешательств и имеющие выраженный дефицит костной ткани в области сустава, нарушение целостности тазового кольца. Дефект или отсутствие передней и задней колонн усугубляют ситуацию. В таких случаях использование стандартных вертлужных ревизионных компонентов не решает задачу надежной фиксации элементов эндопротеза, восстановления анатомии и центра ротации сустава [17].
В мировой литературе появляется все больше сообщений об использовании индивидуальных имплантатов, созданных с использованием аддитивных технологий из титанового порошка и предназначенных для возмещения дефицита костной ткани в тех случаях, когда официнальных конструкций недостаточно [24–26, 31–38].
Выводы
Это исследование представляет обзор применения 3D-моделирования и трехмерной печати в ортопедии на этапах подготовки к эндопротезированию суставов. Представлены обзор развития технологии быстрого прототипирования и некоторые аспекты практического применения в клинической практике. Судя по растущему количеству публикаций, применение аддитивных технологий становится все более частой практикой. Внедрение их в клиническую практику может помочь решить некоторые очень сложные вопросы.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов и собственной финансовой заинтересованности при подготовке данной статьи.
Получено/Received 23.03.2021
Рецензировано/Revised 04.04.2021
Принято в печать/Accepted 14.04.2021
Список литературы
1. Bogner A., Jouneau P.-H., Thollet G., Basset D., Gaut-hier C. A history of scanning electron microscopy developments: Towards ‘‘wet-STEM’’ imaging. Micron. 2007. 38. P. 390-401.
2. Николаенко А.Н. Применение 3D-моделирования и трехмерной печати в хирургии: обзор литературы. Medline.ru. Хирургия. 2018. Т. 18.
3. Frame M. Rapid Prototyping in Orthopaedic Surgery: A User’s Guide. The Scientific World Journal. 2012. Vol. 2012. P. 1-7.
4. Косяков О.М., Гребенніков К.О., Милосердов А.В., Федін Є.М., Бурбурська С.В., Галузинський О.А., Ніколов М.О., Козей А.С. Спосіб інтегрованого тривимірного моделювання індивідуальних анатомічних структур. Патент України 135130; МПК G09B 23/28; A61B 34/10; А61В 5/055; А61В 34/20 (2006.01); B33Y 50/00; G16H 30/40 (2018.01); G06T 15/08 (2011.01); G06T 19/00; заявл. 09.04.2019, опубл. 10.06.2019. Бюл. № 11/2019.
5. Kim G.B. et al. Three-Dimensional Printing: Basic Principles and Applications in Medicine and Radiology. Korean Journal of Radiology. 2016. Vol. 17. № 2. P. 182.
6. Gillaspie E.A. et al. From 3-Dimensional Printingto 5-Dimensional Printing: Enhancing Thoracic Surgical Planningand Resectionof Complex Tumors. The Annalsof Thoracic Surgery. 2016. Vol. 101. № 5. P. 1958-1962.
7. Lantada A.D., Morgado P.L. Enhancing product deve-lopment through CT images, computer-aided design and rapid manufacturing: present capabilities, main applications and challenges. Theory and Applications of CT Imaging and Analysis. InTech, Rijeka, Croatia. 2011. Р. 269-290.
8. Torres K., Staśkiewicz G., Śnieżyński M., Drop A., Maciejewski R. Application of rapid prototyping techniques for modelling of anatomical structures in medical training and education. Folia Morphol. 2011. Vol. 70. № 1. Р. 1-4.
9. Hieu L.C., Zlatov N., Vander Sloten J. et al. Medical ra-pid prototyping applications and methods. Assem Autom. 2005. 25. Р. 284-292.
10. Eva Hnatkova, Petr Kratky and Zdenek Dvorak. Production of anatomical models via rapid prototyping. International Journal Of Circuits, Systems And Signal Processing. 2014. Vol. 8. Р. 479-486.
11. Cloonan A.J., Shahmirzadi D., Li R.X., Doyle B.J., Konofagou E.E., McGloughlin T.M. 3D-printed tissue-mimicking phantoms for medical imaging and computational validation applications 3D Print. Addit Manuf. 2014. № 1. Р. 14-23.
12. Wei-Hua A.Wang, Man-ChingLin. STL rapid prototy-ping bio-CAD model for CT medical image segmentation. Computers in Industry. 2010. Vol. 61. Is. 3. P. 187-197.
13. Хофер М. Компьютерная томография. Базовое руководство. 3-е издание, перераб. и доп. М.: Мед. лит., 2011. С. 9.
14. Currie S., Hoggard N., Craven I.J. et al. Understanding MRI: basic MR physics for physicians. Postgraduate Medical Journal. 2013. № 89. Р. 209-223.
15. Марусина М.Я., Казначеева А.О. Современные виды томографии: учебное пособие. СПб.: СПбГУ ИТМО, 2006. С. 20.
16. Kurenov S.N. et al. Three-dimensional printing to facilitate anatomic study, device development, simulation, and planning in thoracic surgery. The Journal of Thoracic and Cardiovascular Surgery. 2015. Vol. 149. № 4. P. 973-979.
17. Rankin T.M. et al. Three-dimensional printing surgical instruments: are we there yet? Journal of Surgical Research. 2014. Vol. 189. № 2. P. 193-197.
18. James M. Duncan, Samuel Nahas, Kashif Akhtar, Jasvinder Daurka. The Use of a 3D Printer in Pre-operative Planning for a Patient Requiring Acetabular Reconstructive Surgery. Journal of Orthopaedic Case Reports. 2015. Vol. 5. P. 23-25.
19. Косяков А.Н., Гребенников К.А., Милосердов А.В., Федин Е.М. Применение пластины индивидуальной конструкции для остеосинтеза при эндопротезировании тазобедренного сустава у больной с застарелым невправленным трансацетабулярным переломом костей таза. Ортопедия, травматология и протезирование. 2019. № 1. С. 96-99.
20. Najiahai Jinsihan, Gele Jin. Recent developments of 3D-printing technique assisted surgery in the management of complex fractures. Int. J. Clin. Exp. Med. 2018. № 11 (11). P. 1578-11583.
21. Huang Z., Song W., Zhang Y., Zhang Q., Zhou D., Zhou X. et al. Three-dimensional printing model improves morphological understanding in acetabular fracture learning. A multicenter, randomized, controlled study. PLoS ONE. 2018. № 13 (1). https://doi.org/10.1371/journal.pone.0191328.
22. Lars Brouwers, Albert F. Pull ter Gunne, Mariska A.C. de Jongh, Frank H.W.M. van der Heijden, Luke P.H. Leenen, Willem R. Spanjersberg, Sven H. van Helden, Diederik O. Verbeek, Mike Bemelman, Koen W.W. Lansink. The Value of 3D Printed Models in Understanding Acetabular Fractures. 3D printing and additive manufacturing. 2018. Vol. 5. № 1. P. 37-45.
23. Филиппенко В.А., Танькут В.А., Маколинец В.И., Гращенкова Т.Н., Мезенцев В.А., Танькут А.В., Акрамов В.Р. Реабилитация пациентов после ревизионного эндопротезирования тазобедренного сустава. Літопис травматології та ортопедії. 2011. № 1-2. С. 270.
24. Тихилов Р.М., Шубняков И.И., Коваленко А.Н., Билык С.С., Цыбин А.В., Денисов А.О. Применение индивидуальной трехфланцевой конструкции при ревизионном эндопротезировании с нарушением целостности тазового кольца (клинический случай). Травматология и ортопедия России. 2016. № 1. С. 108-116.
25. Косяков А.Н., Гребенников К.А., Милосердов А.В., Федин Е.М., Нечай А.А. Возмещение костных дефектов вертлужной впадины с использованием аддитивных технологий. Вісник ортопедії, травматології та протезування. 2018. № 4. С. 64-74.
26. Кавалерский Г.М., Мурылев В.Ю., Рукин Я.А., Лычагин А.В., Елизаров П.М. Применение индивидуальных вертлужных компонентов при ревизионном эндопротезировании тазобедренного сустава. Травматология и ортопедия России. 2016. № 22 (4). Р. 114-121.
27. Корыткин А.А., Захарова Д.В., Новикова Я.С., Горбатов Р.О., Ковалдов К.А., Эль Мудни Ю.М. Опыт применения индивидуальных трехфланцевых вертлужных компонентов при ревизионном эндопротезировании тазобедренного сустава. Травматология и ортопедия России. 2017. № 23 (4). С. 101-111.
28. Andrew J. Hughes, Cathal DeBuitleir, Philip Soden, Brian O’Donnchadha, Anthony Tansey, Ali Abdulkarim, Colm McMahon, and Conor J. Hurson. 3D Printing Aids Acetabular Reconstruction in Complex Revision Hip Arthroplasty. Advan-ces in Orthopedics. Vol. 2017. Article ID 8925050. 7 p. http://dx.doi.org/10.1155/2017/8925050.
29. Hughes A., Soden P., Abdulkarim A., McMahon C., Hurson C. The use of rapid prototyping and 3d printing in revision hip arthroplasty. Orthopaedic Proceedings. Vol. 96-B, № SUPP 10.
30. Stefan Tserovski, Simona Georgieva, Radoil Simeonov, Amir Bigdeli, Heinz Röttinger, Plamen Kinov. Advantages and disadvantages of 3D printing for pre-operative planning of revision hip surgery. Journal of Surgical Case Reports. 2019. № 7. P. 1-4.
31. Коваленко А.Н., Шубняков И.И., Билык С.С., Тихилов Р.М. Современные технологии лечения тяжелых костных дефектов области вертлужной впадины: какие проблемы решают индивидуальные импланты? Политравма. 2017. № 1. С. 65-81.
32. Коваленко А.Н., Шубняков И.И., Билык С.С., Денисов А.О., Тихилов Р.М. Возможности современных технологий визуализации и моделирования в ортопедии и их роль в разработке индивидуальных конструкций в хирургии тазобедренного сустава. Вестник хирургии им. И.И. Грекова. 2016. Т. 175. № 4. С. 46-52.
33. Попович А.А., Суфияров В.Ш., Полозов И.А., Борисов Е.В., Масайло Д.В., Вопиловский П.Н. и др. Применение аддитивных технологий для изготовления индивидуальных компонентов эндопротеза тазобедренного сустава из титановых сплавов. Медицинская техника. 2016. № 3. С. 43-46.
34. Yuvraj A., Bassam A.M. Triflange Acetabular Cup for Severe Acetabular Bone Defect. Biomed J. Sci & Tech. Res. 2017. № 1 (6).
35. Berasi C.C., Berend K.R., Adams J.B., Ruh E.L., Lombardi A.V. Are custom triflange acetabular components effective for reconstruction of catastrophic bone loss? Clin. Orthop. Relat. Res. 2014. № 473 (2). Р. 528-535.
36. Goodman G.P., Engh C.A. The custom triflange cup: build it and they will come. Bone Jt. J. 2016. № 98 (1). Р. 68-72.
37. Hogan C., Ries M. Treatment of massive acetabular bone loss and pelvic discontinuity with a custom triflange component and ilio-sacral fixation based on preoperative CT templating. A report of 2 cases. Hip Int. 2015. № 25 (6). Р. 585-588.
38. Li H., QuX., MaoY., Dai K., Zhu Z. Custom Acetabular Cages Offer Stable fixation and Improved Hip Scores for Revision THA With Severe Bone Defects. Clin. Orthop. Relat. Res. 2015. № 474 (3). Р. 731-740.
/19_2.jpg)

/19.jpg)
/19_3.jpg)
/20.jpg)
/20_2.jpg)
/22.jpg)