Вступ
Артроскопічні хірургічні втручання на колінному суглобі (АКС) сьогодні є найпоширенішими видами хірургічних операцій. Але досі не визначене питання щодо найкращої техніки знеболювання для цього виду хірургії [1]. Будь-яка анестезуюча техніка повинна забезпечувати швидке та безпечне відновлення, що супроводжується добрим контролем післяопераційного болю та задоволенням пацієнта. Тому у хворих, яким проводять артроскопічне втручання на колінному суглобі, такі кінцеві точки, як післяопераційний біль, частота виникнення післяопераційної нудоти та блювання (ПОНБ) і рання реабілітація, вважаються найважливішими факторами для оцінки [2].
Проте є важливими й економічні аспекти, а саме інтраопераційний час, що визначається як хірургічний час, плюс час анестезії, час перебування у палаті відновлення після анестезії, швидкість реадмісії та загальні строки перебування у стаціонарі. Задоволеність пацієнта вважається результатом комбінації вищеза–значених факторів [5].
Останнім десятиріччям медична спільнота посилила свій інтерес до подальшого розвитку амбулаторної хірургії та пов’язаних із цим анестезіологічних методів. Зараз цілком очевидно, що амбулаторне лікування певних патологій не загрожує загальному стану пацієнта, а, навпаки, підвищує задоволеність пацієнта та зменшує витрати на медичну допомогу [6]. Це є першочерговою метою сучасної системи охорони здоров’я.
Окрім більш широкого використання малоінвазивної артроскопічної хірургії колінного суглоба, що дозволяє проводити процедури менш травматично, виникає анестезіологічне завдання, яке полягає у пошуку найоптимальнішої техніки, що відповідала би хірургічним умовам та потребам пацієнта [7]. Оскільки більшість з артроскопічних втручань наразі виконуються в межах стратегії «хірургії одного дня», ця реальність породила необхідність оцінки та порівняння методів анестезії, що зазвичай використовуються при АКС.
Мета дослідження: підвищити якість, ефективність та безпеку анестезіологічного забезпечення артроскопічних втручань на колінному суглобі шляхом удосконалення персоніфікованого періопераційного анестезіологічного менеджменту.
Матеріали та методи
Гіпотеза. Поєднання спінальної анестезії (СА) з внутрішньовенним уведенням дексмедетомідину порівняно з протоколом багатокомпонентної низькопотокової інгаляційної анестезії (БНІА) севофлюраном для АКС сприяє кращому післяопераційному знеболюванню, зниженню частоти ПОНБ, скороченню терміну госпіталізації та підвищує рівень загальної задоволеності пацієнта.
Критерії включення. Пацієнти віком від 18 до 78 років із соматичним класом I–II за ASA, яким запланована АКС.
Критерії виключення. Вік пацієнта молодший від 18 років, наявність супутньої соматичної патології у стані декомпенсації, вагітність, відмова пацієнта від участі в дослідженні.
До цього проспективного рандомізованого незасліпленого дослідження увійшли 142 пацієнти, які були розподілені на дві групи залежно від виду анестезіологічного забезпечення. Рандомізація відбувалася винятково з урахуванням бажання пацієнта отримати той чи інший вид анестезіологічного забезпечення. До першої (експериментальної) групи увійшли па–цієнти, яким була проведена спинномозкова анестезія в поєднанні з внутрішньовенним уведенням дексмедетомідину (n1 = 82); до другої (контрольної) групи увійшли пацієнти, до яких був застосований протокол багатокомпонентної низькопотокової інгаляційної анестезії.
Обидві групи пацієнтів отримували інформацію про методи анестезії, підписували інформовану згоду. Пацієнтів госпіталізували до відділення ортопедії за 1–2 години до операції.
При первинному огляді анестезіолог у всіх пацієн–тів оцінював рівень передопераційного стресу: застосовували спеціальну міжнародну анкету з шести пунктів — Амстердамська шкала передопераційної тривоги та потреби в інформації (APAIS) [3, 4]. Перші два запитання оцінюють анестезіологічний компонент формування тривожності, четверте та п’яте — операційний, третє та шосте запитання свідчать про потребу в поінформованості пацієнтів. У загальному оцінюванні були сформовані два показники як сума балів кожної складової — тривожності (сума балів від 4 до 20) та поінформованості (сума балів від 2 до 10). В осіб із підвищеним хвилюванням проводили аналіз його компонентів за анкетою анестезіологічної та хірургічної передопераційної тривожності (ASPA). Обидві анкети побудовані за п’ятибальною шкалою Лікерта.
Протокол СА (експериментальна група, n1 = 82) в поєднанні з внутрішньовенним уведенням дексмедетомідину: за 30 хвилин до оперативного втручання пацієн–ту вводилася навантажувальна доза дексмедетомідину 1,5–2 мкг/кг/год внутрішньовенно впродовж 20 хвилин.
Після дезінфекції шкіри та знеболювання 2% розчином лідокаїну 2,0 проводилася пункція субарахноїдального простору на рівні L3-L4. Для забезпечення моторного та сенсорного блоку вводився 0,5% розчин бупівакаїну для спінальної анестезії в об’ємі 1,8–2,0.
Після досягнення клінічних ознак ефективної СА розпочиналася постійна внутрішньовенна інфузія декс–медетомідину в дозі 0,5–1,0 мкг/кг/год.
Протокол загальної анестезії (контрольна група, n2 = 60): премедикація за 30 хвилин до оперативного втручання — ондансетрон 8 мг, декскетопрофен 50 мг, пантопразол 40 мг в/в, парацетамол 1000 мг в/в крапельно, лідокаїн 40 мг в/в. Індукція пропофолом 1,5–2,0 мг/кг фракційно до досягнення клінічних симптомів наркозу, фентаніл 0,005% — 0,1 мг. Штучна вентиляція легень проводилася через ларингеальну маску без використання міорелаксантів. Підтримка анестезії: киснево-севофлюранова суміш FiO2 — 50–55 %, севофлюран — 1,4–1,6 на видиху при потоці не більше 1 л/хв при показниках BIS на рівні 45–55. З метою інтраопераційного знеболювання застосовували фентаніл в дозі 1,2–1,5 мкг/кг атм/год, лідокаїн — 1–1,5 мг/кг атм/год.
Інтраопераційний моніторинг пацієнтів в обох групах включав: неінвазивне вимірювання артеріального тиску, частоти серцевих скорочень, пульсо–ксиметрію, ЕКГ. У групі БНІА додатково визначалася концентрація кисню, вуглекислого газу та інгаляційного анестетика на вдиху і видиху, проводилася реєстрація біспекторального індексу в режимі онлайн у літніх пацієнтів.
Пацієнтам в обох групах рівень післяопераційного болю визначався за візуальною аналоговою шкалою (ВАШ) [15]. Оцінка болю за ВАШ проводилася вперше на операційному столі, одразу після закінчення оперативного втручання, далі — через 1, 4, 6, 12 та 24 години після операції двічі (перед знеболюванням та через 30 хвилин після нього).
Інтерпретація даних за шкалою ВАШ: 0 — немає болю; 1–3 бали — слабкий біль; 4–5 балів — помірний біль; 6–9 балів — сильний біль; 10 балів — найсильніший біль, який тільки можна уявити.
Інтерпретація результатів знеболювання: 1) немає болю — 0 балів; 2) адекватне знеболювання — 1–4 бали; 3) необхідне додаткове знеболювання (помірний біль) — 5 балів; 4) необхідне знеболювання наркотичними анальгетиками (сильний біль) — 6–10 балів.
Частота виникнення післяопераційної нудоти та блювання фіксувалася впродовж перших 24 годин післяопераційного періоду в пацієнтів обох груп.
Для об’єктивізації клінічної значущості нудоти використовували шкалу оцінки інтенсивності клінічних проявів ПОНБ, що складається з чотирьох пунктів, де 0 відповідав відсутності ПОНБ, 1 — появі нудоти, 2 — наявності блювання, 3 — розвитку повторного (неод–норазового) блювання. В разі двох або більше епізодів блювоти внутрішньовенно вводили ондансетрон у дозі 4–8 мг або в поєднанні з дексаметазоном 4–8 мг [16].
Обидві групи отримували періопераційну тромбопрофілактику у вигляді компресійних панчох і низькомолекулярного гепарину в профілактичних дозах.
Задоволеність пацієнтів від анестезії визначалася за ВАШ при виписці зі стаціонару.
Статистична обробка результатів дослідження здійснювалася за допомогою пакета аналізу статистичних даних MedCalc v. 18.11 (MedCalc Software Inc., Broekstraat, Бельгія).
Результати
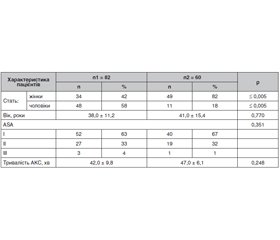
У табл. 1 наведені дані щодо загальної характеристики пацієнтів.
Згідно з наведеними даними табл. 1, не було статистичної різниці за критерієм Стьюдента щодо віку хворих, соматичного статусу за ASA та тривалості хірургічного втручання, але дослідні групи статистично відрізнялися за статтю.
Оцінка передопераційного стресу
Наш аналіз засвідчив, що передопераційний стрес є у кожного пацієнта. Фактори, що сприяють його збільшенню, перш за все пов’язані зі ступенем інформаційної та психологічної передопераційної підготовки, наявності попередніх оперативних утручань. Сприйняття також залежить від віку та статі пацієнта, рівня його освіти. Основні результати оцінювання стресу за шкалою APAIS наведені в табл. 2.
В експериментальній групі кількість осіб із високою тривожністю становила 52,7 %, у контрольній — 79,5 %. Спостерігається суттєва різниця між показниками жінок та чоловіків. Жінки реагували більш емоційно (показник кореляції — r = 0,59; p < 0,05), їхній рівень тривожності дорівнював 15,60 ± 0,53 проти 12,40 ± 0,89 у чоловіків (p < 0,05).
Показники застосованої нами ВАШ передопераційного очікування пацієнтів корелювали із загальним рівнем тривожності (r = 0,52; p < 0,001). Ступінь тривожності, визначений за ВАШ, був дещо меншим в обох групах, ніж за шкалою APAIS, але зі збереженням різниці між ними. Показники ВАШ корелювали з відповідями на запитання шкали анестезіологічної та хірургічної передопераційної тривожності (ASPA) — із загальним показником (r = 0,56; p < 0,001) та окремими запитаннями (від r = 0,42; p < 0,05, до r = 0,65; p < 0,001).
Оцінка больового синдрому
Динаміка показників рівня післяопераційного болю за ВАШ у першу добу після операції наведена в табл. 3.
Відповідно до результатів табл. 3, не було статистично значущих відмінностей між дослідницькими групами щодо середніх балів болю в перші 1, 12 та 24 години після АКС. При рівні больового порогу до 5 балів за ВАШ як знеболювання використовувалися нестероїдні протизапальні засоби (декскетопрофен) та парацетамол, вище 5 балів — наркотичні анальгетики (налбуфін, промедол). Після вищезазначених артроскопічних втручань на колінному суглобі рівень болю за ВАШ у пацієнтів експериментальної групи в середньому не перевищував 3 балів протягом першої післяопераційної доби. У пацієнтів контрольної групи показники рівня болю за ВАШ вірогідно мали тенденцію до поступового зростання в перші вісім післяопераційних годин, але відсоток пацієнтів, які потребували знеболювання наркотичним анальгетиком, був однаковий в обох групах.
Ускладнення, пов’язані з анестезією
Найчастішим ускладненням у групі загальної анестезії був показник болю > 5. Прояви ПОНБ спостерігалися у 10 % пацієнтів контрольної групи та у 4 % осіб в експериментальній групі. У 18 % пацієнтів експериментальної групи та 13 % пацієнтів контрольної групи спостерігалася гіпотонія, що потребувала лікування; один пацієнт експериментальної групи мав клінічну картину постпункційного головного болю, що ніяк не вплинуло на строки перебування у стаціонарі (табл. 4).
Із наведених у табл. 4 даних випливає, що не було статистично значущої різниці за критерієм Стьюдента щодо частоти випадків ускладнень анестезіологічного забезпечення між дослідними групами.
Рівень задоволеності пацієнтів за ВАШ залежно від виду анестезії зазначений у табл. 5.
Задоволеними методом знеболювання почувалися 75 % осіб із групи СА (експериментальна) порівняно з 48 % тих, хто отримував загальну анестезію (контрольна група).
Наші результати свідчать про те, що відповідний вибір пацієнта повинен бути важливим фактором для анестезіолога, та підкреслюють важливість оптимізації інтраопераційних складових, таких як тип анестезії, для подальшої реабілітації пацієнта після артроскопічних втручань на колінному суглобі.
Потреба в поінформованості залишається високою і практично однаковою без різниці між жінками та чоловіками. В нашому дослідженні у пацієнтів із достатнім об’ємом інформації про знеболювання та хід операції ступінь тривожності загалом був нижчий. Проте жінки мали більший рівень передопераційного стресу, ніж чоловіки. Саме з цим фактом ми пов’язуємо частий вибір загальної анестезії жінками. Крім того, загальну анестезію обирали пацієнти, які мали досвід оперативного втручання під регіонарною анестезією без седативного компонента.
Загальні строки госпіталізації були дещо збільшені в групі спинномозкової анестезії.
Взаємозв’язок між СА та госпіталізацією в нашому дослідженні може бути викликаний низкою різних причин. Спінальна анестезія викликає моторну та сенсорну блокаду нижніх кінцівок. Залежно від конкретного місцевого анестетика, що застосовується нейроаксіально, тривалість моторної та сенсорної блокади від спінальної анестезії може становити 6 і більше годин. Але цей факт загалом не вплинув на ступінь задоволеності пацієнта.
Висновки
Нейроаксіальна та загальна анестезії при артроскопічній хірургії колінного суглоба мають переваги та недоліки.
Передопераційна підготовка повинна включати необхідну для пацієнта інформацію про майбутнє знеболювання та хід і тривалість операції.
Прийняття рішення про методи анестезіологічного забезпечення повинно базуватися на бажанні пацієнта та його можливому попередньому оперативному досвіді.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 11.04.2021
Рецензовано/Revised 25.04.2021
Прийнято до друку/Accepted 05.05.2021

/92.jpg)
/93.jpg)