Вступ
Заміщення післярезекційних дефектів довгих кісток у разі їх ураження пухлинним процесом завжди є актуальною проблемою ортопедії. Постійно ведеться пошук «ідеального» матеріалу для заміщення дефектів кісток, застосування якого може призвести до найменшої кількості ускладнень, максимальної «виживаності» імплантата та найкращим функціональним результатам лікування [1, 2]. Найбільш часта локалізація пухлинних уражень — проксимальні відділи плечової, стегнової та великогомілкової кісток, а також дистальний відділ стегнової кістки. Саме зони з ураженням суглобів мають великий інтерес та значення для подальшої доброї функції кінцівки. У разі ураження проксимального та дистального метаепіфізів довгих кісток, безумовно, ставлять показання до заміщення їх післярезекційних дефектів ендопротезами як метод вибору при даних локалізаціях [3–5].
Серед багатого різноманіття матеріалів і методик реконструкції післярезекційних дефектів довгих кісток найбільшої поширеності набули індивідуальне, модульне ендопротезування та біореконструктивні втручання (сегментарна кісткова алопластика та алокомпозитне ендопротезування) [6–9]. Кожен метод має свої переваги та недоліки. У результаті проведених статистичних порівняльних аналізів і метааналізів методик індивідуального ендопротезування та алокомпозитного ендопротезування було виявлено, що під час застосування алокомпозитного ендопротезування спостерігалися найменша кількість інфекційних уражень та кращі функціональні результати (у деяких локалізаціях), ніж у разі застосування індивідуального ендопротезування для заміщення післярезекційних дефектів. Але у разі порівняння ускладнень механічного характеру обидві методики мають такі ускладнення, як переломи металевих конструкцій та, у випадку з алокомпозитним ендопротезуванням, порушення репаративних процесів у зоні контакту кісткового алотрансплантата та кістки реципієнта. Для покращення результатів оперативних втручань з використанням різних методик заміщення післярезекційних дефектів довгих кісток постійно ведуться розробки нових металевих конструкцій і способів виконання даних методик [10–15].
Теоретично-експериментальне дослідження та порівняння характеристик напружено-деформованого стану різних «систем-імплантатів» дозволяє виявити найбільш надійний метод заміщення післярезекційних дефектів довгих кісток та теоретично його обґрунтувати.
Метод кінцевих елементів — один з основних методів вирішення завдань механіки деформованого тіла, теплопровідності, гідромеханіки тощо. Ідея методу складається в апроксимації суцільного середовища з нескінченою кількістю ступенів свободи сукупністю простих елементів, пов’язаних між собою у вузлових точках. Для метода кінцевих елементів характерний широкий діапазон використання, інваріантність відносно до геометрії конструкції та механічних властивостей матеріалів, простота визначення взаємодії конструкції з зовнішнім середовищем (механічне та температурне навантаження, граничні умови тощо), високий ступінь пристосованості до автоматизації всіх етапів розрахунків. Популярність методу пояснюється простотою його фізичної інтерпретації та явним зв’язком з методами Рітца й переміщень, які досить широко використовують у механіці суцільних середовищ [16–19].
Для вивчення механічних властивостей обраних нами конструкцій проведено моделювання різних видів заміщення післярезекційних дефектів стегнової кістки за допомогою методу кінцевих елементів.
Мета дослідження — порівняти дані напружено-деформованих станів у математичних моделях «алокомпозитний ендопротез» та «індивідуальний ендопротез» проксимального відділу стегнової кістки.
Матеріали та методи
Для порівняльного дослідження була обрана локалізація — проксимальний відділ стегнової кістки та різні методики алокомпозитного ендопротезування й індивідуального ендопротезування (без кісткової пластики) та обрано метод кінцевих елементів для досягнення мети, що була визначена.
У лабораторії біомеханіки ДУ «Інститут патології хребта та суглобів ім. проф. М.І. Ситенка НАМН України» створено математичні моделі стегнової кістки з формуванням післярезекційного дефекту її проксимального відділу, що заміщений сегментарним кістковим алотрансплантатом у комбінації з індивідуальним ендопротезом (моделювання алокомпозитного ендопротеза). Модель подана у двох варіантах — з формуванням поперечної остеотомії (у зоні контакту кісткового алотрансплантата та кістки реципієнта) — 1-ша модель (рис. 1а) та з формуванням східцеподібної остеотомії — 2-га модель (рис. 1б).
Кожна модель алокомпозитного ендопротезування досліджувалася окремо з цементним і безцементним прошарком у зоні ніжки ендопротеза та інтрамедулярного каналу кістки реципієнта.
Для порівняння була обрана модель з повною заміною проксимального кінця стегнової кістки індивідуальним ендопротезом без кісткової пластики — 3-тя модель (рис. 1в). Зовнішній вигляд моделей наведено на рис. 1.
По лінії резекції моделювали наявність кісткового регенерату шляхом введення тонкого прошарку, якому надавали значення модулю пружності для імітації стану регенерату через 6 місяців після операції (математичне дослідження алокомпозитного ендопротезування на різних термінах репаративного процесу наведено у статті [13]).
Механічні властивості біологічних тканин (кортикальна та губчаста кістка, хрящ) для математичного моделювання обрано за даними літератури. Матеріал елементів ендопротеза — титан. Механічні характеристики штучних матеріалів обирали за даними технічної літератури [16]. При моделюванні використовували такі характеристики, як Е — модуль пружності (модуль Юнга), ν — коефіцієнт Пуассона. Механічні характеристики матеріалів, що використовували в розрахунках, наведені в табл. 1.
Для навантаження моделі моделювали масу тіла при одноопорному стоянні, для чого до головки стегнової кістки прикладали розподілену силу величиною 1100 Н, а до великого вертлюга прикладали силу дії м’язів, що відводять стегно, величиною 540 Н [17]. Опорна поверхня стопи моделі мала жорстке закріплення. Схема навантаження моделі наведена на рис. 2.
Величини максимальних напружень фіксували в чотирьох зонах на великогомілковій кістці та в трьох точках на ніжці ендопротеза. Схема розташування контрольних точок наведена на рис. 3.
Дослідження напружено-деформованого стану моделей виконували за допомогою методу кінцевих елементів. Як критерій оцінки напруженого стану моделей використовували напруження за Мізесом. Моделювання виконували за допомогою системи автоматизованого проєктування SolidWorks. Розрахунки напружено-деформованого стану моделей виконували за допомогою програмного комплексу CosmosM [18].
Результати та обговорення
У результаті проведеного дослідження були отримані дані про напружено-деформовані стани у запропонованих моделях та проведене їх порівняння. Виявлено різницю між даними у разі застосування алокомпозитного ендопротезування та індивідуального ендопротезування (без кісткової пластики).
Картина розподілу напружень у 1-й моделі (алокомпозитний ендопротез з поперечною остеотомією) з безцементним кріпленням ніжки наведена на рис. 4.
Проведене дослідження показало, що максимальна величина напружень на ніжці ендопротеза, а саме в зоні остеотомії, визначається на досить високому рівні — 75,6 МПа. Доцільно відмітити вирівнювання величин напружень в діафізарній частині стегнової кістки, де вони визначаються в межах від 9,5 до 10,0 МПа.
Картину розподілу напружень в моделі із східцеподібною остеотомією після ендопротезування з безцементним кріпленням ніжки можна спостерігати на рис. 5.
Аналогічна картина спостерігається й при використанні східцеподібної остеотомії при безцементному кріпленні ніжки ендопротеза. Отже, вирівнювання величин напружень в діафізі стегнової кістки відбувається повільніше, ніж при виконанні поперечної остеотомії. Діапазон напружень в діафізарній частині стегнової кістки визначається більш широким — від 7,9 до 13,8 МПа. Дані про величини напружень у контрольних точках моделей з безцементним кріпленням ніжки в найближчий період після ендопротезування зведено до табл. 2.
Розглянемо розподіл напружень в моделі безцементного ендопротезування стегнової кістки без кісткової пластики (рис. 6).
Як показали дослідження, ендопротез без кісткової пластики приймає на себе все навантаження, про що свідчать величини напружень на елементах конструкції, де вони спостерігаються в межах від 21,0 до 43,7 МПа. Маса кісткової тканини при такому способі ендопротезування залишається незначною, тому при утриманні ендопротеза в неї також виникають значні напруження, більші за 20,0 МПа. Також слід відмітити нижчі за попередні варіанти ендопротезуваня напруження на ніжці ендопротеза. Це можна пояснити тим, що ендопротез має опору на кортикальний шар діафіза стегнової кістки, що, в свою чергу, викликає досить значні напруження в кістковій тканині — від 21,5 до 24,2 МПа.
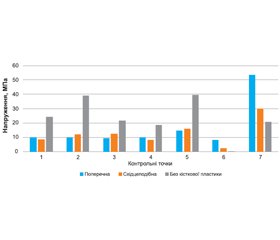
Детальніше порівняти величини напружень в контрольних точках моделей з безцементним кріпленням ніжки у віддалений період після ендопротезування дозволяє діаграма, яка наведена на рис. 7.
Як бачимо, набуття міцності кісткового регенерату призводить до вирівнювання величин напружень як між контрольними точками кожної з моделей, так і між моделями з різними видами остеотомії стегнової кістки. Отже, різниця у величинах напружень на ніжках ендопротезів, а саме в зонах остеотомій та на їх дистальних кінцях, залишається досить значною на користь моделі із східчастою остеотомією.
Розглянемо розподіл напружень в моделі ендопротезування стегнової кістки з цементним кріпленням ніжки без кісткової пластики (рис. 8).
Як показали дослідження, ендопротезування з використанням кісткового цементу без кісткової пластики не призводить до значних знижень величин напружень як в елементах ендопротеза, так і в кістковій тканині. Це відбувається завдяки наявності жорсткої опори ендопротеза на кортикальну кістку по лінії резекції.
Розглянемо картину напружено-деформованого стану моделі з поперечною остеотомією та цементним кріпленням ніжки у віддалений період після ендопротезування, яка наведена на рис. 9.
Як і в моделі з безцементною фіксацією ніжки ендопротеза, підвищення міцності кісткового регенерату в зоні остеотомії при цементному кріпленні ніжки в поєднанні з поперечною остеотомією стегнової кістки дозволяє знизити рівень величин напружень у всіх контрольних точках моделі. Отже, на характер розподілу напружень в моделі ці зміни не мають принципового впливу.
Розподіл напружень в моделі із східцеподібною остеотомією стегнової кістки та цементним кріпленням ніжки ендопротеза у віддалений період після ендопротезування можна спостерігати на рис. 10.
У моделі із східцеподібною остеотомією стегнової кістки та цементним кріпленням ніжки ендопротеза підвищення міцності кісткового регенерату призводить до невеликого зменшення величин напружень у всіх контрольних точках моделей, без принципових змін в характері розподілу цих напружень.
Дані про значення величин напружень в контрольних точках моделей з цементним кріпленням ніжки ендопротеза у віддаленому періоді після ендопротезування наведені в табл. 3.
Для наочного порівняння величин напружень в контрольних точках моделей із цементним кріпленням ніжки ендопротеза у віддаленому періоді після ендопротезування побудована діаграма, яка наведена на рис. 11.
Результати проведеного дослідження дозволяють стверджувати, що виконання остеотомії стегнової кістки у вигляді сходинки (східцеподібна) дозволяє значно знизити рівень напружень саме в зоні остеотомії, що має особливе значення в найближчому післяопераційному періоді після ендопротезування, поки міцність кісткового регенерату по лінії остеотомії не набуває достатнього рівня.
Східцеподібна остеотомія стегнової кістки дозволяє вдвічі знизити рівень механічних напружень в зоні остеотомії. Це відбувається завдяки тому, що виконання розтину у вигляді сходинки дозволяє кістковим фрагментам надавати спротив зсувним переміщенням. Це пояснює й виникнення асиметричних пікових напружень вище та нижче зони остеотомії.
Використання кісткового цементу для фіксації ніжки ендопротеза дозволяє значно знизити рівень напружень навколо ніжки ендопротеза при обох варіантах виконання остеотомії стегнової кістки. Це відбувається за рахунок того, що кістковий цемент, маючи модуль пружності за проміжною величиною між титаном та кістковою тканиною, утворює між ними прошарок, який виконує демпферну функцію, чим згладжує різницю величин деформації металу та кісткової тканини, тим самим знижуючи рівень напружень в них. Саме тому значне зменшення величини напружень в моделях із цементною фіксацією ніжки спостерігається тільки в кістково-мозковому каналі та ніжці ендопротеза.
Ендопротезування без виконання кісткової пластики призводить до виникнення підвищених напружень в кістковій тканині завдяки наявності жорсткої опори ендопротеза на кортикальну кістку в діафізі по лінії її резекції. Цей факт також не дозволяє знизити рівень напружень як в елементах ендопротеза, так і в кістковій тканині при використанні кісткового цементу.
Висновки
1. Виконання остеотомії стегнової кістки у вигляді сходинки (східцеподібної остеотомії) дозволяє вдвічі знизити рівень механічних напружень саме в зоні остеотомії порівняно з моделями з поперечною остеотомією, що має особливе значення на ранніх післяопераційних етапах.
2. Використання кісткового цементу для фіксації ніжки ендопротеза також дозволяє значно знизити рівень напружень у всіх варіантах досліджених моделей за рахунок утворення демпферного прошарку між металом та кістковою тканиною.
3. Рівень напружень в моделях ендопротезування без кісткової пластики не залежить від використання кісткового цементу, а визначається наявністю жорсткої опори ендопротеза на кортикальну кістку по лінії її резекції.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 11.08.2021
Рецензовано/Revised 27.08.2021
Прийнято до друку/Accepted 04.08.2021
Список литературы
1. Gharedaghi M., Peivandi M.T., Mazloomi M. et al. Eva-luation of clinical results and complications of structural allograft reconstruction after bone tumor surgery. Arch. Bone Joint Surg. 2016. 4(3). 236-242.
2. Вирва О.Є., Головіна Я.О., Малик Р.В., Головіна О.О. Системний огляд і метааналіз результатів модульного й алокомпозитного ендопротезування за умов кістково-суглобових дефектів після резекції пухлини. Ортопедія, травматологія і протезування. 2020. 2. 5-15. DOI: 10.15674/0030-5987202025-15.
3. Bloebaum R.D., Merrell M., Gustke K., Simmons M. Retrieval analysis of a hydroxyapatite-coated hip prosthesis. Clin. Orthop. Relat. Res. 1991. 267. 97-102.
4. Calabró T., Van Rooyen R., Piraino I. et al. Reconstruction of the proximal femur with a modular resection prosthesis. Eur. J. Orthop. Surg. Traumatol. 2016. 26(4). 415-421. DOI: 10.1007/s00590-016-1764-0 [Epub 2016 Apr 4].
5. Sandoval P.P.G., Utrilla A.L., Trigueros-Rentero M.A., Lopez-Prats F.A. Mid- to long-term results of allograft-prosthesis composite reconstruction after removal of a distal femoral malignant tumor are comparable to those of the proximal tibia. Knee Surgery, Sports Traumatology, Arthroscopy. 2019. 27. 2218-2225. DOI: /10.1007/s00167-018-5110-4.
7. Capanna R., Donati I.X., Masctti C. et al. Effect of electromagnetic fields on patients undergoing massive bone graft following bone tumor resection: a double blind study. Clin. Orthop. Rclat. Res. 1994. 306. 213-221.
8. Blunn G.W., Briggs T.W., Cannon S.R. et al. Cementless fixation for primary segmental bone tumor endoprostheses. Clin. Orthop. 2000. 372. 223-230.
9. Capanna R., Morris H.G., Campanacci D. et al. Modular uncemented prosthetic reconstruction after resection of tumours of the distal femur. J. Bone Joint Surg. Br. 1994. 76. 178-186.
10. Головіна Я.О. Хірургічний етап лікування пацієнтів з метастатичними ураженнями довгих кісток: Дис. … канд. мед. наук: 14.01.21. Харків, 2013. 170 с.
11. Вырва О.Е., Головина Я.А., Малык Р.В. Аллокомпозитное эндопротезирование при хирургическом лечении пациентов со злокачественными опухолями длинных костей (обзор литературы). Ортопедия, травматология, протезирование. 2015. 2. 120-126.
12. Вирва О.Є., Головіна Я.О., Суббота Я.А. Заміщення післярезекційних дефектів стегнової кістки у лікуванні хворих з метастатичними ураженнями. Ортопедия, травматология и протезирование. 2013. 2. 73-79. DOI: 10.15674/0030-59872013273-79.
13. Вирва О.Є., Головіна Я.О., Карпінський М.Ю., Яресько О.В., Малик Р.В. Дослідження напружено-деформованого стану в системі «імплантат — кістка» на моделі алокомпозитного ендопротеза проксимального відділу стегнової кістки. Травма. 2020. 21(1). 38-48. DOI: 10.22141/1608-1706.1.21.2020.197797.
14. Benedetti M.G., Bonatti E., Malfitano C., Donati D. Comparison of allograft prosthetic composite reconstruction and modular prosthetic replacement in proximal femur bone tumors: functional assessment by gait analysis in 20 patients. Acta Orthop. 2013. 84(2). 218-223. DOI: 10.3109/17453674.2013.773119.
15. McGoveran B.M., Davis A.M., Gross A.E., Bell R.S. Evaluation of the allograftprosthesis composite technique for proximal femoral reconstruction after resection of a primary bone tumour. Can. J. Surg. 1999. 42(1). 3716.
16. Gere J.M., Timoshenko S.P. Mechanics of Material. Boston: PWS Publishing Company, 1997. 912 p.
17. Образцов И.Ф., Адамович И.С., Барер И.С. и др. Проблема прочности в биомеханике: Учебное пособие для техн. и биол. спец. вуз. М.: Высшая школа, 1988. 311 с.
18. Алямовский А.А. SolidWorks/COSMOSWorks. Инженерный анализ методом конечных элементов. М.: ДМК Пресс, 2004. 432 с.
19. Calabró T., Van Rooyen R., Piraino I. et al. Reconstruction of the proximal femur with a modular resection prosthesis. Eur. J. Orthop. Surg. Traumatol. 2016. 26(4). 415-421. DOI: 10.1007/s00590-016-1764-0 [Epub 2016 Apr 4].

/43.jpg)
/43_2.jpg)
/43_3.jpg)
/44.jpg)
/45.jpg)
/46.jpg)
/47_2.jpg)
/47.jpg)